NMR同时定量测定苯二酚三种同分异构体*
2016-09-02敖特根巴雅尔
赵 丹,敖特根巴雅尔
(内蒙古农业大学理学院,内蒙古 呼和浩特 010018)
NMR同时定量测定苯二酚三种同分异构体*
赵丹,敖特根巴雅尔
(内蒙古农业大学理学院,内蒙古呼和浩特010018)
以核磁共振定量测定技术为依据,以甲酸胺为外标,建立定量测定苯二酚三种同分异构体含量的方法。结果得到邻、间、对苯二酚均在线性范围内有良好的线性,回归方程分别:y=-0.00315+40.38201x,r=0.99996;y=0.00254+39.96878x,r=0.99998; y=2.51044E-4+80.31374x,r=0.99992;回收率分别为:100.39%、100.96%、100.09%。本方法取样量少,直接定量,灵敏度高,方法简单,重现性好,而且可以同时测定溶液中这三种物质的含量,可作为苯二酚三种同分异构体定量测定的一种简单方法。
核磁共振(NMR);邻苯二酚;间苯二酚;对苯二酚;外标法;含量测定
苯二酚为重要的精细化工原料及中间体,广泛应用于染料、涂料、农业、医药以及相关化工领域[1-3]。定量测定苯二酚异构体的研究有很多,殷程鹏等[4]用气相色谱法对邻苯二酚和对苯二酚进行分析测定;纪晓红等[5]用高效液相色谱法测定间苯二酚反应液中间苯二酚的含量;吴根华、谢成根、杨继东等分别用荧光法分析测定了苯二酚异构体的含量[6-8]、吴永军、孙进高等分别用电化学法分析研究了邻苯二酚和对苯二酚含量的测定[9-10]。而利用核磁共振法(NMR)对苯二酚异构体进行定量分析的研究相对较少。
尽管 NMR 通常用于结构分析,它正被越来越多的人视为一种重要的定量工具。NMR用于定量分析时最为强大,因为共振信号的积分强度直接与该信号所代表的原子核数成正比。此外,谱图中的所有质子均具有相同的灵敏度,因此确定定量结果不再需要特定化合物的消光系数或校准。NMR 平台高度稳定且线性良好,仅通过浓度外标物的绝对积分和一维谱图就可以方便地对小分子有机物进行准确而精密的定量核磁(Q NMR)测量。因此,Q NMR越来越多的被应用到各个领域[11-19]。
苯二酚的三种同分异构体因空间结构的差异会在核磁共振氢谱上出现不同的特征峰且互不干扰,使NMR法定量测定苯二酚异构体有了先决条件。因此,本研究利用NMR法定量测定苯二酚异构体,与其他方法相比该方法具有灵敏度高、精密度好、准确度高、且无需对样品进行复杂的预处理等优点。
1 实 验
1.1仪器与试剂
Bruker AvanceШ 500 型超导核磁共振波谱仪;DV215CD型分析电子天平,感量0.01 mg。
重水(氘代度为99.8%),美国诺雷尔公司;邻、间、对苯二酚(分析纯,纯度99.5%),北京化工厂生产;甲酸胺(分析纯,纯度98.0%),国药集团化学试剂有限公司。
1.2溶液的配制
准确称取邻苯二酚、间苯二酚、对苯二酚各110.00 mg分别用D2O溶解于10 ml的容量瓶中并定容,配成0.1 mol/L的标准溶液备用。准确称取1.57 mg甲酸胺置于毛细管中加D2O完全溶解,并将其密封用作定量分析的外标。
1.3定量方法
测定核磁共振氢谱中外标物峰s的峰面积As,和样品的峰x的峰面积Ax,按下式计算样品的含量。
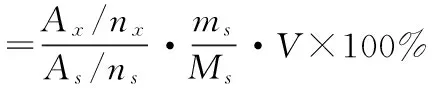
(1)
式中:nx——样品的对应峰的质子数
ns——外标峰对应的质子数
ms——外标物的质量(1.57 mg)
Ms——外标物的摩尔质量(63.06 g/mol)
V——样品的体积(500 μL)
1.4实验参数与仪器的校正
氢谱的弛豫延迟(D1)值为5.0 s,采样温度(T)为25 ℃,采样次数(NS)为16次。按照上述测定条件调整仪器,将样品放入核磁共振波谱仪中,仔细匀场,测定后,调整相位并进行基线校正,选定外标峰和定量峰,积分,每个样品至少重复积分5次。
2 结果与讨论
2.1溶剂的选取
测试溶剂应选择对被测样品和外标物都有很好的溶解性且残留溶剂峰不造成干扰。通过试验,本实验选择D2O为测试溶剂,该溶剂对邻、间、对苯二酚和甲酸胺的溶解性都非常好,且其1H NMR谱中的出峰位置在δ4.80处,与其他信号峰没有干扰,不会对测试结果造成影响(见图1)。

图1 邻、间、对苯二酚溶于D2O的1H NMR谱
2.2外标物的选取

图2 外标物加入样品后的1H NMR谱
按照NMR测定的要求,外标物应具有较高的纯度,所含质子数较少,吸收峰处于较低场与所测的样品峰之间无干扰,按照上诉要求,本实验选择甲酸胺为外标物,甲酸胺1H NMR谱只有一个峰(化学位移在δ8.44处),且与样品的质子峰无干扰,甲酸胺为外标在样品中的1H NMR谱见图2。
2.3定量峰的选取
精密吸取邻、间、对苯二酚溶液各100 μL,D2O 200 μL于NMR管中,并加入外标毛细管,在上诉实验条件下测定溶液的1H NMR谱。
利用NMR方法定量分析必须先对1H NMR谱中的各个质子峰进行归属,明确每个质子峰对应的质子数,再选取合适的定量峰。本实验中,邻、间、对苯二酚的质子峰均不多(见图1),对各个质子峰的归属和定量峰的选取见表1。

表1 样品的质子峰及定量峰的归属
2.4线性关系


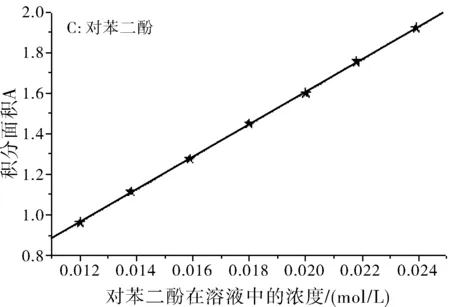
图3 邻、间、对苯二酚的浓度与积分面积的工作曲线
配制不同浓度的邻苯二酚、间苯二酚和对苯二酚标准系列溶液加入外标物进行测定,以被测物质的浓度为横坐标、积分面积为纵坐标,绘制其标准曲线。测定结果见图3。
所得的线性回归方程分别为:
邻苯二酚(0.010~0.022 mol/L):
y=-0.00315+40.38201x r=0.99996
间苯二酚(0.010~0.022 mol/L):
y=0.00254+39.96878x r=0.99998
对苯二酚(0.012~0.024 mol/L):
y=2.51044E-4+80.31374x r=0.99992
其中这三种异构体的最低检测线(LOD)分别为:0.00013 mol/L、0.00009 mol/L、0.00018 mol/L。最低定量限(LOQ)分别为:0.00042 mol/L、0.00030 mol/L、0.00058 mol/L。
根据核磁共振原理,样品在任何浓度范围内, 质子峰面积与样品浓度均呈线性。实验结果表明,用1H NMR法测定邻、间、对苯二酚,在一定的浓度范围内有很好的线性,与理论依据相吻合。
2.5回收率的测定
配制不同浓度的邻苯二酚、间苯二酚和对苯二酚标准系列溶液并加入外标物,测定其回收率。测定结果见表2。
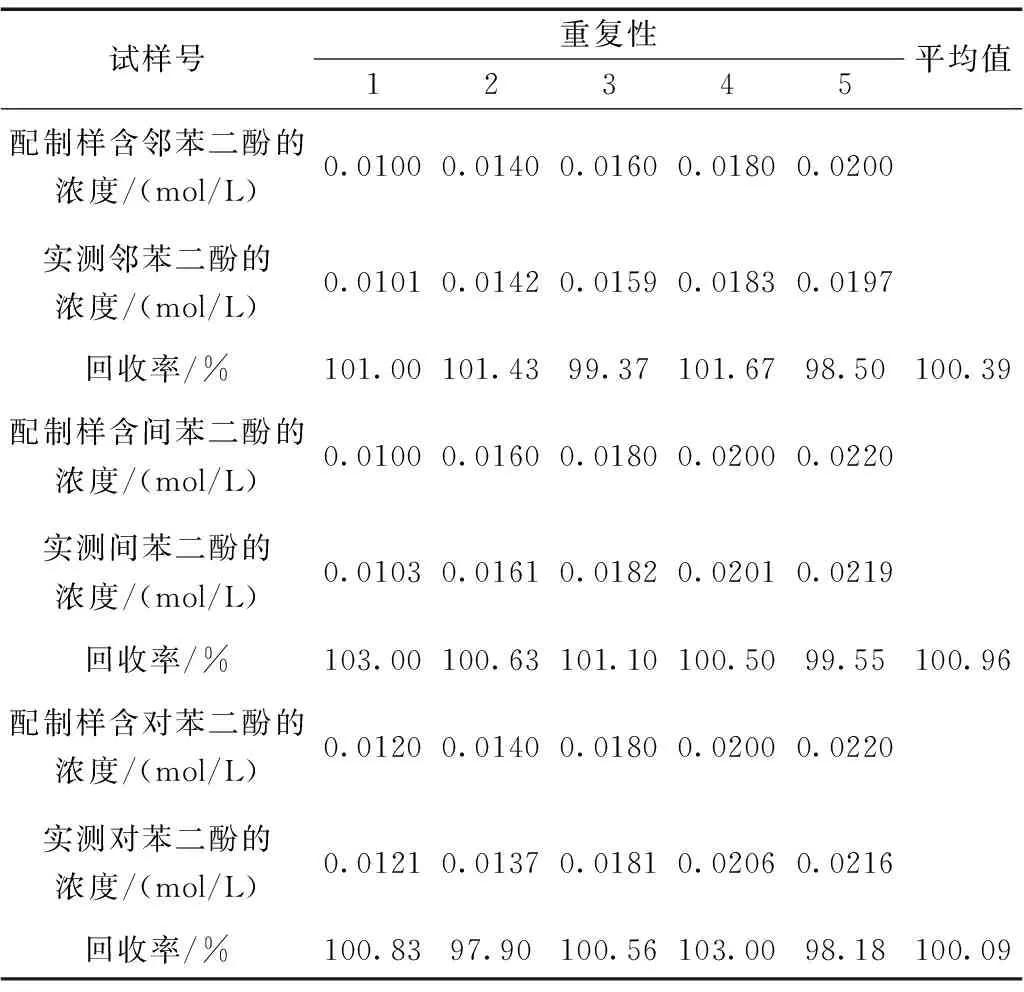
表2 回收率实验结果
2.6重复性的测定
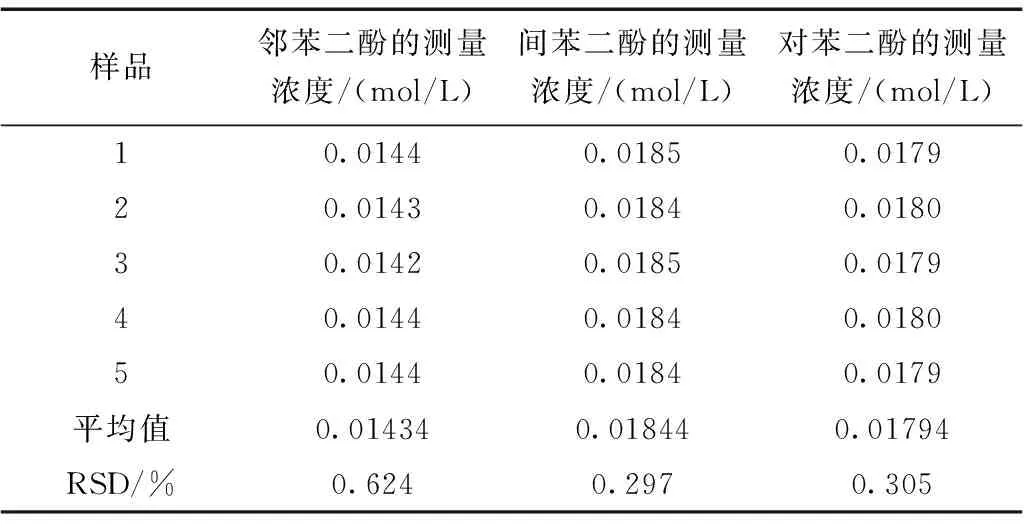
表3 重复性实验结果
精密吸取70 μL邻苯二酚、90 μL间苯二酚和90 μL对苯二酚标准溶液加入250 μL D2O和外标物于NMR管中,平行配制5份样品,测定其重复性。测定结果见表3,实验结果表明,该方法的重复性良好。
2.7精密度的测定
精密吸取70 μL邻苯二酚、90 μL间苯二酚和90 μL对苯二酚标准溶液加入250 μLD2O和外标物于NMR管中,在同一天平行测定5次。测定结果见表4,实验结果表明,仪器的精密度良好。
2.8稳定性的测定
经过测定得知,配制的标准溶液在12小时内的基本保持稳定。测定结果见表5。
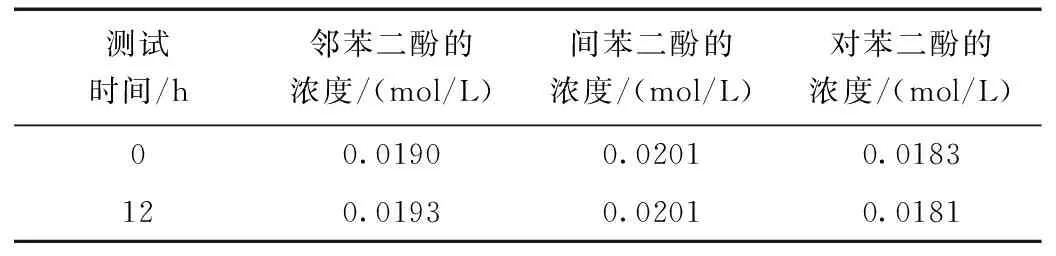
表5 稳定性实验结果
按照上述方法进行实验,结果表明该方法具有简单快速、重现性好、精密度高、稳定性好等特点。
3 结 论
实验结果表明,采用核磁共振波谱法同时测量溶液中邻、间、对苯二酚的含量,线性关系、重现性、回收率、精密度和稳定性均保持良好。此方法具有高效、简便、无需对照品等优点,结构分析和含量测定可以同时进行,可用运到其他异构体的分析测定。而且,此方法不需要纯品做参比标准,选择合适的溶剂和外标物,即可根据目标特征峰的积分强度完成定量分析,对此类结构简单、组分不复发的异构体混合物的定性定量分析具有重要的意义。但是,核磁共振波谱法不适合复杂组分的样品分析,因在分析复杂组分时信号峰容易重叠,影响定量定性分析结果。因此,核磁共振波谱法在对复杂组分的定量分析中还需要进一步的研究和发展。
[1]梁彦秋,孙小寒,冯婧微,等.间苯二酚与牛血清白蛋白的作用机理[J].分析试验室,2010,29(6):81-84.
[2]王俊君,俞从正,赵卫锋,等.邻苯二酚对厌氧微生物的毒性作用[J].皮革与化工,2009,26(1):5-9.
[3]雷忻,洪杰,王文强.间苯二酚与邻苯二酚对泥鳅血清卵黄蛋白原的诱导作用[J].四川动物,2013,32(4):563-566.
[4]殷程鹏,丁欣宇,施磊.邻苯二酚和对苯二酚的气相色谱法分析[J].化工环保,2004,24(S1):384-386.
[5]纪晓红,张莉,邱娟.高效液相色谱法测定间苯二酚反应液中间苯二酚的含量[J].化学分析计量,2010,19(4):69-70.
[6]吴根华,何池洋,陈荣.人工神经网络用于荧光分析法同时测定苯酚和间苯二酚的含量[J].光谱学与光谱分析,2002,22(5):813-815.
[7]谢成根,吴伟,刘小兰.双体系双波长荧光分析法同时测定废水中的间苯二酚和对苯二酚[J].冶金分析,2008,28(2):19-22.
[8]杨继东,张书然,刘绍璞.同步一偏振一导数荧光法同时测定三种苯二酚异构体的研究[J].化学学报,2007,65(20):2309-2314.
[9]吴永军.聚苯胺薄膜修饰电极对邻苯二酚和对苯二酚测定的研究[J].廊坊师范学院学报,2010,10(2):69-73.
[10]孙进高,王广凤,焦守峰,等.纳米La(OH)3修饰电极对邻苯二酚和对苯二酚的同时测定[J].分析化学,2007,35(3):335-339.
[11]黄挺,张伟,全灿,等.定量核磁共振法研究进展[J].化学试剂,2012,34(4):327-332.
[12]张友杰,刘小鹏.药物核磁共振定量分析参数的研究[J].波普学杂志,2007,24(3):289-294.
[13]孙静霞,张正行.NMR在药物定量分析中的应用[J].药物分析杂志,2005,25(1):117-122.
[14]M.Malet-Martino,U.Holzgrabe.NMR techniques in biomedical and pharmaceutical analysis[J].Journal of Pharmaceutical and Biomedical Analysis, 2011,55:1-15.
[15]Erik J.Saude,Carolyn M.Slupsky,and Brian D.Sykes.Optimization of biological fluids for Quantitative accuracy.[J]. Metabolomics,2006,2(3):113-123.
[16]罗虹,朱凤润,金燕.NMR法测定复方制剂3组分的相对含量[J].光谱实验室,2003,20(2):193-195.
[17]阎政礼,杨明生,李添宝,等.蜂蜜中葡糖糖、果糖和蔗糖NMR定量分析研究[J].食品科学2009,30(14):253-255.
[18]Ulrike Holzgrabe.Quantitative NMR spectroscopy in pharmaceutical applications[J].Progress in Nuclear Magnetic Resonance Spectroscopy,2010,57:229-240.
[19]U. Holzgrabe, R. Deubner, C. Schollmayer, B. Waibel.Quantitative NMR spectroscopy—Applications in drug analysis[J].Journal of Pharmaceutical and Biomedical Analysis,2005,38: 806-812.
Simultaneous NMR Determination of Dihydroxybenzene Isomers*
ZHAODan,Aotegenbayaer
(College of Science, Inner Mongolia Agricultural University, Inner Mogolia Huhhot 010018, China)
Base on quantitative nuclear magnetic resonance technology, taking ammonium formate as external standard, a method to determination of dihydroxybenzene isomers was established.The results of Catechol,Resorcinol,Hydroquinone had the good linearity in linear range. The linear regression equations were as follows:y=-0.00315+40.38201x,r=0.99996,y=0.00254+39.96878x,r=0.99998, y=2.51044E-4+80.31374x,r=0.99992.The recovery rates were as follows: 100.39%, 100.96%, 100.09%.This method is less sampling, direct quantitative, high sensitivity,simple,reproducible,and can simultaneous determine the contents of these three substances in solution.This method can be used for the quantitative determination of dihydroxybenzene isomers.
NMR; Catechol; Resorcinol; Hydroquinone; external standard method;assaying
国家自然科学基金项目(21462030);内蒙古高校研究项目(NJZY051)。
赵丹(1991-),女,硕士研究生,主要从事仪器分析方面的研究。
敖特根巴雅尔(1960-),男,教授。
O657.61
A
1001-9677(2016)05-0140-04
