扶正化瘀胶囊的TLC鉴别和丹酚酸B含量测定方法研究
2016-07-26潘一峰李庆喆涂驭斌
潘一峰+李庆喆+涂驭斌
摘 要 目的:完善扶正化瘀胶囊的质量标准。方法:建立了其主要组分丹参、桃仁和五味子的薄层层析鉴别方法;采用反相液相色谱法(RP-HPLC),在C18色谱柱上,以甲醇-乙腈-水-甲酸(30:10:59:1)为流动相,检测波长286 nm,测定了丹酚酸B的含量。结果:薄层图谱斑点清晰,空白对照无干扰。丹酚酸B在4.83~145.05 μg/ml范围内有较好的线性关系。平均回收率(n=9)为99.33%,RSD为1.76%。结论:本方法操作简便、快速,结果可靠,重复性好,可作为该产品的质量控制方法。
关键词 扶正化瘀胶囊 薄层层析 反相液相色谱 丹酚酸B
中图分类号:TQ460.72 文献标识码:A 文章编号:1006-1533(2016)13-0029-04
Study on the methods for the TLC identification and the content determination of salvianolic acid B and other components in Fuzheng Huayu capsules
PAN Yifeng*, LI Qingzhe, TU Yubin(Shanghai Huanghai Pharmaceutical Co. LTD., Shanghai 200942, China)
ABSTRACT Objective: To improve the quality standard for Fuzheng Huayu capsules. Methods: Salviae miltiorrhizaea, Persicae semen, Schisandrae chinensis fructus in these capsules were identified by TLC. The contents of salvianolic acid B were determined by RP-HPLC on a C18 column with a mobile phase of methanol-acetonitrile-water-formic acid (30:10:59:1) at wavelength of 286 nm. Results: The spots on TLC were clear and accurate. The standard curve of salvianolic acid B was linear over the range of 4.83~145.05 μg/ml with an average recovery of 99.33% (RSD 1.76%). Conclusion: The methods are convenient, reliable and accurate for the quality control of Fuzheng Huayu capsules.
KEY WORDS Fuzheng Huayu capsules; TLC; RP-HPLC; salvianolic acid B
扶正化瘀胶囊是上海中医药大学王玉润教授、刘平教授和肝病研究所在几十年临床实践基础上研制的抗肝纤维化药,具有活血祛瘀,益精养肝功能。主要用于乙型肝炎肝纤维化属“瘀血阻络,肝肾不足”证者,症见胁下痞块,胁肋疼痛,面色晦暗,或见赤缕红斑,腰膝酸软,疲倦乏力,头晕目涩,舌质暗红或有瘀斑,苔薄或微黄,脉弦细。扶正化瘀胶囊由丹参、桃仁、绞股蓝、五味子、松花粉、发酵虫草菌粉六味药组成,于2002年8月获批新药证书,其质量标准于2005年转为正式标准[WS3-459( Z-79)-2005( Z) ][1]。但是,该标准欠完善,鉴别项目中缺少五味子、桃仁等药味的鉴别。另外,该标准中用原儿茶醛作为丹参的鉴别,以丹参素钠作为丹参的含量测定,而近年的研究发现丹酚酸B 作为丹参中含量最高的水溶性活性酚酸类化合物,被普遍认为是丹参发挥疗效作用的主要物质之一, 其对肝脏抗纤维化有较好的疗效,药理药效的研究报道也很多[2-6];同时,经体内试验研究表明,丹酚酸B也是扶正化瘀胶囊入血成分之一[7]。目前中国药典中典型的丹参制剂品种有丹参片、复方丹参片、复方丹参滴丸、丹参注射液等,鉴于原鉴别标准中测定的原儿茶醛、丹参素钠则可能是丹酚酸B的降解产物[8],因此我们变更以丹酚酸B作为丹参鉴别和含量测定的依据。
根据上述原因,以中国药典相关研究试验方法为参考依据,我们建立了丹参、桃仁、五味子的薄层鉴别方法和丹酚酸B的含量测定方法,以便有助于提高该产品的质量控制标准。
1 材料和方法
1.1 材料
扶正化瘀胶囊(上海黄海制药有限责任公司),阴性对照样品为自制。对照药材和对照品均为中国药品生物制品检定所提供,批号如下:丹酚酸B对照品(含量测定用,批号:111562-200504); 丹参对照药材120923-200610;丹酚酸B对照品111562-201111;苦杏仁苷对照品110820-200403;五味子甲素对照品110764-200408;五味子对照药材120922-200606。
硅胶G薄层板和硅胶GF254薄层板、流动相所用甲醇、乙腈(色谱纯)均购自美国Merck公司;甲酸为色谱纯(96%,美国Tedia公司);其它试剂均为分析纯。
1.2 仪器
高效液相色谱仪(Agilent 1200,Agilent公司),超声波清洗器(SK7200LHC,上海科导超声仪器有限公司),电子天平(XP-105,梅特勒-托利多);色谱柱:Agilent Zorbax SB-C18(4.6 mm×250 mm,5 μm)。
1.3 TLC鉴别
1)丹参 取扶正化瘀胶囊内容物2 g,加水50 ml,加盐酸0.1 ml,超声处理30 min,滤过,滤液用乙酸乙酯振摇提取2次,每次30 ml,合并乙酸乙酯液,蒸干,残渣加无水乙醇1 ml使溶解,作供试品溶液。另取丹参对照药材1 g,同法制备,作为对照药材溶液。再取丹酚酸B对照品,加甲醇制成0.5 mg/ml溶液,作为对照品溶液。照薄层色谱法试验[9],吸取上述二种溶液各3 μl,分别点于同一硅胶G薄层板上,以甲苯-氯仿-乙酸乙酯-甲醇-甲酸(2:3:4:0.5:2)为展开剂,展层后取出,晾干,以含2%三氯化铁的乙醇溶液喷雾,在105 ℃加热至斑点显色清晰[10]。
2)五味子 取扶正化瘀胶囊内容物5 g,加氯仿20 ml,水浴回流30 min,滤过,滤液蒸干,残渣加甲醇1 ml使溶解,作为供试品溶液。另取五味子对照药材2 g,同法制成对照药材溶液。再取五味子甲素对照品,加甲醇制成1 mg/ml的溶液,作为对照品溶液。照薄层色谱法试验[9],吸取上述二种溶液各5 μl,分别点于同一硅胶GF254薄层板上,以石油醚(30~60 ℃)-甲酸乙酯-甲酸(15∶5∶1)的上层溶液为展开剂,展层后取出,晾干,置紫外灯(254 nm)下检视[10]66。
3)桃仁 取扶正化瘀胶囊内容物5 g,加甲醇30 ml,超声处理30 min,滤过,滤液蒸干,残渣加水3 ml溶解,加于D101型大孔吸附树脂柱吸附(内径1.5 cm,柱高12 cm),以水30 ml洗脱,弃去水液,再用20%乙醇30 ml洗脱,收集洗脱液,蒸干(75~85 ℃),残渣加甲醇1 ml溶解,作为供试品溶液。另取桃仁药材2 g,同法制成药材溶液。再取苦杏仁苷对照品,加甲醇制成2 mg/ml的溶液,作为对照品溶液。照薄层色谱法试验[9],吸取上述两种溶液各5 μl,分别点于同一硅胶G薄层板上,以氯仿-甲醇-水(65∶40∶10)的下层溶液为展开剂,展层后取出,晾干,以含10%硫酸的乙醇溶液喷雾,在105 ℃加热至斑点显色清晰[10]277。
4)阴性样品制备 6味药材(丹参、五味子、桃仁、绞股蓝、松花粉、发酵虫草菌粉)分别缺丹参、五味子或桃仁,按扶正化瘀胶囊提取工艺进行提取,将提取物与辅料配制成的扶正化瘀胶囊阴性样品,按照供试品溶液的制备方法制备,分别用作丹参、五味子或桃仁的阴性对照。
1.4 丹酚酸B含量测定
1.4.1 RP-HPLC测定丹酚酸B
流动相:甲醇-乙腈-水-甲酸=30:10:59:1,流速:1 ml/min,柱温:30 ℃,进样量:10 μl,检测波长286 nm,进行RP-HPLC测定。
1.4.2 溶液制备
1)对照品母液 取丹酚酸B对照品适量,精密称定,加纯水制成每1 ml含193.40 μg/ml。对照品母液依次稀释成不同浓度的对照品溶液,含量(μg/ml)分别为:4.83、9.67、19.34、38.68、58.02、77.36、96.70、145.05。
2)供试品溶液 取扶正化瘀胶囊内容物适量,研细,取约0.1 g,精密称定,置25 ml容量瓶中,加入水约20 ml,超声处理 (功率350 W,频率50 kHz) 20 min,放冷,加水至刻度,摇匀,滤过,取续滤液,即得。
3)空白对照 取五味药材桃仁、五味子、绞股蓝、松花粉、发酵虫草菌粉,按扶正化瘀胶囊提取工艺进行提取,将提取物与辅料配制成的扶正化瘀胶囊空白样品0.1 g,按照供试品溶液的制备方法制备。
1.4.3 提取时间的确定
精密称定本品研细后的粉末约0.1 g,按上述供试品溶液的制备方法制备。分别超声处理10、20、30、40 min,测定丹酚酸B峰面积。据计算,峰面积与称样量的比值(A/m)分别为4.478、4.531、4.533、4.531, 其中,超声10 min的A/m相对其它时间较小,而超声20、30、40 min的A/m相互间较接近,故超声时间定为20 min。
1.4.4 重复性试验
取本品,按照供试品溶液的制备方法制备供试液,按含量测定方法分别测定6次。
1.4.5 精密度试验
取上述重复性试验的一个样品,连续进样测定6次,通过峰面积计算精密度。
1.4.6 准确度试验
加样回收试验:精密称取已测定丹酚酸B含量的供试品(批号:110101,规格:0.3 g)9份,每份约0.1 g,精密加入高、中、低浓度的丹酚酸B对照品溶液,按照上述供试品溶液制备方法制备和测定,每个浓度测定3次。
1.4.7 稳定性考察
取本品,按照供试品制备项下的制备方法制成供试品溶液,分别在室温放置0、1、2、4、8、12 h进样,测定峰面积,考察供试品溶液在12 h内的稳定性。
1.4.8 检测限和定量限
分别按信噪比(S/N)等于3和10时,将相应浓度的样品注入液相色谱仪,确定样品的检测限和定量限。
2 结果
2.1 3种样品的TLC鉴别
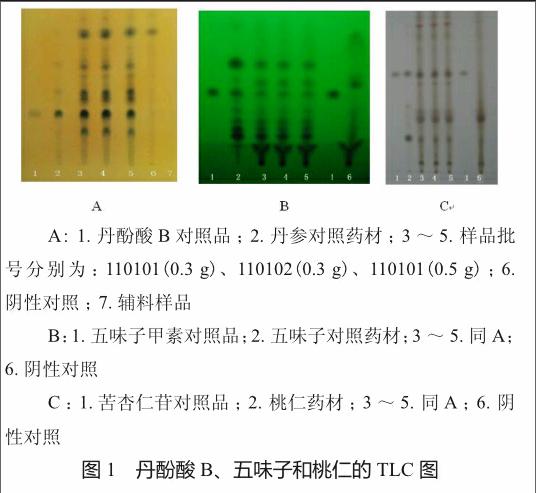
丹酚酸B、五味子和桃仁的供试品和对照品在TLC的相应的位置上均显示相同颜色的斑点。专属性试验表明,不含这3种样品的阴性对照无干扰(图1)。
2.2 丹酚酸B含量测定
2.2.1 专属性试验
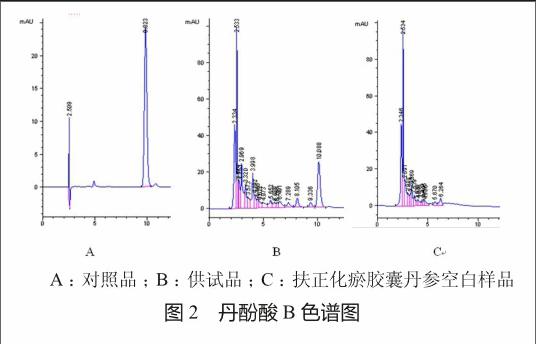
供试品和丹酚酸B对照品的RP-HPLC保留时间相同,丹酚酸B与其他成分的色谱峰分离良好,而空白对照在丹酚酸B的保留时间处无色谱峰出现(图2) 。

2.2.2 线性关系的考察
以丹酚酸B(μg/ml)为横坐标,色谱峰峰面积为纵坐标,绘制标准曲线得回归方程为Y= 10.64X-11.57,相关系数r= 0.999 96,表明丹酚酸B在4.83~145.05 μg/ml范围内有较好的线性关系,可作为该产品质量控制的含量测定方法。
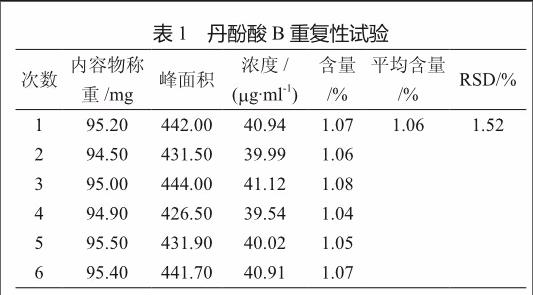
2.2.3 重复性试验
重复性试验的结果表明,RP-HPLC测定本品中丹酚酸B含量的重复性良好,RSD%为1.52%(<2%)(表1)。
2.2.4 精密度试验
精密度试验结果表明RP-HPLC测定丹酚酸B的精密度较好,RSD%为0.17%(<2%)(表2)。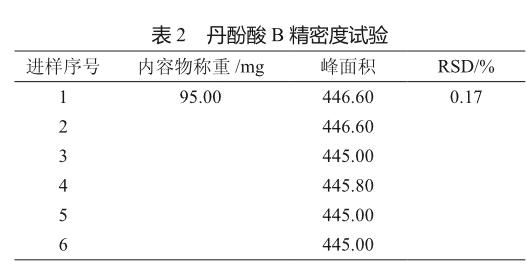
2.2.5 稳定性考察
分别在室温放置0、1、2、4、8、12 h时进样,测得的峰面积分别为465.3、467.1、470.8、465.6、467.1和465.0,RSD%为0.46%(<2%),表明供试品溶液在12 h内稳定。
2.2.6 准确度试验
加样回收试验结果表明,RP-HPLC测定本品中丹酚酸B回收率在95%~102%范围内,平均回收率99.33%,符合《中国药典》2015年版四部指导原则9101的要求[9]374。
2.2.7 检测限和定量限
分别按信噪比(S/N)等于3和10及进样量10 μl时,确定样品的检测限和定量限分别为0.5 μg/ml和1.5 μg/ml。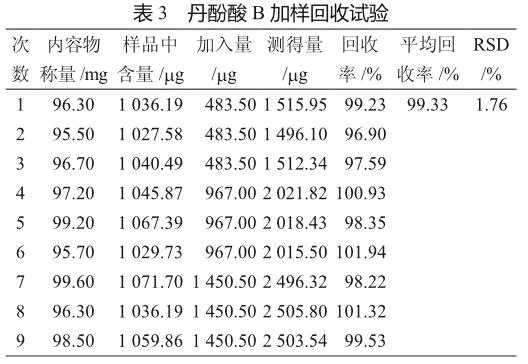
3 讨论
原质量标准对丹参中原儿茶醛进行鉴别,而原儿茶醛是丹酚酸B的降解产物,因此考虑以丹酚酸B作为对照进行鉴别[7]。薄层鉴别方法的展开剂参考了《中国药典》2015版一部中丹参鉴别方法[10]。该方法操作简便,干扰小,稳定,重现性较好。
五味子以果实和种子入药,有效成分为木脂素类化合物[11],参照《中国药典》2015版一部中五味子药材的鉴别[10]66,以五味子甲素为对照品。药典方法中供试品用氯仿溶解,分离效果和重复性较差。最后改用甲醇溶解供试品后点样,操作简便,干扰小,分离效果和重复性都好。
桃仁中化学成分有苷类(如苦杏仁苷、野樱苷等),脂质、糖类、蛋白质、氨基酸、苦杏仁酶、尿囊索酶,精油等,其中苦杏仁苷为主要药效成分[12-13],参考其它文献[14-15]在实验过程中对供试品的处理,用石油醚、乙醚对样品粉末进行脱脂;正丁醇、乙酸乙酯对样品液进行萃取;但TLC显示溶剂拖尾严重、杂质较多,仍无法有效分离,显色剂显色后无法准确判断结果。最后用大孔吸附树脂对供试品溶液进行纯化,并考查了不同乙醇浓度的洗脱液中目标成分的含量,最后采用20%乙醇洗脱,硅胶G薄层板展开,以氯仿-甲醇-水(65∶40∶10)的下层溶液为展开剂,含10%硫酸的乙醇溶液加热显色的条件最优。
我们统计了28批规格为0.3 g和23批规格为0.5 g扶正化瘀胶囊的丹酚酸B含量数据,另外考虑到丹酚酸B在贮存中可能会氧化或分解,从而含量会有一定的降低,因此我们认为扶正化瘀胶囊质量标准中含量测定项下的含量限度应暂定为每粒胶囊含丹酚酸B不得少于2.10 mg(每粒装0.3 g)或不得少于3.50 mg(每粒装0.5 g)较为合适。
参考文献
[1] 国家药典委会. 国家药品标准(新药转正标准)第68册[S]. 国家食品药品监督管理局, 2008: 46-49.
[2] 李雪梅, 李红山, 胡义杨. 中药有效组分抗肝纤维化研究进展[J]. 中西医结合肝病杂志, 2008, 18(3): 186-189.
[3] 胡义杨. 中医药抗肝纤维化的研究[J]. 实用临床医药杂志, 2005, 9(7): 18-22.
[4] 王蓉, 原永芳. 丹酚酸B药理作用的研究概况[J]. 中医药导报, 2011, 17(4): 130-132.
[5] 李认书, 李永强. 丹酚酸的研究进展[J]. 时珍国医国药, 2003, 14(6): 371-373.
[6] 朱金墙, 闫晨, 康立源. 丹酚酸B的稳定性及其降解机理研究进展[J]. 中国中医信息杂志, 2010, 17(12): 113-115.
[7] Yang T, Liu S, Wang CH, et al. Comparative pharmacokinetic and tissue distribution profiles of four major bioactive components in normal and hepatic fibrosis rats after oral administration of Fuzheng Huayu recipe[J]. Pharm Biomed Anal, 2015, 114: 152-158.
[8] 徐德然, 王康才, 王峥涛, 等. 丹参中丹参素、原儿茶醛来源的初步研究[J]. 中国天然药物, 2005, 3(3): 148-150.
[9] 国家药典委员会. 中华人民共和国药典(2015年版) 四部[M]. 北京: 中国医药科技出版社, 2015: 57-58.
[10] 国家药典委员会. 中华人民共和国药典(2015年版) 一部[M]. 北京: 中国医药科技出版社, 2015: 76.
[11] 仰榴青, 吴向阳, 徐佐旗, 等. 五味子及其制剂中木脂素类成分含量测定的研究进展[J]. 中国中药杂志, 2005, 30(9): 650-653.
[12] 许筱凰, 李婷, 王一涛, 等. 桃仁的研究进展[J]. 中草药, 2015, 46(17): 2649-2655.
[13] 王仁芳, 范令刚, 高文远, 等. 桃仁化学成分与药理活性研究进展[J]. 现代药物与临床, 2010, 25(6): 426-429.
[14] 张明光, 孙振瑜, 云青, 等. 小儿咳喘灵冲剂薄层鉴别方法的研究[J]. 内蒙古医学杂志, 2004, 36(11): 902~903.
[15] 王凌, 陈逸红. 黄英咳喘糖浆质量标准研究[J]. 上海中医药大学学报, 2005, 19(4): 54-56, F0003.
