超高效液相色谱法测定注射用头孢替唑钠的有关物质
2016-07-25张红霞
李 智,张红霞,杨 倩
(1.天津市药品检验所,天津 300070;2.武警后勤学院附属医院,天津 300162)
药品质量与检验
超高效液相色谱法测定注射用头孢替唑钠的有关物质
李 智1,张红霞2,杨 倩1
(1.天津市药品检验所,天津 300070;2.武警后勤学院附属医院,天津 300162)
目的:建立超高效液相色谱梯度洗脱法测定注射用头孢替唑钠中的有关物质。方法:采用Waters Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm)色谱柱,以枸橼酸溶液(取枸橼酸3 g加水溶解并稀释至900 ml)-乙腈(90∶10)为流动相A,乙腈为流动相B,线性梯度洗脱;流速:0.3 ml/min;检测波长:254 nm。结果:在0.19~47.08 μg/ml浓度范围内,头孢替唑峰面积与浓度呈良好的线性关系(r=1.000 0)。结论:本法简便快速、专属性强,可作为测定注射用头孢替唑钠有关物质的有效方法。
注射用头孢替唑钠,超高压液相色谱,梯度洗脱,有关物质
头孢替唑钠为半合成的第一代头孢菌素,具广谱抗菌作用,通过抑制细菌细胞壁粘肽的生物合成而达到杀菌作用。头孢替唑钠最先由日本藤泽药品工业株式会社开发;1995年韩国新丰制药株式会社获得进口药品注册证,获准进口;国内首仿企业为哈药集团制药总厂。注射用头孢替唑钠为头孢替唑钠无菌原料直接分装。本品较少发生严重不良反应,不良反应中以过敏反应最常见[1]。
头孢替唑钠和注射用头孢替唑钠收载于《中国药典》2015年版[2]和《日本药局方抗菌性物质医药品手册》2000年版[3]。《中国药典》2015年版及其他现行标准中有关物质检查均采用HPLC法,C18色谱柱,枸橼酸溶液-乙腈(90∶10)为流动相,由于有机相比例较低,等度洗脱很难在短时间内将极性小的杂质冲出色谱柱;此外,本品有关物质含量较少,《中国药典》规定最大单一杂质和总杂质的限度分别为1.0%和1.5%。综上,本实验建立了灵敏度更高、分离效能更好的UPLC梯度洗脱法测定注射用头孢替唑钠中的有关物质,以更好地控制药品的质量,拓展新技术在药物分析方面的应用,并为下一步采用柱切换二维超高效液相色谱质谱联用法研究头孢替唑钠的杂质谱打下基础。
1 仪器与试药
Waters ACQUITY UPLC液相系统,Empower 3色谱工作站(美国沃特世公司),Mettler Toledo XS 205型电子分析天平(瑞士梅特勒公司)。头孢替唑对照品(中国药品生物制品检定研究院,批号130510-200301,纯度90.0%);注射用头孢替唑钠[国内抽样样品,共7批,涉及7家生产企业(1~7)];枸橼酸为分析纯,乙腈为色谱纯,水为纯化水。
2 方法与结果
2.1 色谱条件 色谱柱:Waters Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm);以枸橼酸溶液(取枸橼酸 3 g加水溶解并稀释至 900 ml)-乙腈(90∶10)为流动相A,乙腈为流动相B,按表1进行线性梯度洗脱;流速:0.3 ml/min;柱温40℃;检测波长: 254 nm;进样量2 μl。
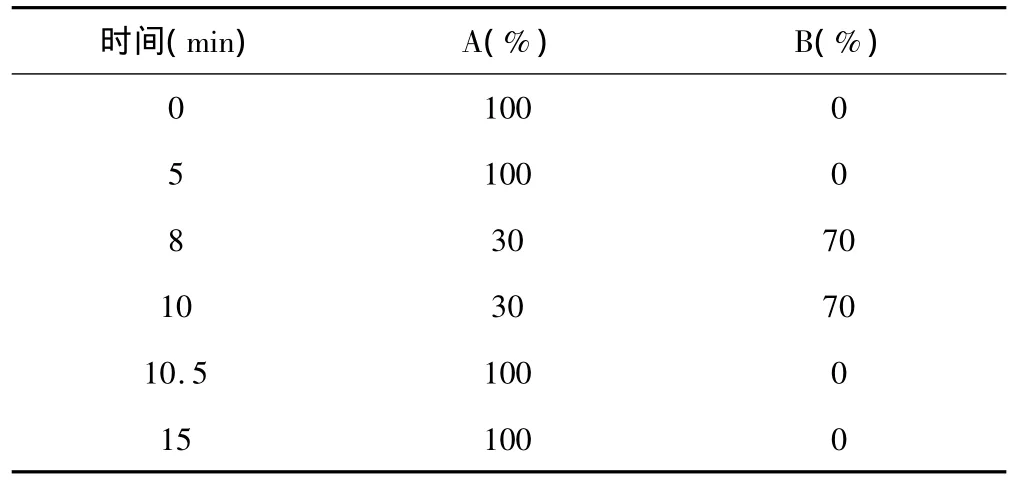
表1 梯度洗脱程序
2.2 溶液的制备
2.2.1 供试品溶液 取本品约25 mg,精密称定,置25 ml量瓶中,加水溶解并稀释至刻度,摇匀,即得。
2.2.2 对照溶液 精密量取供试品溶液1 ml,置100 ml量瓶,用水稀释至刻度,摇匀,即得。
2.2.3 系统适用性试验溶液 取头孢替唑对照品约25 mg,置25 ml量瓶中,加0.1 mol/L氢氧化钠溶液1 ml,放置1 min,加水10 ml,再加0.1 mol/L盐酸溶液1 ml中和,用水稀释至刻度,摇匀,即得系统适用性对照溶液,以溶剂作为空白溶液。分别取系统适用性对照溶液、供试品溶液和空白溶液,按“2.1”项下色谱条件进样分析。色谱图见图1。
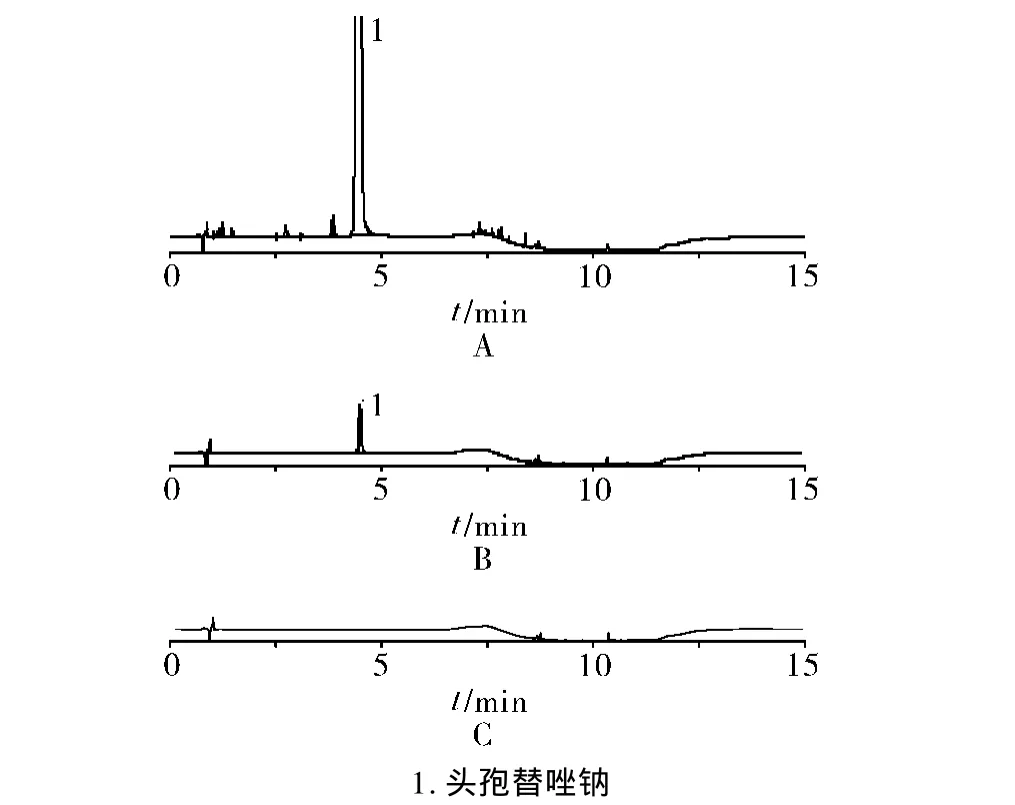
图1 供试品(A)对照品(B)空白(C)UPLC色谱图
2.3 专属性考查试验
2.3.1 酸破坏试验 取本品约10 mg,置具塞试管中,加0.1 mol/L的盐酸溶液1 ml,水浴加热15 min后,加0.1 mol/L的氢氧化钠溶液1 ml和水8 ml,摇匀,按“2.1”项下色谱条件测定,同时随行空白试验。
2.3.2 碱破坏试验 取本品约10 mg,置具塞试管中,加0.1 mol/L的氢氧化钠溶液1 ml,室温放置1 min后,加0.1 mol/L的盐酸溶液1 ml和水8 ml,摇匀,按“2.1”项下色谱条件测定,同时随行空白实验。
2.3.3 氧化破坏试验 取本品约10 mg,置具塞试管中,加30%的过氧化氢溶液1 ml,室温放置1 min后,加水9 ml,摇匀,按“2.1”项下色谱条件测定,同时随行空白试验。
2.3.4 加热破坏试验 取本品约10 mg,置具塞试管中,加水10 ml溶解,摇匀,置水浴加热0.5 h后,放置至室温,按“2.1”项下色谱条件测定。
2.3.5 光照破坏试验 取本品约10 mg,置称量瓶中,加水10 ml溶解,摇匀,置254 nm紫外灯下光照0.5 h后,按“2.1”项下色谱条件测定。专属性试验色谱图见图2,该色谱条件下,头孢替唑的降解产物均能与主峰较好分离,方法专属性良好。
2.4 线性关系考查 取头孢替唑对照品约50 mg,精密称定,置50 ml量瓶中,加溶剂溶解并稀释至刻度,摇匀,作储备液。再分别精密量取储备液适量,用溶剂定量稀释制成浓度为0.2、0.5、1.0、2.0、5.0、10、20和50 μg/ml的溶液,按“2.1”项下色谱条件测定。结果表明,在0.19~47.08 μg/ml浓度范围内,头孢替唑峰面积与浓度呈良好的线性关系,线性方程为 Y= 8 138.9 X-242.4(r=1.000 0)。
2.5 检测限与定量限 精密量取线性关系考查中的溶液适量用水稀释至一定浓度,测定头孢替唑的最小检出限(按S/N=3计算),得到最小检出浓度为0.028 μg/ml,最低定量浓度为0.085 μg/ml。
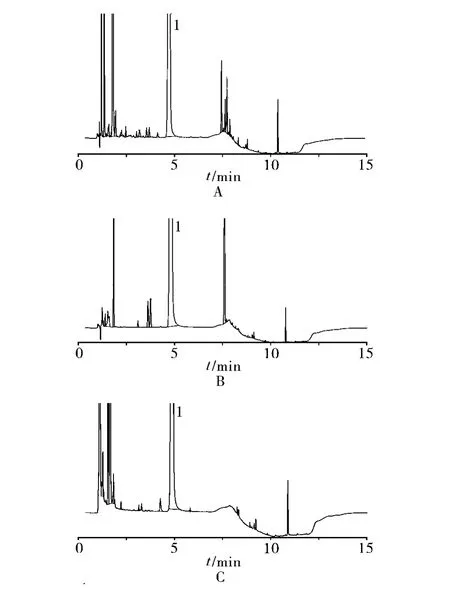
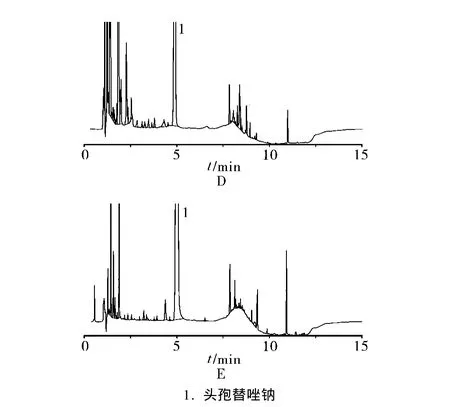
图2 酸破坏(A)碱破坏(B)氧化破坏(C)加热破坏(D)光照破坏(E)色谱图
2.6 精密度试验 取注射用头孢替唑钠样品(生产企业1,批号A1502211-2),称取6份,按“2.1”项下色谱条件测定,计算得最大单一杂质和总杂质测定结果的RSD分别为1.4%和1.1%。
2.7 溶液的稳定性试验 因本品的贮藏条件凉暗干燥处且β-内酰胺类抗生素大多不稳定,故取供试品溶液(生产企业1,批号A1502211-2),分别于4℃条件下放置0、1、2、4、6、8和12 h后进样测试。结果表明,主峰面积的RSD为0.15%,总杂质峰面积的RSD为1.1%,杂质个数未见增加,即供试品溶液于4℃放置12 h基本稳定。
2.8 样品中有关物质的测定 取注射用头孢替唑钠样品7批,按“2.2.1”项下方法操作,按“2.1”项下色谱条件测定。供试品特征色谱图见图3,测定结果见表2。
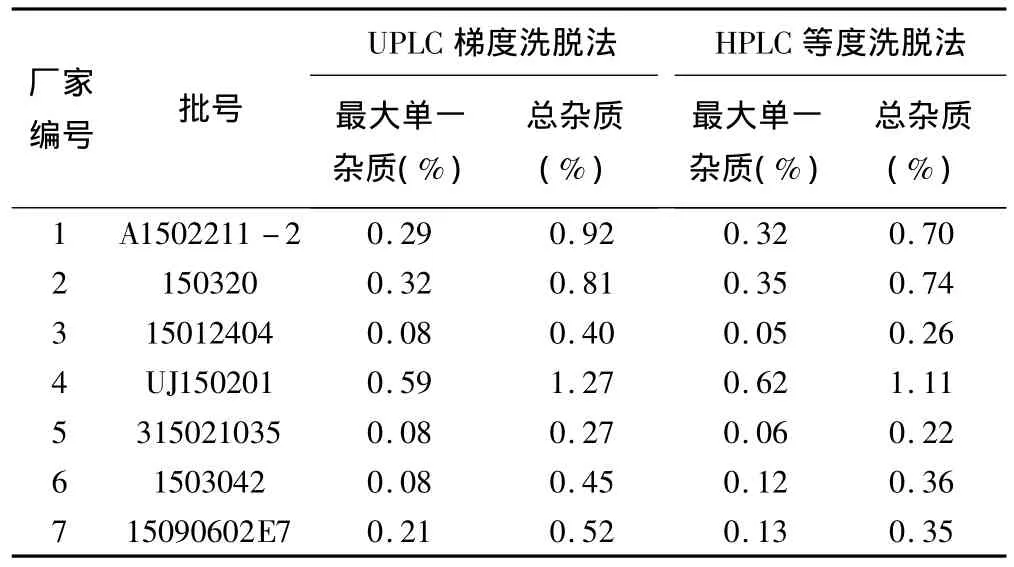
表2 有关物质测定结果
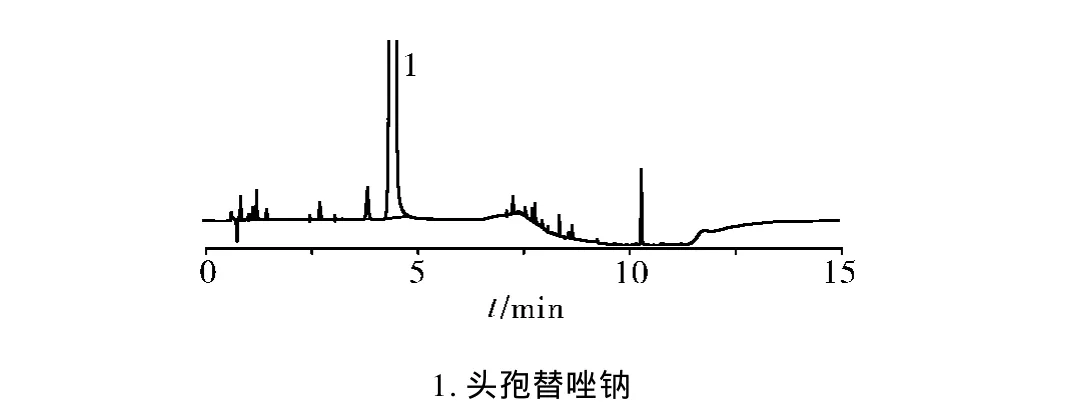
图3 供试品溶液UPLC色谱图
3 讨论
3.1 色谱条件的选择 本法沿用了现行注射用头孢替唑钠标准中有关物质检查所用的枸橼酸溶液-乙腈系统,建立了梯度洗脱方法。此方法与等度洗脱法比较,分析时间明显缩短,分离杂质的能力更强,检出杂质的数量更多,特别是主峰后极性较小杂质的有效检出,明显优于等度洗脱法,见表2、图3和图4。本法快速、灵敏、专属性好,适用于注射头孢替唑钠有关物质的检测。
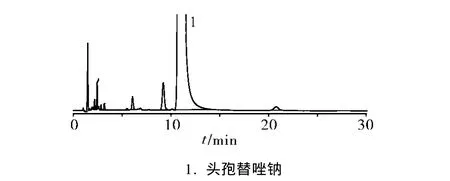
图4 等度洗脱法测定供试品溶液HPLC色谱图
3.2 杂质谱分析 本文所建立的方法可实现杂质的有效分离,经比较,不同厂家生产的注射用头孢替唑钠的杂质谱存在明显差异,杂质谱的差异往往与药品的生产工艺密切相关,同时受到贮藏条件等因素的影响。考虑到UPLC在线柱切换液质联用技术可以适用于流动相中添加了非挥发性盐类的情况,且UPLC较HPLC具有更高的灵敏度,更好的分辨率及更小的柱前死体积[4,5]。因此,本文所建立的方法为下一步采用超高效液相色谱在线柱切换质谱联用技术研究本品杂质的结构研究打下基础。
1 国家药典委员会.中华人民共和国国家药典临床用药须知化学药和生物制品卷(2010年版)[M],北京:中国医药科技出版社,2011:649
2 中国药典[S].二部.2015:290-291
3 日本药局方抗菌性物质医药品手册.2000:Ⅱ78
4 杨亚莉,杨剑宁,胡敏,等.HPLC法分析可利霉素的组分[J].药学学报,2009,44(10):1183-1186
5 杨倩,李伟,曹晓云,等.注射用头孢唑肟钠的杂质谱研究[J].中国药学杂志,2014,49(19):1750-1754
Determination of related substances in ceftezole sodium for injection by UPLC
Li Zhi,Yang Qian
(Tianjin Institute for Drug Control,Tianjin 30070)
Objective:To develop a UPLC method for determination of the related substances in Ceftezole Sodium for Injection.Methods:Waters Acquity UPLC BEH C18column(2.1 mm ×100 mm,1.7 μm)was adopted.Citric acid solution(3 g of citric acid in 900 ml of water)-acetonitrile(90∶10)was used as mobile phase A,and acetonitrile as mobile phase B.Gradient elution was applied.The flow rate was 0.3 ml/min.The detection wave length was at 254 nm.Results:The linear range of ceftezole sodium was between 0.19 μg/ml and 47.08 μg/ml(r=1.000 0).This method manifested fine repeatability,specificity and good stability of the test solution.Conclusion:This method is convenient,quick,specific and suitable for determination of the related substances of Ceftezole Sodium for Injection.
ceftezole sodium for injection,UPLC,gradient elution,related substances
R927.2
A
1006-5687(2016)03-0001-03
2016-02-17
