光致氯生水合电子降解二甲基亚硝胺的研究*
2016-07-18邢露张超杰周琪
邢露 张超杰 周琪
(同济大学环境科学与工程学院 上海200092)
光致氯生水合电子降解二甲基亚硝胺的研究*
邢露张超杰周琪
(同济大学环境科学与工程学院上海200092)
摘要采用紫外光致水合电子这一新型技术降解水中的痕量NDMA,初步研究了紫外光致水合电子对NDMA的降解效能,重点考察了NDMA的一级分解产物DMA、亚硝酸盐及硝酸盐进一步的降解情况,并与紫外直接光解进行比较。结果表明,与紫外直接光解相比,紫外光致水合电子不仅能加快NDMA本身的降解速率,还能有效地促使NDMA的分解产物进一步降解,从而达到控制NDMA的再生、降低水的化学风险的目的。这项研究对于彻底消除水中的二甲基亚硝胺污染具有一定的理论指导意义。
关键词二甲基亚硝胺水合电子降解NaCl
0引言
N-二甲基亚硝胺(N-Nitrosodimethylamine,NDMA)作为饮用水中一种潜在的致癌物质,越来越受到人们的关注。经过研究发现,相比于反渗透、吸附、高级氧化法等去除NDMA的常规方法,紫外辐射是一种较为经济、有效的方法,这主要跟NDMA的感光性质有关。但紫外辐射法也存在着严重的不足:NDMA在UV的照射下分解的产物主要为二甲胺(DMA)和亚硝酸盐(DMA和亚硝酸盐同时也是NDMA的前质物),而UV无法降解这两种物质,所以在后续的加氯消毒处理过程中,DMA和亚硝酸盐会再次结合,重新生成NDMA。
水合电子作为一种很强的还原剂(氧化还原电位为2.77 V),已经被广泛应用于各个领域。在前期UV降解NDMA 的基础上,采用了紫外光致水合电子这一高效还原技术来降解水中的痕量NDMA。根据相关文献报道[1],氯离子在100~200 nm的紫外光照射下,能够光解生成水合电子。因此,本实验选用氯离子作为水合电子的发生剂,在185 nm紫外光的照射下,初步研究了光致水合电子对NDMA的降解效能,并与常规的紫外直接光解法进行比较;利用气相色谱-质谱联用技术对NDMA及其降解中间产物进行定性和定量分析,同时重点考察了NDMA降解的产物DMA、亚硝酸盐及硝酸盐进一步的降解情况,从而得出水合电子还原法的优势所在,拟为优化NDMA的去除工艺提供技术参考。
1实验部分
1.1仪器和试剂
高效液相色谱仪(Accela UPLC);质谱仪(TSQ QuantumTMAccess MS);离子色谱(ICS-1000);精密pH计(320P-01)。
N-二甲基亚硝胺(N-Nitrosodimethylamine,NDMA)和二甲胺(Dimethylamine,DMA)购自Fluka公司(Buchs,Swizerland),其纯度>99%;硝酸钠、亚硝酸钠及其他试剂均为分析纯。去离子水由Milli-Q纯水机制得。
1.2实验方法
试验装置如图1所示,该反应器主要材质为不锈钢材质,内壁为光滑镜面;主体结构和反应器顶盖之间采用硅胶圈和密封口进行密封,紫外灯固定在反应器中心位置。反应所用紫外灯购自贺利氏特种光源有限公司,发射波长185 nm,功率为14 W的低压水银汞灯。
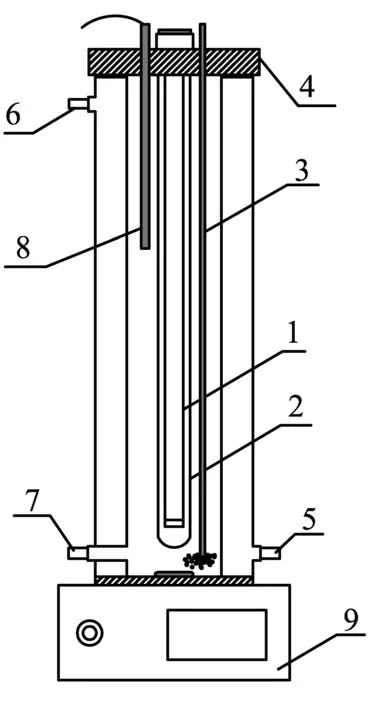
1-紫外灯;2-石英套管;3-曝气管;4-密封盖(附橡
胶垫圈);5-循环水进水阀门;6-循环出水阀门;
7-取样口;8-温度探头;9-恒温磁力搅拌器
图1反应装置示意
在如图1所示的不锈钢反应器中加入一定体积用水,通He气30 min去除水体中的溶解氧,随后立即加入一定量NaCl溶液,将反应器密封,用NaOH溶液调节初始pH。开启磁力搅拌器,同时开启紫外灯,此时反应生成的水合电子能够进一步去除水体中的溶解氧。待15 min后,将紫外灯关闭,迅速注入一定浓度的NDMA储备液,开启紫外灯进行光降解反应。在不同的时间间隔取出水样放于带聚四氟乙烯衬垫的棕色玻璃瓶中,并用铝箔包好直至分析。
1.3分析方法
采用HPLC-MS/MS对NDMA和DMA进行分析。对于高效液相色谱,色谱柱为美国ThermoFisher公司生产的Thermo Hypersil Gold C18柱(2.1×150 mm,填充粒径为3 μm)。进样量为10 μL,流动相采用甲醇和2 mmol/L醋酸铵溶液,流速均设为250 μL/min,采用梯度洗脱;质谱仪和高效液相色谱仪的接口采用电喷雾电离源(negative electrospray ionization source,ESI),并在正电离模式下运行。对所有目标分析物而言,喷雾电压均为+3 500 V;鞘气压力、离子吹扫气压力和辅气压力分别设为35 au(arbitrary units,au)、0 au和5 au;毛细管温度设为320 ℃。三组四级杆质谱仪在选择反应监测(selected reaction monitoring,SRM)模式下运行,并优化各种目标分析物和内标的质谱条件,使其定量离子的强度达到最大。

2结果与讨论
2.1光致水合电子降解NDMA
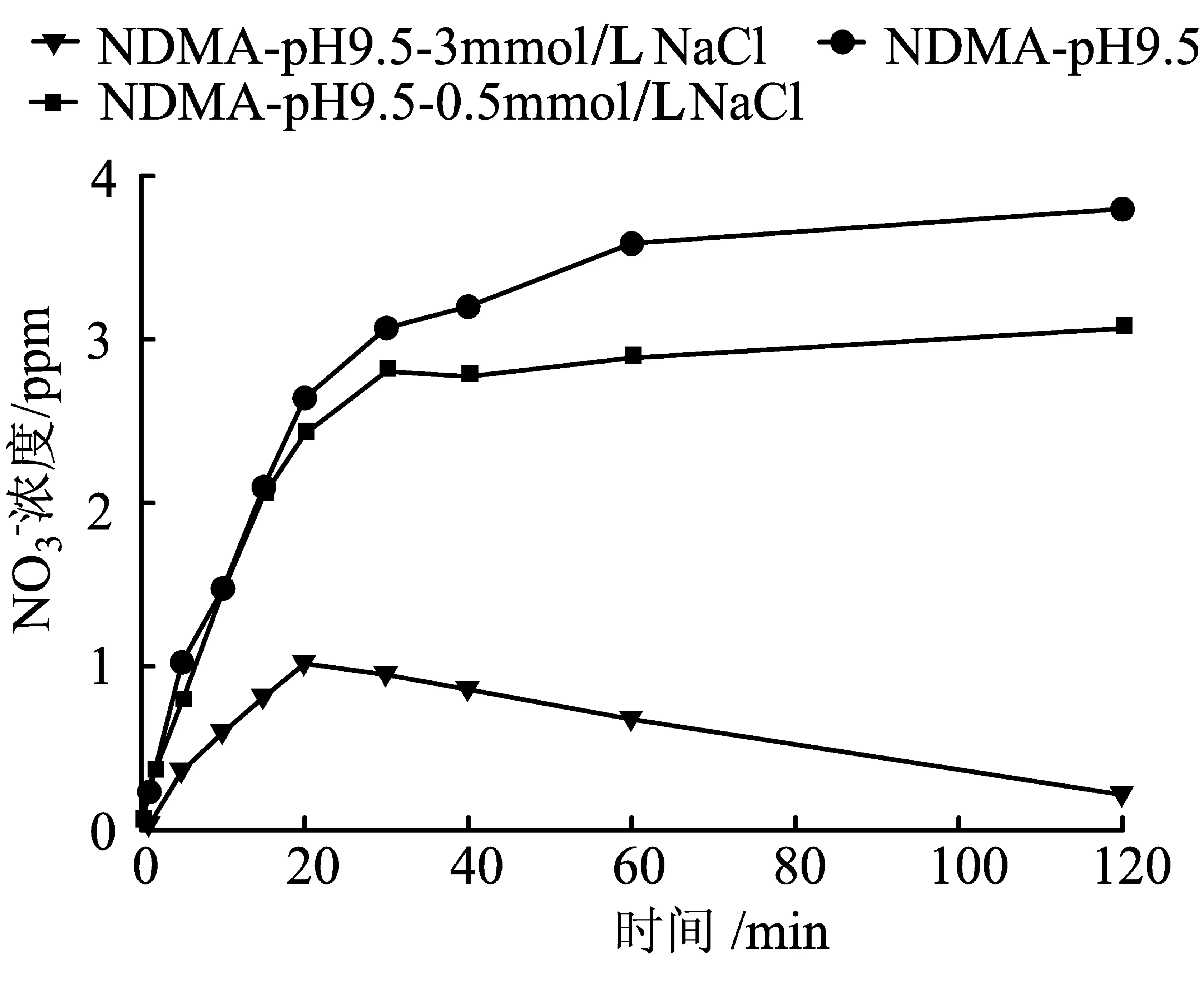
本节设计了三个对照实验:第一个实验不添加NaCl,其余反应条件均与水合电子反应条件相同;第二个实验和第三个实验的反应条件与水合电子反应条件相同,只在NaCl的浓度上有所变化;且三个实验均在He的气氛下进行,反应器中NDMA的初始浓度为0.135 mmol/L,采用NaOH调节溶液pH至9.5。不同反应条件下NDMA的降解过程见图2。
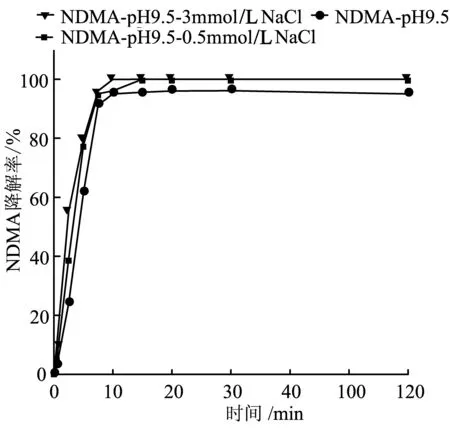
图2不同反应条件下NDMA的降解率随时间变化趋势
由于NDMA具有很强的光活性,三种反应条件下NDMA的最终去除率都很高。从图中可以看出,条件二(即NDMA+UV+He+pH 9.5+0.5 mmol/L NaCl)和条件三(即NDMA+UV+He+pH 9.5+3 mmol/L NaCl)在30 min时NDMA的去除率已经接近100%,而条件一(即NDMA+UV+He+KI+pH 9.5)在30 min后NDMA的去除率也达到了95%以上,这个结果是与NDMA具有很强的光活性这一特性相一致的----由于NDMA为感光性物质,在单独紫外光的辐射下,短时间就会有很高的去除率。
但三个体系的反应速率却有着明显的差别:相比之下,条件三下的NDMA具有更高的降解速率,在反应5 min的时候就已经达到了55%;条件二次之,为39%;条件一最小,为24%。而水合电子是产生这一差别的主要因素。
一般认为,紫外直接光解NDMA主要存在三种途径:光致氧化、光致消去和光致水解,且酸性环境更利于其降解,因为在酸性环境下,紫外光辐射下形成的激发态NDMA可以发生质子化反应,从而具有更高的活性,致使结构中的N-N键发生异裂,生成产物DMA和亚硝酸盐[2]。而在光致水合电子降解NDMA体系中,紫外光和水合电子同时存在,由于水合电子具有极强的亲核性,可以进攻N-N键,使其更容易发生异裂,从而促进NDMA的降解。有相关文献报道[3],水合电子与NDMA的反应速率常数高达1.41×1010s-1,因此NDMA的快速降解可能是紫外直接降解与水合电子共同作用的结果,而且由条件三和条件二比较可知,随着氯离子的浓度增大,NDMA的降解速率越快,这很可能是水合电子随着氯离子浓度的增大而增多引起的。
以上结果可以说明,紫外光辐射产生的水合电子对于NDMA的降解有着重要作用,它可以明显提高NDMA的降解速率。
2.2产物生成量的比较

2.2.1DMA生成量的变化
图3给出了不同条件下DMA的生成量随时间的变化趋势。对于条件一,DMA的浓度随着时间的变化先达到最大值(0.028 9 mmol/L),然后趋于稳定,之后浓度不再发生变化;而条件二和条件三下的DMA浓度则在达到了最大浓度之后均有所下降:条件二的浓度有着轻微幅度的下降(从0.025 0 mmol/L到0.022 3 mmol/L,而条件三的下降幅度则较大(从0.016 6 mmol/L到0.012 8 mmol/L)。分析认为,由于DMA没有紫外吸收,因此UV不能进一步降解DMA,而水合电子则不受这一情况的限制,它可以进攻DMA分子中C-N键依次生成一甲胺和铵根,从而减少DMA的生成量,降低了NDMA再次生成的可能性。而条件三下降幅度大于条件二,其主要原因在于氯离子的浓度大,从而光照产生了更多水合电子的缘故。
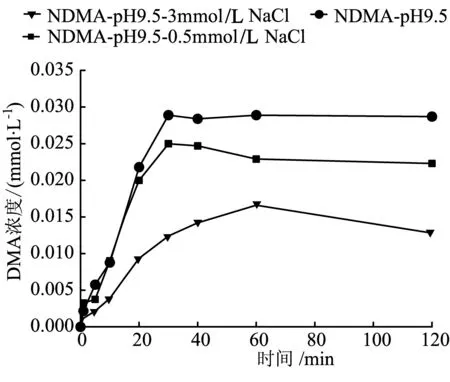
图3不同反应条件下DMA的生成量随时间变化趋势








综上,与直接光解相比,紫外光解NaCl产生的水合电子不仅能加快NDMA本身的降解速率,还能有效地促使NDMA的分解产物进一步降解,从而减少其生成量,达到控制NDMA的再生、彻底降低水的化学风险的目的。
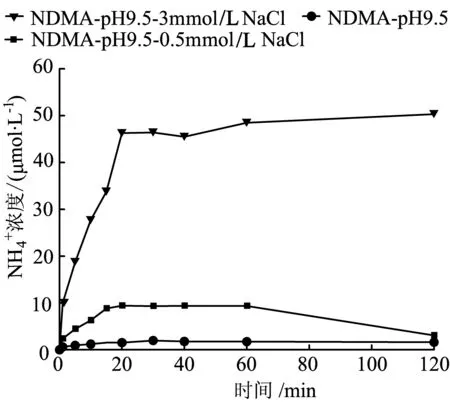

2.3两种体系下的N质量平衡

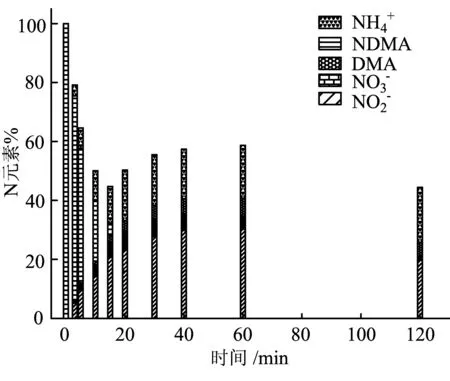
图7NDMA-pH 9.5-3 mmol/L NaCl下的氮气平衡图
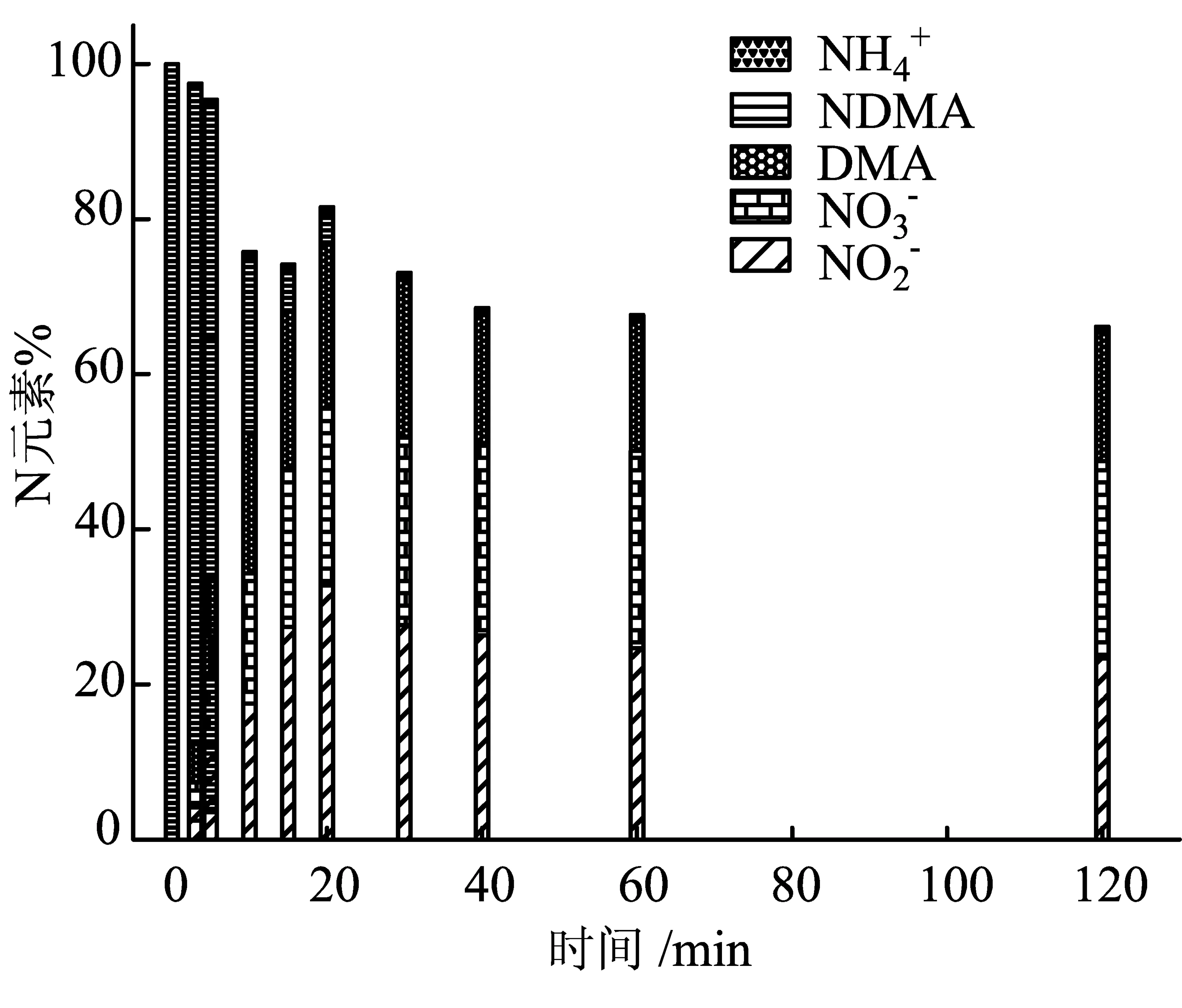
图8直接光照下的氮平衡图
3结论
(1)紫外直接光解法和紫外光致水合电子还原降解法对于NDMA都有很好的去除率,但紫外光致水合电子降解NDMA的速率更快,在反应5 min的时候其去除率就已经达到了55%。
(2)紫外直接光解并不能进一步降解NDMA的分解产物,而紫外光解NaCl产生的水合电子除了能加快NDMA本身的降解速率外,还可以有效地促使NDMA的分解产物进一步降解,从而减少其生成量,达到控制NDMA的再生、彻底降低水的化学风险的目的。

参考文献
[1]Sauer M C, Crowell R A, Shkrob I A. Electron photo detachment from aqueous anions 1. Quantum yields for generation of hydrated electron by 193 and 248 nm laser photo excitation of miscellaneous inorganic anions[J]. The Journal of Physical Chemistry AJ Phys Chem A,2004,108(25):5490-5502.
[2]Changha L, Wonyong C, Youngg Y, et al. UV photolytic mechanism of N-Nitrosodimethylamine in water: Dual pathways to methylamine versus dimethylamine [J]. Environ Sci Technol, 2005,39(7):2101-2106.
[3]Mezyk S P, Cooper W J, Madden K P, et al. Free radical destruction of N-Nitrosodimethylamine in water [J]. Environ Sci Technol,2004,38(11):3161-3167.
[4]StefanM I , BoltonJ R. UV direct photolysis of N-nitrosodimethylamine (NDMA): kinetic and product study[J]. Helvetica Chim. Acta, 2002,85(5):1416-1426.
[5]Matthew G, MartinR, johnr S. Metal-catalyzed reduction of N-Nitrosodimethylamine with hydrogen in water[J]. Environ Sci Technol,2006,40(23):7329-7335.
*基金项目:国家自然科学基金(21177094,2012.01-2015.12)。
作者简介邢露,女,硕士,研究方向为水污染处理。
(收稿日期:2015-05-10)
Research on the Degradation of Nitrosodimethylamine by Photo-induced Chlor-causing Hydrated Electron
XING LuZHANG ChaojieZHOU Qi
(CollegeofEnvironmentalScience&Engineering,TongjiUniversityShanghai200092)
AbstractUV-induced hydrated electron is used for the degradation of NDMA in water. As the major degradation products of NDMA, DMA and nitrite are also the important precursors for NDMA and under certain conditions,DMA and nitrite are likely to regenerate NDMA again. So these products of NDMA degraded by UV-induced hydrated electron are investigated in this paper. The result shows that in the UV-induced hydrated electron system, the more effectual and thorough treatment for NDAM removal from water can be realized due to the reduction in formation of the DMA and nitrite. Compared with conventional methods, the possibility of NDMA regeneration can be controlled effectively by this method, which will be helpful for the ultimate degradation of NDMA in waste water.
Key Wordsnitrosodimethylaminehydrated electrondegradationNaCl
