ω-黑麦碱基因沉默对小麦1B/1R易位系加工品质的影响
2016-07-15柴建芳王海波马秀英张翠绵董福双
柴建芳王海波马秀英 张翠绵 董福双
河北省农林科学院遗传生理研究所/河北省植物转基因中心, 河北石家庄 050051
ω-黑麦碱基因沉默对小麦1B/1R易位系加工品质的影响
柴建芳*王海波*马秀英 张翠绵 董福双
河北省农林科学院遗传生理研究所/河北省植物转基因中心, 河北石家庄 050051
摘 要:ω-黑麦碱是造成小麦 1B/1R易位系加工品质差的一个重要因素, 为探索解决这一问题, 构建了 ω-黑麦碱基因沉默表达载体, 并通过农杆菌介导转化小麦品种金禾9123, 获得3个T0代转基因植株, 再经连续的扩繁和PCR检测, 获得纯合转基因 T4代株系。酸性 PAGE检测结果表明, 这些纯合转基因株系中 ω-黑麦碱的总表达量平均下降53%。这些 ω-黑麦碱基因沉默的转基因株系的面筋指数、沉降值和稳定时间均显著提高, 而其农艺性状, 如株高、穗粒数、千粒重和小区产量, 均没有受到不良影响, 说明沉默 ω-黑麦碱基因可以在不影响产量的前提下提高小麦1B/1R易位系的加工品质。
关键词:小麦1B/1R易位系; 黑麦碱; RNA干扰; 基因沉默; 加工品质
本项目由河北省自然科学基金项目(C2014301005)资助。
This study was supported by the Natural Science Foundation of Hebei Province, China (C2014301005).
URL∶ http∶//www.cnki.net/kcms/detail/11.1809.S.20160311.1605.010.html
小麦1B/1R易位系具有抗性好、高产和适应性广等优点, 在我国大面积推广的高产小麦品种中占有很大的比例[1]。目前, 来自黑麦品种 Petkus的抗病基因已失去抗性[2-3], 新的非Petkus来源的抗病小麦1B/1R易位系已陆续培育成功[4-5], 显示1B/1R易位系仍将在未来的小麦育种和生产上发挥重要作用。但是, 小麦 1B/1R易位系普遍存在加工品质差的问题, 主要表现为面筋强度低、耐揉性差和面团发黏, 对面包和面条加工品质都有明显的不良影响[6-7]。研究认为, 小麦1B/1R易位系1RS染色体上的ω-黑麦碱基因是导致面团加工品质变差的一个重要原因[8],因此, 封阻 ω-黑麦碱基因的表达可能是改善小麦1B/1R易位系加工品质的一条有效途径。
为封阻ω-黑麦碱基因的表达, 利用ph基因诱导同源染色体重组和利用 1R染色体的单体附加系自交已创造了不含ω-黑麦碱基因的小麦1B/1R易位系[9-10],但高产和抗逆等有利基因是否会随ω-黑麦碱基因一同丢失, 目前尚不清楚。
RNA干扰(RNAi)是近年来发展起来的一项新技术[11-12], 可用来沉默多个序列高度相似基因的表达, 在小麦上已成功应用[13-14]。ω-黑麦碱基因是一个包括多个成员的基因家族, 不同家族成员之间DNA序列高度相似[15], 适合用RNA干扰封阻ω-黑麦碱基因的表达。本研究旨在明确ω-黑麦碱基因沉默是否会对小麦重要农艺性状造成影响, 该基因沉默技术能否应用于小麦1B/1R易位系加工品质的遗传改良。
1 材料与方法
1.1 试验材料
1B/1R易位系兰考906和非1B/1R易位系中国春用于克隆构建表达载体的相关基因片段, 1B/1R易位系金禾9123用于遗传转化。金禾9123由本研究团队选育, 2008年通过黄淮北片审定, 2012年通过黄淮南片审定, 但该品种加工品质比较差(农业部农作物品种审定第1877号公告)。
从兰考906花后15 d的籽粒中提取总RNA, 用植物RNA提取及第一链cDNA合成试剂盒(北京全式金生物技术有限公司), 按说明书程序反转录合成第一链cDNA。
1.2 ω-黑麦碱基因RNA干扰表达载体的构建
ω-黑麦碱基因 RNA干扰片段由正向 ω-黑麦碱基因片段、含内含子的DNA片段和反向ω-黑麦碱基因片段3部分依次连接组成。根据我们[15]报道的ω-黑麦碱基因不同成员编码区的序列, 选取编码区5′相对保守的区段设计引物, 引物序列为 P3-1∶5′-ttcccggg ccttcctcatctttgtcct-3′ (下画线部分为Sma I酶切位点); P4-1∶ 5′-taggatcc gctctggtctctggggttg-3′ (下画线部分为BamH I酶切位点)。以兰考906的cDNA为模板进行PCR扩增, 扩增参数为94℃ 4 min; 94 ℃ 45 s, 65℃ 45 s, 72℃ 1 min, 30个循环; 72℃ 7 min。对 PCR产物进行克隆测序, 选取其中一个与Chai等[15]报道的黑麦碱序列完全一致的克隆作为载体构建黑麦碱基因的正向片段。
设计反 P4-1/反 P3-1引物对, 前者序列为5′-AATTTCTAgA AgCTCTggTCTCTggggTTg-3′ (下画线部分为Xba I酶切位点), 后者序列为5′-AATAgAgCTC CCTTCCTCATCTTTgTCCT-3′ (下画线部分为Sac I酶切位点)。以上述含正向黑麦碱基因片段的克隆为模板进行PCR扩增, 扩增参数相同获得反向的黑麦碱基因片段。
利用P内1/P内2引物对, 从小麦的蜡质蛋白基因扩增携带内含子的DNA片段, 引物序列P内1为5′-AATTggATCCggCggCCTCggCgACgTCCTCg-3′(下画线部分为 BamH I酶切位点); P内 2为5′-AATTTCTAgA ACCCggTgACCgTTggCCTgCA-3′(下画线部分为 Xba I酶切位点)。以中国春基因组DNA为模板进行PCR扩增, 扩增参数与扩增正向黑麦碱基因片段时相同, 扩增后对产物进行克隆测序,选取与Murai等[16]报道的小麦Waxy基因第一内含子序列完全一致的片段构建载体。
在用pBS-T克隆试剂盒进行克隆时会出现一些没有插入片段的蓝斑, 选择一个蓝斑摇菌提质粒得到闭环的pBS-T质粒载体, 该载体具有Sma I-BamH I-Xba I-Sac I结构的多克隆位点。以该质粒载体为中间载体, 依次通过Sma I-BamH I双酶切、BamH I-Xba I双酶切和Xba I-Sac I双酶切把正向的黑麦碱基因片段、含内含子的DNA片段和反向的黑麦碱基因片段连接起来, 再用Sma I/Sac I双酶切, 把植物双元表达载体pAHC25中的Gus基因替换为已连接好的黑麦碱基因RNA干扰片段“正向黑麦碱基因片段-内含子片段-反向黑麦碱基因片段”, 得到抗性筛选基因为 Bar基因的黑麦碱基因沉默表达载体pAHC25-Sec。为得到适于农杆菌转化的黑麦碱基因沉默表达载体, 进一步用Hind III/EcoR I部分双酶切上述pAHC25-Sec表达载体, 回收6.1 kb的片段并将其与同样双酶切的农杆菌表达载体pCAMBIA0390连接, 得到可用于农杆菌转化的黑麦碱基因沉默表达载体 pCAMBIA0390-Sec (图 1),该表达载体的抗性筛选基因为Bar基因。

图1 黑麦碱沉默表达载体pCAMBIA0390-Sec结构示意图Fig.1 Schematic diagram of pCAMBIA0390-Sec expression vector
1.3 农杆菌转化
取金禾9123开花后12~15 d的籽粒, 先用70%酒精溶液浸泡1 min, 1%次氯酸钠溶液消毒10 min,再以无菌水冲洗4次; 在无菌条件下用手术刀片挑取幼胚盾片朝上放到愈伤组织诱导培养基 SD2上(MS培养基+1 mg L-1VB1+150 mg L-1天门冬酰胺+2 mg L-12,4-D+30 g L-1蔗糖+3 g L-1植物胶, pH 5.8), 于25℃黑暗条件下诱导愈伤组织, 4~10 d后进行转化。
将预培养的幼胚愈伤组织放入含有黑麦碱沉默表达载体的农杆菌 EH105侵染液(1/10MS无机盐+3%蔗糖+1%葡萄糖+100 μmol L-1乙酰丁香酮, pH 5.4, 菌液OD600值为0.5)侵染30 min, 然后于装有无菌滤纸的平皿中 23℃黑暗条件下共培养 2~3 d, 再将其转移到SD2+300 mg L-1羧卞青霉素的抑菌培养基上恢复培养 2周, 及分化培养基(1/2MS+2%蔗糖+300 mg L-1羧卞青霉素+5 mg L-1玉米素+3~5 mg L-1Bialaphos) 25℃光照条件下分化筛选2周, 将抗Bialaphos (Bar基因抗性)的再生芽转移到 1/2MS+ 2%蔗糖+0.3 mg L-1IAA+0.5 mg L-1多效唑培养基上壮苗, 再生植株生长到苗高 6~8 cm、根系较好时移入培养钵, 幼苗在 4~8℃下春化 20 d后移栽到温室。
1.4 小麦抗性再生植株的分子检测及Basta涂叶检测
当小麦抗性再生植株生长至 4~5片叶时, 用CTAB法提取叶片的基因组DNA进行PCR检测。检测引物为ω-sec-P3 (5′-ccttcctcatctttgtcctc-3′)和P内2 (5′-acccggtgaccgttggcctgca-3′), 扩增区域为正向黑麦碱基因片段加上内含子片段, 扩增片段大小为548 bp。扩增程序为94℃ 5 min; 94℃ 30 s, 60℃ 30 s, 72℃ 1 min, 35个循环; 72℃ 10 min。
用记号笔在植株倒数第2片叶距叶尖1 cm处画上横线, 用100 mg L-1Basta溶液双面涂抹横线到叶尖的部位, 1周后观察涂抹部位颜色变化情况。
1.5 种子醇溶蛋白与高低分子量麦谷蛋白的电泳检测及其统计分析
采用酸性聚丙烯酰胺凝胶电泳(A-PAGE)检测种子醇溶蛋白[17], 采用SDS-PAGE检测高、低分子量麦谷蛋白[18]。用Image J 149v软件量化处理醇溶蛋白电泳中ω-黑麦碱条带的亮度, 并用DPS v3.01软件统计分析。
1.6 转基因小麦的农艺性状与加工品质测定及其统计分析
将得到的3个T4代纯合转基因株系及其受体对照金禾 9123按随机区组设计进行小区产量比较试验, 每个小区种5行, 行长4 m, 每行播240粒种子,行距30 cm, 3次重复, 收获前从每小区随机选20个茎秆调查株高和穗粒数, 收获后称取小区产量和千粒重, 委托河北省农作物品种品质检测中心测定蛋白质含量、吸水率、湿面筋含量、面筋指数、Zeleny沉降值和稳定时间。试验结果选用DPS v3.01软件统计分析。
2 结果与分析
2.1 阳性转基因植株的获得
通过农杆菌介导的遗传转化, 得到金禾9123的10个T0代抗性再生植株, 其中3株为目的基因PCR阳性(图2)。用100 mg L-1Basta溶液涂叶处理表明,PCR阳性植株叶片涂抹部位颜色没有变化, 而其他7株叶片涂抹部位变黄, 从而排除了农杆菌污染导致 PCR假阳性的可能性, 说明目的基因已整合到 3个小麦植株的基因组中。
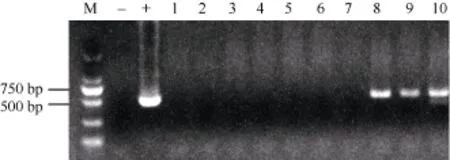
图2 T0代转基因植株的PCR检测Fig.2 Electrophoregram of PCR products from T0putative transgenic wheat plants
2.2 纯合转基因株系的获得与 ω-黑麦碱基因的表达
T0代阳性转基因植株经连续自交和 PCR检测,从T2代分离群体中获得纯合转基因株系, 经过进一步的扩繁和 PCR检测, 转基因性状能够稳定遗传,最终得到3个T4代纯合转基因株系(K1-5、K1-15和K1-16), 并且收获了足够种子用于小区产量比较试验。酸性PAGE检测结果显示, 在4个ω-黑麦碱条带中, 除表达量最弱的条带 2变化不明显外, 转基因株系的其他 3个黑麦碱条带的表达量均显著降低(图3), 转基因株系ω-黑麦碱基因的总表达量为受体品种ω-黑麦碱基因总表达量的47.5% (表1)。其他非黑麦碱条带没有出现一致变弱的情况, 说明黑麦碱基因沉默具有较高的特异性。
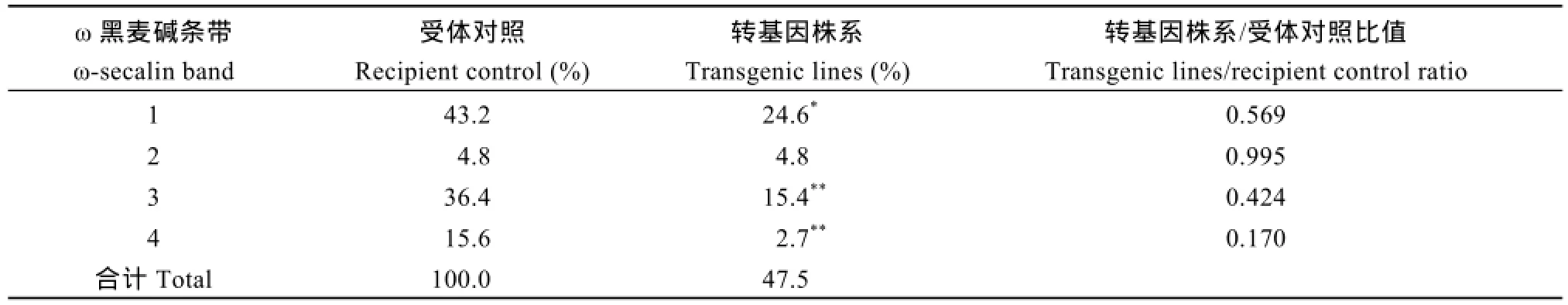
表1 转基因小麦株系及其受体对照种子中不同ω-黑麦碱的表达量比较Table 1 Comparison of ω-secalins in seeds of wheat transgenic lines and the non-transgenic recipient

图3 转基因小麦种子中ω黑麦碱的酸性PAGE检测Fig.3 Detection of ω secalin in transgenic wheat seeds by acid PAGE
为了解ω-黑麦碱基因表达沉默对麦谷蛋白基因表达的影响, 对3个纯合转基因株系及其对照进行了高低分子量麦谷蛋白的电泳检测, 结果转基因株系麦谷蛋白各条带的表达量与对照相比没有明显变化(图4), 说明ω-黑麦碱基因沉默没有影响麦谷蛋白基因的表达。
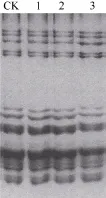
图4 转基因小麦种子中麦谷蛋白的SDS-PAGE检测Fig.4 Detection of glutenin subunits in transgenic wheat seeds by SDS-PAGE
2.3 转基因小麦的加工品质
3个转基因株系的籽粒蛋白质含量、吸水率和湿面筋含量与受体对照没有显著差异, 但面筋指数明显提高, 其中2个株系与对照达到显著差异, 沉降值和稳定时间也比对照显著提高(表2), 说明 ω-黑麦碱基因的沉默显著提高了金禾9123的加工品质。
2.4 转基因小麦的农艺表现
3个转基因株系的株高、穗粒数、千粒重和小区产量与对照非常接近(表 3), 株系间差异均不显著, 说明沉默黑麦碱基因的表达没有影响转基因株系的农艺表现。

表2 转基因小麦及其受体品种金禾9123的籽粒加工品质Table 2 Grain processing quality of transgenic lines and their receptor
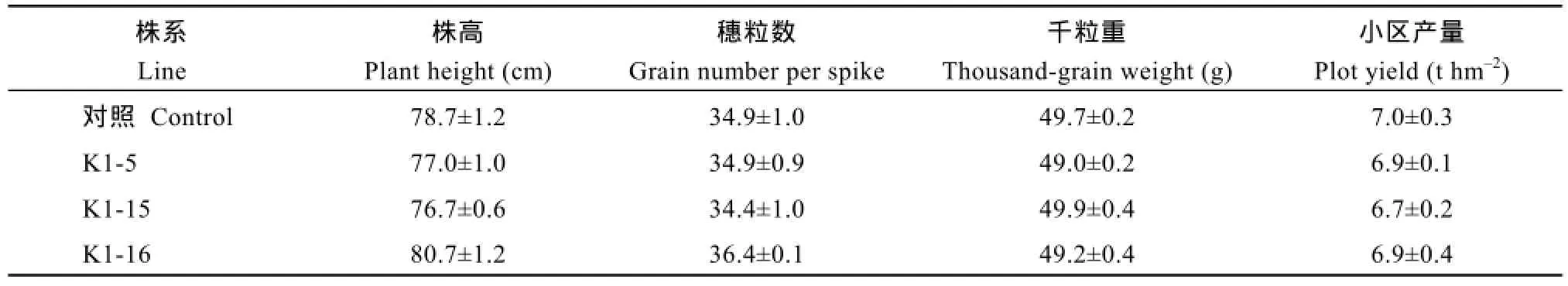
表3 转基因小麦及其受体品种金禾9123的农艺性状Table 3 Agronomic traits of transgenic lines and their receptor
3 讨论
1B/1R易位系金禾9123是一个高产品种, 加工品质较差, 不利于推广应用。本研究尝试利用 ω-黑麦碱基因沉默技术来改善金禾9123的加工品质, 发现ω-黑麦碱基因沉默在不影响产量的前提下确实能显著提高金禾9123的加工品质。在本研究中, ω-黑麦碱基因的沉默效率平均为 52.5%, 沉默效率不高,可能与使用的Ubiquitin启动子有关, Gil-Humanes等[19]用种子特异性启动子构建的沉默表达载体转化小麦取得了更高程度的沉默效果。目前, 我们也构建了由小麦种子特异性启动子驱动的ω-黑麦碱基因沉默表达载体, 并通过基因枪法共转化小麦 1B/1R易位系科农199, 得到了沉默效果更好的转基因株系, 其加工品质提高的幅度更为显著, 相关结果将另文报道。由此推测, 通过沉默 ω-黑麦碱基因的表达可以改良小麦1B/1R易位系的品质。
ω-黑麦碱是一类高度水溶性的蛋白[20]。本研究中, 转基因株系的湿面筋含量没有提高, 麦谷蛋白各组分的表达量也没有明显变化, 而转基因株系的面筋指数却显著提高, 说明转基因株系用与对照相同量的面筋产生了更多的不溶性面筋聚合体。这暗示ω-黑麦碱对不溶性面筋聚合体的形成产生了不良影响, 但 ω-黑麦碱如何影响不溶性面筋聚合体的形成, 值得进一步研究。
本研究得到的ω-黑麦碱基因沉默株系与以往报道的 ω-黑麦碱基因缺失材料[9-10]有不同特点。据报道, 小麦1B/1R易位系的1RS上有一个控制根系大小的基因, 且该基因位于 ω-黑麦碱基因的附近[21]。在文献报道的 ω-黑麦碱基因缺失材料[9-10]中, 控制根系大小的基因是否已随ω-黑麦碱基因区段一同丢失尚不清楚, 因为缺乏相关农艺性状的报道, 而 ω-黑麦碱基因沉默株系由于不涉及染色体区段缺失,不会导致邻近的根系大小相关基因的丢失, 本研究中ω-黑麦碱基因沉默株系的农艺性状没有受到不良影响恰好证明这一点。另外, 基因沉默性状作为一个显性性状[22-23], 可在不同 1RS来源的小麦 1B/1R易位系上应用, 不会因为 ω-黑麦碱基因缺失材料上的抗性基因失去抗性而失去应用价值, 其应用范围应更广。
4 结论
利用RNA干扰技术沉默ω-黑麦碱基因的表达,显著提高了金禾9123的加工品质, 且未对其重要农艺性状造成不良影响, 是改善小麦 1B/1R易位系加工品质的有效手段。
References
[1]周阳, 何中虎, 张改生, 夏兰琴, 陈新民, 高永超, 井赵斌, 于广军.1BL/1RS易位系在我国小麦育种中的应用.作物学报,2004, 30∶ 531-535 Zhou Y, He Z H, Zhang G S, Xia L Q, Chen X M, Gao Y C, Jing Z B, Yu G J.Utilization of 1BL/1RS translocation in wheat breeding in China.Acta Agron Sin, 2004, 30∶ 531-535 (in Chinese with English abstract)
[2]杨足君, 任正隆.抗白粉病基因 Pm8在四川小麦中遗传表达初步研究.四川农业大学学报, 1997, 15∶ 452-456 Yang Z J, Ren Z L.Expression of gene Pm8 for resistance to powdery mildew in wheat for Sichuan.J Sichuan Agric Univ,1997, 15∶ 452-456 (in Chinese with English abstract)
[3]Shi Z X, Chen X M, Line R F, Leung H, Wellings C R.Development of resistance gene analog polymorphism markers for the Yr9 gene resistance to wheat stripe rust.Genome, 2001, 44∶509-516
[4]Lei M P, Li G R, Liu C, Yang Z J.Characterization of wheat-Secale africanum introgression lines reveals evolutionary aspects of chromosome 1R in rye.Genome, 2012, 55∶ 765-774
[5]Yang M Y, Ren T H, Yan B J, Li Z, Ren Z L.Diversity resistance to Puccinia striiformis f.sp tritici in rye chromosome arm 1RS expressed in wheat.Genet Mol Res, 2014, 13∶ 8783-8793
[6]Dhaliwal A S, Mares D J, Marshall D R.Measurement of dough surface stickness associated with 1B/1R chromosome translocation in bread wheats.Cereal Sci, 1990, 12∶ 165-175
[7]刘建军, 何中虎, Peña R J, 赵振东.1BL/1RS易位对小麦加工品质的影响.作物学报, 2004, 30∶ 149-153 Liu J J, He Z H, Peña R J, Zhao Z D.The effects of 1B/1R translocation on grain quality and noodle quality of bread wheat.Acta Agron Sin, 2004, 30∶ 149-153 (in Chinese with English abstract)
[8]Graybosh R A, Peterson C J, Hansen L E, Mattern P J.Relation-ships between protein solubility characteristics, 1BL/1RS, high molecular weight glutenin composition, and end-use quality in winter wheat germ plasm.Cereal Chem, 1990, 67∶ 342-349
[9]Lukaszewski A J.Manipulation of the 1RS·1BL translocation in wheat by induced homoeologous recombination.Crop Sci, 2000,40∶ 216-225
[10]Fu S, Tang Z, Ren Z, Zhang H.Transfer to wheat (Triticum aestivum) of small chromosome segments from rye (Secale cereale)carrying disease resistance genes.J Appl Genet, 2010, 51∶115-121
[11]Scott M H, Amy A C, Gregory J H.Post-transcriptional gene silencing by double-stranded RNA.Nat Rev Genet, 2001, 2∶110-119
[12]Phillip A S, RNA interference.Genes & Develop, 2001, 15∶485-490
[13]Li J R, Zhao W, Li Q Z, Ye X G, An B Y, Li X, Zhang X S.RNA silencing of waxy gene results in low levels of amylose in the seeds of transgenic wheat (Triticum aestivum L.).Acta Genet Sin,2005, 32∶ 846-854
[14]孙重霞, 杨凤萍, 张婷, 隋晓燕, 梁荣奇, Liu Q, 张晓东, 李保云.利用RNAi技术抑制籽粒PPO合成改良小麦面粉白度的研究.中国农业科学, 2013, 46∶ 1104-1113 Sun C X, Yang F P, Zhang T, Sui X Y, Liang R Q, Liu Q, Zhang X D, Li B Y.Down-regulation of the expression of grain ppo genes to improve wheat dough whiteness by RNA interference.Sci Agric Sin, 2013, 46∶ 1104-1113 (in Chinese with English abstract)
[15]Chai J F, Liu X, Jia J Z.Homoeologous cloning of ω-secalin gene family in a wheat 1BL/1RS translocation.Cell Res, 2005, 15∶658-664
[16]Murai J, Taira T, Ohta D.Isolation and characterization of the three Waxy genes encoding the granule-bound starch synthase in hexaploid wheat.Gene, 1999, 234∶ 71-79
[17]张学勇, 杨欣明, 董玉琛.醇溶蛋白电泳在小麦种质资源遗传分析中的应用.中国农业科学, 1995, 28(4)∶ 25-32 Zhang X Y, Yang X M, Dong Y C.Genetic analysis of wheat germplasm by acid polyacrylamide gel electrophoresis of gliadins.Sci Agric Sin, 1995, 28(4)∶ 25-32 (in Chinese with English abstract)
[18]纪军, 刘冬成, 王静, 李俊明, 张爱民.一种小麦高、低分子量麦谷蛋白亚基的提取方法.遗传, 2008, 30∶ 123-126 Ji J, Liu D C, Wang J, Li J M, Zhang A M.A method of extraction and separation of wheat gluten.Hereditas (Beijing), 2008, 30∶123-126 (in Chinese with English abstract)
[19]Gil-Humanes J, Pistón F, Tollefsen S, Sollid L M, Barro F.Effective shutdown in the expression of celiac disease-related wheat gliadin T-cell epitopes by RNA interference.Proc Natl Acad Sci USA, 2010, 107∶ 17023-17028
[20]Hussain A, Lukow O M.Characterization of the 1B/1R translocation in wheat using water extractable protein concentrate.Euphytica, 1994, 78∶ 109-113
[21]Sharma S, Bhat P R, Ehdaie B, Close T J, Lukaszewski A J,Waines J G.Integrated genetic map and genetic analysis of a region associated with root traits on the short arm of rye chromosome 1 in bread wheat.Theor Appl Genet, 2009, 119∶ 783-793
[22]相微微, 张怀刚, 王道文, 柳觐, 刘宝龙.转基因小麦沉默的HMW-GS基因的遗传及表达.麦类作物学报, 2009, 29∶185-188 Xiang W W, Zhang H G, Wang D W, Liu J, Liu B L.Inheritance and expression of silenced HMW-GS genes in wheat.J Triticeae Crops, 2009, 29∶ 185-188 (in Chinese with English abstract)
[23]武茹, 高德荣, 别同德, 张晓, 赵芸, 程顺和.转基因小麦1Dx5基因沉默的遗传表达和品质效应分析.麦类作物学报,2010, 30∶ 991-996 Wu R, Gao D R, Bie T D, Zhang X, Zhao Y, Cheng S H.Genetic analysis and quality effects of 1Dx5 subunit silent in transgenic wheat.J Triticeae Crops, 2010, 30∶ 991-996 (in Chinese with English abstract)
DOI:10.3724/SP.J.1006.2016.00627
*通讯作者(
Corresponding authors)∶ 柴建芳, E-mail∶ chai87652130@163.com; 王海波, E-mail∶ nkywanghb@163.com
收稿日期Received()∶ 2015-09-28; Accepted(接受日期)∶ 2016-03-02; Published online(网络出版日期)∶ 2016-03-11.
Effect of ω-Secalin Gene Silencing on Processing Quality of Wheat 1B/1R Translocation Line
CHAI Jian-Fang*, WANG Hai-Bo*, MA Xiu-Ying, ZHANG Cui-Mian, and DONG Fu-Shuang
Genetics and Physiology Institute, Hebei Academy of Agriculture and Forestry Sciences/Plant Genetic Engineering Center of Hebei Province,Shijiazhuang 050051, China
Abstract:Omega-secalin is an important factor for the poor processing quality of wheat 1B/1R translocation lines.In this study,an expression vector of silencing ω-secalin gene was constructed and transferred into wheat variety Jinhe 9123 via Agrobacterium tumefaciens strain EH105.The three T0transgenic plants obtained were consecutively multiplied after PCR validation until the T4lines.Acid-PAGE assay indicated that total amount of ω-secalins in the transgenic lines decreased 53% on average compared with that in their respective control.In the three homozygous transgenic lines, gluten index, precipitation value, and stabilization time increased significantly, whereas the agronomic traits, such as plant height, grain number per spike, 1000-grain weight and plot yield, had no significant changes compared with those in the wild type.These results suggest that silencing ω-secalin genes can improve the processing quality of wheat 1B/1R translocation lines on the premise of not affecting grain yield.
Keywords:Wheat 1B/1R translocation line; Secalin; RNAi; Gene silencing; Processing quality
