Pb(Ⅱ)印迹磁性复合吸附剂在水溶液中吸附行为的FAAS法分析
2016-07-12吕晓华赵梦奇李建军司马义努尔拉
吕晓华,赵梦奇,李建军,司马义·努尔拉*
1.新疆大学化学化工学院, 新疆 乌鲁木齐 830046 2.阿拉山口出入境检验检疫局, 新疆 阿拉山口 833418
Pb(Ⅱ)印迹磁性复合吸附剂在水溶液中吸附行为的FAAS法分析
吕晓华1, 2,赵梦奇1,李建军1,司马义·努尔拉1*
1.新疆大学化学化工学院, 新疆 乌鲁木齐 830046 2.阿拉山口出入境检验检疫局, 新疆 阿拉山口 833418
以壳聚糖为单体,磁性纳米Fe3O4为载体,环氧氯丙烷为交联剂,利用本体聚合法制备的Pb(Ⅱ)印迹磁性复合吸附剂,可实现从水溶液中快速吸附分离Pb(Ⅱ)。印迹和非印迹吸附剂采用FTIR表征, FAAS法分析吸附过程中pH、吸附时间、初始浓度和温度等影响。结果发现,随着溶液pH值的增加, Pb(Ⅱ)-MICA对Pb(Ⅱ)的吸附容量在溶液pH 5~6时达到最大,当吸附时间为120 min, 最大吸附容量为32.48 mg·g-1。吸附剂对Pb(Ⅱ)的Pb2+/Cu2+, Pb2+/Cd2+, Pb2+/Ni2+, Pb2+/Zn2+的相对选择性系数分别是MNICA的28.11, 91.14, 76.54, 33.06倍, 显示出对Pb2+具有良好的吸附选择性。Langmuir等温吸附模型与平衡吸附数据吻合(r2=1,饱和吸附容量为33.87 mg·g-1)。动力学和热力学研究结果表明,吸附过程属于Langmuir型单层吸附,受化学作用控制,是自发、放热、焓驱动的过程。
印迹磁性复合吸附剂; 原子吸收光谱法; 铅离子; 吸附性
引 言
铅是对人体健康最有危害的重金属元素之一,重金属铅高毒性和非生物降解性,会损害人体新陈代谢系统[1-2], 许多国家和世界组织为此都规定了铅的允许值。涉及到环境、食品、生物和医药样品等复杂基体中微/痕量铅的高选择性分离富集方法特别引人关注。目前,选择分离富集重金属的方法主要有化学沉淀、膜分离、离子交换、电化学和活性炭吸附。然而,多数方法由于存在反应条件苛刻、效率运行费高或易产生二次污染等缺点,使其应用价值大大受到限制[3]。其中吸附法易操作、对毒性物质敏感度低、分离效果好,被认为是很有前途的重金属分离富集方法之一。但传统吸附剂又存在吸附容量小、机械强度差、分离时间长和成本高等问题。基于分子印迹技术制备的印迹聚合物兼备生物和化学识别体系的优点,可从复杂样品中选择分离富集模板分子及结构类似物,在复杂样品的前处理领域显示出良好的发展潜力与应用前景[4-6]。以纳米磁性粒子为载体与印迹技术相结合制备的磁性印迹复合物比传统的印迹材料更易实现快速分离,操作简单,用于复杂样品的前处理时,具有高效和快速等优点,是未来印迹技术发展的重要方向[7-9]。
研究中以壳聚糖为单体,磁性纳米Fe3O4为载体,环氧氯丙烷为交联剂,利用本体聚合法制备了Pb(Ⅱ)印迹磁性复合吸附剂Pb(Ⅱ)-MICA [Pb(Ⅱ) ion imprinted magnetic composite adsorbent]。并用FAAS法研究了吸附剂在水溶液中对Pb(Ⅱ)的吸附和选择性。吸附和选择实验结果表明Pb(Ⅱ)-MICA对Pb2+具有良好的吸附容量和选择识别能力。通过探讨吸附过程的动力学、吸附等温线和热力学,提出了Pb(Ⅱ)印迹磁性复合吸附剂的印迹吸附控制机理,为印迹磁性复合吸附剂的制备、应用及结构设计提供理论指导。
1 实验部分
1.1 主要仪器
傅里叶变换红外光谱仪为BRUKER公司的EQU IN OX-55型, 原子吸收光谱仪为Thermo Electron公司的SOLAARM6型; 恒温气浴震荡器为上海梅香仪器有限公司的CHA-S; 多功能参数仪为METTLER TOLEDO公司; 铅, 铜, 镉, 镍, 锌空心阴极灯。
1.2 试剂与药品
铅、镉、铜、锌、镍标准溶液(1.000 g·L-1); 壳聚糖(脱乙酰度大于90%)、乙酸、环氧氯丙烷等购于天津化学试剂厂。硝酸铅购于天津博迪化工有限公司。氢氧化钠购于天津光复科技发展有限公司。EDTA购于天津盛奥化学试剂有限公司。以上试剂均为分析纯。纳米磁性Fe3O4粒子:自制[10]。实验用去离子水。
1.3 Pb(Ⅱ)-MICA的制备
取0.2 g壳聚糖溶于醋酸溶液(2.5%,v/v),加入5 mL硝酸铅溶液(5 500 mg·L-1)混和,在室温下强力搅拌6 h。使壳聚糖与Pb(Ⅱ)充分络合,再加入0.2 g Fe3O4粒子和0.4 mL环氧氯丙烷溶液,调节溶液pH值为10左右。30 ℃恒温水浴,均匀搅拌交联反应3 h后,加固化剂室温固化8 h,过滤并于真空干燥箱50 ℃烘干,研成粉末。用0.2 mol·L-1EDTA溶液洗至Pb(Ⅱ)检不出,0.2 mol·L-1NaOH溶液和去离子水洗至溶液呈中性。于真空干燥箱中50 ℃干燥,过100目筛(0.154 mm), 备用。
非印迹磁性复合吸附剂(MNICA)的制备方法与上述过程相似,只是不加模板Pb(Ⅱ)。
1.4 吸附实验

2 结果与讨论
2.1 红外光谱分析
KBr压片法测得壳聚糖、非印迹磁性复合吸附剂(MNICA)、洗脱前(MICA)和洗脱后Pb(Ⅱ)-MICA的红外光谱见图1。

图1 (a) MNICA, (b) 洗脱后Pb(Ⅱ)-MICA,(c) 洗脱前MICA,(d) CTS的红谱图
Fig.1 Infrared spectra of (a) MNICA (b) Pb(Ⅱ)-MICA (c) MICA before leaching Pb(Ⅱ) (d) CTS
由图1可知,壳聚糖(CTS)形成配合物后,形成氢键缔合的O—H伸缩振动吸收峰和N—H伸缩振动吸收峰重叠而增宽的多重吸收峰,3 444,1 597和1 667 cm-1处的N—H伸缩振动峰及1 380 cm-1处的γC—N分别发生一定的位移和强度变化,1 089 cm-1处的γas(C—OH)也发生了一定的位移,说明壳聚糖结构中的—NH2和—OH都参与了Pb(Ⅱ)配位。比较Pb(Ⅱ)非印迹和印迹谱图(a和b)最大的差异在于3 422 cm-1的多重峰, 891 cm-1C—O伸缩峰,说明壳聚糖与交联剂也发生了反应。
2.2 吸附行为研究
2.2.1 时间对吸附性的影响及吸附动力学
采用静态吸附法研究Pb(Ⅱ)-MICA经不同吸附时间对Pb2+的吸附行为。结果如图2所示,吸附容量在60 min时迅速增加,随时间的延长,吸附速率逐渐减慢,吸附量也接近饱和。120 min时,基本达到吸附平衡,说明印迹空穴的存在有利于Pb(Ⅱ)与功能团的螯合。分别用Lagergren准一级和McKay准二级反应动力学模型对Pb(Ⅱ)-MICA吸附行为进行模拟。通过比较平衡时吸附容量的理论值(3.948 mg·g-1)和实验值(3.928 mg·g-1),准二级动力学理论值更接近实验值。由图3和图4可知, Lagergren方程的拟合曲线r2值为0.883 7,McKay方程拟合曲线的r2值为1,后者的相关系数高于前者。Pb(Ⅱ)-MICA对的Pb2+吸附过程符合McKay模型且对Pb2+的吸附行为受化学吸附控制[11-12]。
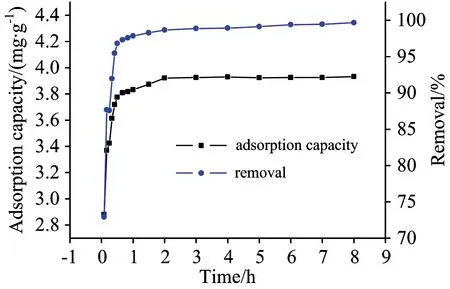
图2 时间的影响

图3 吸附Pb(Ⅱ)的Lagergren方程准一级拟合曲线
2.2.2 pH值对吸附性影响

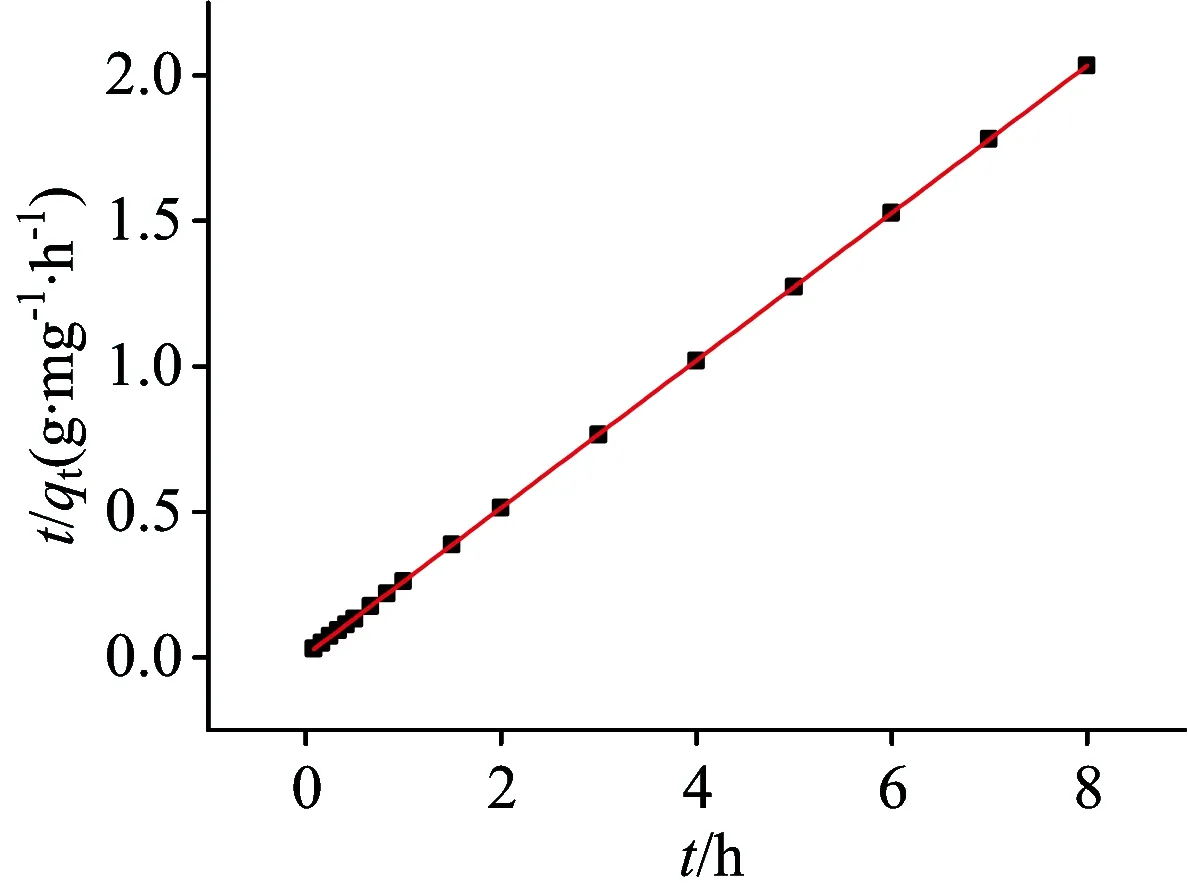
图4 吸附Pb(Ⅱ)的Mckay方程准二级拟合曲线
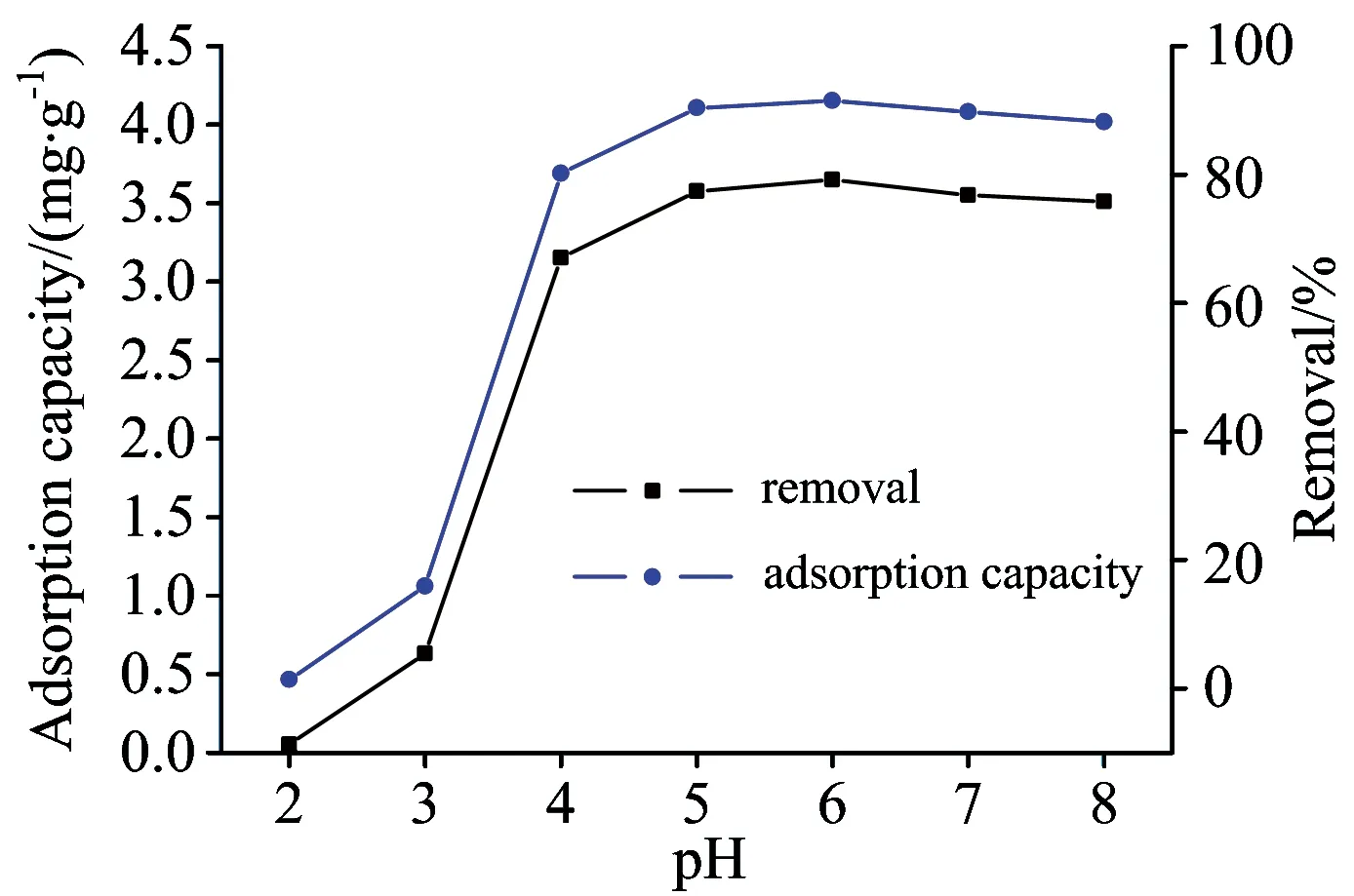
图5 pH值的影响
2.2.3 初始溶液浓度对吸附性的影响及吸附等温线
Pb(Ⅱ)初始浓度对吸附性能的影响如图6所示: 吸附容量随着Pb(Ⅱ)初始浓度的增加而增加,当Pb2+浓度200 mg·L-1时,吸附容量缓慢接近一个稳定值。这是由于在初始状态时,吸附剂表面存在大量可以增加吸附容量的吸附空位,吸附达到平衡时,多数吸附空位被离子占有,导致吸附能力的降低。从图6中可知Pb(Ⅱ)-MICA的饱和吸附容量为32.48 mg·g-1。
通过langmuir无量纲平衡参数的分离系数RL分析,当RL<1, 吸附剂具有良好的吸附能力,RL>1则不利于吸附,由图7可知,复合吸附剂对铅离子吸附的RL均在0~1之间,表明印迹的复合吸附剂对铅离子有良好的吸附性,RL随着离子初始溶度的增加而减小,也说明在一定范围内离子浓度越高对吸附越有利。
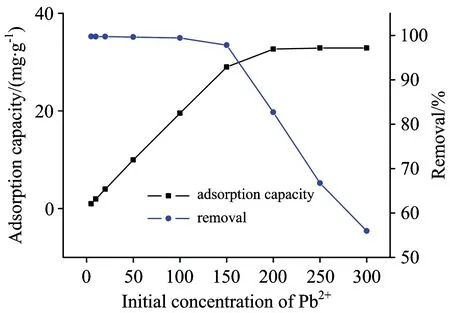
图6 Pb(Ⅱ)初始浓度的影响

图7 RL和c0的关系曲线
利用Freundlich和langmuir吸附等温线模型分析,吸附等温方程中校正值r2分别为0.987 8和0.998 6,都呈现很好的线性关系。从langmuir模型中得出25 ℃时吸附系数kL为: 2.287 L·mg-1, 吸附剂对Pb(Ⅱ)的饱和吸附容量为33.87 mg·g-1与实验数值相近。吸附过程属于langmuir型单层吸附,吸附位点是等效的没有干扰,吸附作用力来自于微粒表面氨基中的N和羟基中的O原子对金属离子的螯合作用。
2.2.4 温度对吸附性能的影响及吸附热力学
在不同温度下进行了Pb(Ⅱ)-MICA对Pb(Ⅱ)等温吸附实验,结果显示Pb(Ⅱ)的吸附量随着温度的升高而减少。采用langmuir等温方程式计算吸附过程的Gibbs自由能改变值ΔG,焓变ΔH及熵变ΔS等[16],结果见表1。
结果表明:在研究的温度范围内,ΔH<0,表明Pb(Ⅱ)-MICA对Pb(Ⅱ)吸附过程为放热过程,所以吸附量会随温度的升高而降低。ΔS>0显示吸附过程中体系自由度增大,ΔG<0吸附是自发的,ΔG随温度升高而增大,说明升温不利于吸附能力的增加。|ΔH|>|TΔS|,表明吸附是焓驱动过程。

表1 Pb(Ⅱ)-MICA吸附性能的热力学参数
2.2.5 其他金属离子对吸附性能的影响
分别取0.5 g Pb(Ⅱ)-MICA和MNICA对20 mL, 100 mg·L-1Pb2+和选择与Pb2+价态和粒子半径相近的Cu2+,Cd2+,Ni2+和Zn2+作为竞争离子,吸附120 min后,用磁体将吸附剂与水溶液分离,测试各离子浓度。由图8可知,Pb(Ⅱ)-MICA对Pb2+有较高的吸附容量,而对竞争离子的吸附容量则相对较低,而MNICA在相同条件下,对竞争离子和Pb2+的吸附容量没有显著差别。
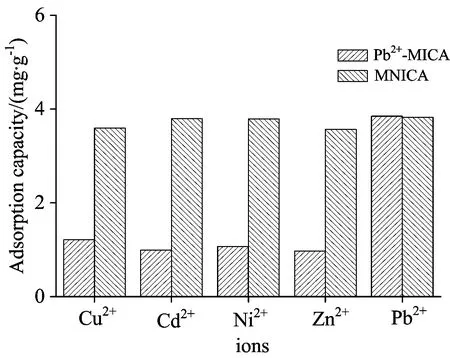
图8 Pb(Ⅱ)-MICA和MNICA对Pb2+的选择吸附性
以相对选择系数评价Pb(Ⅱ)-MICA与MNICA对Pb2+吸附的选择能力,Pb(Ⅱ)-MICA对不同离子的分配系数kd,选择系数k和相对选择系数k′的计算,其计算结果如表2所示。结果表明,即使存在其他离子干扰的情况下,Pb(Ⅱ)-MICA也能对Pb2+有很好的选择性吸附作用。Pb(Ⅱ)-MICA对Pb2+的Pb2+/Cu2+, Pb2+/Cd2+, Pb2+/Ni2+, Pb2+/Zn2+的相对选择性系数分别是MNICA的28.11, 91.14, 76.54, 33.06倍,这是由于印迹孔的几何形状和铅离子的几何形状吻合, 从而显示出高度的选择性。
表2 Pb(Ⅱ)的分配系数,选择系数和相对选择系数
Table 2 Distribution coefficient selectivity coefficient and relativity selectivity coefficient of Pb(Ⅱ)

IronsMNICAPb(Ⅱ)-MICAkd/(L·g-1)kkd/(L·g-1)kk'Pb2+5.93-7.40--Cu2+1.982.990.08784.1528.11Cd2+4.861.220.066111.191.14Ni2+4.531.310.073100.276.54Zn2+1.723.450.064114.033.06
3 结 论
通过FAAS分析Pb(Ⅱ)印迹磁性复合吸附剂吸附水溶液中Pb(Ⅱ)行为的研究结果表明,以铅离子为模板,壳聚糖为单体,环氧氯丙烷为交联剂,将磁性纳米四氧化三铁分散至溶液中,利用本体聚合法制备的Pb(Ⅱ)-MICA通过磁体实现固液的快速分离。120 min时,吸附过程达到平衡,在溶液pH为5~6,可获得最大吸附容量32.48 mg·g-1。铅离子与其他金属离子的相对选择系数计算结果表明,印迹相比非印迹磁性复合吸附剂对Pb(Ⅱ)具有优先选择性。等温模型与平衡吸附数据吻合(r2>0.988),吸附属Langmuir型单层吸附。动力学研究结果表明,吸附过程符合McKay准二级反应动力学模型(r2=1),吸附过程主要受化学作用控制。吸附剂对Pb(Ⅱ)的ΔG,ΔH均为负值且|ΔH|>|TΔS|,说明吸附是一个自发、放热、焓驱动的过程。
[1] Gama E M, Lima A S, Lemos V A.Journal of Hazardous Material, 2006, 136: 757.
[2] Bahrami A, Besharati-Seidani A, Abbaspour A.Electrochimica Acta,2014, 118: 92.
[3] Zhang X, Su H J, Tan T W, et al.Journal of Hazardous Material, 2008, 68: 284.
[4] Homeira E, Elahe M, Mostafa M A,et al.Chem.Eng.J., 2013, 215: 315.
[5] HUANG Yi, ZHANG Qing-jie, LIU Min, et al(黄 怡,张青杰,刘 敏).Chinese Journal of Chromatograph(色谱), 2012, 30(1): 56.
[6] DENG Bo(邓 勃).Chinese Journal of Inorganic Analytical Chemistry(中国无机分析化学), 2011, 1(1): 2.
[7] Omid Sadeghi, Forouzan Aboufazeli, Hamid Rezalotfizadehzhad, et al.Food Anal.Methods, 2013, 6: 754.
[8] Homeira Ebrahimzadeha, AliAkbar Asgharinezhada, Elahe Moazzena.Journal of Food Composition and Analysis, 2015, 41: 74.
[9] Guo B, Deng F, Zhao Y.Applied Surface Science, 2014, 292: 438.
[10] XIAO Ling,CHEN Yue-ying(肖 玲, 陈乐英).Ion Exchange and Adsorption(离子交换与吸附), 2008, 24(3): 194.
[11] Bhattacharya A K,Naiya T K, Mandal S N,et al.J.Chem.Eng., 2008, 137: 535.
[12] Chen Anwei, Zeng Guangming, Chen Guiqiu,et al.J.Chem.Eng., 2012, 191: 88.
[13] Nguyen Van Suc, Ho Thi Yeu Ly.Chemistry Engineering & Process Technology, 2012, 3(2): 3.
[14] CHENG Xing, YANG Zhao-xia, ZHANG Zhao-hui, et al(程 星, 杨朝霞, 张朝辉).Chinese Journal of Analytical Chemistry(分析化学), 2013, 41(9): 1409.
[15] WANG Ling-ling, YAN Yong-sheng, DENG Yue-hua, et al(王玲玲, 闫永胜, 邓月华,等).Chinese Journal of Analytical Chemistry(分析化学), 2009, 37(4): 539.
[16] Munagapati V S, Yarramuthi V, Nadavala S K, et al.J.Chem.Eng., 2010, 157: 36.
(Received Feb.5, 2015; accepted May 8, 2015)
*Corresponding author
Adsorption Behavior of Pb(Ⅱ) Ion Imprinted Magnetic Composite Adsorbent in Aqueous Solution by FAAS
LÜ Xiao-hua1, 2, ZHAO Meng-qi1, LI Jian-jun1, Ismayil Nurulla1*
1.College of Chemistry and Engineering, Xinjiang University, Urumqi 830046, 2.Alashankou Entry-Exit Inspection and Quarantine Bureau, Alashankou 833418, China
Pb(Ⅱ) Ion Imprinted Magnetic Composite Adsorbent (Pb(Ⅱ)-MICA) was prepared for the quick separation of Pb(Ⅱ) from aqueous solutions by bulk polymenrization with chitosan as the functional monomer, the magnetic iron oxide nano-particles as carrier and epichlorohydrin as the cross-link agent.The Pb(Ⅱ)-MICA and MNICA were characterized by FTIR.The Effects of the adsorption process including pH, contact time, initial concentration and temperature were investigated by FAAS.It was found that with the increasing of PH value, the adsorption capacity of Pb(Ⅱ)-MICA for Pb(Ⅱ) reached the peak in the range of pH 5.0~6.0.The maximum adsorption capacity was 32.48 mg·g-1when the adsorption time was up to 120 min.The relative selectivity coefficient of Pb(Ⅱ) and other metal ion on Pb(Ⅱ) -MICA were 28.11, 91.14, 76.54, 33.06 times compared with MNICA.The results show that the Pb(Ⅱ)-MICA displayed strong affinity for Pb(Ⅱ) in the solution and exhibited selectivity for Pb(Ⅱ) ion in the presence of Cu2+,Cd2+,Ni2+and Zn2+.The Langmuir adsorption isotherm models were fit to the adsorption equilibrium data well (r2=1, the saturation adsorption capacities were 33.87 mg·g-1).The adsorption dynamics and thermodynamics of Pb(Ⅱ) -MICA for Pb(Ⅱ) were investigated, the results indicated a Langmuir mono-layer mode process of Pb(Ⅱ) on the Pb(Ⅱ)-MICA was dominated by chemical action.An exothermic and spontaneous adsorption process of Pb(Ⅱ) on the Pb(Ⅱ)-MICA was driven by enthalpy.
Imprinted magnetic composite adsorbent; FAAS; Lead ion; Adsorption
2015-02-05,
2015-05-08
国家自然科学基金项目(51403179)资助
吕晓华,1975年生,新疆大学化学化工学院博士研究生 e-mail: xjciqlxh@163.com *通讯联系人 e-mail: ismayilnu@sohu.com
O657.3
A
10.3964/j.issn.1000-0593(2016)05-1483-05
猜你喜欢
杂志排行
光谱学与光谱分析的其它文章
- Native Defect Luminescence of Zinc Oxide Films and Its Potential Application as White Light Sources
- Study on the Multi-Spectral True Temperature Pyrometer for Explosion Transient of Thermo-Baric Explosives
- 蛋白饲料原料粗蛋白含量近红外光谱模型转移研究
- 小波变换和连续投影算法在火龙果总酸无损检测中的应用
- 增强的UV-B辐射对高粱幼苗光合和抗氧化系统的影响
- Spectrum Quantitative Analysis Based on Bootstrap-SVM Model with Small Sample Set
