助剂对Co-Mo/γ-Al2O3催化剂加氢脱硫反应氢耗的影响
2016-07-05龙湘云陈文斌
陈 硕, 龙湘云, 陈文斌, 聂 红
(中国石化 石油化工科学研究院, 北京 100083)
助剂对Co-Mo/γ-Al2O3催化剂加氢脱硫反应氢耗的影响
陈硕, 龙湘云, 陈文斌, 聂红
(中国石化 石油化工科学研究院, 北京 100083)
摘要:以4,6-二甲基二苯并噻吩与1-甲基萘的混合体系为对象,考察Co-Mo/γ-Al2O3催化剂中n(Co)/n(Co+Mo)对其催化加氢脱硫反应的加氢脱硫活性、加氢脱硫选择性、芳烃饱和活性以及反应氢耗的影响,并采用H2-TPR、XRD、Raman、TEM、XPS等表征手段对催化剂进行分析表征。结果表明,当n(Co)/n(Co+Mo)为0.3时,Co-Mo/γ-Al2O3中金属组分与载体间相互作用力最弱,硫化态催化剂Co-Mo-S相的比例、活性金属Mo的硫化度最高,MoS2片晶的平均长度最短。相应地,该催化剂的加氢脱硫活性、加氢脱芳活性、直接脱硫选择性达到最高值,同时脱除每摩尔硫的氢耗、脱除每摩尔硫时芳烃饱和反应的氢耗均最低,即H2利用率最高。活性金属存在形态特别是Co-Mo-S活性相数量是影响催化剂加氢脱硫活性、加氢脱芳活性、加氢脱硫选择性以及H2利用率的重要因素。
关键词:n(Co)/n(Co+Mo); 加氢脱硫; 加氢脱芳; 活性; 选择性; 氢耗
随着国内油品质量升级的加快,生产超低硫柴油成为日益紧迫的任务。在清洁柴油加氢精制过程中发生的化学反应主要有加氢脱硫(HDS)、加氢脱氮(HDN)和加氢脱芳(HDA),需要消耗大量的H2,尤其针对芳烃含量较高的柴油[1-2]。HDA反应无疑可以改善柴油的质量,但当柴油的硫含量和质量达到指标要求后,过多的饱和芳烃则会使H2的消耗大幅增加。加氢脱硫装置中H2的消耗是装置的主要操作费用之一。H2成本昂贵,且制氢过程碳排放量大。无论从节约H2角度还是降低碳排放角度考虑,均希望在实现脱硫目标的同时,尽可能合理利用或减少H2的消耗。
柴油中H2的消耗主要来自HDS和HDA反应。柴油中硫化物的脱除途径主要分为直接脱除硫(DDS)和加氢脱除硫(HYD) 2种[3]。对于4,6-二甲基二苯并噻吩(4,6-DMDBT)而言,在DDS反应路径中,4,6-DMDBT分子通过直接氢解脱除S原子生成二甲基联苯;在HYD反应路径中,4,6-DMDBT分子中芳环首先加氢饱和,然后再通过氢解反应脱除S原子,最终生成二甲基环己基苯、二甲基联环己烷[4-7]。4,6-DMDBT主要通过HYD途径脱硫[8-10]。显然,DDS途径消耗的H2少于HYD途径。HDA反应机理与HYD途径中的芳环加氢步骤类似[11],反应过程中H2消耗量同样较大。因此,氢耗不仅与原料油硫含量、反应条件等因素有关[12],加氢精制催化剂本身的性能对反应过程中产生的氢耗也有重要影响。提高DDS选择性,减少HDA反应的发生,将非常有助于降低反应氢耗。由此可见,调节催化剂的加氢脱硫选择性具有重要意义。
一般认为,在工业上已经普遍应用的柴油超深度脱硫催化剂中,Co-Mo型催化剂具有相对较强的直接脱硫能力和相对较弱的芳烃饱和能力,具有DDS选择性高、反应氢耗低的特点[13]。为使其选择性达到更高的水平,需要寻找能够明显提高其加氢脱硫选择性的因素。研究表明,在Mo基硫化物催化剂中,引入助剂Co不仅影响催化剂的活性,而且对其加氢脱硫选择性存在较大影响;在一定含量范围内,Co的引入使得HYD途径的选择性降低,DDS途径选择性增加[14-15]。为了进一步调节催化剂的加氢脱硫选择性,降低反应过程的H2消耗,笔者以4,6-DMDBT和1-甲基萘(1-MN)为模型化合物,考察了助剂对Co-Mo催化剂加氢脱硫选择性以及反应过程中H2消耗的影响。
1实验部分
1.1催化剂制备
采用催化剂长岭分公司生产的拟薄水铝石(孔容为1.21 cm3/g)作为载体原料,使用挤条机制备成型载体。成型后载体在120℃下干燥3 h,并在600℃下焙烧3 h后获得催化剂所需载体。
以(NH4)6Mo7O24·4H2O、Co(NO3)2·6H2O作为前驱物,采用孔饱和分步浸渍法制备一系列具有不同助剂含量的催化剂。助剂含量以n(Co)/n(Co+Mo)表示,如非特别指出,n(Co)/n(Co+Mo)均指催化剂的体相金属摩尔比。第一步,将含Mo前驱物的溶液浸渍载体2 h,然后120℃下干燥3 h和400℃下焙烧3 h,得到含Mo催化剂。第二步,将金属Co引入含Mo催化剂中,制备条件与第一步相同。制备得到的各催化剂中MoO3的质量分数相同,n(Co)/n(Co+Mo)分别为0、0.1、0.2、0.3、0.4、0.5、0.6。
1.2催化剂活性评价
采用高压微型反应器加氢实验装置评价催化剂活性。催化剂装填量0.6 g,置于反应器恒温段,其余部分装填石英砂。在评价之前,用CS2质量分数为5%的环己烷溶液作为硫化油,在压力6.4 MPa、硫化油流速0.4 mL/min、H2流速365 mL/min的条件下,对催化剂进行预硫化4 h。然后,切换成原料油进行活性评价。以4,6-DMDBT作为HDS反应模型化合物,以1-MN作为HDA反应模型化合物配制原料油,其组成为w(4,6-DMDBT)=0.45%、w(1-MN)=40%、w(CS2)=1.2%、w(n-C10)=57.85%。在原料油体积空速12 h-1、氢/油体积比500、反应压力6.4 MPa、反应温度分别为280、300、320℃条件下,进行HDS和HDA反应。反应稳定2.5 h后取样。采用Agilent 7890A系列气相色谱仪归一法测定反应原料和产物组成,分别按式(1)~(3)计算4,6-DMDBT的转化率(x(4,6-DMDBT))、1-MN的转化率(x(1-MN))和反应产物i的选择性(Si)。
x(4,6-DMDBT)=
(wo(4,6-DMDBT)-wp(4,6-DMDBT))/wo(4,6-DMDBT)
(1)
x(1-MN)=(wo(1-MN)-wp(1-MN))/wo(1-MN)
(2)
Si=wi/∑wi
(3)
式(1)~(3)中,wo(4,6-DMDBT)、wo(1-MN)分别为原料中4,6-DMDBT和1-MN的质量分数;wp(4,6-DMDBT)、wp(1-MN)分别为反应产物中4,6-DMDBT和1-MN的质量分数;wi为反应产物i的质量分数。
以SDDS表示DDS反应总产物选择性,以SHYD表示HYD反应总产物选择性(等于加氢未脱硫产物和加氢脱硫产物选择性之和)。以SDDS/HYD表示DDS途径的相对选择性,如式(4)所示。
SDDS/HYD=SDDS/SHYD
(4)
为了考察HDS和HDA反应中消耗的H2量,分别按式(5)~(8)计算脱除每摩尔硫的硫化物时消耗的H2量(Hr,平均硫化物氢耗)、硫化物转化消耗的H2总量(Hv,硫化物总氢耗)、芳烃转化消耗的H2总量(Hf,芳烃总氢耗)、脱除每摩尔硫时HDA反应消耗的H2量(Hz,摩尔脱硫芳烃氢耗)。
Hr=∑(Si×Hd/Mie)/∑(Si/Mie)
(5)
Hv=Hr×680×x(4,6-DMDBT)×∑Sie×10-6/32
(6)
Hf=x(1-MN)×MH2×∑(Si×Hd/Miu)
(7)
Hz=Hf×32/(680×x(4,6-DMDBT)×∑Sie)
(8)
式(5)~(8)中,Hd表示生成每摩尔反应产物i消耗的H2的物质的量,Mie、Miu和MH2分别表示HDS产物ie、HDA产物iu和H2的相对分子质量,Sie表示HDS产物ie的选择性。
1.3催化剂表征
1.3.1氧化态催化剂表征
采用Philips XPERT散射仪测定催化剂和载体的XRD谱,CuKα射线,γ=0.154 nm,2θ为5°~70°。采用Jobin Yvon Lab RAM HR UV-NIR型共聚焦显微拉曼光谱仪测定样品的拉曼光谱(Raman)。采用美国Micromeritics公司AutoChemⅡ2920多功能吸附仪进行氧化态催化剂的程序升温还原(H2-TPR)实验,H2/Ar混合气流速50 cm3/min,H2体积分数10%,升温速率10℃/min,升至1000℃。
1.3.2硫化态催化剂TEM表征
在进行TEM表征之前,先在内径为20 mm的微型固定床反应器内对氧化态催化剂进行硫化处理。将1 g颗粒度为40~60目的催化剂置于反应器恒温段内,其余部分装填石英砂,并用石英布隔开。用CS2质量分数为5%的环己烷溶液作为硫化油,在硫化压力6.4 MPa、硫化油流速0.4 mL/min、H2流速365 mL/min的条件下硫化4 h。
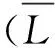
(9)
(10)
式(9)、(10)中,Lm为片晶m的长度;QLm为长度为Lm的片晶总数;Nm为片晶m的堆叠层数;CNm为层数为Nm的片晶的数目;k为统计区域内的条纹总数。
1.3.3硫化态催化剂XPS表征
采用Thermo Fischer-VG ESCALAB 250分光仪测定硫化态催化剂的XPS谱。以MgKα靶作为激发源,分析室压力小于5×10-8Pa,以Al2p(74.4eV)谱峰作为内标,对荷电效应引起的谱峰位移进行校正。分析前的硫化态催化剂浸泡于环己烷溶液中,避免与空气接触氧化。将所得XPS谱进行拟合,获得Mo3d、Co2p、S2p结合能。 采用XPSPEAK Version4.0分别对Mo3d、Co2p能谱进行拟合分峰,根据峰面积计算得到各相应价态Co、Mo含量。根据XPS测定的硫化态催化剂表面上Co、Mo的摩尔分数计算催化剂的表面金属摩尔比,用n′ (Co)/n′ (Co+Mo)表示。
2结果与讨论
2.1Co-Mo/γ-Al2O3催化加氢反应活性
不同n(Co)/n(Co+Mo)的Co-Mo/γ-Al2O3催化HDS活性及HDA活性评价结果示于图1。可以看出,采用n(Co)/n(Co+Mo)为0.3的Co-Mo/γ-Al2O3催化剂,HDS、HDA转化率均达到最大值;反应温度越高,脱硫、脱芳转化率越大。
2.2Co-Mo/γ-Al2O3催化HDS的反应路径选择性
图2给出了不同n(Co)/n(Co+Mo)的Co-Mo/γ-Al2O3催化HDS的DDS途径的相对选择性SDDS/HYD。可以看出,当n(Co)/n(Co+Mo)<0.3时,随着Co-Mo/γ-Al2O3催化剂中n(Co)/n(Co+Mo)增加,SDDS/HYD大幅增加,在n(Co)/n(Co+Mo)为0.3处,SDDS/HYD达到最大值,即直接脱硫途径相对选择性最高;继续增加n(Co)/n(Co+Mo),SDDS/HYD反而缓慢下降。同时,采用同一Co-Mo/γ-Al2O3催化剂时,随着反应温度的提高,SDDS/HYD提高,说明高温有利于硫化物通过DDS途径进行脱硫反应。此外,还可以看出,4,6-DMDBT主要通过HYD途径进行脱硫,DDS途径所占比例较小。催化剂选择性的改变可能是由于催化剂活性中心的类型发生了变化,助剂Co含量的变化可能使得DDS活性中心数目和HYD活性中心数目的比例发生改变。在硫化态催化剂中,一般认为,DDS活性中心为与Co相连的MoS2活性相中心,而未与Co相连的MoS2活性中心为HYD活性中心[16]。因此,随着Co在MoS2边位上的吸附,与Co相连的活性中心数量增加,而HYD活性中心的比例则可能相对降低,最终导致在HDS和HDA过程中反应路径选择性的改变。
2.3Co-Mo/γ-Al2O3催化加氢反应氢耗
不同n(Co)/n(Co+Mo)的Co-Mo/γ-Al2O3催化HDS反应过程中的氢耗,包括硫化物总氢耗、平均硫化物氢耗、芳烃总氢耗和摩尔脱硫芳烃氢耗,如图3所示。可以看出,硫化物总氢耗随着n(Co)/n(Co+Mo)的增加呈现出先增加后降低的趋势,在n(Co)/n(Co+Mo)为0.3时达到最高值,这与催化剂的HDS活性随n(Co)/n(Co+Mo)的变化规律相同。催化剂HDS活性越高,在相同反应条件下脱除的硫化物则越多,因此其硫化物总氢耗也更高。与硫化物总氢耗不同,随n(Co)/n(Co+Mo)增加,平均硫化物氢耗呈现出先降低后增加的趋势,且n(Co)/n(Co+Mo)为0.3时催化剂的平均硫化物氢耗最低,即脱除每摩尔硫时消耗的H2量最少,此时DDS途径选择性最高(见图2),即硫化物更多地通过氢耗较低的DDS途径脱除,因此,平均到脱除每摩尔硫所消耗的H2最低。另外,提高反应温度,催化剂脱除每摩尔硫的氢耗呈现降低趋势,这与催化剂SDDS/HYD随反应温度提高而增加有关。
从图3还可以看出,随着n(Co)/n(Co+Mo)增加,芳烃总氢耗先增加后减小,并在n(Co)/n(Co+Mo)为0.3处达到最大值,这与HDA转化率变化规律相一致。此外,反应温度越高,芳烃总氢耗越大。引入Co以后,摩尔脱硫芳烃氢耗大幅降低,并在n(Co)/n(Co+Mo)为0.3处达到最低值,表明催化剂在脱除每摩尔硫时用于HDA反应的H2量最少,H2的利用效率最高。而且,当反应温度升高时,摩尔脱硫芳烃氢耗降低。这同样可以用SDDS/HYD的变化来解释。当SDDS/HYD较高时,意味着其DDS途径相对选择性较高,HYD途径相对选择性则较低,由于HDA反应机理与HYD途径中的芳环加氢步骤类似,因此脱除每摩尔硫时HDA反应所消耗的H2量也有所降低。
2.4Co-Mo/γ-Al2O3催化剂表征结果
2.4.1XRD表征结果
Co-Mo/γ-Al2O3氧化态催化剂的XRD谱如图4所示。其中,45.6°和66.9°处的衍射峰归属为γ-Al2O3的特征衍射峰[17]。对于n(Co)/n(Co+Mo)<0.3的催化剂而言,除了γ-Al2O3特征峰外没有其它衍射峰出现,说明活性金属在载体中分散均匀,没有生成新的物相。对于n(Co)/n(Co+Mo)为0.4、0.5、0.6的催化剂而言,在26.6°处出现了Co与Mo相互作用生成的β-CoMoO4的特征衍射峰[18]。n(Co)/n(Co+Mo)为0.5、0.6的催化剂在36.9°处还出现了Co3O4的特征衍射峰,且其强度随n(Co)/n(Co+Mo)的增加而变强。β-CoMoO4不能转化为Co-Mo-S活性相,Co3O4则是非活性物种Co9S8的前驱体[19]。这些无活性或者低活性物种的存在,一方面降低了活性金属的利用率,另一方面,当Co含量较高时,Co3O4硫化后生成较大的Co9S8晶粒,可能覆盖或阻塞活性位,导致催化剂活性降低。
2.4.2Raman表征结果
不同n(Co)/n(Co+Mo)的Co-Mo/γ-Al2O3氧化态催化剂的Raman谱示于图5。位于940 cm-1左右的吸收峰归属为六配位Mo物种[20]。金属Mo在催化剂上通常有六配位Mo和四配位Mo 2种存在形态。其中六配位Mo物种易于还原硫化,是Co-Mo催化剂活性的主要来源。由图5可以看出,n(Co)/n(Co+Mo)为0.3的催化剂940 cm-1处峰面积最大,其对应的六配位Mo物种含量应该也最高。n(Co)/n(Co+Mo)增加或减小,六配位Mo物种含量都相应减少,相应的催化剂活性也应该相对降低。这与活性评价结果相一致。此外,对于n(Co)/n(Co+Mo)为0.5、0.6的催化剂,在695 cm-1处出现了Co3O4的特征峰[21],说明Co未能完全与Mo发生作用,多余的Co以氧化物的形式存在于催化剂中,这与XRD表征结果相一致。
2.4.3H2-TPR表征结果
不同n(Co)/n(Co+Mo) 的Co-Mo/γ-Al2O3氧化态催化剂的H2-TPR曲线如图6所示。可以看出,随着n(Co)/n(Co+Mo)增加,高温还原峰和低温还原峰均向低温方向偏移,在n(Co)/n(Co+Mo)为0.3时高温还原峰温度和低温还原峰温度均达到最低值,说明该催化剂中活性金属与载体之间相互作用力最弱。当活性金属与载体之间相互作用力较弱时,CoO、MoO3形成混合相的几率增加,有利于Co、Mo硫化和Co-Mo-S相的形成,相应催化剂活性也较高,这与活性评价结果相一致。
2.4.4XPS表征结果
对不同n(Co)/n(Co+Mo)的硫化态催化剂进行了XPS表征,结果示于图7。参考Qiu等[22]提出的分峰规则对Mo3d图谱进行分峰拟合,拟合结果示于图8。可以看出,Mo3dXPS谱解迭后主要呈现3组Mo3d双峰。第1组双峰出现在229 eV和232.4 eV左右,归属为MoS2中的Mo4+;第2组双峰出现在230.6 eV和233.8 eV左右,归属为氧硫化物中没有完全硫化的Mo5+;第3组双峰出现在232.8 eV和236.0 eV左右,归属为难以被硫化的Mo6+。根据拟合峰峰面积可以计算得到不同n(Co)/n(Co+Mo)催化剂的Mo硫化度。
对硫化态催化剂的Co2pXPS谱同样进行了分峰拟合,拟合结果也示于图8。参考Gandubert等[23]的研究结果,并考虑了电子转移对助剂金属原子电子结合能的影响确定峰位归属。可以看出,Co2pXPS谱解迭后主要呈现3个峰。第1个峰出现在779 eV左右,归属为Co-Mo-S相;第2个峰出现在781 eV左右,归属为Co-O振动峰;第3个峰出现在785 eV左右,归属为Co2+[24]。
对Co-Mo/γ-Al2O3催化剂各物种进行定量分析,结果列于表1。Mo物种硫化度可以用w(Mo4+)/w(Mo)表示。可以看出,随着n(Co)/n(Co+Mo)增加,Co-Mo/γ-Al2O3催化剂中Mo硫化度不断增加,n(Co)/n(Co+Mo)为0.3的催化剂硫化度最高;n(Co)/n(Co+Mo)继续增加,Mo硫化度反而降低。比较催化剂中Mo硫化度和催化剂HDS活性随n(Co)/n(Co+Mo)的变化规律可知,二者变化趋势基本一致。此外,根据XPS方法测定的表面Mo、Co摩尔分数计算了硫化态催化剂的表面金属摩尔比(n′(Co)/n′(Co+Mo)),结果也列于表1。对比n(Co)/n(Co+Mo)可知,当n(Co)/n(Co+Mo)≤0.3时,n′(Co)/n′ (Co+Mo)与n(Co)/n(Co+Mo)基本相同,表明Co原子处于较好的分散状态。当n(Co)/n(Co+Mo)>0.3时,n′(Co)/n′(Co+Mo) 的分散性开始降低,与XRD和Raman表征结果相一致。上述结果表明,在n(Co)/n(Co+Mo)为0.3时,Co-Mo/γ-Al2O3催化剂表面MoS2边角位被Co完全饱和,Co的分散也最好;当n(Co)/n(Co+Mo)继续增加,Co的分散性变差,多余的Co可能以单独的硫化物的形式存在,这种硫化物可能覆盖或阻塞活性位,会造成催化剂活性降低。 根据Co2p谱拟合峰峰面积可以计算Co-Mo-S相在全部Co物种中所占比例,以Co-Mo-S相质量分数与Co物种总质量分数的比值w(Co-Mo-S)/w(Co)表示,结果也列于表1。相对于MoS2活性相而言,Co-Mo-S相具有更高的DDS活性[14]。由表1可以看出,在n(Co)/n(Co+Mo)为0.3处,硫化态催化剂中Co-Mo-S相含量最多,故该催化剂具有最高的HDS活性以及DDS选择性。 2.4.5TEM表征结果 图9给出了不同n(Co)/n(Co+Mo)的硫化态催化剂的TEM照片。可以看出,单Mo催化剂上MoS2片晶数目较少,长度较长;引入助剂Co后,n(Co)/n(Co+Mo)在0.1~0.3范围内,MoS2片晶数量明显增加,其长度缩短,分散更加均匀;当n(Co)/n(Co+Mo)继续增加,MoS2分散性变差;对于n(Co)/n(Co+Mo)为0.6的催化剂,MoS2有明显聚集现象。 统计得到各硫化态催化剂上MoS2片晶的平均长度和平均堆叠层数列于表2。可以看出,引入助剂Co后,催化剂活性相平均片晶长度表现出先缩短后增长的规律,并在n(Co)/n(Co+Mo)为0.3处达到最短。片晶长度越短,活性相暴露的边角活性位越多,催化剂HDS活性越高,这与活性评价结果相一致。 3结论 (1)当n(Co)/n(Co+Mo)≤0.3时,随助剂Co含量增加,金属-载体之间相互作用强度降低,Mo硫化度增加,MoS2片晶平均长度缩短但数量增加,所形成的Co-Mo-S活性相数量也越多。与催化剂的结构性质变化相一致,催化剂的HDS活性、HDA活性、SDDS/HYD以及氢利用率都不断增加。 (2)当n(Co)/n(Co+Mo)>0.3时,MoS2晶粒易发生聚集,Co的分散度降低,并逐渐形成β-CoMoO4和Co氧化物物种,使得催化剂的HDS活性和HDA活性降低,SDDS/HYD降低,Hz增加,H2利用率降低。 (3)Co-Mo-S活性相的数量对Co-Mo/γ-Al2O3催化剂的HDS活性、HDA活性、SDDS/HYD以及H2的利用率具有至关重要的作用。催化剂选择性的改变可能是由于催化剂活性中心的类型发生了变化,助剂Co含量的变化可能使得DDS活性中心数目和HYD活性中心数目的比例产生了改变。 参考文献 [1] 李大东. 加氢处理工艺与工程[M]. 北京: 中国石化出版社, 2004: 120. [2] SARBAK Z. Acidity and catalytic activity of cobalt-molybdena catalyst supported on alumina: The effect of incorporation sequence of sodium and fluoride ions[J]. Applied Catalysis A: General, 1997, 164(1-2): 13-19. [3] 左东华, 谢玉萍, 聂红,等. 4,6-二甲基二苯并噻吩加氢脱硫反应机理的研究ⅠNiW体系催化剂的催化行为[J].催化学报, 2002, 22(3): 271-275.(ZUO Donghua, XIE Yuping, NIE Hong, et al. Study of the reaction mechanism of the hydrodesulferization of 4,6-DMDBT Ⅰ The catalytic behavior of the NiW catalyst[J]. Chinese Journal of Catalysis, 2002, 22(3): 271-275.) [4] EGOROVA M, PRINS R. Hydrodesulfurization of dibenzothiophene and 4,6-dimethyldibenzothiophene over sulfided NiMo/γ-Al2O3, CoMo/γ-Al2O3, and Mo/γ-Al2O3catalysts[J]. Journal of Catalysis, 2004, 225(2):417-427. [5] SHAFI R, HUTCHINGS G J. Hydrodesulfurization of hindered dibenzothiophenes: an overview[J]. Catalysis Today, 2000, 59(3-4): 423-442. [6] 徐永强,刘晨光. 4,6-二甲基二苯并噻吩在Co-Mo/γ-Al2O3上加氢脱硫反应机理的研究[J]. 炼油技术与工程. 2003, 33(8): 21-25.(XU Yongqiang, LIU Chenguang. Study of the reaction mechanism of the hydrodesulferization of 4,6-DMDBT over CoMo/γ-Al2O3[J]. Refining Technology and Engineering, 2003, 33(8):21-25.) [7] GATES B C, TOPSØE H. Reactivities in deep catalytic hydrodesulfurization: challenges, opportunities, and the importance of 4-methyldibenzothiophene and 4,6-dimethyldibenzothiophene[J]. Polyhedron, 1997, 16(18): 3213-3217. [8] KABE T, ISHIHARA A, TAJIMA H. Hydrodesulfurization of sulfur-containing polyaromatic compounds in light oil[J]. Industrial & Engineering Chemistry Research, 1992, 31(6): 1577-1580. [9] MA X, SAKANISHI K, MOCHIDA I. Hydrodesulfurization reactivities of various sulfur compounds in vacuum gas oil[J]. Industrial & Engineering Chemistry Research, 1996, 35(8): 2487-2494. [10] BATAILLE F, LEMBERTON J L, PÉROT G, et al. Sulfided Mo and CoMo supported on zeolite as hydrodesulfurization catalysts: Transformation of dibenzothiophene and 4,6-dimethyldibenzothiophene[J]. Applied Catalysis A: General, 2001, 220(1): 191-205.[11] STANISLAUS A, COOPER B H. Aromatic hydrogenation catalysis: A review[J]. Catalysis Reviews-Science and Engineering, 1994, 36(1): 75-123. [12] 李明,肖风良,赵战东. 影响蜡油加氢处理装置氢耗因素的分析[J]. 炼油技术与工程, 2013, 42(10): 24-26.(LI Ming, XIAO Fengliang, ZHAO Zhandong. Analysis of the factors influencing the hydrogen consumption of the hydrotreating device of the wax oil[J]. Refining Technology and Engineering, 2013, 42(10): 24-26.) [13] 王刚,赵野,胡胜,等. 新一代DZD-1柴油加氢精制催化剂的研制[J]. 工业催化, 2003, 11(10): 12-18.(WANG Gang, ZHAO Ye, HU Sheng. The development of the new generation of DZD-1 diesel oil hydrofining catalyst[J]. Industrial Catalysis, 2003, 11(10): 12-18.) [14] 何鸣元. 石油炼制和基本有机化学品合成的绿色化学[M]. 北京: 中国石化出版社, 2005: 189.[15] NIKULSHIN P A, MOZHAEV A V, PIMERZIN A A, et al. CoMo/Al2O3catalysts prepared on the basis of Co2Mo10-heteropolyacid and cobalt citrate: Effect of Co/Mo ratio[J]. Fuel, 2012, 100(4): 24-33. [16] BATAILLE F, LEMBERTON J, MICHAUD P, et al. Alkyldibenzothiophenes hydrodesulfurization-promoter effect, reactivity, and reaction mechanism[J]. Journal of Catalysis, 2000, 191(2): 409-422. [17] 鲁佳,马磊,江大好,等.γ-Al2O3载体孔结构对负载钯催化剂催化C9石油树脂加氢性能的影响[J]. 石油化工, 2011,40(10): 1105-1109.(LU Jia, MA Lei, JIANG Dahao, 等. The influence of the structure of theγ-Al2O3support on the hydrotreating property of the C9petroleum resin of the Pd catalyst[J]. Petrochemical Technology, 2011,40(10): 1105-1109.) [18] KIM D W, LEE D K, IHM S K. CoMo bimetallic nitride catalysts for thiophene HDS[J]. Catalysis Letters, 1997, 43(1-2): 91-95. [19] WIVEL C, CLAUSEN B S, CANDIA R. Mssbauer emission studies of calcined Co-Mo/Al2O3catalysts: Catalytic significance of Co precursors[J]. J Catal, 1984, 87(2): 497-513. [20] 袁蕙,徐广通, 齐和日玛,等. 激光拉曼光谱在加氢脱硫催化剂Co-Mo/Al2O3中的应用研究[J]. 光谱学与光谱分析, 2014, 34(2): 435-438.(YUAN Hui, XU Guagntong, Qiherima. The application of the Laser Raman spectroscopy in the study of the Co-Mo/Al2O3[J]. Spectroscopy and Spectral Analysis, 2014, 34(2): 435-438.) [21] XIAO T, YORK A P E, AL-MEGREN H, et al. Preparation and characterisation of bimetallic cobalt and molybdenum carbides[J]. Journal of Catalysis, 2001, 202(1): 100-109. [22] QIU L, XU G. Peak overlaps and corresponding solutions in the X-ray photoelectron spectroscopic study of hydrodesulfurization catalysts[J]. Applied Surface Science, 2010, 256(11): 3413-3417. [23] GANDUBERT A D, KREBS E, LEGENS C, et al. Optimal promoter edge decoration of CoMoS catalysts: A combined theoretical and experimental study[J]. Catalysis Today, 2008, 130(1): 149-159. [24] 邱丽美,齐和日玛, 刘清河,等. X射线光电子能谱法研究加氢脱硫催化剂中活性元素的化学态[J]. 石油学报(石油加工), 2011, 17(4): 638-642.(QIU Limei, Qiherima, LIU Qinghe,et al. Study of the chemical state of the active elements in the HDS catalyst by the X-ray photoelectron spectroscopy[J].Acta Petrolei Sinica (Petroleum Processing Section), 2011, 17(4): 638-642.) Influence of the Promoter of Co-Mo/γ-Al2O3on the Hydrogen Consumption in Hydrodesulfrization Reaction CHEN Shuo, LONG Xiangyun, CHEN Wenbin, NIE Hong (ResearchInstituteofPetroleumProcessing,SINOPEC,Beijing, 100083) Key words:n(Co)/n(Co+Mo); hydrodesulfurization; hydrodearomatization; activity; selectivity; hydrogen consumption Abstract:The hydrodesulfurization of 4,6-dimethyldibenzothiophene was studied in the presence of 1-methylnaphthalene in order to investigate the influence of then(Co)/n(Co+Mo) in Co-Mo/γ-Al2O3catalyst on the activity of the catalyst, and the selectivity and hydrogen consumption in hydrodesulfurization. The oxidic Co-Mo/γ-Al2O3were characterized by H2-TPR, XRD, Raman and the sulfided Co-Mo/γ-Al2O3were characterized by TEM, XPS. The results indicated that whenn(Co)/n(Co+Mo) equaled to 0.3, the metal-support interaction in the oxidic catalysts was weakest, the proportion of the Co-Mo-S phase in the sulfide catalyst and the sulfidation degree reached the highest level, and the average length of the MoS2slabs was shortest. Accordingly, the activity and the direct desulfurization selectivity reached the maximum, whereas the average hydrogen consumption of one mole removed sulfur and the average hydrogen consumption of the aromatics of one mole removed sulfur reached the lowest level. The type of the active phase and especially the amount of the Co-Mo-S phase were the important factors affecting the activity, selectivity and the utility efficiency of the hydrogen. 收稿日期:2015-03-05 基金项目:国家重点基础研究发展“973”计划项目(2012CB224802)基金资助 文章编号:1001-8719(2016)02-0244-10 中图分类号:TE624.431+TQ426.98 文献标识码:A doi:10.3969/j.issn.1001-8719.2016.02.004 第一作者: 陈硕,男,硕士研究生,从事柴油加氢催化剂的研究;Tel: 010-82368083;E-mail:chenshuo.ripp@sinopec.com 通讯联系人: 陈文斌,男,高级工程师,博士,从事柴油加氢催化剂的研究;Tel:010-82368120;E-mail:chenwb.ripp@sinopec.com
