三疣梭子蟹腺苷酸转移酶(ANT)基因的克隆与分析
2016-06-23李冰玥朱冬发邱锡尔周彦琦柳志业谢熙
李冰玥 朱冬发 邱锡尔 周彦琦 柳志业 谢熙
(宁波大学海洋学院,宁波 315211)
三疣梭子蟹腺苷酸转移酶(ANT)基因的克隆与分析
李冰玥 朱冬发 邱锡尔 周彦琦 柳志业 谢熙
(宁波大学海洋学院,宁波 315211)
腺苷酸转移酶(Adenine nucleotide translocase,ANT)是线粒体内膜上负责能量分子传导的转运蛋白,在能量代谢中起着关键作用。为了研究ANT基因在甲壳动物蜕皮中的作用,采用RT-PCR和cDNA末端快速扩增技术(RACE技术)克隆得到三疣梭子蟹ANT基因的序列全长(GenBank登录号:KM921660),该序列全长1 414 bp,包括132 bp的5'端非编码区,352 bp的3'段非编码区,具有930 bp的完整开放阅读框(ORF),编码309个氨基酸。将该ANT基因序列推导的氨基酸序列与已公布的其他物种ANT序列进行系统进化树分析发现,三疣梭子蟹ANT基因与其他甲壳动物ANT基因聚为一支,其中与拟穴青蟹ANT一致性高达96%。通过氨基酸序列比对发现,三疣梭子蟹ANT序列具有3个保守的线粒体穿膜功能结构域,是形成能量分子传导的转运通道,催化细胞质中ADP和线粒体内ATP间进行跨膜交换。采用实时荧光定量PCR技术,分析三疣梭子蟹ANT基因的组织差异表达,结果表明ANT基因在三疣梭子蟹肌肉(Ms)中的表达量最高,在其他组织中表达量均较低,具显著差异(P<0.05);在三疣梭子蟹蜕皮周期中,肌肉中ANT基因的表达量A期最高(P<0.05),然后下降,至C期最低,随后又逐渐上升至D1期,在D1期出现第2个峰值后再逐渐下降。研究结果说明ANT基因与三疣梭子蟹肌肉活动密切相关,可能在蜕皮调控中发挥重要作用。
三疣梭子蟹;腺苷酸转移酶;克隆;能量转运;表达水平
腺苷酸转移酶(Adenine nucleotide translocase,ANT)属于真核细胞线粒体内膜上的转运蛋白家族成员[1-3],作为代谢物载体参与线粒体的各种活动[2,4,5]。ANT在线粒体内膜上分布最为丰富,约占细胞线粒体总蛋白的1%-10%[6],其主要功能是催化细胞质中ADP和线粒体内ATP间进行跨膜交换,是保持细胞内能量平衡的关键成分[7]。近年来的研究表明,ANT 在线粒体内膜的穿膜孔洞的形成和细胞凋亡诱导过程中起重要作用[8-10],是各种细胞凋亡因子或凋亡抑制因子的作用靶位[11-14]。生物体大约1/3-1/2的基础电子传递由ANT催化,它是保持细胞内能量代谢的关键蛋白[15,16],另也有研究表明,ANT 参与了肿瘤坏死因子诱导的细胞凋亡[17]。
ANT 蛋白通过两个分别含有ATP/ADP 结合位点的亚基的构象变化来实现细胞质中ADP和线粒体内ATP 间的跨膜交换[18],是生物体内能量产生和消耗的重要连接[19]。大多数真核生物至少有2个不同的ANT基因[16],目前已从凡纳滨对虾(Litopenaeus vannamei)、斑节对虾(Penaeus monodon)、拟穴青蟹(Scylla paramamosain)等甲壳动物中克隆到其同源基因,它们在进化上高度保守。但至今尚未见三疣梭子蟹ANT基因的相关报道。
三疣梭子蟹(Portunus trituberculatus)是我国沿海的重要经济蟹类,蜕皮是甲壳动物蜕去旧的外骨骼,个体增大后新甲壳迅速硬化为外骨骼的过程。但是,到目前为止,对其蜕皮发生的机制仍然不是很清楚,特别是其蜕皮周期的分子调控机理。因此,本研究克隆了三疣梭子蟹ANT的cDNA序列,并对其组织差异表达和蜕皮周期中的表达变化进行了分析,旨在对阐明三疣梭子蟹蜕皮的分子调控机理提供一定的基础数据。
1 材料与方法
1.1 材料
实验取材的三疣梭子蟹暂养于宁波市宁海县得水育苗场。采用形态观察法将三疣梭子蟹的蜕皮周期分为蜕皮后期(A期和B期)、蜕皮间期(C期)、蜕皮前期(D0、D1、D2、D3和D4亚期)和蜕皮期(E期)4个阶段[20]。解剖取C期三疣梭子蟹大颚器、Y器、肌肉、脑、心脏、眼柄、胸神经节、肠、表皮和肝胰腺用于组织表达差异性分析,采集各期(除E期外)三疣梭子蟹肌肉组织进行蜕皮周期中ANT基因的表达差异变化分析。蜕皮周期各期均选取4只螃蟹做平行实验,由于E期的时间较短不利于采集到适合做统计分析的样本,故只采集了其他各期的样本。解剖获得的新鲜组织暂时浸泡于RNA保护液(生工生物工程(上海)有限公司)中,置于-20℃暂存。
1.2 方法
1.2.1 总RNA的提取 将保存在RNA保护液中的样品转移至Trizol(生工生物工程(上海)有限公司)溶液中,按说明书所述步骤提取各个样品中的总RNA。
1.2.2 cDNA的合成 取Ms组织提取的总RNA,按 照 PrimeScriptRTreagent Kit(Perfect Real Time,TaKaRa)试剂盒说明书步骤,反转录得到第一链cDNA。3'-RACE扩增所需的3'-RACE-cDNA以AP(表1)为接头引物,参照上述方法反转录获得;5'-RACE扩 增 所 需 的5'-RACE-cDNA按 照SMARTerTMRACE cDNA Amplification Kit试剂盒说明书合成。cDNA均置于-20℃下保存备用。
1.2.3 三疣梭子蟹ANT基因核心片段的扩增 根据NCBI已公布的甲壳动物ANT核苷酸序列,利用primer5.0软件设计并筛选出一对引物ANT-F,ANT-R(表1)。以第一链cDNA为模板,进行PCR扩增(体系为25 μL,扩增条件:95℃预变性5 min;95℃ 50 s,57℃ 50 s,72℃ 50 s,34个循环;72℃充分延伸5 min,反应结束)。扩增产物经过电泳、琼脂糖凝胶回收并纯化,与pMD18-T载体连接再转入E.coli DH5α感受态细胞。经过菌落PCR检测后挑选阳性克隆菌落,扩大培养后将菌液送至生工生物工程(上海)有限公司测序。
1.2.4 三疣梭子蟹ANT基因3'RACE和5' RACE的扩增 根据已测得的核心序列和AP接头分别设计特异性引物ANT-3F1、ANT-3F2、ANT-3F3和3'outer、3'inner(表1),进行巢氏PCR扩增。第一轮PCR以3'RACE-cDNA为 模 板,ANT-3F1、ANT-3F2和3'outer为上下游引物进行PCR扩增(体系为25 μL,扩增条件:95℃预变性5 min;95℃ 50 s,56℃ 50 s,72℃ 50 s,34个循环;72℃充分延伸5 min,反应结束)。第二轮以第一轮扩增产物为cDNA模板,ANT-3F2、ANT-3F3和3'inner为上下游引物进行PCR扩增(体系为25 μL,扩增条件:95℃预变性5 min;95℃ 50 s,57℃ 50 s,72℃ 50 s,34个循环;72℃充分延伸5 min,反应结束)。
3'RACE产物的测序结果,按照SMARTerTMRACE cDNA Amplification Kit 说明合成5' RACE-cDNA并设计下游特异性引物ANT-5R1、ANT-5R2、ANT-5R3,以5'outer、5'inner(表1)为上游引物,同理进行两轮PCR扩增。后续操作参照1.2.3。

表1 PCR引物序列
1.2.5 序列分析 利用Vector NTI 10.0测序软件将核心序列和3'RACE和5'RACE的测序结果进行拼接,获得三疣梭子蟹ANT基因的cDNA全长。利用NCBI 在线ORF Finder工具确定ANT基因的开放阅读框(ORF)序列,并翻译成氨基酸序列;利用ClustalX软件将该氨基酸序列与已公布的ANT氨基酸序列进行同源性比对分析,并用MEGA 4.0软件构建系统进化树;利用ExPASy Proteomics Server(http://ca.expasy.org/)所提供的ProtParam tool蛋白质分析软件分析氨基酸序列;使用Signal 3.0 Server(http:// www.cbs.dtu.dk/services/SignalP)预测信号肽,TMHMM在 线 工 具 (http://www.cbs.dtu.dk/services/ TMHMM/)预测氨基酸跨膜区域。
1.2.6 实时荧光定量(qRT-PCR) 取需要的组织利用与1.2.1相同的 Trizol 法抽取总RNA后,取1.0 μg RNA用 PrimeScript Rtreagent Kit(Perfect Real Time)试剂盒反转录得到cDNA。根据 ANT cDNA 全长设计一对特异性引物ANTYG-F1和ANTYG-F2(表1)检测ANT基因在不同组织中的表达量,以β-actin作为内参。qRT-PCR的反应条件:95℃ 2 min;95℃ 5 s,55.3℃ 20 s,68℃ 20 s,共40个循环;95℃ 15s,55℃ 15 s,升温25 min,95℃ 15 s。用SPSS17.0统计分析软件对获得的数据进行分析。
2 结果
2.1 三疣梭子蟹ANT基因cDNA全长与序列分析
基于ANT基因的同源核苷酸序列,利用primer5.0设计两对引物ANT-F和ANT-R进行PCR克隆得到1 091 bp的核心序列。3'RACE 以ANT-3F1、ANT-3F2、ANT-3F3和 3'outer、3'inner为 引物,扩增获得903 bp的3'端片段;5'RACE以ANT-5R1、ANT-5R2、ANT-5R3和5'outer、5'inner为引物,扩增得535 bp的5'端片段。通过拼接后获得总长为1 414 bp的ANT序列cDNA全长,GenBank登录号:KM921660。5'端非编码区为132 bp,3'端非编码区为352 bp,开放阅读框(ORF)长度为930 bp,编码309个氨基酸。利用ExPASy网站在线ProtParam tool预测其分子式为C4185H6958N1414O1752S351,分子量大小约为116 368.7 Da,预测等电点为4.98,富含Gly(27.9%)、Cys(24.8%)、Thr(23.8%)、和Ala(23.5%)等。不稳定系数为42.42,说明三疣梭子蟹ANT蛋白并不稳定。该氨基酸亲水性总和G RAVY(Gran d average of hydropathicity)为0.765,属于亲水性蛋白。
在线Signal软件(http:// www.cbs.dtu.dk/ser vices/ SignalP)对其编码区氨基酸序列进行分析,未 发现有信号肽,说明三疣梭子蟹ANT不属于分泌蛋白。在线TMHMM工具分析发现该氨基酸序列没有跨膜结构。NCBI在线Conserved Domain Search工具对氨基酸序列进行结构域分析,发现ANT蛋白具有3个重复的同源的线粒体跨膜结构域,分别在第148-441位、466-756位、754-1044位(图1)。在NCBI上将该序列编码区氨基酸序列进行BLAST搜索比对,BLAST结果发现,与已公布的其他物种ANT氨基酸序列相比,PtANT与拟穴青蟹(S. paramamosain)的ANT一致性最高,达到96%,与凡纳滨对虾(L. vannamei)、斑节对虾(P. monodon)和日本囊对虾(M. japonicus)的ANT也均达到90%左右,与昆虫和脊椎动物的ANT也有较高的一致性,达到68%以上(图2)。从NCBI蛋白序列数据库中选取具有代表性的甲壳动物、昆虫和脊椎动物ANT氨基酸序列,用MEGA 4.0软件的邻位法(Neighbor-Joining)构建系统进化树,设置重复次数(Replications)为1 000。从进化树结果(图3)来看,三疣梭子蟹与拟穴青蟹亲缘关系最近,而后与凡纳滨对虾、斑节对虾、日本囊对虾等甲壳动物聚为一支;肩突硬蜱(Ixodes scapularis)、黑腹果蝇(Drosophila melanogaster)等昆虫聚为一大支后与脊椎动物的ANT1、ANT2、ANT3三种亚型聚为一大支,最后脊椎动物的ANT4亚型单独聚为一支,符合生物进化上的地位关系。

图1 三疣梭子蟹ANT全长cDNA核苷酸序列和编码区氨基酸序列
2.2 ANT基因在三疣梭子蟹不同组织中的表达差异分析
采用荧光定量PCR检测了三疣梭子蟹ANT基因在心脏、肝胰腺、表皮、胸腺神经节、脑、肌肉、Y器、眼柄、大颚器和肠共10个组织中的表达相对量。结果(图4)显示,该基因在肌肉(Ms)中的表达量最高(P<0.05),大颚器等9种组织中的表达量均较低。
文中在研究Minimax算法的基础上,通过将Minimax算法转化为可以求解的非线性规划问题对多口径多波束反射面天线进行赋形。为说明问题,设定参数建模设计了一个四口径多波束天线,将口径面的相位值作为优化对象,由口径场法根据口径面的电场值和设定的相位值,求得远区场的场值。将其中的边缘波束增益和副瓣电平值作为目标函数,通过优化得到赋形后的口径面相位值,然后离散化反射面得到赋形后反射面上任一点的位置信息,得到重构后的反射面,从而达到提高天线C/I值的目的。赋形后的反射面其C/I值相比于赋形前提高2 dB,达到了比较好的目的,具有一定的工程应用的价值。
2.3 ANT基因在蜕皮周期的表达水平分析
组织表达结果显示,ANT基因在三疣梭子蟹Ms中表达量最高,所以选择Ms为实验材料进行ANT基因在蜕皮周期中的表达水平变化分析。qRT-PCR的结果(图5)表明三疣梭子蟹Ms中的ANT基因在整个蜕皮周期中均有表达,在蜕皮A期最高,降低至C期最低,再逐渐升高在D1期达到第二个小高峰,随后又逐渐下降,最终在D4期降至最低。

图2 三疣梭子蟹与其它物种ANT氨基酸序列多重比对结果
3 讨论
线粒体是细胞内主要的ATP生产中心,ANT在催化细胞质中ADP和线粒体内ATP进行跨膜交换时起着重要的作用,是保持细胞内能量平衡的关键成分。本实验克隆得到了三疣梭子蟹ANT的全长cDNA序列(PtANT),该序列全长1 414 bp,包含一个930 bp的开放阅读框(ORF),编码309个氨基酸。PtANT主要由3个同源的线粒体跨膜结构域组成,分别在其第6-104位、113-209位和208-305位,每个结构域含2个跨膜区。这与目前已知许多物种的腺苷酸转移酶具有相似的结构功能域。BLAST结果发现,与已公布的其他物种ANT氨基酸序列相比,PtANT与拟穴青蟹的ANT一致性最高,达到96%,与凡纳滨对虾、斑节对虾和日本囊对虾的ANT也均达到90%左右,与昆虫和脊椎动物的ANT也有较高的一致性,达到68%以上。该结果表明各物种间的ANT具有良好的一致性,各物种ANT可能具有相似的功能。值得注意的是,进化树结果显示哺乳动物的ANT4单独聚为一大支,而其他ANT亚型则与甲壳及昆虫的ANT聚在一起,这说明本研究克隆得到的PtANT以及现有甲壳动物及昆虫的ANT应该不属于ANT4,但PtANT究竟属于其他一种ANT还有待进一步研究。
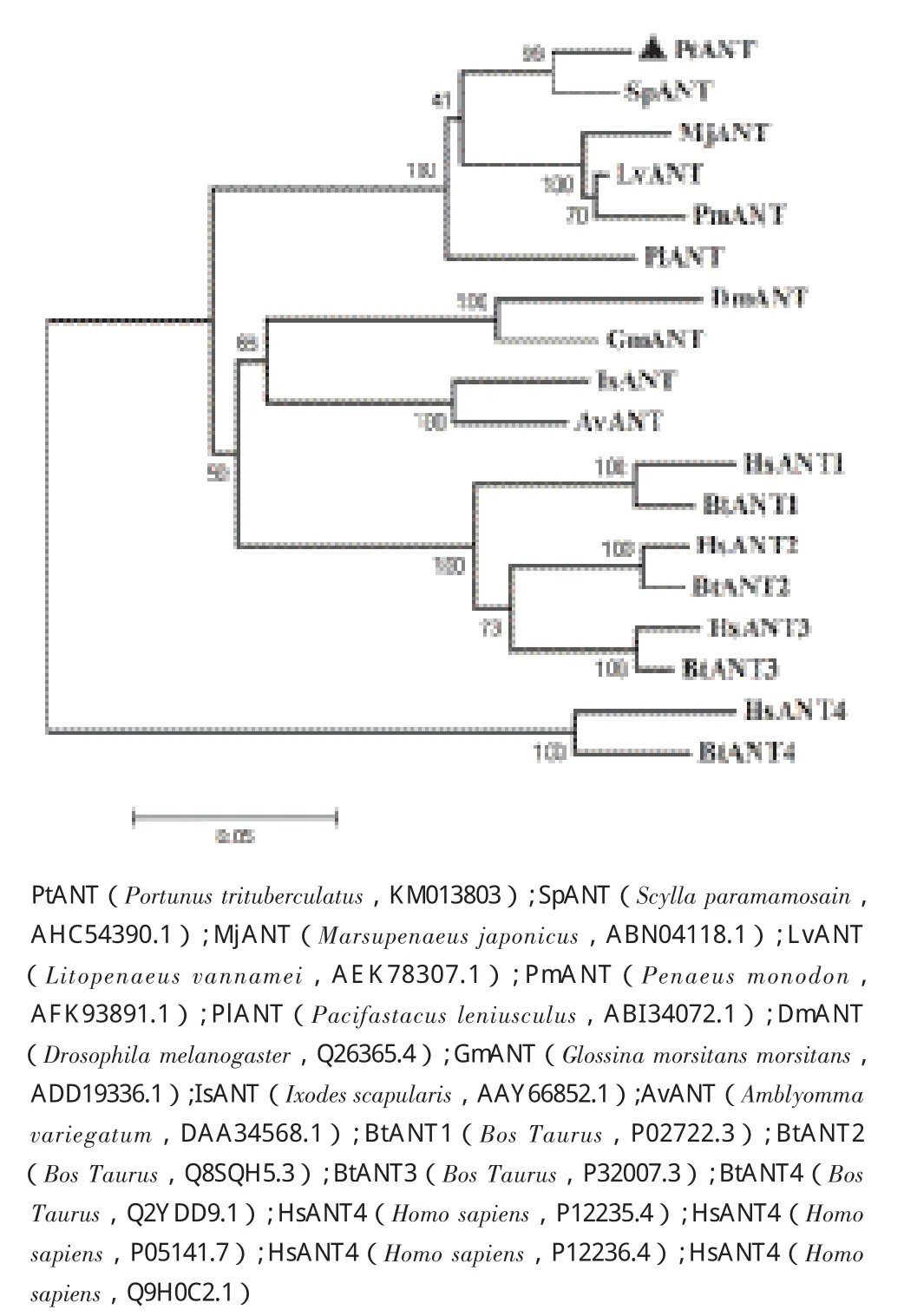
图3 三疣梭子蟹ANT氨基酸序列系统进化树
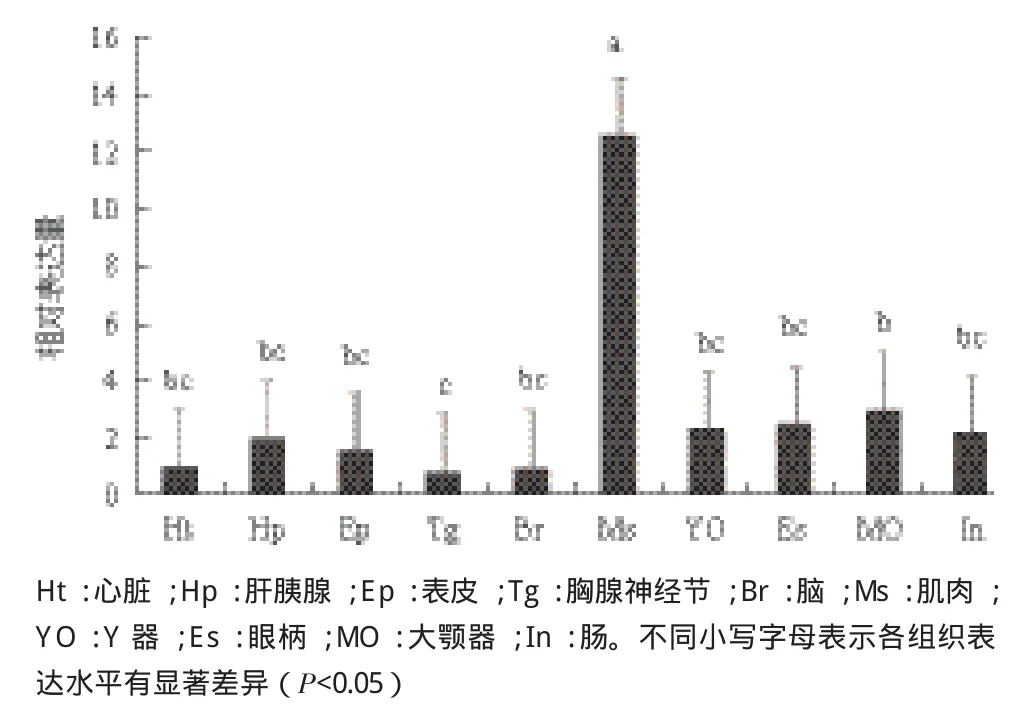
图4 ANT基因在三疣梭子蟹各组织中的相对表达水平
组织表达结果显示PtANT在三疣梭子蟹各个组织中均有表达,其在肌肉中表达量最高,显著高于其他各个组织。这可能与肌肉对线粒体提供的能量需求较大有关,再一次表明了ANT在保持细胞内能量平衡时的重要作用。该结果与孙文文等[20]在研究斑节对虾ANT(PmANT)的结果相似。但斑节对虾中PmANT在心脏中也有很高的表达,拟穴青蟹的ANT也在心脏中表达量最高,而本研究中PtANT在心脏中表达水平较低,这表明本研究克隆获得的PtANT与斑节对虾及拟穴青蟹的ANT在功能上可能并不一致。
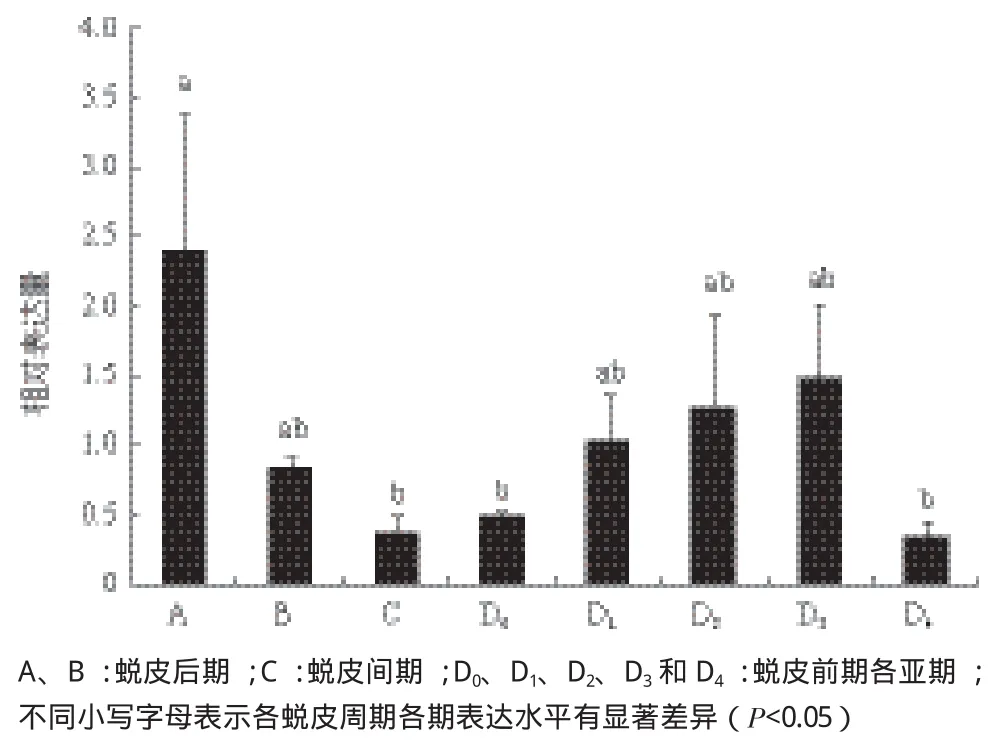
图5 Ms中ANT基因在三疣梭子蟹蜕皮周期中的相对表达差异
肌肉中的ANT基因在三疣梭子蟹蜕皮周期中的表达也有所差异。三疣梭子蟹ANT在蜕皮A期转录水平最高,这可能与三疣梭子蟹刚完成蜕皮过程有关。三疣梭子蟹蜕皮时肌肉消耗了大量能量;另一方面在蜕皮后仍需要继续吸水增大体积[21],还要消耗较多的能量,腺苷酸转移酶的表达量也就相对较高。而在蜕皮间期(C期),三疣梭子蟹体内的含水量下降,营养物质开始积累,为下一次的蜕皮做物质准备,此时因为新表皮还没有形成,能量消耗较少,所以ANT的表达量最低。D0期时,新壳开始分泌但还未成形,ANT的表达量开始逐渐升高,并保持在一个较高水平,从D1到D3,都处于新壳在不断分泌的过程,所以腺苷酸转移酶的相对表达量都较C期有所升高,为新表皮的生成提供所需的能量。
4 结论
本研究克隆了三疣梭子蟹ANT基因的cDNA全长,其氨基酸序列与拟穴青蟹的同源性最高。该基因在三疣梭子蟹心脏、肝胰腺、表皮、胸腺神经节、大脑、肌肉、Y器、眼柄、大颚器、肠组织中均有表达,在肌肉组织中的表达量最高。ANT基因在蜕皮后期A期中表达量最高,在蜕皮间期C期中表达量最低。说明ANT基因可能在蜕皮周期的能量转运中起着重要的作用。
[1]Monica S, Cecilia L, Cecilia S. The evolution of the adenine nucleotide translocase family[J]. Gene, 2004, 333:51-59.
[2]Bof M, Brandolin G, Satre M, et al. The mitochondrial adenine nucleotide translocator from Dictyostelium discoideum, functional characterization and DNA sequencing[J]. Eur J Biochem, 1999, 259(3):795-800.
[3]Martin DB, Julian LP, Augustine O, et al. The basal proton conductance of mitochondria depends on adenine nucleotide translocase content[J]. Biochem J, 2005, 392:353-362.
[4]Santamaria M, Lanave C, Saccone C. The evolution of the adenine nucleotide translocase family[J]. Gene, 2004, 333:51-59.
[5]Brand MD, Pakay JL, Ocloo A, et al. The basal proton conductance of mitochondria depends on adenine nucleotide translocase content[J]. Biochemical Journal, 2005, 392:353-362.
[6]Niu BL, Weng HB, He LH, et al. Cloning and analysis of adenine nucleotide translocase gene in Helicoverpa armigera[J]. Hereditas, 2008, 30(1):81-86.
[7]Atlante A, Bobba A, De Bari L, et al. Caspase-dependent alteration of the ADP/ATP translocator triggers the mitochondrial permeability transition which is not required for the low-potassium-dependent apoptosis of cerebellar granule cells[J]. J Neurochem, 2006, 97(4):1166-1181.
[8]Walther T, Tschöpe C, Sterner-Kock A, et al. Accelerated mitochondrial adenosine diphosphate/adenosine triphosphate transport improves hypertension-induced heart disease[J]. Circulation, 2007, 115(3):333-344.
[9]Halestrap A. Biochemistry:a pore way to die[J]. Nature, 2005, 434:578-579.
[10]Kantrow SP, Tatro LG, Piantadosi CA. Oxidative stress and adenine nucleotide control of mitochondrial permeability transition[J]. Free Radical Biology and Medicine, 2000, 28(2):251-260.
[11]Garcia N, Mart Nez-abundis E, Pav NN, et al. Copper induces permeability transition through its interaction with the adenine nucleotide translocase[J]. Cell Biological International, 2007, 31(9):893-899.
[12]Monkkonen H, Auriola A, Lehenkari P, et al. Anew endogenous ATP analog(ApppI)inhibits he mitochondrial adenine nucleotide translocase(ANT)and is responsible for the apoptosis induced by nitrogen-containing bisphosphonates[J]. British Journal of Pharmacology, 2006, 147:437-445.
[13]Atlante A, Bobba A, De Bari L, et al. Caspasedependent alteration of the ADP/ATP translocator triggers the mitochondrial permeability transition which is not required for the low-potassium-dependent apoptosis of cerebellar granulecells[J]. Journal of Neurochemistry, 2006, 97(4):1166-1181.
[14]Klingebberg M. Transport viewed as a catalytic process[J]. Biochimie, 2007, 89(9):1042-1048.
[15]Zhang YQ, Roote J, Brogna S, et al. Stress sensitive Bencodes an adenine nucleotide translocase in Drosophila melanogaster[J]. Genetics, 1999, 153(2):891-903.
[16]Brustovetsky N, Klingenberg M. Mitochondrial ADP/ATP carrier can be reversibly converted into a large channel by Ca2+[J]. Biochemistry, 1996, 35:8483-8488.
[17]Yang Z, Cheng W, Hong L, et al. Adenine nucleotide(ADP/ATP)translocase 3 participates in the tumor necrosisfactor induced apoptosis of MCF-7 cells[J]. Molecular Biology of the Cell, 2007, 18(11):4681-4689.
[18]Thuswaldner S, Lagerstedt J O, Rojas-Stutz M, et al. Identification, expression, and functional analyses of a thylakoid ATP/ADP carrier from Arabidopsis[J]. Journal of Biochemistry, 2007, 282:8848-8859.
[19]Doerner A, Pauschinger M, Badorff A, et al. Tissue-specific transcription pattern of the adenine nucleotide translocases isoforms in humans[J]. FEBS Letters, 1997, 414:258-262.
[20]孙文文, 周发林, 黄建华, 等. 斑节对虾腺苷酸转移酶(PmANT)基因的cDNA 克隆与表达分析[J]. 上海海洋大学学报, 2013, 22(1):7-16.
[21]沈洁, 朱冬发, 胡则辉, 等. 三疣梭子蟹蜕皮周期的分期[J].水产学报, 2001, 35(10):1481-1487.
(责任编辑 李楠)
Cloning and Analysis of Gene for Adenine Nucleotide Translocase in Portunus trituberculatus
LI Bing-yue ZHU Dong-fa QIU Xi-er ZHOU Yan-qi LIU Zhi-ye XIE Xi
(School of Marine Sciences,Ningbo University,Ningbo 315211)
Adenine nucleotide translocase(ANT)is a transport protein responsible for the conduction of energy molecules in the inner membrane of mitochondria,playing a vital role in the energy metabolism. In order to study the role of ANT gene in the molting of crustacean,a full-length cDNA of ANT gene(GenBank access number:KM921660)was cloned from Portunus trituberculatus using RT-PCR and RACE. Sequence analysis showed that it was 1 414 bp long,including a 132 bp 5' non-coding region,a 352 bp 3' non-coding region,and a 930 bp coding region,and encoded 309 amino acids. The phylogenetic comparison of ANT gene sequence between P. trituberculatus and other species revealed that ANT gene from P. trituberculatus and other species clustered as one same branch,and the similarity with Scylla paramamosain was up to 96%. Amino acid alignment proved that it had 3 conserved mitochondrial transmembrane domains,forming a channel for the conduction of energy molecules,and catalyzing transmembrane exchange between ATP in mitochondria and ADP in cytoplasm. Real-time PCR results indicated that ANT gene expressed in all 10 different tissues with the highest expression in muscle,while quite low in all other tissues,and there were significant differences among the expressions of the tissues(P<0.05). During the whole molting process,the level of ANT in muscle reached the maximum at postmolt(stage A),then began to decline until the least during intermolt(stage C),and then gradually rose until the second peak at stage D1,then declined again. The combined result indicated that ANT gene was closely correlated with the activity of muscle of P. trituberculatus,and might play an essential role in the molting.
Portunus trituberculatus;ADP/ATP translocases(ANT);clone;energy transportation;expression level
10.13560/j.cnki.biotech.bull.1985.2016.05.016
2015-06-08
国家自然科学基金项目(41376152),浙江省自然科学基金项目(LY13C190006)
李冰玥,女,研究方向:甲壳动物发育生物学;E-mail:15757828736@163.com
朱冬发,男,博士,教授,研究方向:甲壳动物发育生物学;E-mail:zhudongfa@nbu.edu.cn
