修饰性肽核酸的细胞转运
2016-06-23刘春冬王建华曾芳重庆大学生物工程学院重庆400044
刘春冬,王建华,曾芳重庆大学 生物工程学院,重庆 400044
修饰性肽核酸的细胞转运
刘春冬,王建华,曾芳
重庆大学 生物工程学院,重庆 400044
刘春冬, 王建华, 曾芳. 修饰性肽核酸的细胞转运. 生物工程学报, 2016, 32(3): 292–305.
Liu CD, Wang JH, Zeng F. Cellular delivery of modified peptide nucleic acids: a review. Chin J Biotech, 2016, 32(3): 292–305.
摘 要:肽核酸是人工合成的寡核苷酸类似物,以N-(2-氨乙基) 甘氨酸结构单元替代DNA分子中的戊糖-磷酸结构。与天然核酸相比,肽核酸可以更高效地与DNA或RNA特异性杂交,在分子生物学和基因药物领域具有良好的应用前景。但是,肽核酸骨架呈电中性,难以高效穿过细胞膜,这成为工程应用的最大障碍。为了改善肽核酸的细胞转运性能,对肽核酸进行化学修饰是近年来的研究热点。结合近十年来文献报道和本实验室的工作,对肽核酸的骨架修饰和配合物结合修饰两类增强细胞转运的修饰方法进行综述,并对修饰性肽核酸细胞转运研究中存在的问题以及未来的研究趋势及其应用提出了见解。
关键词:肽核酸,修饰,细胞转运
Received: June 15, 2015; Accepted: August 31, 2015
Supported by: The Natural Science Major Project of Chongqing Natural Science Foundation (No. cstc2013jjB0011), Chongqing Application Development Project (No. cstc2013yykfB10013), Agricultural Science and Technology Achievements Funds of Sichuan Province (No. 14NZ0027-1).
重庆市自然科学基金重点项目 (No. cstc2013jjB0011),重庆市应用开发计划项目 (No. cstc2013yykfB10013),四川省农业科技成果转化资金项目 (No. 14NZ0027-1) 资助。
网络出版时间:2015-09-17 网络出版地址:http://www.cnki.net/kcms/detail/11.1998.Q.20150917.1533.001.html
1991年,丹麦哥本哈根大学生物化学家Nielsen等[1]通过计算机设计,首次提出了肽核酸 (Peptide nucleic acid,PNA),它是一种人工合成的DNA和RNA类似物。在肽核酸分子中,N-(2-氨乙基) 甘氨酸结构单元通过酰胺键连接构成骨架以替代核酸分子中戊糖-磷酸结构,碱基则通过亚甲羰键与骨架仲氨基上的N相连(图1)。这种与天然核酸相似的空间结构使得PNA能以碱基互补配对原则与DNA或RNA杂交[2]。与天然核酸相比,PNA具有以下优点:骨架的柔韧性和电中性使其与DNA或RNA杂交的亲和力更高[3];结构中不含氨基酸残基或磷酸戊糖单元,因此不受核酸酶或蛋白酶降解,生物稳定性高[4];非手性构象便于单体合成和纯化[5];骨架含重复的酰胺键结构,因此可以使用固相合成方法合成寡聚物[6]。

图1 PNA (a) 和DNA (b) 的骨架结构Fig. 1 Backbones of PNA (a) and DNA (b).
然而,未修饰PNA在应用时仍存在以下缺点:亲水性的结构很难透过细胞膜,导致细胞摄入差;与靶序列结合不具备方向性;电中性引起PNA分子自聚集导致水溶性差[7]。其中,PNA的跨细胞膜转运难题成为应用的最大障碍,跨膜转运困难使PNA难以到达细胞内,影响了与胞内靶点的结合,降低了生物利用度[8]。因此,增强PNA的细胞摄入水平是工程应用的关键之一。迄今,在这方面取得一定成效的方法可分为以下3类。第一,早期研究主要集中在对细胞膜结构的改造,如电致孔法[9]、渗透化细胞法[10],该方法基于对靶细胞膜结构的修饰,难以适用于PNA工程化应用。第二,对PNA转运形式进行改造,如与DNA协同转运[11]、脂质体包埋[12]、纳米粒协助转运[13],其中,采用与纳米粒共价连接取得了较好的成效。Bertucci 等[14]将PNA共价连接到L型沸石纳米晶体表面,并用生物可降解的聚-L-赖氨酸进行包衣,选用Helen Lane细胞 (HeLa) 考察转运情况,结果表明,该连接复合物的细胞摄取率明显增加。Ma等[15]将PNA与多孔二氧化硅纳米颗粒(Mesoporous silica nanoparticles,MSNP) 通过二硫键共价连接得到PNA-SS-MSNP连接复合物,在MSNP协助转运下,复合物以内吞方式进入HeLa细胞,随后胞内高浓度的谷胱甘肽断裂二硫键,释放出反义PNA,并有效沉默B细胞淋巴瘤-2 (B-cell lymphoma 2,Bcl-2) 蛋白表达。McNeer等[16]将聚合物纳米粒作为载体加载三聚体PNA,该纳米粒能顺利转运至囊性纤维化支气管上皮细胞 (Cystic fibrosis bronchial epithelial cells,CFBE) 内,并校正F508del基因突变。第三,对PNA结构进行化学修饰。化学修饰法具有操作方便、形式多样、适合体内研究等优点,因此备受关注。本文结合本实验室研究成果,对近十年来合成的各种增强细胞转运性能的化学修饰PNA进行综述,总结了修饰性肽核酸细胞转运研究中存在的问题,并对未来的研究趋势及其应用提出了见解。
1 骨架修饰型PNA的细胞转运
自PNA提出以后,对其结构单元进行化学修饰成为研究重点之一。PNA结构单元的修饰可分为碱基的替换和骨架结构的改造。多数情况下,碱基替换会影响PNA的杂交性能,从而降低PNA的生物活性。目前碱基替换研究主要是为了在PNA中引入荧光基团,Matarazzo等[17]用吖啶基氨基尿嘧啶替换普通碱基,该基团既保留了一定的杂交能力,同时又具有荧光特性。迄今,有关碱基替换型PNA的细胞转运研究不多,Bischof等[18]用含钌一氧化碳释放分子(CO-releasing molecules,CORMs) 替换普通碱基,在该基团的协助下,PNA转运效率提高,而且自身的CORM特性不会改变。在PNA结构单元修饰中,骨架修饰是改善PNA细胞转运性能的主要措施。骨架修饰指对PNA的N-(2-氨乙基) 甘氨酸单元结构进行改造,骨架修饰PNA在增加水溶性和增强杂交性能方面取得了一定的成功,而且,部分骨架修饰PNA还具备诸如光学性能、自组装等特殊优点,拓展了PNA的应用范围[19-20]。在骨架修饰法中,关键是不能影响杂交性能,PNA与DNA或RNA的特异性结合是PNA大多数应用的前提条件。Hyrup 等[21]指出无论是改变两个酰胺键之间的骨架长度,还是改变碱基与氨基之间的骨架长度都会降低PNA与DNA或RNA的特异性结合能力。因此,我们认为PNA的骨架修饰应遵循不改变基本空间构型的原则,可以采取骨架取代修饰或者替换骨架原子构成等修饰方法。
1.1取代骨架上H原子
PNA骨架上有3种类型亚甲基,通过改变亚甲基上取代基团的种类,可以得到不同类型的PNA。早期研究以不同α氨基酸为起始原料,合成了多种骨架修饰型PNA,Nielsen等[22]研究了以赖氨酸、丝氨酸、谷氨酸、天冬氨酸、异亮氨酸残基为骨架的修饰型PNA的杂交特性,发现只有D-赖氨酸的Tm值升高,其他PNA的Tm值均下降。目前,对亚甲基上H原子的取代是PNA骨架修饰的重要方法。Maison等[23]采用乌吉反应 (Ugi reaction),以胺、羧酸、异腈、醛 (或酮) 4种组分为原料发生缩合反应,通过变换各组分结构可以一步合成各种类型的骨架取代PNA (图2)。这种取代修饰使得PNA单体成为手性分子,而且各光学异构体的水溶性、杂交性能等往往有差异,通过适当筛选,能找到性能更加优异的PNA。Mitra等[24]用氨甲基(Aminomethylene,am) 取代PNA骨架中α位和γ位的H原子,得到了α-S-amPNA、α-R-amPNA 和γ-S-amPNA 3种骨架修饰型PNA(图3A–C)。通过与特异性结合的cDNA杂交,发现与未经修饰的PNA相比,α-S-amPNA、α-R-amPNA和γ-S-amPNA的Tm值都相应增大,最高增加10 ℃,这表明该结构与DNA特异性结合能力增强。随后,选用HeLa细胞研究了am-PNA进入细胞的能力。结果表明,3种修饰型am-PNA的细胞摄入水平都比未经修饰的PNA高,而且,其细胞转运能力具体表现为:γ位修饰大于α位修饰,R构型大于S构型。Kumar等[25]用氨丙基取代PNA骨架中γ位的H原子,得到了Cγ-氨基丙烯 PNA (amp-PNA) (图3D)。和特异性DNA的杂交实验表明,与未经修饰的PNA相比,其Tm值增大,而且其杂交性能优于碳链长度为4的氨丁基PNA。在人乳腺癌细胞(Michigan cancer foundation-7,MCF-7) 转运实验中发现amp-PNA能高效进入该细胞,并聚集在细胞核附近。

图2 Ugi 4CC法合成PNA单体Fig. 2 Synthesis of PNA monomer via Ugi 4CC reaction. i: MeOH, 20 ℃, 48 h, 90%.

图3 am-PNA和amp-PNA的化学结构Fig. 3 Chemical structures of am-PNAs and amp-PNA.
1.2骨架上引入环状结构
将环状结构引入PNA是得到骨架修饰型PNA的重要方法之一,主要选择较稳定的五元环和六元环。其中,带五元环的PNA因其结构较好地模拟了DNA中戊糖环,受到人们的重视。合成时可以选择自身含有五元环结构的脯氨酸作为起始原料。Suparpprom等[26]合成了骨架结构为脯氨酰基-2-氨基环戊羧酸 (Prolyl-2-aminocyclopentanecarboxylic acid,ACPC) 的ACPC-PNA (图4A),这种带有吡咯烷基的PNA具有很强的刚性结构特性。其中构型为 (1S,2S)-ACPC-PNA具有良好的杂交性能,Tm值大于85 ℃,高于相应DNA-DNA的Tm值。Merino 等[27]合成了含有异恶唑烷结构的Isoxazolidinyl PNA (Isox-PNA) (图4B),该骨架结构可以质子化,有利于PNA的细胞转运,同时还具有良好的水溶性。目前,对环状结构PNA的研究主要涉及提高水溶性和杂交性能,在细胞转运方面还缺乏研究数据。
1.3替换骨架上C原子
对骨架C原子替换具有不改变PNA构型的优点,通常不会降低PNA的杂交性能。Kitamatsu 等[28]合成了带有吡咯环的含氧吡咯烷PNA(POPNA) 和含氨基吡咯烷PNA (PAPNA) (图5)。在POPNA中,O原子替换C原子,即醚键代替亚甲基,醚键骨架柔韧性更好,与DNA或RNA结合牢固,其水溶性也相应提高。在中国仓鼠卵巢细胞 (CHO) 中的吸收实验表明,与甘氨酸骨架PNA相比,其水溶性、杂交特性以及细胞摄取都得到了改善。在PAPNA中,N原子替换C原子,即叔氨基代替亚甲基,叔氨基可质子化,其所带的阳离子电荷有利于跨细胞膜转运。CHO细胞转运实验研究表明,由PAPNA组成的寡聚PNA细胞摄入效率高,但与DNA和RNA的杂交特异性差,而由POPNA组成的寡聚PNA细胞摄入效率低。将2个单元PAPNA和7个单元POPNA聚合形成混合寡聚PNA,发现杂交特异性和细胞摄入效率均较好。
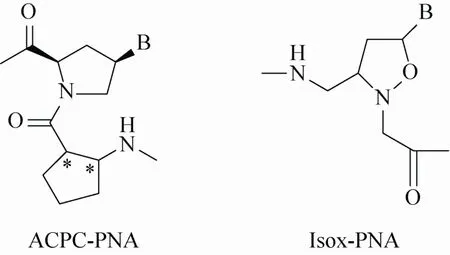
图4 骨架中含有环状结构的PNAFig. 4 PNA with cyclic structure in backbone.

图5 POPNA (a) 和PAPNA (b) 的化学结构Fig. 5 Chemical structures of POPNA (a) and PAPNA (b).
2 PNA连接物的细胞转运
PNA连接物 (PNA conjugates) 是指将PNA和配体直接共价结合,或者通过中介基团将两者共价连接,得到PNA-配体复合物。Koppelhus 等[29]认为,PNA实现工程应用的前提之一是其自身分子能高效通过细胞膜。我们认为诸如细胞微注射法、电穿孔法和电渗透法虽然转运效率较高,但在体内使用受限,不适合临床应用。对PNA分子结构的整体修饰,尤其是寻找合适的配体,制备跨膜转运性能优越的PNA连接物是一种有效的手段。以配体共价修饰制备连接物的方法不仅具备高效的细胞传递性能,而且在杂交性能、细胞毒性等方面具有一定优势,具有工程应用的潜力。近年来,对PNA分子进行整体修饰,寻找合适的配体,取得了一些成功的研究成果,这也可能是今后将PNA工程化开发研究的一个趋势。
2.1PNA-CPP连接物
目前,在种类众多的PNA连接物中,使用最广泛的是PNA-CPP。细胞穿透肽 (Cell penetrating peptide,CPP) 是一类能携带各种类型大分子物质穿过细胞膜,进入细胞内部的多肽。一般为带正电荷的长短不一的短肽,富含精氨酸、赖氨酸等碱性氨基酸残基,正电荷特性有助于与细胞表面的特定位点结合[30]。CPP作为引导物质已广泛应用于DNA、RNA以及药物分子的跨膜转运,借鉴这些经验,将CPP引入PNA传递体系,取得了较好的成效。细胞对PNA-CPP共价连接物主要通过类似胞吞的内化作用,使PNA成功进入胞浆的泡囊中。表1和表2总结了近十年来在PNA转运体系普遍采用且有效的CPP,主要有以下6种:1) 单聚精氨酸和赖氨酸类 (Simple oligoarginines and oligolysines);2) HIV反式激活蛋白 (HIV transactivator protein,Tat);3) 核定位序列(Nuclear localization signal,NLS);4) (KFF)3K;5) M918;6) 信号肽 (Signal peptide)。

表1 用于转运的PNA-CPP连接物Table 1 Examples for delivery of PNA-CPP conjugates

表2 CPP的氨基酸序列Table 2 Sequences of selected CPPs
研究表明,各种富含精氨酸和赖氨酸的多肽具有细胞转运活性,虽然它们的一级结构和二级结构各异,其转运机理既不同于细胞膜内吞作用,也不同于细胞表面受体结合作用[40]。一般认为,氨基酸残基数目对PNA转运活性有显著影响,具有较好转运效率的残基数为5到12个。Bendifallah等[33]考察了精氨酸残基数的影响情况,发现PNA-Arg9连接物的细胞转运效率大于 Arg7和 Arg8,他们认为适当增加氨基酸残基数可以提高PNA-Arg的细胞摄入。另一种常用的单聚多肽是聚赖氨酸,Albertshofer等[32]发现连接八聚L-赖氨酸的PNA能高效通过鼠BCL1细胞膜。1988年,人们首次发现了Tat反式激活蛋白穿透细胞膜的功能,之后被应用于诸如β-半乳糖苷酶、辣根过氧化物酶等各种大分子物质的跨膜转运[41]。Folini等[34]将PNA与Tat共价连接,发现连接物能顺利进入DU145癌细胞,并与胞内特定mRNA特异性结合,该连接物与其他传递方法相比有效地提高了PNA的生物利用度。Su等[35]采用固相合成法合成了PNA-AEEA-Tat连接物,并以浓度依赖方式高效地进入了3T3细胞。NLS能与核载体相互作用,主要应用于将大分子转运至细胞核。有研究发现NLS也能促进PNA的细胞摄入水平,Joshi 等[36]将NLS共价连接到PNA上,并研究了它们进入细菌和哺乳动物细胞的情况,发现连接物转运效率是未经修饰PNA的2倍。但是,Bendifallah等[33]将NLS与其他引导化合物进行比较后发现PNA-NLS的转运效率不是很好。(KFF)3K也是一种常用的引导化合物。Ghosal 等[37]分别研究了D型和L型的(KFF)3K协助PNA进入细胞情况,发现只有L型的L((KFF)3K)具有很好的效果,而同样序列的D型多肽没有促进PNA的跨膜转运。M918是一种含有22个氨基酸残基的多肽,富含精氨酸。Lee等[38]在HT-29-luc细胞中研究了PNA-M918连接物的细胞转运情况,发现该连接物能有效地进入细胞,并特异性沉默相应基因。而且在高达25 µmol/L浓度下,M918既不会损伤细胞膜,也不会对细胞增殖产生影响,非常适合体内应用。信号肽可以直接引导蛋白质穿过真核细胞的内质网膜和原核细胞的内膜,其序列往往包含由疏水氨基酸残基构成的疏水核。研究表明信号肽的协助转运作用主要是由于其疏水区域和细胞膜上双分子层脂质的相互作用,Li等[39]认为这种相互作用要求信号肽的氨基酸残基数为5到15个。他们将一种15个氨基酸残基的信号肽及两种类似多肽分别连接到含10个胸腺嘧啶碱基的PNA的N末端,并研究了3种连接物进入红细胞的情况,结果表明3种连接物都增强了PNA的细胞摄入水平,而且十五肽的协助转运效率最好;但是十五肽连接物的水溶性差,而另外两种六肽和十肽连接物的水溶性较好。
2.2PNA-亲脂性配体连接物
PNA与疏水性化合物或类脂共价结合所形成的连接物具有某些优异的特性。例如,在PNA 的N末端连接疏水性长碳链,在C末端连接氨基酸残基,该连接物具有良好的亲水亲油性,与DNA杂交时表现出更好特异性[42]。该连接物还可自组装成球形胶束,在生物传感器、基因药物等方面具有应用潜力[43]。而且PNA-亲脂性配体连接物在细胞转运方面也显示出很好的性能。表3总结了近十年来成功用于PNA转运的亲脂性配体化合物。
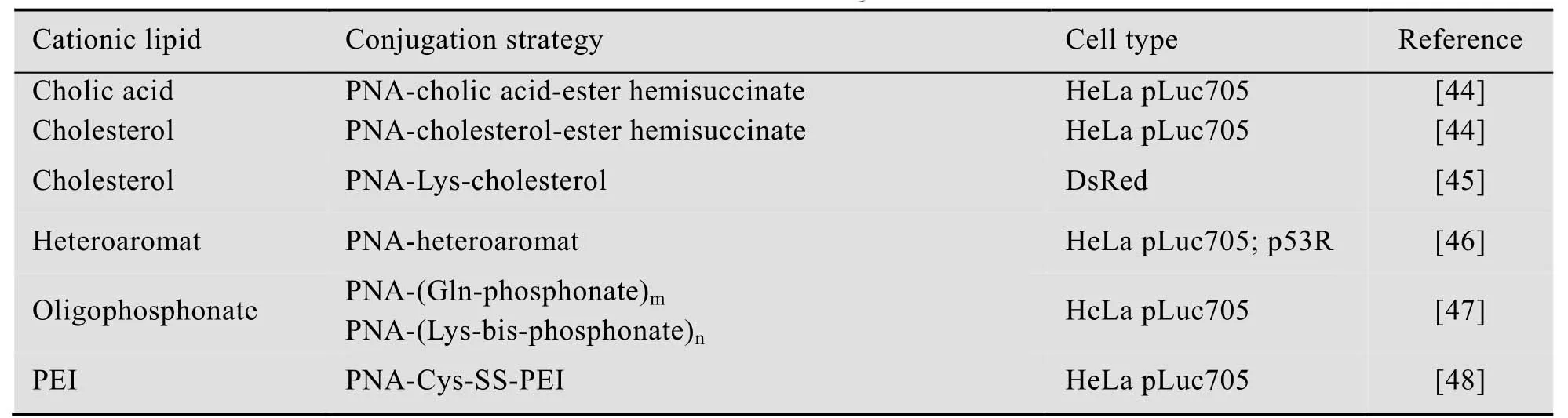
表3 用于转运的PNA-亲脂性配体连接物Table 3 Examples for delivery of PNA-lipophilic ligand conjugates
亲脂性配体中适合于细胞转运的一类物质是具有一定亲水亲油平衡值的类脂,在跨细胞膜转运时,亲水一端朝向胞外水溶性环境,而疏水一端则朝向细胞膜并与细胞膜作用。这种修饰典型代表是胆酸和胆固醇共价连接PNA,该连接物在体内还具有一定的肝脏靶向作用,具有开发成肝脏靶向制剂的潜力[44]。Shiraishi 等[44]将PNA通过半琥珀酸酯键与胆固醇或胆酸结合,并在HeLa pLuc705细胞中对复合物的跨膜转运性能进行测试,结果表明所得到的复合物高效地通过细胞膜,而且PNA-胆酸复合物的水溶性更好。Joshi等[45]将PNA与胆固醇通过赖氨酸连接,制备了一种高效的磁共振造影剂,其转运性能和DNA特异性结合性能都很好。此外,疏水性较强的芳杂环化合物与PNA结合也显示出较好的转运活性。Shiraishi等[46]研究了多种芳杂环化合物修饰PNA及其细胞转运情况,这些芳杂环化合物包括吖啶、苯并咪唑、咔唑、蒽醌、芘、卟啉、萘嵌间二氮杂苯、烟酸己可碱、紫菜碱、补骨脂等,并采用HeLa pLuc705和p53R细胞考察这些PNA连接物的转运情况。结果表明,芳杂环化合物具有普遍增强PNA转运的功能,其中吖啶和烟酸已可碱与PNA形成的连接物活性最高。但是,目前还不清楚芳杂环的结构与转运活性之间的关系。另一类适用于增强转运的亲脂性配体是聚合物,在PNA中成功应用的有聚磷酸酯、聚乙烯胺 (PEI)、聚乙二醇 (PEG) 等。Shiraishi等[47]合成了聚合度分别为3、7、10的PNA-聚谷氨酰胺磷酸酯和聚合度分别为4、5、6的PNA-聚赖氨酸二磷酸酯PNA连接物,并在HeLa pLuc705细胞中进行转运实验。结果表明,将聚磷酸酯共价连接在PNA上显著地增强了PNA的细胞转运,而且不影响其杂交特异性和亲和性。此外,磷酸酯的数目对PNA的转运有影响,六聚赖氨酸二磷酸酯连接物的活性最强,与未修饰PNA相比,其细胞摄取率可增加20倍。Berthold等[48]将PNA通过二硫键与聚乙烯胺连接得到PNA-PEI复合物,并在HeLa pLuc705细胞中进行细胞传递实验,结果表明,PEI可以作为PNA转入细胞的高效引导物,而且不受胞内溶酶体的影响。
上述亲脂性配体中,诸如胆固醇、聚磷酸酯、PEI、PEG等都属于阳离子型转运介质。Llovera等[49]指出阳离子型连接物与细胞膜表面亲和力强,而PNA细胞转运效率与细胞表面PNA浓度密切相关,这是上述配体具有高效转运性能的重要原因之一。同时我们发现,前文所述的PAPNA、Isox-PNA、am-PNA、amp-PNA以及CPP都具有带正电荷性质,其转运性能也与自身所带正电荷相关。因此我们认为,在今后合成PNA新单体和寻找新配合物中,为了提高PNA转运性能,可以考虑将引入带正电荷基团作为一种有效的措施。

表4 用于转运的PNA-功能性配体连接物Table 4 Examples for delivery of PNA- functional ligand conjugates
2.3PNA-功能性配体连接物
近年来,将PNA开发成基因药物是研究热点之一,然而导致PNA成药性差的最大障碍依然是细胞转运难题。将PNA与合适的具有药理活性的功能性配体共价连接是PNA药物开发中的一种成功尝试。PNA-功能性配体连接物的成功设计不仅改善了PNA的细胞摄入水平,同时也将功能性配体化合物导入细胞,实现PNA和功能性配体双重治疗作用。该连接物中,配体不仅仅具有协助转运的作用,还能发挥自身药理活性。表4总结了近年来研究的具有增强PNA转运的功能性配体化合物。
本实验室在PNA-功能性配体连接物方面做了一些研究工作,王建华[50-51]研究了PNA与氟尼辛和阿司匹林的共价连接物的合成方法,所得到的两种连接物具有良好的细胞转运性能。氟尼辛是一种非甾体抗炎解热镇痛药,主要治疗病毒性感染引起的猪无名高热综合征和急性高热炎症。本实验室制备的PNA-弗尼辛连接物在用量为2 mg/kg时,仔猪的体温降低值为0.56 ℃;而单独使用弗尼辛用量为4 mg/kg时,仔猪的体温降低值为0.57 ℃;单独使用PNA用量为10 mg/kg时,仔猪的体温降低值为0.74 ℃。PNA与氟尼辛共价连接所合成的连接物对猪高热病混合感染引起的疾病具有显著治疗效果,而且效果比单独使用PNA或者氟尼辛好。阿司匹林是一种历史悠久的解热镇痛药,具有解热、镇痛、抗炎、抗风湿、抗血小板凝集以及提高免疫力等药理作用。动物实验研究表明,分别将阿司匹林、PNA和PNA-阿司匹林连接物给药4周后,体内白细胞水平分别为 (22.9±3.7)×109/L、(23.1±4.6)×109/L和(26.2±2.9)×109/L;免疫球蛋白G浓度分别为 (53.69±8.97) mg/mL、(47.12±4.53) mg/mL、(62.36±9.58) mg/mL;超氧化物歧化酶浓度分别为(23.99±1.26) μg/mL、(18.02±2.45) μg/mL、(29.60±1.78) μg/mL。PNA-阿司匹林连接物能明显提高生物体内白细胞、免疫球蛋白G和超氧化物歧化酶水平,可用于制备免疫增强剂,应用前景较好。
具有较好细胞转运性能的PNA-功能性配体连接物还有以下几种。Bendifallah等[52]提出了一种连接PNA与功能性配体的2-([N-Boc-氨基乙酸]甲氧基) 苯甲酸酯键结构,通过该酯键结构将PNA与金刚烷共价连接得到PNA-酯键-金刚烷连接物。通过IMR-90细胞中的转运实验和HeLa pLuc705细胞的反义活性实验,发现该连接物能顺利进入IMR-90细胞并在细胞核附近聚集,其反义活性有一定的提高,但不太显著。该连接物另一特性是结构中的酯键在体外稳定;而在体内,由于酶的作用,稳定性下降2 000–3 000倍。因此,PNA-酯键-金刚烷连接物在体内能分解为PNA和金刚烷,这种酯键结构具有开发成“前药”的潜力。Das等[53]发现PNA与新霉素的连接物具有良好的细胞摄入水平,而且,减少氨基基团数目,得到的PNA-氨基葡萄糖胺连接物的转运效果更好。新霉素是一种氨基糖苷类抗生素,通过与16S rRNA结合,导致 mRNA编码错误,从而抑制细菌蛋白质合成。将6-氨基葡萄糖胺环与HIV-1 TAR RNA互补的十六聚PNA连接,所得到的连接物与靶序列结合牢固,而且在被HIV-1感染的细胞中,有效地抑制了病毒复制,而在同样条件下,未修饰PNA很难进入细胞。Browne等[54]将PNA以不同的方式与两种维生素E连接,其中一种带有长碳链,得到的连接复合物中部分具有较好的杂交特性,并且提高了PNA的细胞摄入水平和生物利用度。而且维生素E自身是一种特高免疫力的药物,具有清除体内自由基、抗衰老的功能。因此,这种连接物不但不会有细胞毒性,而且还具有PNA与维生素E的协同治疗的潜在应用。
3 结语与展望
PNA自1991年提出以来,由于具有优异的杂交性能、稳定的结构特性及方便有效的合成方法受到重视,随着各种新单体的成功合成和寡聚体修饰的研究,PNA的应用领域不断拓展。早期作为分子生物学工具,在基因检测、医疗诊断和生物传感器等方面取得了较好的应用。近年来,对PNA的研究的热点之一转向基因治疗,通过对PNA的修饰与改造,开发PNA反义药物的潜力。目前,PNA在反义药物方面应用的最大障碍是细胞转运差,并导致生物利用度低,成药性差。
为提高PNA的细胞转运,包括细胞膜改造、骨架修饰、配体修饰等方法的成功应用,在改善PNA细胞摄入水平差的难题上已取得了一定进展,部分地解决了这些问题。但是,目前的研究主要处于体外细胞水平,PNA在生物体内的吸收、代谢及细胞转运方面还有待于进一步探讨。迄今还没有PNA药物进入临床研究阶段,这与PNA的生物利用度和细胞毒性等方面的缺陷,以及缺乏体内研究数据有关。
今后,改善PNA的细胞转运性能是研究的重点之一。我们认为对PNA自身结构的修饰在成药性方面比细胞膜渗透法和电致孔法更为有效,开发适合的骨架结构和寻找有效的配体引导化合物可能是促进PNA在反义药物方面取得突破的一项重要工作。目前,已报道的骨架修饰型PNA大约有几十种,从水溶性、杂交性能、细胞转运性能等筛选指标出发,部分骨架修饰PNA具有较好的应用前景。同时,PNA的杂交性能与骨架空间构型密切相关,对PNA骨架进行修饰应在保持其骨架基本构型不变的基础上进行。这给PNA的骨架修饰提出了较为苛刻的要求,并在一定程度上限制了骨架修饰型PNA的结构变化。而通过选择合适的配体,与PNA共价连接形成PNA-配体连接物不改变PNA自身特性,但赋予PNA在诸如细胞毒性、药理活性以及细胞摄取率等方面更优异的性能,具有更好的应用前景。本实验室将抗病毒药物和增强免疫力药物与PNA寡聚体N末端共价连接,动物临床实验结果表明,PNA-药物连接物治疗效果更好。同时,我们认为可以在以下几方面作尝试:第一,将PNA骨架修饰与配体连接物修饰结合,首先合成具有良好转运潜力的骨架修饰单体PNA,在聚合时,在寡聚体末端或中间引入引导配体,综合利用两种修饰的优点;第二,将PNA修饰物与制剂开发手段结合,如采用脂质体、纳米粒等制剂新技术协助修饰型PNA转运,促进PNA的临床应用;第三,开发具有增强转运的功能性化合物,如前所述,维生素E、阿司匹林、氟尼辛等药物既可作为PNA转运引导化合物,同时自身又具有特定的药理活性,这种PNA连接物具有双重治疗的优异性能。
REFERENCES
[1] Nielsen PE, Egholm M, Berg RH, et al. Sequence-selective recognition of DNA by strand displacement with a thymine-substituted polyamide. Science, 1991, 254(5037): 1497–1500.
[2] Brown SC, Thomson SA, Veal JM, et al. NMR solution structure of a peptide nucleic acid complexed with RNA. Science, 1994, 265(5173): 777–780.
[3] Pandey VN, Upadhyay A, Chaubey B. Prospects for antisense peptide nucleic acid (PNA) therapies for HIV. Expert Opin Biol Ther, 2009, 9(8): 975–989.
[4] Kovács G, Timár Z, Kupihár Z, et al. Synthesis and analysis of peptide nucleic acid oligomers using Fmoc/acyl-protected monomers. J Chem Soc Perkin Trans, 2002, 10(10): 1266–1270.
[5] Falkiewicz B, Kolodziejczyk AS, Liberek B, et al. Synthesis of achiral and chiral peptide nucleic acid (PNA) monomers using Mitsunobu reaction. Tetrahedron, 2001, 57(37): 7909–7917.
[6] Ditmangklo B, Boonlua C, Suparpprom C, et al. Reductive alkylation and sequential reductive alkylation-click chemistry for on-solid-support modification of pyrrolidinyl peptide nucleic acid. Bioconjugate Chem, 2013, 24(4): 614–625.
[7] Balaji BS, Gallazzi F, Jia F, et al. An efficient, convenient solid-phase synthesis of amino acid-modified peptide nucleic acid monomers and oligomers. Bioconjugate Chem, 2006, 17(2): 551–558.
[8] Shiraishi T, Nielsen PE. Enhanced delivery of cell-penetrating peptide-peptide nucleic acid conjugates by endosomal disruption. Nat Protoc, 2006, 1(2): 633–636.
[9] Joergensen M, Agerholm-Larsen B, Nielsen PE, et al. Efficiency of cellular delivery of antisense peptide nucleic acid by electroporation depends on charge and electroporation geometry. Oligonucleotides, 2011, 21(1): 29–37.
[10] Faruqi AF, Egholm M, Glazer PM. Peptide nucleic acid-targeted mutagenesis of a chromosomal gene in mouse cells. Proc Natl Acad Sci USA, 1998, 95(4): 1398–1403.
[11] Liang KW, Hoffman EP, Huang L. Targeted delivery of plasmid DNA to myogenic cells via transferrin-conjugated peptide nucleic acid. Mol Ther, 2000, 1(3): 236–243.
[12] Chen HL, Hu QH, Liang WQ. Effect of pluronic on cellular uptake of cationic liposomes-mediated antisense oligonucleotides. Pharmazie, 2004, 59(2): 131–133.
[13] Anstaett P, Gasser G. Peptide nucleic acid-an opportunity for bio-nanotechnology. Chim Int J Chem, 2014, 68(4): 264–268.
[14] Bertucci A, Lülf H, Septiadi D, et al. Intracellular delivery of peptide nucleic acid and organic molecules using zeolite-L nanocrystals. Adv Healthc Mater, 2014, 3(11): 1812–1817.
[15] Ma X, Devi G, Qu QY, et al. Intracellular delivery of antisense peptide nucleic acid by fluorescent mesoporous silica nanoparticles. Bioconjugate Chem, 2014, 25(8): 1412–1420.
[16] McNeer NA, Anandalingam K, Fields RJ, et al. Nanoparticles that deliver triplex-forming peptide nucleic acid molecules correct F508del CFTR in airway epithelium. Nat Commun, 2015, 6: 6952.
[17] Matarazzo A, Moustafa ME, Hudson RHE. 5-(Acridin-9-ylamino)uracil-A hydrolytically labile nucleobase modification in peptide nucleic acid. Can J Chem, 2013, 91(12): 1202–1206.
[18] Bischof C, Joshi T, Dimri A, et al. Synthesis, spectroscopic properties, and photoinduced CO-release studies of functionalized ruthenium (II) polypyridyl complexes: versatile building blocks for development of CORM-peptide nucleic acid bioconjugates. Inorg Chem, 2013, 52(16): 9297–9308.
[19] Uno T, Tabata H, Kawai T. Peptide-nucleic acid-modified ion-sensitive field-effect transistor-based biosensor for direct detection of DNA hybridization. Anal Chem, 2007, 79(1): 52–59.
[20] Vernille JP, Kovell LC, Schneider JW. Peptide nucleic acid (PNA) amphiphiles: synthesis, self-assembly, and duplex stability. Bioconjugate Chem, 2004, 15(6): 1314–1321.
[21] Hyrup B, Nielsen PE. Peptide nucleic acids (PNA): synthesis, properties and potential applications. Bioorgan Med Chem, 1996, 4(1): 5–23.
[22] Nielsen PE, Haaima G, Lohse A, et al. Peptide nucleic acids (PNAs) containing thymine monomers derived from chiral amino acids: hybridization and solubility properties of D-lysine PNA. Angew Chem Int Edit, 1996, 35(17): 1939–1942.
[23] Maison W, Schlemminger I, Westerhoff O, et al. Modified PNAs: a simple method for the synthesis of monomeric building blocks. Bioorg Med Chem Lett, 1999, 9(4): 581–584.
[24] Mitra R, Ganesh KN. Aminomethylene peptide nucleic acid (am-PNA): synthesis, regio-/stereospecific DNA binding, and differential cell uptake of (α/γ, R/S) am-PNA Analogues. J Org Chem, 2012, 77(13): 5696–5704.
[25] Kumar P, Jain DR. Cγ-aminopropylene peptide nucleic acid (amp-PNA): chiral cationic PNAs with superior PNA: DNA/RNA duplex stability and cellular uptake. Tetrahedron, 2015, 71(21): 3378–3384.
[26] Suparpprom C, Srisuwannaket C, Sangvanich P, et al. Synthesis and oligodeoxynucleotide binding properties of pyrrolidinyl peptide nucleic acids bearing prolyl-2-aminocyclopentanecarboxylic acid (ACPC) backbones. Tetrahedron Lett, 2005, 46(16): 2833–2837.
[27] Merino P, Tejero T, Matés J, et al. 3-(aminomethyl)-2-(carboxymethyl) isoxazolidinyl nucleosides: building blocks for peptide nucleic acid analogues. Tetr: Asymm, 2007, 18(13): 1517–1520.
[28] Kitamatsu M, Takahashi A, Ohtsuki T, et al. Synthesis of pyrrolidine-based oxy-peptide nucleic acids carrying four types of nucleobases and their transport into cytoplasm. Tetrahedron, 2010, 66(51): 9659–9666.
[29] Koppelhus U, Nielsen PE. Cellular delivery of peptide nucleic acid (PNA). Adv Drug Deliver Rev, 2003, 55(2): 267–280.
[30] Saleh AF, Arzumanov A, Abes R, et al. Synthesis and splice-redirecting activity of branched, arginine-rich peptide dendrimer conjugates of peptide nucleic acid oligonucleotides.Bioconjugate Chem, 2010, 21(10): 1902–1911.
[31] Kitamatsu M, Matsuzaki R, Sisido M. Cellular uptake of pyrrolidine-based oxy-peptide nucleic acid. Biopolymers, 2005, 80(4): 552.
[32] Albertshofer K, Siwkowski AM, Wancewicz EV, et al. Structure-activity relationship study on a simple cationic peptide motif for cellular delivery of antisense peptide nucleic acid. J Med Chem, 2005, 48(21): 6741–6749.
[33] Bendifallah N, Rasmussen FW, Zachar V, et al. Evaluation of cell-penetrating peptides (CPPs) as vehicles for intracellular delivery of antisense peptide nucleic acid (PNA). Bioconjugate Chem, 2006, 17(3): 750–758.
[34] Folini M, Bandiera R, Millo E, et al. Photochemically enhanced delivery of a cell-penetrating peptide nucleic acid conjugate targeting human telomerase reverse transcriptase: effects on telomere status and proliferative potential of human prostate cancer cells. Cell Proliferat, 2007, 40(6): 905–920.
[35] Su W, Mishra R, Pfeuffer J, et al. Synthesis and cellular uptake of a MR contrast agent coupled to an antisense peptide nucleic acid-cell-penetrating peptide conjugate. Contrast Media Mol Imaging, 2007, 2: 42–49.
[36] Joshi T, Gasser G, Martin LL, et al. Specific uptake and interactions of peptide nucleic acid derivatives with biomimetic membranes. RSC Adv, 2012, 2(11): 4703–4712.
[37] Ghosal A, Vitali A, Stach JEM, et al. Role of sbmA in the uptake of peptide nucleic acid (PNA)-peptide conjugates in E. coli. ACS Chem Biol, 2013, 8(2): 360–367.
[38] Lee SH, Moroz E, Castagner B, et al. Activatable cell penetrating peptide-peptide nucleic acid conjugate via reduction of azobenzene PEG chains. J Am Chem Soc, 2014, 136(37): 12868–12871.
[39] Li XX, Zhang LR, Lu JF, et al. Signal peptide mimics conjugated to peptide nucleic acid: a promising solution for improving cell membrane permeability. Bioconjugate Chem, 2003, 14(1): 153–157.
[40] Futaki S, Suzuki T, Ohashi W, et al. Arginine-rich peptides–an abundant source of membrane-permeable peptides having potential as carriers for intracellular protein delivery. J Biol Chem, 2001, 276(8): 5836–5840.
[41] Veldhoen S, Laufer SD, Restle T. Recent developments in peptide-based nucleic acid delivery. Int J Mol Sci, 2008, 9(7): 1276–1320.
[42] Marques BF, Schneider JW. Sequence-specific binding of DNA to liposomes containing di-alkyl peptide nucleic acid (PNA) amphiphiles. Langmuir, 2005, 21(6): 2488–2494.
[43] Liu LH, Li ZY, Rong L, et al. Self-assembly of hybridized peptide nucleic acid amphiphiles. ACS Macro Lett, 2014, 3(5): 467–471.
[44] Shiraishi T, Nielsen PE. Nanomolar cellular antisense activity of peptide nucleic acid (PNA) cholic acid ("umbrella") and cholesterol conjugates delivered by cationic lipids. Bioconjugate Chem, 2012, 23(2): 196–202.
[45] Joshi R, Mishra R, Pohmann R, et al. MR contrast agent composed of cholesterol and peptide nucleic acids: design, synthesis and cellular uptake. Bioorg Med Chem Lett, 2010, 20(7): 2238–2241.
[46] Shiraishi T, Bendifallah N, Nielsen PE. Cellular delivery of polyheteroaromate-peptide nucleic acid conjugates mediated by cationic lipids. Bioconjugate Chem, 2006, 17(1): 189–194.
[47] Shiraishi T, Hamzavi R, Nielsen PE. Subnanomolar antisense activity of phosphonate-peptide nucleic acid (PNA) conjugates delivered by cationic lipids to HeLacells. Nucleic Acids Res, 2008, 36(13): 4424–4432. [48] Berthold PR, Shiraishi T, Nielsen PE. Cellular delivery and antisense effects of peptide nucleic acid conjugated to polyethyleneimine via disulfide linkers. Bioconjugate Chem, 2010, 21(10): 1933–1938.
[49] Llovera L, Berthold P, Nielsen PE, et al. Cell number and transfection volume dependent peptide nucleic acid antisense activity by cationic delivery methods. Artif DNA PNA XNA, 2012, 3(1): 22–27.
[50] Wang JH, Chen CL, Li CH, et al. Preparation and application of modified peptide nucleic acids oligomer carrying aspirin: CN, 201110181844.7. 2011-12-21 (in Chinese).
王建华, 陈春林, 李成洪, 等. 阿司匹林修饰性肽核酸寡聚体及其制备方法和应用: 中国, 201110181844.7. 2011-12-21.
[51] Wang JH. Synthesis of PNA-flunixin conjugates and their use in treatment of mixed infection of swine diseases caused by high fever: CN, 201110181861.0. 2011-12-21 (in Chinese).
王建华. 治疗猪高热病混合感染的氟尼辛肽核酸寡聚体复合物及合成方法: 中国, 201110181861.0. 2011-12-21.
[52] Bendifallah N, Kristensen E, Dahl O, et al. Synthesis and properties of ester-linked peptide nucleic acid prodrug conjugates. Bioconjugate Chem, 2003, 14(3): 588–592.
[53] Das I, Désiré J, Manvar D, et al. A peptide nucleic acid-aminosugar conjugate targeting transactivation response element of HIV-1 RNA genome shows a high bioavailability in human cells and strongly inhibits Tat-mediated transactivation of HIV-1 transcription. J Med Chem, 2012, 55(13): 6021–6032.
[54] Browne EC, Langford SJ, Abbott BM. Synthesis and effects of conjugated tocopherol analogues on peptide nucleic acid hybridisation. Org Biomol Chem, 2013, 11(39): 6744–6750.
(本文责编 陈宏宇)
Cellular delivery of modified peptide nucleic acids: a review
Chundong Liu, Jianhua Wang, and Fang Zeng
Bioengineering College of Chongqing University, Chongqing 400044, China
Abstract:Peptide nucleic acid (PNA) is a DNA surrogate in which the phosphate deoxyribose backbone of DNA is replaced by repeating N-(2-aminoethyl)glycine units. PNA can hybridize to the complementary DNA and RNA with higher affinity than their oligonucleotide counterparts. This character of PNA not only makes it a new tool for the studies of molecular biology but also the potential candidate for gene-targeting drugs. The non-ionic backbone of PNA leads to stablehybrids with the nucleic acids, but at the same time, the neutral backbone results in poor cellular uptake. To address this problem, studies on modified PNA progress rapidly in recent years. We reviewed literature reports combined with our study about the delivery methods, including backbone modified PNA and PNA-ligand conjugates, and the cellular uptake of modified PNA. In addition, we summarized the problems and future prospect of the cellular delivery of modified PNA.
Keywords:peptide nucleic acids, modified, cellular delivery
Corresponding author:Jianhua Wang. Tel: +86-23-65102507; E-mail: wjh@cqu.edu.cn
