血友病B替代治疗药物研究现状及进展
2016-06-22严红曾凡一1上海市儿童医院上海交通大学附属儿童医院上海医学遗传研究所上海2000402卫生部医学胚胎分子生物学重点实验室暨上海市胚胎与生殖工程重点实验室上海200040
严红,曾凡一1 上海市儿童医院 上海交通大学附属儿童医院 上海医学遗传研究所,上海 2000402 卫生部医学胚胎分子生物学重点实验室暨上海市胚胎与生殖工程重点实验室,上海 200040
血友病B替代治疗药物研究现状及进展
严红1,2,曾凡一1,2
1 上海市儿童医院 上海交通大学附属儿童医院 上海医学遗传研究所,上海 200040
2 卫生部医学胚胎分子生物学重点实验室暨上海市胚胎与生殖工程重点实验室,上海 200040
严红, 曾凡一. 血友病B替代治疗药物研究现状及进展. 生物工程学报, 2016, 32(2): 164–171.
Yan H, Zeng FY. Hemophilia B replacement therapy drugs. Chin J Biotech, 2016, 32(2): 164–171.
摘 要:血友病B是一种X染色体连锁的隐性遗传性出血性疾病,患者因体内缺乏凝血因子IX (FIX) 而易发生出血事件,病情严重程度与FIX的缺乏程度相关,严重影响患者的寿命和生存质量。文中通过相关文献资料的查阅和整理,对血友病B替代治疗药物进行归纳和综述,重点阐述上市重组凝血因子IX制品和相关在研药物尤其是长效凝血因子IX的研究进展,为血友病B治疗药物的研发提供基础。
关键词:血友病B,凝血因子IX替代治疗药物,长效凝血因子IX
Received: May 29, 2015; Accepted: October 29, 2015
Supported by: National Natural Science Foundation of China (No. 81500108).
国家自然科学基金 (No. 81500108) 资助。
血友病B是一种X染色体连锁的隐性遗传性出血性疾病,是第二大类血友病亚型 (第一大血友病亚型为血友病A)。该病在男性新生儿中的发病率约为1/25 000,据估计我国血友病B患者总数约为20 000名,占血友病患者总数的15%−20%[1-2]。血友病B因患者体内缺乏FIX (Factor IX,凝血因子IX) 引发,病情的严重程度与病人体内FIX的缺乏程度相关;重症血友病B患者体内的FIX含量小于正常人的1%,患者频繁发生自发性出血,如关节内出血、软组织血肿、腹腔出血和脑出血等,最终导致严重的关节病、慢性疼痛、残疾和死亡,显著影响患者的寿命和生存质量[3]。
FIX替代治疗药物一直是血友病B药物的研发热点,近两年来除已有的FIX替代治疗药物外,还涌现了大量的候选药物,该部分药物的信息亟待总结和更新。下面就血友病B上市和在研FIX替代药物分别作重点介绍。
1 血友病B替代治疗药物现状和研发进展
血友病B替代治疗有按需治疗和预防治疗两种方式。按需治疗是指在患者发生出血症状时接受FIX注射控制出血情况,是一种应急策略;而预防治疗是指为预防出血事件发生,血友病B重症患者每周定期注射FIX 2−3次的给药方法[4]。按照来源的不同,上市的FIX替代治疗药物分为血浆富集来源FIX (pdFIX,plasma-derived FIX)和重组细胞表达来源FIX (rFIX,recombinant FIX)两大类,在研药物中还有乳腺生物反应器来源FIX;重组细胞表达的FIX还可以分为传统重组FIX药物和长效重组FIX药物两类,表1汇总了目前上市和在研的重组FIX制品。
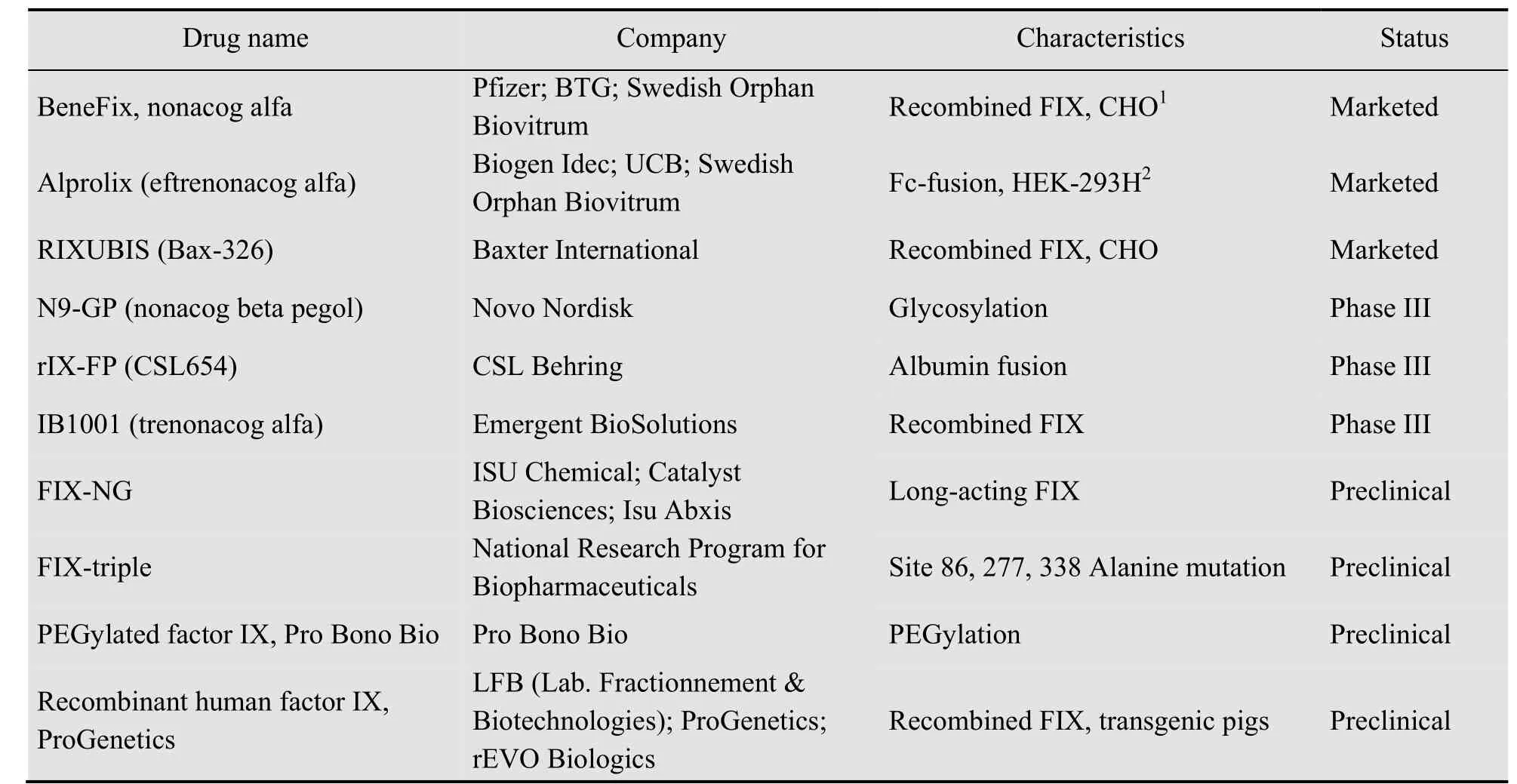
表1 上市和在研重组FIX药物汇总表Table 1 Marketed and in research recombinant FIXs
1.1血液来源凝血因子IX
血浆富集的FIX,指的是从人血浆中提取而来的凝血因子IX制品 (下简称为pdFIX,plasma derived FIX)。pdFIX制品可有效控制患者的出血状况,并且显著降低患者用药过程中血栓发生的风险,也曾经常被用于预防治疗,但因来源于人血液,存在传播血液感染病的风险 (血液传播的病毒、支原体,如肝炎病毒和HIV病毒等)。
血源性感染风险是pdFIX制品面临的最大问题。20世纪80年代,美国和欧洲曾发生血友病患者大规模感染血液疾病的事件,约有60%–80%重症血友病患者因用药感染了HIV病毒[5]。为降低血源性感染的风险,新一代pdFIX制品致力于通过改进纯化工艺,增加去病毒效率来减少病毒感染的可能性,但是仍然无法杜绝潜在朊病毒、未包装病毒和其他未知病原体的感染风险;此外,由于提取工艺对血浆质量要求高,且血浆来源有限,该类产品价格也较为昂贵,随着重组FIX的上市,pdFIX正逐渐被取代[6]。
1.2传统重组蛋白来源凝血因子IX
1998年,首个重组人凝血因子IX (rFIX) 制品获准在美国上市,商品名为贝赋 (BeneFIX,辉瑞 (Pfizer) 公司)。该rFIX制品是由CHO(中国仓鼠卵巢细胞) 所表达的重组蛋白。贝赋与pdFIX相比,临床效果一致,副反应发生情况也类似,但因生产过程中不涉及人或动物血浆,避免了血源性污染的风险。临床数据显示两者的在体半衰期相似 (pdFIX为32.7±7.4 h,贝赋为36.0±12.8 h),但是贝赋的回收率比pdFIX低30%左右,可能是因为CHO细胞所表达的rFIX翻译后修饰情况与天然FIX相比有所差异造成;儿童患者的FIX血浆分布高于成人患者,这种回收率的差异在儿童患者中更为明显[7-8]。头对头 (Head-to-head) 比较两者临床效果的实验较少,现有的一些相关试验显示rFIX确实有比较低的回收率,但是两者的止血效果类似,并不影响贝赋的临床效果[9]。贝赋在中国血友病B患者中的临床试验结果与之前在白种人患者中进行的临床试验结果一致,可有效控制85%以上的出血事件,患者中没有发生FIX抑制物或血栓症,也没有发现新的与治疗相关的副作用[10]。
近日,美国FDA批准了第二例rFIX制品上市——Bax 326 (商品名RIXUBIS,美国Baxter Healthcare公司,2013年6月上市)。Bax 326也是CHO细胞所表达的重组蛋白,与BeneFIX不同的是,Bax 326在生产过程中rFIX是与人野生型furin蛋白共表达的,furin蛋白能够促进rFIX的剪切,但在成品中furin最终被去除[11]。临床结果显示,Bax 326的预防给药、按需给药、术中给药效果和药代动力学都与贝赋一致,并且有良好的安全性,是当今美国唯一被批准用于常规预防给药的FIX制品[12]。Bax 326成品所含的激活形式FIX (FIXa, activated FIX) 更低,这更加保证了Bax 326在临床使用的安全性(FIXa是产品相关的杂质,其水平越高引发血栓的副反应发生频率越高)[13]。
1.3长效重组蛋白来源凝血因子IX
传统rFIX制品的半衰期大约为33.8 h (在儿童体内rFIX的半衰期要更短,约为20 h左右[14]),进行预防给药的剂量通常为30−40 IU/kg,患者需要每2−3 d注射1次,以期维持血浆FIX水平1%以上[15]。长半衰期FIX制品能够缓解反复静脉注射给病人带来的不便,是当前血友病药物的研发热点。延长rFIX半衰期的主要手段有融合表达法和PEG聚合化法,前者又包括白蛋白融合法 (rFIX-FP) 和Fc片段融合法 (rFIX-Fc,Fc是人免疫球蛋白IgG的Fc片段)[16]。
1.3.1FIX-Fc融合表达药物
Fc是人免疫球蛋白IgG的Fc区域,当目标蛋白与Fc区域进行融合表达后,通过Fc区域与新生Fc蛋白受体 (FcRn,neonatal Fc receptor)结合,该受体可保护目标蛋白-Fc融合蛋白被细胞内吞后不被降解,最终被再次带回细胞表面释放入血浆,实现血浆半衰期的延长[17]。同时,Fc融合表达的方法也可以增加目标蛋白的分子质量,降低肾脏清除率,该方法已经被批准用于延长一系列慢性疾病药物的半衰期,是增加生物药物半衰期的常用手段[18-19]。
首个FIX和Fc融合重组表达药物 (rFIX-Fc) 于2014年3月通过美国FDA批准上市,商品名为Alprolix (百健艾迪 (Biogen Idec) 公司)[20]。Alprolix是人IgG1的双链Fc片段N末端共价结合单个FIX分子形成的融合蛋白,由HEK-293H细胞 (人源细胞) 表达,该细胞同时表达PC5(一种加工酶,帮助FIX前肽的充分剪切)[21]。在血友病B小鼠模型上的实验结果显示,该rFIX-Fc制品与传统rFIX制品药效等同,但是FIX活性时间得到延长。临床前药物代谢动力学研究显示,在大鼠和小鼠模型中rFIX-Fc的半衰期分别为34.8和46.2 h,而传统rFIX的半衰期分别为13.2和12.3 h。与此一致,在其他动物模型上 (猴子,狗) rFIX-Fc的半衰期也比传统rFIX增加了3−4倍。而在Fc受体敲除小鼠模型中两者的半衰期类似,这表明rFIX-Fc半衰期的增加主要通过Fc融合作用实现[22]。长期临床III期研究 (B-LONG研究) 显示,rFIX-Fc在血友病B患者中的平均半衰期为82.1 h,传统rFIX的平均半衰期为33.8 h (延长2.4倍);同时,在患者体内没有检测到FIX抑制物的形成,也没有免疫反应发生,具有良好的安全性[15]。
1.3.2FIX-白蛋白融合表达药物
白蛋白融合技术最初被用于延长细胞因子类制品 (IFNs, ILs) 的半衰期,通过增加目标蛋白的分子量降低肾脏清除率来延长生物制品的半衰期。白蛋白还能够遮蔽目标蛋白,使目标蛋白免受一些胰酶的消化并且降低免疫原性[23]。
直接将FIX与白蛋白融合重组表达会导致FIX的生物活性降低[24],因此在研的该类药物rIX-FP (杰特贝林 (CSL Behring) 公司),在FIX与白蛋白序列之间添加了一段可切割的连接序列,添加的序列在FIX被激活时被剪切从而不影响FIX的活性。该药已经完成的临床I期研究显示,与传统rFIX相比,rFIX-FP的半衰期增加5倍,回收率增加44%,清除率降低7倍;病人没有出现特殊的免疫反应,也没有rFIX-FP抑制物形成。综合来看,rFIX-FP的半衰期延长效果和安全性良好,该药物的临床试验正在进行中[25-26]。
1.3.3FIX-PEG化修饰药物
PEG化是指将单甲氧基PEG分子共价结合在蛋白质的可用表面基团的过程。这种共价结合通过增加目标蛋白的分子大小、降低肾小球滤过来增加目标蛋白的半衰期,同时也能包裹蛋白表面减少目标蛋白被蛋白酶的降解或清除[27]。
N9-GP (在研PEG化FIX药物,诺和诺德(Novo Nordisk) 公司),是一个在FIX活性肽段连接40 kDa PEG分子的修饰FIX制品,当FIX被激活时PEG分子可被去除[28]。临床试验结果显示,对之前使用过传统FIX制品进行治疗的患者,N9-GP累积给药3次可使FIX半衰期增加5倍 (平均半衰期为110 h),累积回收率增加20%;试验观测到一例严重的超敏反应,此外,虽然所有参与者体内均没有检测到FIX抑制物,但是有3例病人产生非抑制性抗体 (可能是抗PEG抗体),针对该药的其他临床试验还在进行中[29]。
1.3.4其他长效FIX药物
其他长效FIX药物还包括FIX羧基末端肽修饰 (CTP) 药物和FIX高糖基化修饰药物。前者在血友病B小鼠模型上的结果显示,FIX半衰期增加4倍,出血密度和时间降低,但是FIX的特异活性也被降低;FIX高糖基化修饰药物,与天然FIX (2个糖基化位点) 相比多2个糖基化位点,在血友病B小鼠模型上使半衰期增加2.4倍,清除率降低5.4倍,但目前还没有临床数据公布[30]。
值得注意的是,这些针对新型FIX药物的试验结果可能由于选择的检测方法不同而有所差异,也可能因一步法试验 (FIX活性检测试验)中选择的试剂不同而有所差异[31]。目前针对特定药物来比较不同实验室和试剂之间差异的试验还在进行当中,统一检测方法与标准将更有利于比较不同药物的疗效。
1.4乳腺生物反应器来源凝血因子IX
尽管重组细胞生产的FIX制品能够很好地降低病人感染血液传播疾病的可能性,并且能有效控制病人的出血情况,但是其价格昂贵,一般患者难以接受。对于一个重症血友病B患者来说,平均每年要花费13万美元的治疗费用,其中还不算FIX预防治疗的花费,这种高额的治疗费用使得约80%的患者不能得到完善的治疗[32-33]。因此,目前急需建立一个高效、廉价、大量制备FIX的方法,让更多的患者得到良好的救治,同时使FIX口服给药研究以及寻找更好给药方式的工作得以开展。
据报道,转基因动物乳腺反应器能够表达人FIX,表达速率在克/每升/每小时的级别。与重组细胞相比,动物生物反应器的生产成本要相对低廉,是廉价大量生产FIX的一个潜力方向[34]。笔者单位上海医学遗传研究所利用牛乳腺生物反应器实现了人FIX的高效表达,其水平是血浆和CHO细胞FIX表达水平的50倍以上,与国外猪乳腺生物反应器生产的人FIX制品同处于临床前研究阶段 (Recombinant Human Factor IX, ProGenes公司)。牛乳腺生物反应器所表达的FIX相比血液来源的天然FIX,凝血活性提高了100倍;初步的结构分析结果表明,其蛋白结构、糖基化修饰、羧基化、二硫键也与天然的FIX基本一致 (数据未发表)。目前,正在进行牛乳腺生物反应器来源的FIX在小鼠模型中在体半衰期和稳定性等相关特性的研究。
2 总结与展望
在过去20年中,由于FIX替代药物的发展,血友病B患者的生活质量得到了大幅提升,特别是在西方发达国家,高标准的血友病护理使得血友病B患者的寿命达到正常人群水平。从长期效果来看,血友病B预防给药好于按需给药,可以显著减少出血事件反复发生引起的后遗症;长效FIX产品能够有效降低患者预防给药次数,减轻痛苦,是最具研究价值和实际意义的血友病B药物开发方向;但同时,还需在研究中对这些新型FIX制品进行严密监控,以判定修饰的FIX是否存在安全隐患。总之,当前的FIX替代药物能够极大地改善血友病B患者的治疗状况,但同时,由于价格高昂、半衰期通常较短等原因,患者常需要频繁、大量的输注FIX替代药物,也是当前FIX替代治疗药物需要改进的方向。
我国和其他发展中国家与西方发达国家相比,血友病B患者的治疗需求还远未被满足,多数的血友病B患者迫于经济压力没有得到有效与及时的诊疗。贝赋是目前我国市场上唯一的FIX制品,2013年5月才正式在我国上市,并且价格昂贵,多数重症患者仅在发生出血事件时进行给药,远没有实现预防治疗,患者常在30岁左右就因关节内反复出血引发的后遗症而致残,严重影响患者的寿命和生存质量。值得注意的是,血友病B治疗的社会总经济负担并不能只考虑药物价格,还需结合患者的长期健康状况以及血友病关节炎的治疗和护理费用来综合考量。因此大量生产价格低廉的FIX制品对减轻患者负担、改善患者生活质量以及实现预防给药有积极作用。笔者单位上海医学遗传研究所利用牛乳腺生物反应器实现了人FIX高效表达,经鉴定结构与人血液来源的天然FIX相一致,多种翻译后修饰正确,临床前体内和体外活性试验均具有高效凝血活性 (数据未发表),与CHO表达体系相比具有明显优势。动物乳腺生物反应器大幅降低FIX的生产成本的特点,使得生产大量廉价FIX成为可能,这将从根本上改变血友病B病人的治疗现状,特别是对发展中和欠发达国家的患者来说意义重大。
综上所述,FIX制品是当前血友病B治疗的主要药物,该类药物可较好地预防和控制患者出血事件的发生;而相比于西方发达国家,我国血友病B患者由于经济压力、药品短缺等多种原因,远没有得到良好的治疗,开发廉价FIX制品是亟待解决的问题,也是我国血友病B药物研发领域致力的方向。当前国际上血友病B药物的研发重点是长效FIX制品,美国已批准一例长效FIX制品上市,其余多种长效FIX制品正处于临床前或临床试验阶段,相信长效FIX的上市和普及会给血友病B患者的治疗带来更大的改善,并推动血友病B治疗药物和治疗方式的发展。
REFERENCES
[1] WFH. Report on the annual global survey 2012. Montreal, 2013.
[2] Thrombosis and hemostasis group of Hematology branch of Chinese Medical Association, China hemophilia collaboration group. Diagnosis and treatment of haemophilia-Chinese expert consensus (2013). Chin J Hematol, 2013, 34(5): 461–463.
中华医学会血液学分会血栓与止血学组, 中国血友病协作组. 血友病诊断与治疗中国专家共识(2013年版). 中华血液学杂志, 2013, 34(5): 461–463.
[3] Mannucci PM, Tuddenham EGD. The hemophilias-from royal genes to gene therapy. New Engl J Med, 2001, 344(23): 1773–1779.
[4] Berntorp E, Shapiro AD. Modern haemophilia care. Lancet, 2012, 379(9824): 1447–1456.
[5] Key NS, Negrier C. Coagulation factor concentrates: past, present, and future. Lancet, 2007, 370(9585): 439–448.
[6] Ludlam CA, Turner ML. Managing the risk of transmission of variant Creutzfeldt Jakob disease by blood products. Brit J Haematol, 2006, 132(1): 13–24.
[7] Björkman S, Shapiro AD, Berntorp E.Pharmacokinetics of recombinant factor IX in relation to age of the patient: implications for dosing in prophylaxis. Haemophilia, 2001, 7(2): 133–139.
[8] Chowdary P, Dasani H, Jones JAH, et al. Recombinant factor IX (BeneFix®) by adjusted continuous infusion: a study of stability, sterility and clinical experience. Haemophilia, 2001, 7(2): 140–145.
[9] Lissitchkov T, Matysiak M, Zavilska K, et al. Head-to-head comparison of the pharmacokinetic profiles of a high-purity factor IX concentrate (AlphaNine®) and a recombinant factor IX (BeneFix®) in patients with severe haemophilia B. Haemophilia, 2013, 19(5): 674–678.
[10] Yang R, Zhao Y, Wang X, et al. Evaluation of the safety and efficacy of recombinant factor IX (nonacog alfa) in minimally treated and previously treated Chinese patients with haemophilia B. Haemophilia, 2012, 18(5): e374–e378.
[11] Dietrich B, Schiviz A, Hoellriegl W, et al. Preclinical safety and efficacy of a new recombinant FIX drug product for treatment of hemophilia B. Int J Hematol, 2013, 98(5): 525–532.
[12] Windyga J, Solano Trujillo MH, Hafeman AE. BAX326 (RIXUBIS): a novel recombinant factor IX for the control and prevention of bleeding episodes in adults and children with hemophilia B. Ther Adv Hematol, 2014, 5(5): 168–180.
[13] Turecek PL, Abbühl B, Tangada SD, et al. Nonacog gamma, a novel recombinant factor IX with low factor IXa content for treatment and prophylaxis of bleeding episodes. Expert Rev Clin Pharmacol, 2015, 8(2): 163–177.
[14] Nagel K, Decker K, Goldsmith R, et al. Pharmacokinetics of recombinant and plasma-derived factor IX products in pediatric patients with severe hemophilia B. Blood Coagul Fibrin, 2015, 26(1): 113–114.
[15] Powell JS, Pasi KJ, Ragni MV, et al. Phase 3 study of recombinant factor IX Fc fusion protein in hemophilia B. New Engl J Med, 2013, 369(24): 2313–2323.
[16] Shapiro A. Development of long-acting recombinant FVIII and FIX Fc fusion proteins for the management of hemophilia. Expert Opin Biol Ther, 2013, 13(9): 1287–1297.
[17] Pipe SW. Hemophilia: new protein therapeutics. Hematology Am Soc Hematol Educ Program, 2010, 2010: 203–209.
[18] Krueger GG, Ellis CN. Alefacept therapy produces remission for patients with chronic plaque psoriasis. Brit J Dermatol, 2003, 148(4): 784–788.
[19] Genovese MC, Becker JC, Schiff M, et al. Abatacept for rheumatoid arthritis refractory to tumor necrosis factor α inhibition. New Engl J Med, 2005, 353(11): 1114–1123.
[20] Roopenian DC, Akilesh S. Fcrn: the neonatal Fc receptor comes of age. Nat Rev Immunol, 2007, 7(9): 715–725.
[21] Ducore JM, Miguelino MG, Powell JS. Alprolix (recombinant Factor IX Fc fusion protein): extended half-life product for the prophylaxis and treatment of hemophilia B. Expert Rev Hematol, 2014, 7(5): 559–571.
[22] Peters RT, Low SC, Kamphaus GD, et al. Prolonged activity of factor IX as a monomeric Fc fusion protein. Blood, 2010, 115(10): 2057–2064. [23] Kratz F. Albumin as a drug carrier: design of prodrugs, drug conjugates and nanoparticles. J Control Rel, 2008, 132(3): 171–183.
[24] Sheffield WP, Mamdani A, Hortelano G, et al. Effects of genetic fusion of factor IX to albumin on in vivo clearance in mice and rabbits. Br J Haematol, 2004, 126(4): 565–573.
[25] Santagostino E, Negrier C, Klamroth R, et al. Safety and pharmacokinetics of a novel recombinant fusion protein linking coagulation factor IX with albumin (rIX-FP) in hemophilia b patients. Blood, 2012, 120(12): 2405–2411.
[26] Santagostino E. PROLONG-9FP clinical development program--phase I results of recombinant fusion protein linking coagulation factor IX with recombinant albumin (rIX-FP).Thromb Res, 2013, 131 Suppl 2: S7–S10.
[27] Veronese FM, Mero A. The impact of PEGylation on biological therapies. BioDrugs, 2008, 22(5): 315–329.
[28] Negrier C, Knobe K, Tiede A, et al. Enhanced pharmacokinetic properties of a glycoPEGylated recombinant factor IX: a first human dose trial in patients with hemophilia B. Blood, 2011, 118(10): 2695–2701.
[29] Collins PW, Young G, Knobe K, et al. Recombinant long-acting glycoPEGylated factor IX in hemophilia B: a multinational randomized phase 3 trial. Blood, 2014, 124 (26): 3880–3886.
[30] Bolt G, Bjelke JR, Hermit MB, et al. Hyperglycosylation prolongs the circulation of coagulation factor IX. J Thromb Haemost, 2012, 10(11): 2397–2398.
[31] Hubbard AR, Dodt J, Lee T, et al. Recommendations on the potency labelling of factor VIII and factor IX concentrates. J Thromb Haemost, 2013, 11(5): 988–989.
[32] WFH. Key issues in hemophilia treatment [EB/OL]. [2015-03-01].http://www1.wfh.org/publication/files/p df-1218.pdf.
[33] Globe DR, Curtis RG, Koerper MA. Utilization of care in hemophilia: a resource-based method for cost analysis from the Haemophilia Utilization Group Study (HUGS). Haemophilia, 2004, 10 Suppl 1: 63–70.
[34] Lindsay M, Gil GC, Cadiz A, et al. Purification of recombinant DNA-derived factor IX produced in transgenic pig milk and fractionation of active and inactive subpopulations. J Chromatogr A, 2004, 1026(1/2): 149–157.
(本文责编陈宏宇)
Hemophilia B replacement therapy drugs
Hong Yan1,2, and Fanyi Zeng1,2
1 Shanghai Institute of Medical Genetics, Shanghai Children’s Hospital, Shanghai Jiao Tong University, Shanghai 200040, China
2 Key Laboratory of Embryo Molecular Biology, Ministry of Health & Shanghai Key Laboratory of Embryo and Reproduction Engineering, Shanghai 200040, China
Abstract:Hemophilia B is an X chromosome linked hereditary hemorrhagic disease, which is caused by the lose function mutation of factor IX (FIX), and significantly affects the patients’ lifespan and life quality. The severity of hemophilia B depends on the FIX level in the plasma. By referring to the relevant literatures, we reviewed and summarized hemophilia B replacement therapies. Specifically, we focus on recombinant factor IX products on the market and those in the pipeline, especially on the long-acting factor IX drugs, to provide the basis for researches of new hemophilia B drugs.
Keywords:hemophilia B, factor IX replacement drugs, long-acting factor IX
Corresponding author:Fanyi Zeng. Tel: +86-21-62472308; Fax: +86-21-62475476; E-mail: fzeng@sjtu.edu.cn
