T2期胃癌临床病理特征及多层螺旋CT术前TNM分期价值*
2016-06-15戚庭月赵建溪李华莉贺文广李文华汪登斌吴湘如张文杰
郭 辰,任 刚△,蔡 嵘,戚庭月,赵建溪,陈 健,李华莉,贺文广,李文华,汪登斌,吴湘如,张文杰
(1.上海交通大学医学院附属新华医院放射科,上海 200092;2.上海交通大学医学院附属瑞金医院放疗科,上海 200025;3.江苏省扬州市第一人民医院超声科 225001;4.上海交通大学医学院附属新华医院病理科,上海 200092;5.上海交通大学医学院附属新华医院普外科,上海 200092)
T2期胃癌临床病理特征及多层螺旋CT术前TNM分期价值*
郭辰1,任刚1△,蔡嵘2,戚庭月3,赵建溪1,陈健1,李华莉1,贺文广1,李文华1,汪登斌1,吴湘如4,张文杰5
(1.上海交通大学医学院附属新华医院放射科,上海 200092;2.上海交通大学医学院附属瑞金医院放疗科,上海 200025;3.江苏省扬州市第一人民医院超声科225001;4.上海交通大学医学院附属新华医院病理科,上海 200092;5.上海交通大学医学院附属新华医院普外科,上海 200092)
[摘要]目的探讨T2期胃癌临床病理特征及多层螺旋CT(MSCT)在T2期胃癌术前TNM分期中的价值。方法单因素分析93例T2期胃癌患者的临床病理特征,并行MSCT术前TNM分期,与术后病理检查结果进行对照。结果浅肌层癌 (T2a)和深肌层癌(T2b)两组患者在临床病理特征上差异无统计学意义(P>0.05)。MSCT对T2期胃癌T分期准确率为91.40%(85/93);N分期准确率为66.67%(62/93),其中对pN0、pN1、pN2和pN3期判断的准确率分别为68.18%(30/44)、65.00%(26/40)、60.00%(3/5)和75.00%(3/4);TNM分期的准确率为67.74%(63/93),其中Ⅰ、Ⅱ、Ⅲ和Ⅳ期分期准确率分别为68.18%(30/44)、64.10%(25/39)、60.00%(3/5)和100%(5/5)。结论T2a和T2b患者在临床病理特征上没有显著差异。MSCT动态增强扫描对T2期胃癌术前TNM分期具有重要的临床价值。
[关键词]体层摄影术,螺旋计算机;胃肿瘤;肿瘤分期;T2期胃癌;多层螺旋CT;术前TNM分期;临床病理特征
准确的胃癌术前分期对拟定临床治疗方案及评估预后等方面具有非常重要的价值。特别是需要实施腹腔镜或内镜治疗、新辅助化疗等技术时,正确的术前分期变得更为重要[1-2]。大量临床研究发现,在胃癌手术病例中,因术前分期不准确导致约20%病例因无法根治性切除而只行了剖腹探查术[3-4]。CT是目前临床应用最广泛的胃癌影像诊断手段,多层螺旋CT (MSCT)的发展为胃癌诊断提供了更为方便、准确的方法,多期动态增强扫描可以观察病变的早期强化和(或)门脉期、平衡期的延迟强化,有助于早期发现病变[5]。近年来随着MSCT及相关软件的不断升级,使其在胃癌术前分期中起到越来越重要的作用[6]。本研究应用MSCT检查确定T2期胃癌术前TNM分期,并与术后病理及分期对比,探讨MSCT检查在T2期胃癌术前分期中的应用价值。
1资料与方法
1.1一般资料收集上海交通大学医学院附属新华医院和附属瑞金医院2003年10月至2012年5月行MSCT增强检查并经病理证实的93例T2期胃癌患者完整资料。所有患者行根治性手术治疗。纳入标准:(1)胃镜活检病理确诊为胃癌;(2)胃癌患者一般情况能耐受胃癌根治术;(3)年龄小于或等于85岁;(4)体检颈部淋巴结无转移,无大量腹腔积液;(5)术前除外肺、肝等远处转移;(6)患者入组2周内不存在大出血、胃穿孔、梗阻等急诊手术指征;(7)患者依从性好;(8)初次诊断,未接受治疗。排除标准:(1)对654-2和(或)碘剂过敏、禁忌的患者(比如青光眼、前列腺肥大);(2)严重心、肝、肾功能障碍者,以及甲状腺毒症者;(3)扫描参数下图像质量差,或(和)胃充盈差无法清晰显示病灶;(4)残胃患者;(5)MSCT检查时间与手术时间间隔超过2周者。
1.2方法
1.2.1检查设备及扫描方法新华医院和瑞金医院Siemens Somatom Definition 64层双源CT、Philips 256层Brillance iCT机、Philips 64层Brillance CT机及相应的图像后处理工作站。患者于CT检查前1 d晚餐后禁食。扫描前向患者及家属解释说明扫描时、扫描后注意事项,并进行呼吸屏气训练。检查前1~2 h患者口服水750 mL,检查前15 min再口服250 mL,并嘱患者饮水时尽量避免吞入空气。平扫后立即动态增强扫描,对比剂选用碘海醇或优维显(规格为350 mgI/mL或320 mgI/mL),采用LF双筒高压注射器经肘静脉团注对比剂,剂量100 mL/人,速率3.0 mL/s,动脉期、静脉期、平衡期延迟时间分别为28、60、120 s。扫描参数为120 kV,电流为自动毫安技术,范围为200~250 mAs,扫描层厚及间距均为5 mm容积扫描。FOV 35~40 cm,矩阵512×512,旋转时间0.5 s/圈,螺距1.0,标准重建。扫描范围:膈顶至髂嵴水平,疑大范围转移者扫描范围包括盆腔。对原始数据以1.0 mm 层厚重建,即将所获得的容积扫描数据传输至工作站,利用同机配备的软件进行图像后处理。
1.2.2胃扩张评价标准口服温水后,胃扩张充盈程度以测量胃小弯处胃壁的厚度,胃壁厚度小于3.5 mm为满意,胃壁厚度大于3.6 mm为不满意。
1.2.3T2期胃癌的细分标准浅肌层癌(T2a)是指肿瘤浸润不突破固有肌层肌间神经丛,深肌层癌(T2b)是指肿瘤浸润深度突破固有肌层肌间神经丛。
1.2.4病理学诊断及TNM分期标准依照the Japanese Classification of Gastric Carcinoma标准[7],T2期胃癌指肿瘤组织侵犯固有肌层。进展期胃癌大体类型分为Type 1型(mass)、Type 2型(ulcerative)、Type 3型(infiltrative ulcerative)和Type 4型(diffuse infiltrative)。组织学上,乳头状癌和管状腺癌统称为分化型癌,而低分化腺癌和印戒细胞癌统称为未分化型癌。局部淋巴结按照原发肿瘤的位置分为3组。N0:无淋巴结转移;N1:转移至第1组淋巴结,而没有第2或第3组淋巴结转移;N2:转移到第2组淋巴结,而没有第3组淋巴结转移;N3:转移到第3组淋巴结;NX:不明。TNM分期分为4期,即Ⅰ期(ⅠA期和ⅠB期)、Ⅱ期、Ⅲ期(ⅢA期和ⅢB期)和Ⅳ期,其中若出现肝转移(H1)、腹膜转移(P1)、腹腔细胞学阳性(CY1)和其他部位远处转移(M1),即为Ⅳ期;同时若N分期达N3期也判定为Ⅳ期。
1.2.5CT TNM分期标准T和N分期参考D′elia等[8]提出的标准。T0:无胃壁改变的征象,脂肪间隙正常;T1:单层结构时,非透壁性显著强化,无论是否伴有局部胃壁增厚,多层结构时,局部胃壁增厚和显著强化而没有中、外层的中断;T2:单层结构时,胃壁透壁性强化并局灶性增厚,多层结构时,胃壁异常强化并中层(3层结构时)、外层(2层结构时)中断,且增厚胃壁处的外缘光整或有少许小线状软组织条索影延伸至周围脂肪间隙内;T3:增厚胃壁外缘呈网状或不规则状不规则,或者病变周围脂肪层模糊;T3或T4:胃肿瘤和邻近器官间的脂肪间隙消失;T4:肉眼见浸润至邻近器官。胃周淋巴结短径大于6 mm或胃周以外淋巴结短径(8 mm判定为局部淋巴结受累;淋巴结恶性受累的其他标准包括淋巴结近乎圆形(长径/短径小于1.5),淋巴结的脂肪门移位或消失,淋巴结显著或不均匀强化。计算经MSCT检查后确定的术前TNM分期的准确率(与术后TNM分期比较)。一致性评价:Kappa≤0.40表明一致性差,0.40
1.2.6图像处理由两名主治以上高年资医师分别对原始横轴位及薄层图像进行分析,记录病灶的部位、大小、范围等情况,作出具体的TNM分期判断;意见不统一时再次对相应病例进行分析,协商后作出一致判定。

2结果
2.1临床病理特征入组的93例T2期胃癌患者中,男60例(64.5%),女33例(35.5%),年龄24~82岁,中位年龄58岁。临床症状多为上腹部不适及疼痛、黑便和体质量下降,病史3 d至2年。93位患者于手术中共摘取淋巴结2 215枚,其中经病理证实为淋巴结转移的为283枚,见表1。单因素分析T2a和T2b患者临床病理特征,结果显示在诸如年龄、性别、肿瘤位置、肿瘤最大径、胃切除类型、切除淋巴结数量、大体分型、肿瘤分化、pN分期、pTNM 分期、淋巴管浸润、静脉浸润、神经浸润等诸多临床病理特征上,两组患者差异无统计学意义(P>0.05),见表1。
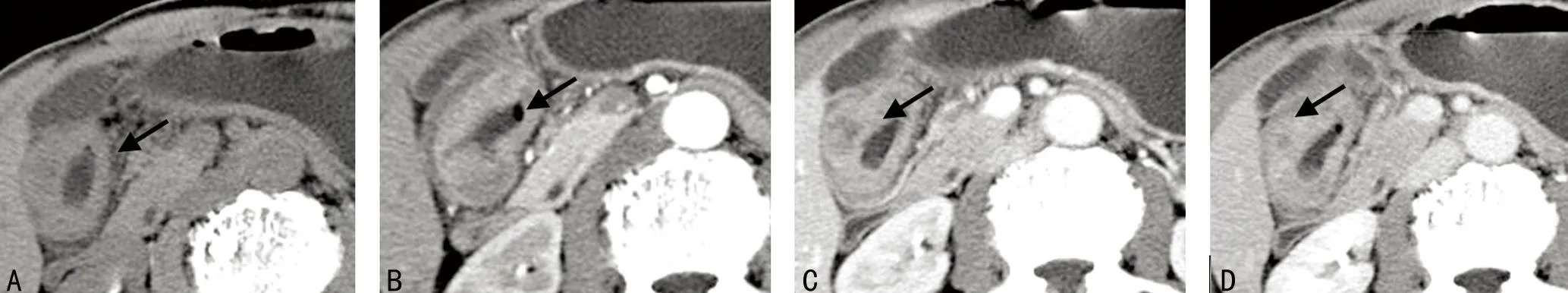
A:CT平扫示胃窦部胃壁局部明显增厚,密度欠均匀;B:动脉期示增厚胃壁明显强化;C:实质期示增厚胃壁持续强化,浆膜面光整;D:平衡期示增厚胃壁呈持续强化。
图1胃窦部腺癌,累及胃小弯全周(箭头)

A:CT平扫示胃小弯可见肿大的淋巴结影,边缘欠光整,密度欠均匀,短径约7 mm,CT值约40 HU;B:增强后动脉期淋巴结CT值约62 HU,呈中度强化;C:实质期CT值约为83 HU,呈持续强化;D:冠状位显示病灶与转移淋巴结。

图2 胃窦部腺癌N1期,第3组淋巴结转移(箭头)
-:无数据。
2.2MSCT术前T分期结果与术后病理比较,术前MSCT增强扫描对93例T2期胃癌T分期判断的总体准确率为91.40%(85/93),过高分期(误判为T3期)4例,过低分期(误判为T1期)4例,见图1。
2.3MSCT术前N分期结果CT术前分期中57例患者出现淋巴结转移,36例无转移。经术后病理证实,49例患者出现局部或远处淋巴结转移,44例未见淋巴结转移,与病理结果对照,N分期总体准确率为66.67%(Kappa=0.481 7,符合度较高),见表2、图2。

表2 T2期胃癌MSCT术前与术后病理N分期对照
2.4MSCT术前TNM分期结果与术后病理相比,MSCT对T2期胃癌术前TNM分期的判断准确率为67.74%(Kappa=0.500 9,符合度较高),见表3。

表3 T2期胃癌MDCT术前与术后病理
3讨论
临床上对以CT结果进行胃癌术前分期判定仍然存在争议,一些相关研究对采用CT 诊断胃癌分期的相关数据相差很大,其分期的准确性42.0%~60.0%[9-10]。20世纪90年代末期以来,MSCT 开始应用于临床并得到普及,无论是其图像质量、数据采集能力还是其影像重建能力和扫描速度等方面都取得了长足的进步,使其对胃癌的检查准确率更加提高,明显拓展了胃癌分期的视野。
本研究选用水作为阴性对比剂,其主要优势在于:水与胃壁密度差异大;流动性好,体位变化时因重力作用可观察胃壁各部;没有任何不良反应,可根据需要增加用量;增强扫描时可以与异常强化的胃壁形成明显的对比而不产生伪影及容积效应等。Takao于1998 年提出了胃癌MSCT 2次给药、3次扫描的新方法,而后关于MSCT 检查技术在胃癌诊断和分期研究的报道也相继出现,从而获取了动脉相、门静脉相及延迟相共3个时相的扫描图像,并证实这种多次扫描方法对于胃癌的T 分期准确率达到了前所未有的高度。并且由于第2次给药使得小动脉、小静脉强化,而淋巴结呈现部分边缘强化,从而对淋巴结的鉴别及分期起了重要作用。本研究采用MSCT三期动态增强扫描。其中,28 s(动脉期)主要用于检出胃癌原发病灶,尤其对于早期胃癌,胃壁局部增厚不是很明显的患者很重要;60 s(门脉期)有助于胃癌周围转移性淋巴结的检出;120 s(延迟期)主要用于判定胃癌浸润胃壁深度,尤其在区分T1、T2期肿瘤方面有很大帮助。
胃癌术前分期对临床治疗方案的选择和是否手术治疗具有重要的指导意义。本组93例胃癌患者MSCT分期与术后病理分期对照,T分期准确率为91.40%,N分期准确率为66.67% ,TNM分期准确率分67.74%,与本团队先前的研究(文献[11-12])及文献[13-14]报道相似,经一致性检验MSCT对胃癌分期与手术病理分期一致性较好,说明MSCT在T2期胃癌的术前分期中有较高的临床价值。MSCT 图像上部分胃壁的层次难以做出清晰显示,呈现单层结构影像表现,对T分期带来难度,导致过高或过低分期。将T2期高估为T3期的原因可能是:虽然胃壁局限性增厚较重,但病理上癌细胞未浸润浆膜层;胃周炎性反应所致脂肪间隙模糊而被误认为癌性浸润;部分患者明显消瘦,脂肪层过少,造成胃周脂肪间隙模糊;病灶与局部肿大淋巴结邻近或融合而显示肿瘤外侵。肿瘤组织对浆膜面的微小浸润MSCT无法检测到是造成过低分期的重要因素。进展期胃癌应观察动脉期和门静脉期增强表现,这样才能较为准确地判断胃癌的浸润程度(T分期)。此外,CT图像上难以明确地显示癌灶向周围脂肪组织的浸润范围,但在磁共振成像(MRI)的弥散加权成像(DWI)序列上则可以明确判断,进而有助于T2和T3期病灶的准确区分。淋巴结转移是胃癌的主转移的主要方式,同时也是胃癌分期的一个难点。本研究中,N分期准确性与T、TNM 相比相对较低,究其原因,可能有:N分期对淋巴结转移的判断主要依据淋巴结肿大及增强扫描后出现异常强化,但与其他原因引起的淋巴结肿大常不易区分,容易误诊;胃小弯侧的浸润肿瘤常与肿大淋巴结融合,致淋巴结判断低估;位于幽门上下区、肝十二指肠韧带区及胰后区域的淋巴结容易漏诊;对小淋巴结可能漏诊,可通过薄层扫描、多方位多平面重建(MPR)、窄间距重组后的连续回放观察等方法,同时结合淋巴结的形态及动态增强征象可提高N分期准确性。
本研究仍存在不足:(1)由于近年来胃癌治疗手段的发展,2011年日本胃癌协会已经根据实际情况,将胃癌的病理TNM分期更新至第3版[15],与之前的病理分期比较,对具有更大预后判断价值的T1、T4期进行了更细致的分期。(2)还无法做到MSCT判定的阳性淋巴结与手术切除的淋巴结进行一一对应,只能借助于日本分期法,以分组分站的方式记录淋巴结,将CT判定与手术病理相对应。
随着胃癌分期在世界范围内的统一,CT设备的不断更新,扫描速度不断提高,以及软件的不断开发,MSCT检查对术前早期胃癌分期的准确性也会越来越高,为外科医师制订合理的治疗策略提供依据[16]。目前多排螺旋CT在判断胃癌淋巴结转移方面没有统一的标准,在N分期的准确度尚待提高,应用CT判断胃癌淋巴结转移有待进一步的研究。
参考文献
[1]Mehmedovic A,Mesihovic R,Saray A,et al.Gastric cancer staging:EUS and CT[J].Med Arch,2014,68(1):34-36.
[2]Cho JW.The role of endoscopic ultrasonography in T staging:early gastric cancer and esophageal cancer[J].Clin Endosc,2013,46(3):239-242.
[3]Park CH,Park JC,Kim EH,et al.Learning curve for EUS in gastric cancer T staging by using cumulative sum analysis[J].Gastrointest Endosc,2015,81(4):898-905.
[4]Ishigami S,Uenosono Y,Arigami T,et al.Clinical utility of perioperative staging laparoscopy for advanced gastric cancer[J].World J Surg Oncol,2014,12(1):350.
[5]Hallinan JT,Venkatesh SK.Gastric carcinoma:imaging diagnosis,staging and assessment of treatment response[J].Cancer Imaging,2013(13):212-227.
[6]Hallinan JT,Venkatesh SK,Peter L,et al.CT volumetry for gastric carcinoma:association with TNM stage[J].Eur Radiol,2014,24(12):3105-3114.
[7]Jgc A.Japanese classification of gastric carcinoma-2nd English edition-[J].Gastric Cancer,1998,1(1):10-24.[8]D′elia F,Zingarelli A,Palli D,et al.Hydro-dynamic CT preoperative staging of gastric cancer:correlation with pathological findings.A prospective study of 107 cases[J].Eur Radiol,2000,10(12):1877-1885.
[9]Fujikawa H,Yoshikawa T,Hasegawa S,et al.Diagnostic value of computed tomography for staging of clinical T1gastric cancer[J].Ann Surg Oncol,2014,21(9):3002-3007.
[10]Shi L,Yan F,Pan Z,et al.Stomach virtual non-enhanced CT with second-generation,dual-energy CT:a preliminary study[J].PLoS One,2014,9(11):e112295.
[11]任刚,蔡嵘,薛建平,等.T2期胃癌的临床病理特征和CT评估[J].临床放射学杂志,2008,27(2):215-219.
[12]任刚,蔡嵘,陈克敏.多排螺旋CT在检测早期胃癌淋巴结转移中的临床价值评估[J].中华肿瘤杂志,2007,29(11):852-855.
[13]Hasegawa S,Yoshikawa T,Shirai J,et al.A prospective validation study to diagnose serosal invasion and nodal metastases of gastric cancer by multidetector-row CT[J].Ann Surg Oncol,2013,20(6):2016-2022.
[14]Burbidge S,Mahady K,Naik K.The role of CT and staging laparoscopy in the staging of gastric cancer[J].Clin Radiol,2013,68(3):251-255.
[15]Japanese Gastric Cancer Association.Japanese classification of gastric carcinoma:3rd English edition[J].Gastric Cancer,2011,14(2):101-112.
[16]曹长琦,李士杰,闫炎,等.小探头内镜超声检查在早期胃癌T分期中的应用[J].中华消化外科杂志,2015,14(3):212-215.
The clinicopathology features of the T2gastric cancer and value of enhanced multiphasic spiral CT in TNM staging of T2gastric cancer*
GuoChen1,RenGang1△,CaiRong2,QiTingyue3,ZhaoJianxi1,ChenJian1,LiHuali1,HeWenguang1,LiWenhua1,WangDengbin1,WuXiangru4,ZhangWenjie5
(1.DepartmentofRadiology,XinHuaHospital,ShanghaiJiaoTongUniversitySchoolofMedicine,Shanghai200092,China;2.DepartmentofRadiotherapy,RuijinHospital,ShanghaiJiaoTongUniversitySchoolofMedicine,Shanghai200025,China;3.DepartmentofUltrasound,FirstClinicalMedicalCollegeofYangzhouUniversity,Yangzhou,Jiangsu225001,China;4.DepartmentofPathology,XinHuaHospital,ShanghaiJiaoTongUniversitySchoolofMedicine,Shanghai200092,China;5.DepartmentofGeneralSurgery,XinHuaHospital,ShanghaiJiaoTongUniversitySchoolofMedicine,Shanghai200092,China)
[Abstract]ObjectiveTo explore the clinicopathological characters of T2 gastric cancer and the value of MSCT in the preoperative TNM staging of T2 gastric cancer.MethodsA total of 93 patients with T2 gastric cancer were included in our study and underwent preoperative MSCT staging,who were confirmed by pathologic results.Then the results were compared with those of pathologic TNM staging.Also the clinicopathological features of the T2 gastric cancer were analyzed.ResultsThere were no statistically significant differences in the clinicopathological characters among T2aand T2bpatients (P>0.05).Comparing with pathologic TNM stage,the T staging accuracy of MSCT was 91.40%(85/93),the N staging accuracies of CT was 66.67%(62/93),in which,68.18%(30/44),65.00%(26/40),60.00%(3/5) and 75.00%(3/4) were for pN0,pN1,pN2 and pN3.And the TNM staging accuracies of CT was 67.74%(63/93),in which,68.18%(30/44),64.10%(25/39),60.00%(3/5) and 100%(5/5) were for stage Ⅰ,Ⅱ,Ⅲ and Ⅳ.ConclusionThere are no significant different on clinicopathology features among T2aand T2bpatients.MSCT can clearly determine the preoperative TNM staging of T2 gastric cancer.
[Key words]tomography,spiral computed;stomach neoplasms;neoplasm staging;T2 gastric cancer;multi-slice spiral computed tomography;preoperative TNM staging;clinicopathology features
doi:论著·临床研究10.3969/j.issn.1671-8348.2016.03.023
*基金项目:江苏省科技计划基金资助项目(BL2014064);上海交通大学医学院科研基金资助项目(09XJ21013);上海市卫生局科研基金资助项目(2010029);上海市卫生局科研基金资助项目(2010057);上海市科委科研基金资助项目(124119a0300);上海市教委科研基金资助项目(12Y2034)。
作者简介:郭辰(1988-),住院医师,硕士,主要从事胃肠道肿瘤的影像学及相关基础研究。△通讯作者,E-mail:rengang527@163.com。
[中图分类号]R445.3
[文献标识码]A
[文章编号]1671-8348(2016)03-0362-04
(收稿日期:2015-08-28修回日期:2015-10-18)
