101例埃索美拉唑不良反应文献分析
2016-06-03倪倍倍刘晓英乔伟立毕鹏飞殷衍磊于江州
倪倍倍,刘晓英,乔伟立,毕鹏飞,代 梦,殷衍磊,于江州,李 静
(青岛大学附属医院药学部,山东 青岛 266000)
101例埃索美拉唑不良反应文献分析
倪倍倍*,刘晓英,乔伟立,毕鹏飞,代梦,殷衍磊,于江州,李静#
(青岛大学附属医院药学部,山东 青岛266000)
DOI10.14009/j.issn.1672-2124.2016.04.043
摘要目的:了解埃索美拉唑引发药品不良反应(adverse drug reaction,ADR)的情况,为临床合理用药提供参考。方法:以“埃索美拉唑”“esomeprazole”为关键词,检索1995—2015年中国医院数字图书馆期刊全文数据库、万方数据库、维普数据库和Pubmed医学文献检索系统中有关埃索美拉唑致ADR的文献,并对患者的性别、年龄、ADR出现时间、ADR累及器官和(或)系统与临床表现、解救措施以及转归情况进行统计分析。结果:共检索到101例相关病例。埃索美拉唑致ADR多发生在60~79岁年龄段,占53.47%;ADR可累及多个器官和(或)系统,主要为消化系统(33.66%)和泌尿系统(12.87%)。结论:临床应重视埃索美拉唑所致ADR,以确保用药安全。
关键词埃索美拉唑; 药品不良反应; 文献分析
埃索美拉唑为奥美拉唑的S-异构体,是第一个用于临床的光学异构体质子泵抑制剂(proton pump inhibitors,PPI)。相比奥美拉唑,埃索美拉唑的口服生物利用度更高,抑酸效果更好,对超过6个月的糜烂性反流性食管炎患者的有效率可高达90%以上[1]。临床上主要用于胃溃疡、十二指肠溃疡、胃食管反流性疾病、应激性溃疡出血、上消化道出血、根除幽门螺杆菌、卓-艾综合征等的治疗。但随着临床应用的增多,除了常见的消化系统和泌尿系统药品不良反应(adverse drug reaction,ADR)外,近年来新的ADR报道也逐渐增多。本调查对埃索美拉唑引发ADR的文献报道进行分析整理,为临床合理用药提供参考。
1资料与方法
1.1资料来源
以“埃索美拉唑”“esomeprazole”为关键词,检索1995—2015年中国医院数字图书馆期刊全文数据库、万方数据库、维普数据库、Pubmed等相关数据库,并查阅原始文献。结果共检索到有效中文文献24篇,涉及病例16例;符合要求的外文文献80篇,涉及病例85例。
1.2方法
查阅上述文献中有关埃索美拉唑致ADR的描述,统计分析患者的基本情况、用药情况、ADR出现时间、ADR累及器官和(或)系统与临床表现、解救措施以及转归情况等。
2结果
2.1患者的性别与年龄分布
发生ADR患者的性别与年龄分布见表1。
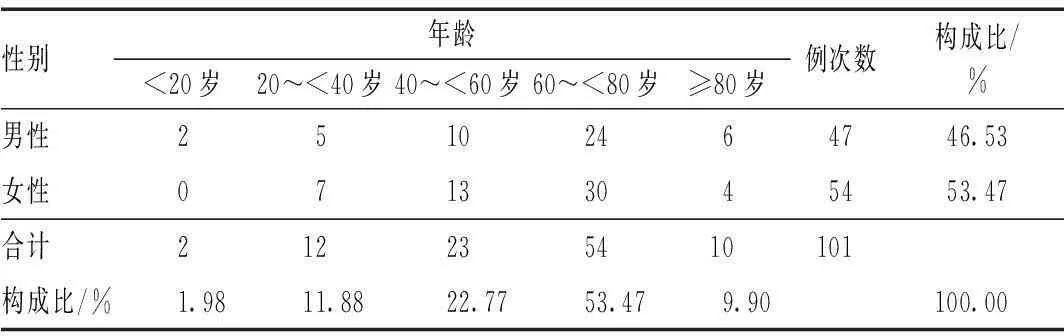
表1 发生ADR患者的性别与年龄分布
2.2引发ADR的给药途径及出现ADR的时间分布
引发ADR的给药途径及出现ADR的时间分布见表2。
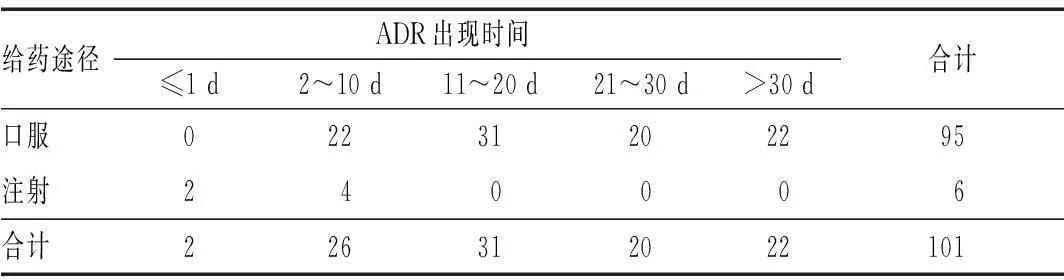
表 2 引发ADR的给药途径及出现ADR的时间分布
2.3ADR涉及器官和(或)系统及临床表现
ADR涉及器官和(或)系统及临床表现见表3。
2.4ADR转归时间及解救措施
101例ADR患者中,停药后对症治疗的有65例,停药后未治疗的有25例,未知的有11例。其中,痊愈的有61例,好转的有27例,转归不详的有11例,死亡2例。
3讨论
3.1发生ADR的患者性别与年龄
本调查涉及的101例患者中,年龄在60~79岁者最多,共有54例,占53.47%。所有患者中,男性47例,占46.53%;女性54例,占53.47%。
3.2ADR发生时间
由表2可见,口服给药引发的ADR多出现在10 d以后,共有73例;而注射给药引发的ADR全部出现在10 d以内。
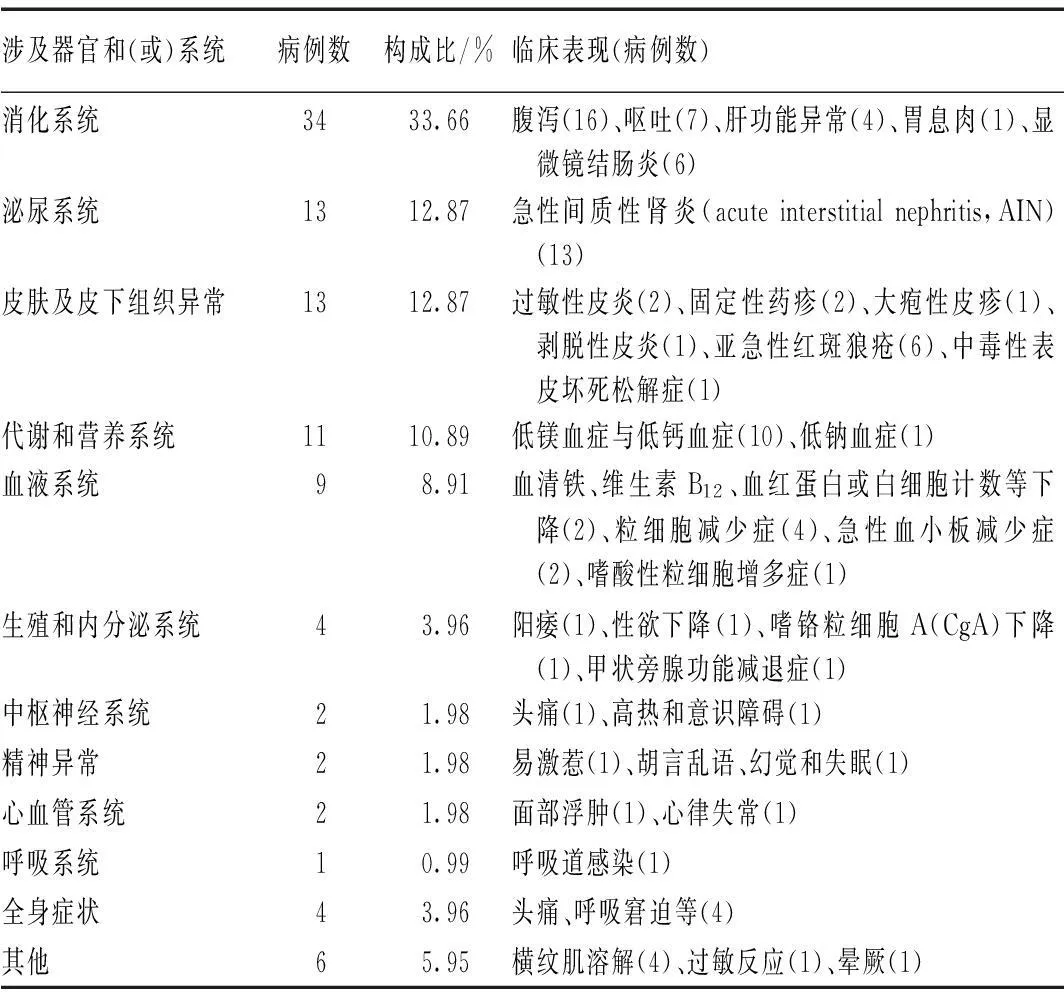
表3 ADR涉及器官和(或)系统及临床表现
3.3ADR的临床表现及相关因素分析
埃索美拉唑引发的ADR分布范围广泛,以消化系统最多,占33.66%,主要表现为腹泻、呕吐。其次为泌尿系统和皮肤及其皮下组织,分别占12.87%。泌尿系统主要是AIN。发生AIN的患者可能表现为恶心、呕吐、腰痛或发热等不典型症状[2]。多数患者经激素治疗后肾功能恢复良好,而伴有糖尿病的患者可能需要永久性透析依赖。产生AIN的原因,被认为是肝、肾CYP微粒体酶的基因多态性致肾内药物及其代谢物增加而加重了药物毒性[3]。埃索美拉唑主要经CYP2C19代谢。快代谢性CYP2C19(如CYP2C19*17)加快底物代谢,可增加毒性代谢物。埃索美拉唑所致血液系统的毒性占8.91%,主要是罕见的粒细胞减少症,其可能机制为骨髓毒性机制[4]。CYP2C19的基因多态性是诱导药源性粒细胞缺乏症的重要因素[5]。
埃索美拉唑引发的代谢和营养相关的ADR占10.89%,主要是低镁血症[6]和低钙血症[7]。Kuipers等[8]报道了埃索美拉唑所致的低镁血症及由低镁血症引起的精神错乱。低镁血症的临床表现包括手足抽搐、惊厥、震颤、心房颤动、室上性心动过速、Q-T间期异常。有研究结果发现,使用PPI后从尿液排出的镁减少,提示与胃肠道镁的吸收减少有关[6]。可能机制为胃肠道中二价阳离子如镁、钙由细胞膜上载体镁和镁调控蛋白(TRPM)6/7介导进入细胞内。使用PPI后,氢离子浓度下降,使这种介导作用降低。低镁血症还可使甲状旁腺激素分泌受损,导致低血钙。而对PPI引起骨折尚有其他解释。PPI可能诱导甲状旁腺功能亢进,甲状旁腺激素释放增加,直接降低骨密度;还可改变破骨细胞微环境,影响骨的形成和重建。包括埃索美拉唑在内的PPI除影响钙、镁的吸收外,还会影响维生素B12的吸收[9]。
李萍等[10]报道的1例埃索美拉唑引发精神异常患者,是在患者血镁水平正常前提下发生的。患者出现胡言乱语、幻觉和失眠等精神异常及中枢性高热[11],可能与埃索美拉唑较其他PPI更易透过血-脑脊液屏障有关。
埃索美拉唑等PPI增加感染风险,主要包括肺炎和艰难梭菌相关性腹泻。正常情况下,胃液较低的pH是防御致病菌入侵的重要屏障,PPI通过提高胃液的pH,导致机会致病菌过度生长、移位,产生毒素,进而引起感染性腹泻。艰难梭菌的感染与宿主肠道微环境发生改变有关。如果胃内过度生长的细菌移位于呼吸道,就可能增加感染社区获得性肺炎的风险。PPI发生肺炎的危险期是用药后的14 d内,更长时间使用并不增加感染风险。
埃索美拉唑导致的CgA升高的机制尚不明确。CgA是重要的肿瘤标志物。服用PPI刺激正常的神经内分泌细胞大量释放CgA,需要临床医师特别注意的是,这可能导致神经内分泌肿瘤的假阳性诊断[12]。
PPI联用阿司匹林/氯吡格雷可能使心血管不良事件发生率增加。可能机制为阿司匹林在正常胃酸环境下,被动扩散进入胃黏膜,pH升高降低了阿司匹林的亲脂性,影响了其生物利用度[13]。PPI和氯吡格雷联用时竞争CYP2C19结合位点,导致氯吡格雷抗血小板活性降低,复发性心血管事件发生率增加。因目前的研究尚不能排除其他混杂因素的影响,PPI是否降低了氯吡格雷抗血小板聚集功能尚无统一定论,但至少对联用阿司匹林/氯吡格雷和PPI提出了警告。Asuman等[14]报道了1例患者联用埃索美拉唑选择性5-羟色胺再摄取抑制(SSRI)后出现紧张、敏感、攻击性等易激惹行为,可能与埃索美拉唑通过改变胃内pH而改变西酞普兰的血浆浓度有关。临床应对PPI与SSRI类药的相互作用给予关注。
除上述表现以外,埃索美拉唑还可能引起各种皮肤病变[15]、阳痿[16]、横纹肌溶解[17]等。
由于埃索美拉唑的肝毒性,长期用药者特别是用药1年以上者,应定期监测肝功能。肝功能不良的患者,不宜长期大量应用。老年及肾功能不良的患者用药需慎重,因PPI引起的间质性肾炎起病隐匿,无特异性,应定期检查肾功能。由于埃索美拉唑等PPI可能增加骨折风险,老年患者及患有骨质疏松症者应尽量使用较低剂量或较短疗程,及时补充钙剂和维生素D。对社区获得性肺炎高危人群如儿童、老年患者、免疫缺陷患者及肺部疾病患者,仅在必须用药时方可使用。患者用药过程中出现粒细胞减少,应考虑可能为埃索美拉唑的ADR,及时停药。而使用氯吡格雷的冠心病患者,应尽量选择使用药物相互作用较小的泮托拉唑。
综上所述,埃索美拉唑引起的ADR涉及多个器官和(或)系统,且新的严重的ADR不断出现,需要引起重视。虽然埃索美拉唑的ADR总体发生率较低(1%~3%),但使用范围广,人口基数大,且有些ADR是致命性的,如横纹肌溶解、粒细胞减少、低镁血症、低钙血症等。临床使用要注意用法用量和适应证,避免滥用。联合用药时,需考虑到埃索美拉唑对胃肠道内环境的改变和药动学特点。尤其要注意与易引起低镁血症的药物(如地高辛、利尿剂等)、伏立康唑及SSRI类药的联用,以最大限度地保证临床用药的安全。
参考文献
[1]Thitiphuree S,Talley NJ.Esomeprazole,a new proton pump inhibitor:pharmacological characteristics and clinical efficacy[J].Int J Clin Pract,2000,54(8):537-541.
[2]Sampathkumar K,Ramalingam R,Prabakar A,et al.Acute interstitial nephritis due to proton pump inhibitors[J].Indian J Nephrol,2013,23(4):304-307.
[3]Brewster UC,Perazella MA.Proton pump inhibitors and the kidney:Critical review[J].Clin Nephrol,2007,68(2):65-72.
[4]Dury S,Nardi J,Gozalo C,et al.Agranulocytosis induced by proton pump inhibitors[J].J Clin Gastroenterol,2012,46(10):859.
[5]李雨,邓娇,李昊燃.埃索美拉唑致粒细胞缺乏症1例[J].中国医院用药评价与分析,2014,14(9):863-864.
[6]刘琛.长期使用质子泵抑制剂增加低镁血症风险[J].药物不良反应杂志,2011,13(2):84.
[7]Cundy T,Mackay J.Proton pump inhibitors and severe hypomagn-esaemia[J].Curr Opin Gastroenterol,2011,27(2):180-185.
[8]Kuipers MT,Thang HD,Arntzenius AB.Hypomagnesaemia due to use of proton pump inhibitors — a review[J].Neth J Med,2009,67(5):169-172.
[9]Thomson A,Sauve M,Kassam N,et al.Safety of the long-term use of proton pump inhibitors[J].World J Gastroenterol,2010,16(19):2323-2330.
[10]李萍,陈玉文,刘海燕.静脉滴注埃索美拉唑致精神异常[J].药物不良反应杂志,2013,15(4):230-231.
[11]Grattagliano I,Portincasa P,Mastronardi M,et al.Esomeprazole-induced centeral fever with severe myalgia[J].Ann Pharmacother,2005,39(4):757-760.
[12]Gori G,Spinelli G,Spinelli C,et al.Esomeprazole-induced hyperchromograninemia in the absence of concomitant Hypergastri-nemia[J].Nat Rev Gastroenterol Hepatol,2010,7(11):642-646.
[13]Charlot M,Grove EL,Hansen PR,et al.Proton pump inhibitor use and risk of adverse cardiovascular events in aspirin treated patients with first time myocardial infarction:nationwide propensity score matched study[J].BMJ,2011,342(19):1135-1142.
[14]Celikbilek A,Celikbilek M,Akyol L,et al.Esomeprazole-induced irritability[J].Acta Neurol Belg,2014,114(3):251-252.
[15]Chularojanamontri L,Jiamton S,Manapajon A,et al.Cutaneous reactions to proton pump inhibitors:a case-control study[J].J Drugs Dermatol,2012,11(10):e43-47.
[16]杨庆敏,李士峰.埃索美拉唑致阳痿1例[J].中国医院药学杂志,2005,25(10):961.
[17]曲彩红,雷姿颖.伏立康唑与埃索美拉唑联用致乙肝肝硬化并肺部侵袭性真菌感染患者横纹肌溶解症[J].今日药学,2011,21(11):686-688.
Literature Analysis on 101 Cases of Adverse Drug Reactions Induced by Esomeprazole
NI Beibei, LIU Xiaoying, QIAO Weili, BI Pengfei, DAI Meng, YIN Yanlei, YU Jiangzhou, LI Jing
(Dept.of Pharmacy, the Affiliated Hospital of Qingdao University, Shandong Qingdao 266000, China)
ABSTRACTOBJECTIVE:To investigate the adverse drug reaction (ADR) induced by esomeprazole, and provide reference for the rational drug use in clinic. METHODS: To set “esomeprazole” as the key words, literatures related to ADR induced by esomeprazole in CHDL, Wanfang, VIP database and Pubmed during 1995-2015 were retrieved, statistical analysis was conducted on the patients’ gender, age, occurrence time of ADR, ADR-involved organs and systems and clinical manifestations, rescue measures and prognosis. RESULTS: Totally 101 cases were retrieved. ADR induced by esomeprazole most were seen during 60-79 years old(53.47%); ADR can involve multiple organs and(or) systems, mainly manifested as digestive system reaction (33.66%) and urinary system(12.87%). CONCLUSIONS: Great importance should be attached to ADR monitoring, so as to ensure the medication safety.
KEYWORDSEsomeprazole; Adverse drug reaction; Literature analysis
(收稿日期:2015-09-10)
中图分类号R969.3
文献标志码A
文章编号1672-2124(2016)04-0546-03
#通信作者:副主任药师。研究方向:医院药学。E-mail:lijing7112@126.com
*药师,硕士。研究方向:临床药学。E-mail:nibeibeiabce@163.com
