痛风诊断标准的演变及新标准解读
2016-05-25综述刘志红审校
安 玉 综述 刘志红 审校
·医学继续教育·
痛风诊断标准的演变及新标准解读
安 玉 综述 刘志红 审校
痛风是一种常见的代谢性疾病,临床可表现高尿酸血症、急性关节炎、反复痛风石沉积和慢性关节炎,并可导致肾脏损害。目前已有多种痛风诊断标准,其中最常用的是1977年美国风湿病学会制定的急性痛风性关节炎分类标准,但该标准已不能满足目前临床和研究的需求。最近美国风湿病学会和欧洲抗风湿联盟协作推出痛风诊断的新标准。本文就痛风诊断标准的演变和新标准的制订作一综述。
痛风 诊断标准 美国风湿病学会/欧洲抗风湿联盟
痛风是一组由嘌呤代谢紊乱引起血尿酸水平升高,单钠尿酸盐(MSU)晶体沉积,从而引起组织损伤的临床综合征。临床可表现高尿酸血症、急性痛风性关节炎、反复痛风石沉积、慢性关节炎和关节功能障碍,并可导致痛风性肾病、尿酸性肾结石和急性肾损伤[1]。目前有多种痛风诊断的指南和推荐意见,其中以1977年美国风湿病学会(American Rheumatism Association,ARA,1988年后改称American College of Rheumatology,ACR)制定的急性痛风性关节炎分类标准应用最为广泛[2]。随着现代影像学技术的快速发展和临床试验的广泛开展,该标准已不能满足临床和研究的需求。最近ACR和欧洲抗风湿联盟(European League Against Rheumatism,EULAR)协作推出了痛风诊断的新标准。本文就痛风诊断标准的演变和新标准的制订作一综述。
痛风诊断标准回顾
1961年,Mccarty等[3]在偏振光显微镜下观察到痛风患者关节滑液中的MSU结晶。此后,在关节滑液或痛风石中检出MSU结晶成为痛风诊断的“金标准”。然而,由于痛风患者大部分就诊于基层医疗机构,而该项检查需依赖关节腔穿刺术及专业人员观察,其临床可行性受到很大限制。因此,制订痛风的临床分类标准仍有必要。
1963年公布的罗马标准包括以下四条:(1)血尿酸水平男性>7 mg/dl,女性>6 mg/dl;(2)出现痛风石;(3)滑液或组织中找到MSU结晶;(4)突发的关节疼痛、肿胀,2周内缓解。其中符合2条即可诊断痛风。1966年的纽约标准对罗马标准进行修订,将MSU结晶单独列出作为诊断痛风的充分标准,在临床标准中去掉血尿酸水平,增加了痛风发作的部位(足痛风)及对秋水仙碱的治疗反应[2]。
1977年,ARA组织38位来自美国的风湿病专家对706例患者的数据进行分析(包括178例原发性痛风,299例类风湿性关节炎,110例假性痛风,119例急性化脓性关节炎),制定了急性痛风性关节炎诊断的分类标准(表1)[4]。该标准除仍将MSU结晶列为痛风诊断的充分标准外,进一步将临床分类细化为12条标准,并增加了痛风导致关节损伤的X线影像学改变。2010年Pelez-Ballestas等[5]通过对549例痛风患者的横断面分析,根据本国痛风患者的症状特点提出墨西哥标准,此标准可视为ARA标准的简化。

表1 1977年美国风湿病学会急性痛风性关节炎分类标准[4]
需要指出的是,上述四项诊断标准在制定过程中,均从仅有临床诊断而缺乏MSU结晶证实的痛风患者中分析总结得出。2010年,Janssens等[6]对328例由家庭医师诊断为痛风的单关节炎患者进行关节滑液分析检查(其中209例患者证实有MSU结晶),通过多因素Logistic回归分析对不同的临床表现与MSU结晶之间的相关性进行评分,提出了痛风诊断的荷兰标准(表2)。该标准旨在针对就诊于基层医疗诊所、无条件进行关节滑液分析的急性单关节炎患者,评分≥8分考虑痛风,评分<8且>4分提示需进一步行关节滑液分析确诊,诊断的ROC曲线下面积为0.85。
2006年,EULAR在临床研究工作组(ESCISIT)的指导下,由来自13个国家的19位风湿病专家组成的专家组对痛风的诊断和治疗提出相应的建议,推出痛风和高尿酸血症的诊治指南,并于2011年进行修订[7-8]。然而,尽管对痛风的认识不断深入,ARA标准至今仍是临床应用最为广泛的痛风诊断标准,2011年中华医学会风湿病学分会公布的“原发性痛风诊断和治疗指南”仍沿用该标准对急性痛风性关节炎的进行诊断[9]。

表2 2010年荷兰标准[6]
≤4分可排除痛风,≥8分考虑痛风,<8且>4分提示 需行关节液分析
现有诊断标准的局限性
既往研究表明,尽管目前已有多种痛风诊断标准,但并无一项标准能兼顾较高的敏感性与特异性。将MSU结晶这一金标准纳入诊断标准提高了诊断的特异性,但其敏感性有限,且部分无症状的高尿酸血症患者也可出现关节滑液MSU结晶[2]。研究表明,罗马标准和纽约标准的敏感性分别为64%~82%和64%~80%,ARA标准的敏感性为70%~85%,特异性为64%~97%[10-12]。另一项纳入167例患者(其中MSU结晶证实的痛风75例)的验证研究显示,墨西哥标准的敏感性与特异性分别为97.3%和95.6%,但该研究中对照样本并未行关节液检查,且痛风患者中痛风石的发生率高达81%,降低了研究结果的普适性[13]。
随着现代影像技术的发展,新的影像学手段在显示尿酸盐沉积中展现了独特的优势(图1)。超声在尿酸盐沉积的部位可发现特征性的“双边征”,表现为关节透明软骨表面不规则的高回声带,且不随声波的探测角度改变[14]。不同研究显示这种“双边征”对诊断痛风的特异性高达95%~100%,敏感性也可达21%~92%[15-17]。双源CT(dual energy computed tomography,DECT)带有2套球管(管电压分别80 kV和140 kV),可无创、快速扫描检测区域,并自带特异性分析软件,能更准确地识别并分离尿酸盐(绿色伪彩)和钙盐(红色伪彩)[18-19]。而现有的诊断标准并未纳入这些新的影像学技术。
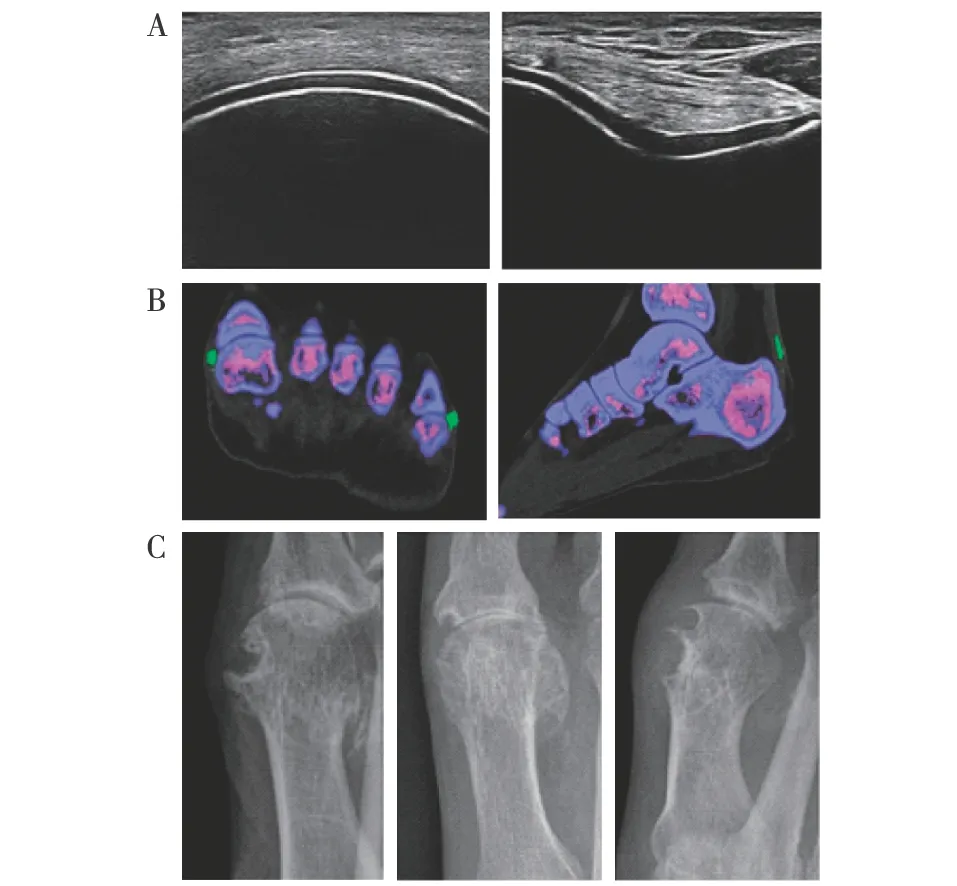
图1 痛风的典型影像学改变 A:股骨关节软骨表面超声“双边征”,左图为纵切面,右图为横切面;B:DECT显示尿酸盐沉积征象,左图为第一及第五跖趾关节周围尿酸盐沉积,右图显示跟腱尿酸盐沉积;C:X线显示第一跖趾关节侵蚀证据,表现为骨皮质破坏,可见硬化带、边缘突出
此外,近年来痛风的治疗也取得不少进展,新型药物的临床试验及痛风相关危险因素、基因组学、流行病学等研究均有赖于准确的病例入组。如前所述,痛风患者多就诊于基层医疗机构或急诊,无法进行关节腔穿刺和偏振光显微镜检查。且现有的诊断标准多针对急性痛风性关节炎,对广大处于痛风发作间歇期和慢性关节炎期的患者并不适用。如何在临床研究中纳入相对均质且缺乏MSU结晶证实的痛风患者,是目前痛风研究的一个难题。
ACR/EULAR痛风分类标准简介
为了解决上述标准的局限性,使痛风诊断标准更好地为临床科研工作服务,2015年ACR和EULAR共同提出了新的痛风分类标准(表3)[20]。该标准的制订分为以下三个步骤:
(1)拟定诊断条款。首先通过Delphi法采集痛风的临床特点,由来自不同国家的44位临床医师与9例痛风患者分别描述其认为与痛风相关的表现,通过专家调查法得出一组诊断条款[21]。其次对收集到的条款进行验证(SUGAR研究)[22],从16个不同的国家募集983例痛风患者,所有患者均对有症状的关节或皮下结节进行了穿刺检查,并完善了影像学检查,其中653例患者对上述条款进行了测定,余下330例患者进行了后续的验证研究。最后还对有关痛风新的影像学技术进行了系统的文献复习[23]。

表3 2015年美国风湿病学会/欧洲抗风湿联盟痛风分类标准[20]
MSU:单钠尿酸盐;DECT:双源CT;*:无相关检查结果或尿酸水平在≥4且<6 mg/dl(≥0.24且<0.36 mmol/L)均记为0分,总分≥8分即可诊断痛风
(2)由17位风湿病专家、2位保健医生和1位流行病学家组成的专家座谈小组通过等级法对30例拟诊为痛风的患者资料进行排序,采用决策分析法得出初步诊断标准,包括入排标准、充分标准和具体分类,然后通过离散选择模型和决策分析达成共识,确定每项分类的相对权重。
(3)对SUGAR研究中的数据进行分析,选取敏感性和特异性之和最高的得分点作为诊断的截点,其假阴性率和假阳性率分别为13.9%和10.5%。然后用SUGAR研究中余下的330例患者资料对新标准的效能进行验证,并与现有的诊断标准进行比较。
验证研究结果显示,新标准的敏感性和特异性分别为0.92和0.89,ROC曲线下面积为0.95。当剔除关节滑液分析和影像学检查结果(记为0分)时,该标准的敏感性和特异性分表为0.85和0.78,ROC曲线下面积仍有0.89。对比1977年ARA标准的敏感性和特异性分表为1.0和0.51,ROC曲线下面积为0.83,荷兰标准的敏感性和特异性分别为0.95和0.59,ROC曲线下面积为0.87,其余各标准的特异性均不超过0.78,显示了新标准的优越性[20]。
ACR/EULAR痛风分类标准的解读
ACR/EULAR痛风分类标准包含了痛风的临床表现(受累关节类型、症状发作特点、时间进程及痛风石)、实验室检查(血尿酸水平、关节滑液分析)及影像学特点(X线、超声或DECT),总分为23分,≥8分即可诊断痛风。既保留的传统观念上的痛风特点,又加入了新的影像学技术。研究结果来自较大的国际化的样本库,说明其应用于临床具有较高的普适性。且该标准首次在分类中引入了负分的机制,即当血尿酸水平<4 mg/dl或关节液分析MSU阴性时,认为此种情况不支持痛风的诊断,分别减去4分和2分。验证研究结果表明该标准兼顾了较高的敏感性与特异性,其诊断效能高于目前已有的诊断标准,尤其是缺乏关节滑液分析和影像学检查结果时,该标准仍具备较高的敏感性与特异性,显示了良好的可操作性。
值得一提的是,由于该标准制定的初衷在于为观察性研究和临床试验纳入相对均质的痛风患者,考虑到一些与痛风相关的特征如患者对药物治疗的反应、家族史、痛风相关的危险因素和合并症等,有可能会对未来探讨这些因素的研究造成干扰,因而并未将其纳入诊断标准中。
另外,该标准的不足之处在于诊断标准中新的影像学技术特征来自于文献复习,相关数据较少,且多为经验性研究。未来随着影像学技术的进一步发展,更多特征性的痛风影像学改变可能会被纳入新的诊断标准中。
小结:经过数十年的发展,痛风的诊断标准逐渐趋于完善。2015年ACR/EULAR痛风分类标准较全面的囊括了痛风的临床表现、实验室检查和影像学表现,操作简便,验证研究显示其具有较高的敏感性和特异性,诊断效能优于目前已有的诊断标准,为痛风的临床诊治和科研工作提供了一个新工具。
1 Yuan HY,Zhang XH,Zhang XL,et al.Analysis of patents on anti-gout therapies issued in China.Expert Opin Ther Pat,2014,24(5):555-572.
2 Dalbeth N,Fransen J,Jansen TL,et al.New classification criteria for gout:a framework for progress.Rheumatology (Oxford),2013,52(10):1748-1753.
3 Mccarty DJ,Hollander JL.Identification of urate crystals in gouty synovial fluid.Ann Intern Med,1961,54:452-460.
4 Wallace SL,Robinson H,Masi AT,et al.Preliminary criteria for the classification of the acute arthritis of primary gout.Arthritis Rheum,1977,20(3):895-900.
5 Peláez-Ballestas I,Hernández Cuevas C,Burgos-Vargas R,et al.Diagnosis of chronic gout:evaluating the american college of rheumatology proposal,European league against rheumatism recommendations,and clinical judgment.J Rheumatol,2010,37(8):1743-1748.
6 Janssens HJ,Fransen J,van de Lisdonk EH,et al.A diagnostic rule for acute gouty arthritis in primary care without joint fluid analysis.Arch Intern Med,2010,170(13):1120-1126.
7 Zhang W,Doherty M,Pascual E,et al.EULAR evidence based recommendations for gout.Part I:Diagnosis.Report of a task force of the Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT).Ann Rheum Dis,2006,65(10):1301-1311.
8 Hamburger M,Baraf HS,Adamson TC 3rd,et al.2011 recommendations for the diagnosis and management of gout and hyperuricemia.Phys Sportsmed,2011,39(4):98-123.
9 中华医学会风湿病学分会.原发性痛风诊断和治疗指南.中华风湿病学杂志2011,15(6):410-413.
10 Rigby AS,Wood PH.Serum uric acid levels and gout:what does this herald for the population? Clin Exp Rheumatol,1994,12(4):395-400.
11 Malik A,Schumacher HR,Dinnella JE,et al.Clinical diagnostic criteria for gout:comparison with the gold standard of synovial fluid crystal analysis.J Clin Rheumatol,2009,15(1):22-24.
12 Janssens HJ,Janssen M,van de Lisdonk EH,et al.Limited validity of the American College of Rheumatology criteria for classifying patients with gout in primary care.Ann Rheum Dis,2010,69(6):1255-1256.
13 Vázquez-Mellado J,Hernández-Cuevas CB,Alvarez-Hernández E,et al.The diagnostic value of the proposal for clinical gout diagnosis (CGD).Clin Rheumatol,2012,31(3):429-434.
14 Naredo E,Uson J,Jiménez-Palop M,et al.Ultrasound-detected musculoskeletal urate crystal deposition:which joints and what findings should be assessed for diagnosing gout? Ann Rheum Dis,2014,73(8):1522-1528.
15 Ottaviani S,Richette P,Allard A,et al.Ultrasonography in gout:a case-control study.Clin Exp Rheumatol,2012,30(4):499-504.
16 Filippucci E,Riveros MG,Georgescu D,Hyaline cartilage involvement in patients with gout and calcium pyrophosphate deposition disease.An ultrasound study.Osteoarthritis Cartilage,2009,17(2):178-181.
17 Rettenbacher T,Ennemoser S,Weirich H,Ulmer H,Hartig F,et al.Diagnostic imaging of gout:comparison of high-resolution US versus conventional X-ray.Eur Radiol,2008,18(3):621-630.
18 Glazebrook KN,Guimarães LS,Murthy NS,et al.Identification of intraarticular and periarticular uric acid crystals with dual-energy CT:initial evaluation.Radiology,2011,261(2):516-524.
19 Mallinson PI,Coupal T,Reisinger C,et al.Artifacts in dual-energy CT gout protocol:a review of 50 suspected cases with an artifact identification guide.AJR Am J Roentgenol,2014,203(1):W103-W109.
20 Neogi T,Jansen TL,Dalbeth N,et al.2015 Gout classification criteria:an American College of Rheumatology/European League Against Rheumatism collaborative initiative.Ann Rheum Dis,2015,74(10):1789-1798.
21 Prowse RL,Dalbeth N,Kavanaugh A,et al.A delphi exercise to identify characteristic features of gout - opinions from patients and physicians,the first stage in developing new classification criteria.J Rheumatol,2013,40(4):498-505.
22 Taylor WJ,Fransen J,Jansen TL,et al.Study for Updated Gout Classification Criteria:Identification of Features to Classify Gout.Arthritis Care Res (Hoboken),2015,67(9):1304-1315.
23 Ogdie A,Taylor WJ,Weatherall M,et al.Imaging modalities for the classification of gout:systematic literature review and meta-analysis.Ann Rheum Dis,2015,74(10):1868-1874.
(本文编辑 莫 非 凡 心)
A new classification criteria for gout and its development
ANYu,LIUZhihong
NationalClinicalResearchCenterofKidneyDiseases,JinglingHospital,NanjingUniversitySchoolofMedicine,Nanjing210016,China
Gout is a common metabolic disorder characterized by hyperuricemia, acute gouty arthritis, recurrent tophi deposition and chronic arthritis, and usually resulting in kidney damage. There are several existing classification criteria for gout. The most widely used one is the 1977 American Rheumatology preliminary criteria for the classification of the acute arthritis of primary gout, in spite of obvious limitations. Recently a new classification criteria was developed by the American College of Rheumatology and the European League Against Rheumatism. This review is to introduce the development of classification criteria for gout and the formulation of the new classification.
gout classification criteria American College of Rheumatology/European League Against Rheumatism
10.3969/cndt.j.issn.1006-298X.2016.02.014
南京军区南京总医院肾脏科 国家肾脏疾病临床医学研究中心 全军肾脏病研究所(南京,210016)
2015-12-18
