煤基活性炭的氧化改性及其对Cd2+的吸附性能∗
2016-05-16王娅娅唐亚昆高莎莎周蓉刘浪
王娅娅,唐亚昆,高莎莎,周蓉,刘浪
(1.新疆大学化学化工学院,新疆乌鲁木齐830046;2.能源材料化学教育部重点实验室,新疆乌鲁木齐830046;3.新疆大学学报编辑部,新疆乌鲁木齐830046)
0 引言
重金属离子是常见的有毒污染物,不能被生物降解,易产生毒性反应,且毒性具有长期持续性等特点[1].重金属废水排入水体中会造成严重的污染环境,因此重金属废水的有效治理在国内外引起广泛重视.目前去除水中重金属离子的方法主要有混凝法、气浮法、离子交换法和膜分离技术等[2−6],采用这些传统的工艺不仅消耗大量能源,而且易产生二次废物.然而吸附法因具有适应范围广、净化效率高、吸附剂可重复使用等优点,是去除水中重金属离子的最为有效快捷的方法.因此,开发高效的去除重金属离子的吸附材料变得尤为重要.
活性炭是一种多孔的吸附材料,具有比表面积大,表面官能团丰富,因而被广泛应用于水净化,环境保护等领域[7].根据原料的不同,活性炭可分为木质活性炭、果壳类活性炭(椰壳、杏核、核桃壳、橄榄壳等)、煤质活性炭和石油焦活性炭等种类.相对于木质和果壳类活性炭,煤质活性炭由于其原料来源广泛,品种齐全,价格相对低廉,发展速度较快.新疆煤炭预测量达2.19万亿吨,约占全国预测资源总量的40%,位居全国首位.基于新疆丰富的煤炭资源优势,开展新型煤基碳材料的制备和应用研究,将会促进新疆煤炭资源的综合利用,从而延长新疆煤化工产业链.但以煤为基质制备传统的活性炭对重金属离子的吸附量太低,不能满足实际需求.近年来,采用越来越多的方法对活性炭进行修饰,以改善其对重金属离子的吸附行为[8−10].经大量研究表明,表面修饰的活性炭可显著提高对重金属离子的吸附性能.因而,对活性炭进行表面化学改性是提高其吸附性能的一种较为有效的手段.目前对活性炭表面改性的方法主要有氧化改性、还原改性、负载金属改性等[11−13].而用HNO3氧化处理的活性炭,其表面可产生较多的酸性基团,从而获得较高的阳离子交换容量,对重金属离子有较高的吸附交换能力[14−16].
本文以新疆库车煤为原料,以KOH为活化剂,在1:2碱碳比下,采用化学活化法制备煤基活性炭,并用不同浓度的硝酸通过加热回流方式对制备的活性炭进行表面改性处理,探讨了改性前后活性炭的结构变化及表面官能团对重金属离子吸附性能的影响.结果表明:改性活性炭由于具有丰富的含氧官能团和吸附位点对重金属离子Cd2+有较大的吸附,并探讨了其吸附机理.
1 实验部分
1.1 试剂
新疆库车煤炭,氢氧化钾(KOH,分析纯,天津市盛淼精细化工有限公司),盐酸(HCl,优极纯,洛阳市兴隆化工有限公司),氢氧化钠(NaOH,分析纯,天津市百世化工有限公司)硝酸(HNO3,分析纯,成都市科龙化工试剂厂),硝酸铅(PbNO3,分析纯,天津市盛奥化学试剂有限公司),甲基红、溴甲酚绿、氯化镉(CdCl2.2H2O)均为天津市光复科技发展有限公司,酚酞(天津市福晨试剂厂),实验用水均为蒸馏水.

表1 新疆库车煤样分析(%)
1.2 活性炭的制备
采用固相化学活化法制备活性炭:按KOH与煤炭质量比为1︰2和4︰1进行称量,将其在玛瑙研钵中均匀混合,移至刚玉舟,置于管式炉内,在氮气保护下,以5◦C/min速度加热至800◦C,活化60 min,等温度降至室温后取出,磨细,然后用2 mol.L−1的盐酸进行酸洗脱灰,抽滤,用蒸馏水将滤液洗至中性,收集样品于烘箱中110◦C干燥6 h,得产品活性炭,分别将其命名为AC、AC1.
称取3份AC(1 g)分别投入到体积浓度为90%、60%、30%的100 mLHNO3溶液中,在70◦C的条件下回流12 h,冷却后,抽滤,反复洗涤至中性,再于80◦C烘箱中烘干至恒重.最后得改性活性碳,分别标记为AC-90,AC-60,AC-30.
1.3 Boehm滴定
具体步骤为:称取3份酸处理后的样品各200mg,加入50mL0.05 mol/L的NaHCO3、Na2CO3和NaOH溶液中,密封并振荡反应24 h.每份溶液过滤后,滤液用0.05 mol/L HCI反滴定剩余碱液,求得碱液反应量,从而计算出活性炭表面酸性基团的量.
1.4 改性活性炭吸附动力学实验
取100 mL一定质量浓度Cd2+溶液于200 mL锥形瓶中,用0.1 mol/L HCl或0.1 mol/L NaOH调节溶液pH值,加入0.05 g吸附剂样品,放入振荡器内在室温以180 r/min的速度振荡12 h后过滤,取上清液测Cd2+的质量浓度.
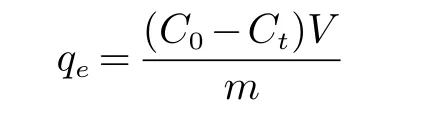
qe:活性炭单位质量所吸附的量(mg/g);C0:溶液初始浓度(mg/L);Ct:溶液终了浓度(mg/L);V:溶液体积(L);m:活性炭质量(g).
1.5 活性炭样品的表征
采用美国Micromeritics ASAP 2020全自动物理吸附仪对样品进行比表面积(BET)和孔结构(BJH)分析:以高纯氮为吸附质在77K对样品进行N2吸脱附测试,对微孔材料的孔结构分析采用Horvaih-Kawazoe方程,由t-plot法计算微孔的比表面积和孔容积,在相对压力P/P0=0.95时测得总孔容积;采用德国Bruker公司生产的EQUINOX-55 spectrometer型红外光谱分析仪定性分析样品表面含氧、氮官能团;采用日本日立公司的Z-2000型原子吸收测试仪进行离子浓度测试.
2 结果与讨论
利用煤为原料,采用KOH化学活性法制备活性炭,其中碱碳比是影响活性炭比表面积和孔结构的重要因素.一般来说,随着碱碳比的增加,活性炭的比表面积增大.当碱碳比为4:1时,我们制备的活性炭比表面积达2 930 m2/g,远大于碱碳比1:2条件下制备的活性炭的比表面积1 104 m2/g(表2).然而当把这两种活性炭作为对重金属Cd2+离子的吸附剂时,在100 mg/L Cd2+离子浓度的溶液中,其吸附量分别为6.0 mg/g和5.5 mg/g,这一结果表明,活性炭的比表面积增大,其对重金属离子的吸附量增加不显著.也就是说活性炭的比表面积与吸附重金属离子量并不成正比.然而传统化学活化法通常采用大量的强碱来活化造孔,大量碱的使用提高了生产成本,而且高温下对设备有较强腐蚀作用,活化后产品洗涤时用水量大.因此降低活化剂用量以及洗涤用水量是煤基活性炭活化工艺中需要迫切解决的一个技术难题之一.从原料来源、成本及产品性能方面综合考虑,我们选择碱碳比1:2条件下制备的活性炭作为后续的表面改性的研究对象.
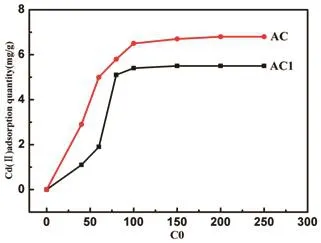
图1 不同碱碳比的活性炭对Cd2+的吸附
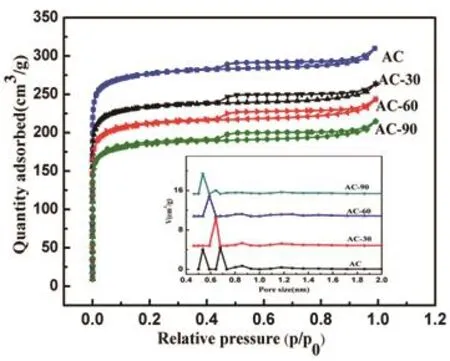
图2 硝酸改性前后活性炭的N2吸脱附曲线和孔径分布图
2.1 活性炭的孔结构及比表面积分析
图2是在77K下,AC,AC-30,AC-60,AC-90的氮气吸脱附曲线,根据IUPAC分类法,这些活性炭的吸附类型属于I型曲线[17−18].从表2可以得出,经HNO3氧化处理的活性碳的结构有很大的变化,未氧化AC比表面积为1 104 m2/g,经过硝酸氧化后AC-90的比表面积已减小至736 m2/g,并随着氧化程度的增加氧化活性炭的总孔容和微孔孔容都呈现逐渐降低趋势,且平均孔径变大,这是由于硝酸浓度的增大,氧化程度也随之增加,在孔的入口处和微孔壁上形成了大量的含氧基团,阻止气体进入孔道,减少了N2的吸附量,因此活性炭比表面及孔结构发生了很大变化.
2.2 活性炭的组成分析
图3是活性炭氧化改性前后的傅里叶变换红外光谱.从图可以看出,经HNO3氧化改性的活性炭的吸收峰相对强度发生了变化,且产生了新的吸收峰.在3 425 cm−1处的峰为O-H键伸缩振动峰,该峰在改性后的样品中强度明显增强.同时,还发现AC-30,AC-60在1 716 cm−1附近出现了新峰,这可归属于氧化后活性炭表面的羧基中C=O键的伸缩振动[19],然而AC-90在1 628 cm−1和1 410 cm−1附近出现了离子化羧基(COO-)中C=O键的不对称和对称伸缩振动[20].上述结果表明:活性炭经过硝酸氧化改性后,在表面引入了大量的含氧官能团,为通过离子交换或配合等方式吸附溶液中的重金属离子提供了途径.
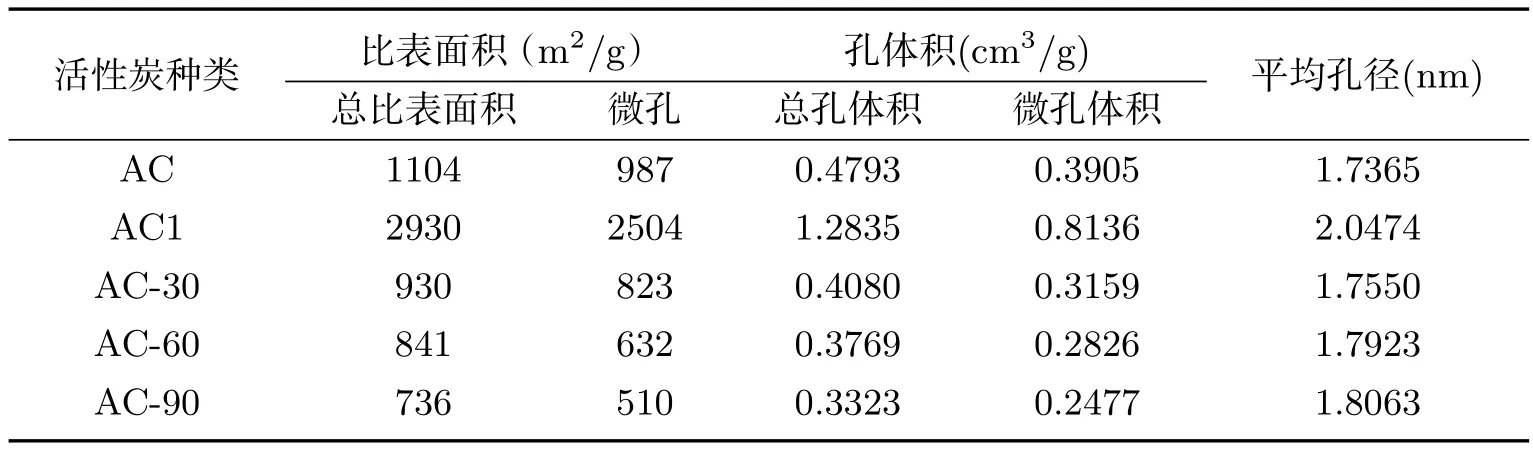
表2 硝酸改性前后活性炭的比表面积和孔结构参数
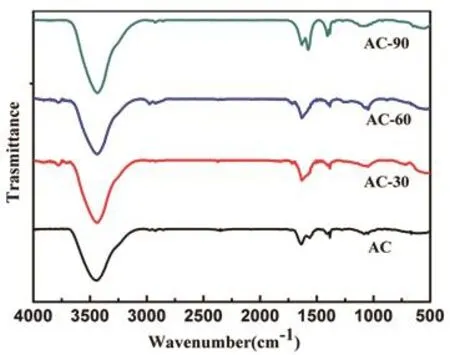
图3 活性炭改性前后的红外图谱
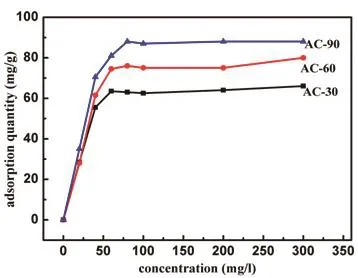
图4 溶液初始浓度对活性炭吸附Cd2+的影响
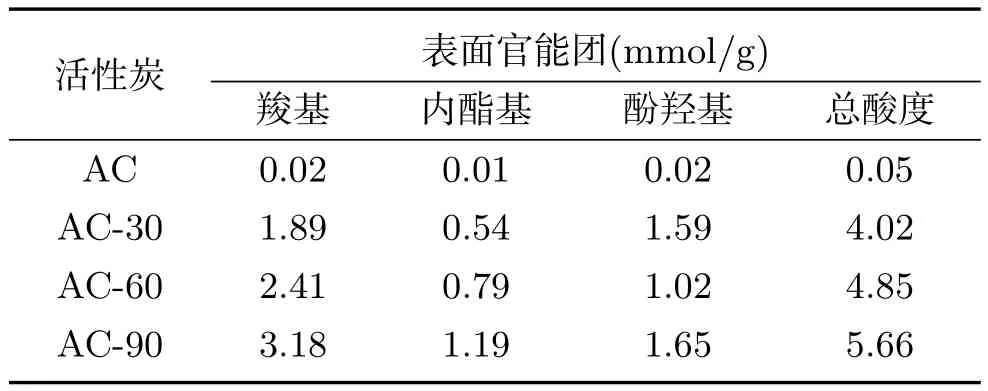
表3 不同氧化程度活性炭的伯姆滴定结果
为了进一步确定活性炭表面各类官能团的含量,我们采用Boehm滴定法进行分析.活性炭表面酸碱性主要由羧基、内酯基、酚羟基和羰基引起,而Boehm滴定法是根据不同强度的碱与不同含氧官能团反应进行定性与定量分析.一般认为,NaHCO3(pK=6.37)仅中和羧基,Na2CO3(pK=10.25)中和羧基和内酯基,NaOH(pK=15.74)中和羧基、内酯基和酚羟基[21−22].从表3中数据可以得知,由于AC表面有少量强酸性的表面基团(如羧基),因此AC不与Na2CO3和NaHCO3反应.经过不同程度的氧化,表面羧基、内酯基、酚羟基等官能团的含量都有不同程度的增加,未氧化的AC表面上的羧基为0.02 mmol/g,而用不同浓度的HNO3氧化后,AC-30,AC-60,和AC-90表面上的羧基分别为1.89,2.41和3.18 mmol/g.它们的总酸度由改性前0.05 mmol/g增大到5.66 mmol/g(AC-90).上述结果表明:随着氧化程度的增强,活性炭表面酸性能官团逐渐增多,表面总酸性也增强,经过90%浓硝酸氧化处理后,活性炭表面获得了最大的酸度.
2.3 活性炭的吸附性能研究
2.3.1 初始浓度对吸附的影响
配制不同浓度的Cd2+溶液,分别取100 mL一定质量浓度Cd2+溶液于250 mL锥形瓶中,调节pH值为6,分别投入0.05 g的AC-90,AC-60,AC-30,25◦C下在180 r/min摇床下振荡240 min,测定Cd2+浓度,考察浓度对吸附的影响规律.从图4中可以看出,三个样品在溶液浓度小于75 mg/L时,对Cd2+的吸附量随着溶液浓度的增加而急剧增加,当溶液浓度超过75 mg/L后,样品对Cd2+的吸附量变化不大.在溶液浓度为100 mg/L时,AC-30、AC-60、AC-90对Cd2+的吸附量依次为64 mg/g、80 mg/g、91 mg/g,远远大于未改性的活性炭对Cd2+的吸附量5.5 mg/g.研究结果表明:硝酸改性可以显著增加活性炭对Cd2+的吸附量,这是由于活性炭经强氧化的硝酸处理后活性炭表面引入了大量的含氧官能团,尤其是表面含氧酸性官能团增多,具有酸性表面基团的活性炭有阳离子交换特性,其中羧基-COOH的大量生成对于金属离子吸附具有重要的贡献,羧基对金属离子的吸附主要是通过螯合反应而发生的,反应方程式用下式来表示[23]:Mn++n(-COOH)=(-COO−)nM+nH+.因此,氧化改性后的活性炭对金属离子的吸附能力明显提高,其中AC-90对100mg/L的Cd2+溶液吸附量最大.
2.3.2 吸附时间对吸附的影响
移取100 mL的100 mg/L的Cd2+溶液于250 mL的锥形瓶中,称取50 mg AC-90的样品,调节pH值到6,25◦C下在180 r/min摇床下振荡240 min,测定Cd2+浓度,考察时间对吸附的影响规律.图5为AC-90在不同时间对Cd2+的吸附行为.由图5可知,在起始的30 min内,样品AC-90对金属离子的吸附量随接触时间的增加而急剧增大,超过30 min后,吸附量变化趋于平缓,最后达到吸附平衡.在1 h时,AC-90对Cd2+的吸附量达到61 mg/g.因此,金属离子达到吸附平衡的时间选择1 h最佳.
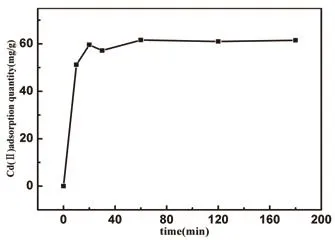
图5 吸附时间对活性炭吸附Cd2+的影响
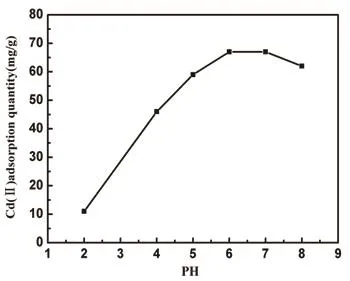
图6 pH值对活性炭吸附Cd2+的影响
2.3.3 pH对吸附的影响
移取100 mL配制好的100 mg/L Cd2+溶液于250 mL的锥形瓶中,称取50 mg AC-90样品,调节溶液的pH值为2,4,5,6,7,8于25◦C摇晃1 h过滤,测定Cd2+浓度,考察pH对吸附的影响规律.从图6可以看出在酸性条件下随着pH值的逐渐增大,吸附量呈增加趋势,当在pH值为6时吸附量达到最大.这是由于在酸性条件下,吸附剂表面正电荷增多,吸附剂对Cd2+的静电排斥加大,对吸附不利.与此同时,吸附作用受pH影响很大主要是因为在离子交换中H+会与Cd2+竞争吸附位点,使去除率降低[24].随着pH的上升,H+与Cd2+之间的竞争会逐渐减弱,因为表面活性位点会带更多的负电荷,这样能够通过静电引力作用,吸附金属离子,可以推测离子交换和静电吸引是主要的吸附机制作用.
2.4 吸附动力学研究
为了研究表面氧化改性活性炭对Cd2+的吸附过程如何进行,采用一级动力学模型和表观二级动力学模型对实验数据进行拟合:

(2)式中qe和qt分别为平衡吸附量和吸附时间为t时刻的吸附量;t为吸附时间;k1和k2分别为吸附速率常数.
拟合结果见表4,由表可知,一级动力学模型和二级动力学模型的拟合结果中二级动力学拟合线性相关系数R2均接近于1,且二级动力学模型所得平衡吸附量53.8 mg/g与实验所得平衡吸附量61.5 mg/g接近,因此Cd2+浓度随吸附时间的变化关系可以很好地用准二级动力学方程进行模拟,这表示改性活性炭对金属离子的吸附过程遵循二级反应机理,吸附速率被化学吸附所控制.
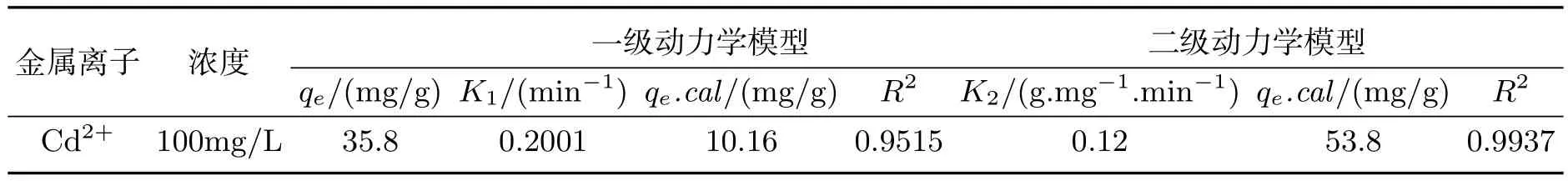
表4 改性活性炭吸附Cd2+的动力学模型参数
2.5 吸附等温模型研究
Langmuir吸附等温线模型是基于吸附剂的表面只能发生单分子层吸附的假设提出的,Freundlich模型则提供了一种单组份吸附平衡的经验描述.应用Langmuir、Freundlich吸附模型对实验数据进行拟合,计算得到各模型参数列于表5中.从表5可知,改性活性炭对Cd2+的Langmuir吸附模型线性相关系数R2为0.999 9,而Freundlich吸附模型线性相关系数R2为0.981 8,说明Langmuir吸附等温方程更适合描述改性活性炭对Cd2+的吸附,因此推测Cd2+在改性活性炭表面发生单分子层吸附达到平衡.
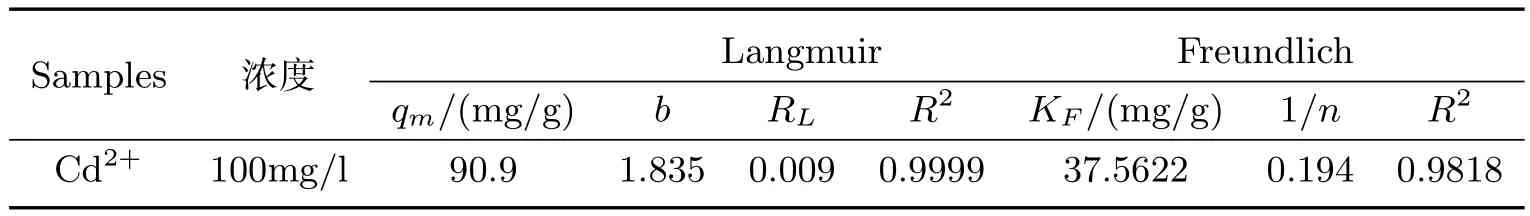
表5 改性活性炭吸附Cd2+的热力学模型参数
3 结论
本文以煤为原料制备了氧化改性活性炭,通过红外光谱、Boehm滴定和孔径测试表明氧化改性活性炭含氧官能团增多,比表面积减小,平均孔径增大,对重金属Cd2+吸附能力增强.这是由于活性炭的吸附性主要依赖于其表面化学结构,硝酸改性后活性炭表面含氧官能团增多,亲水性增强,吸附位点增多,致使吸附效率提高、去除率增加.该方法制备的活性炭具有比表面积高,收率高,活化温度低、活化时间短等优点,更重要的是所用的活化剂用量小、环境污染小,吸附效率高,吸附能力强,因而具有很大的工业应用价值.这对实现重金属离子的工业化应用有重要的意义,也为实际应用提供了新的思路.
参考文献:
[1]徐友宁,张江华,柯海玲,等.某金矿区农田土壤重金属污染的人体健康风险[J].地质通报,2014,33(8):1240-1252.
[2]陈文松,韦朝海.Fenton氧化-混凝法处理印染废水的研究[J].工业水处理,2004,24:39-41.
[3]康万利,张黎明,杜会颖,等.气浮法处理油田污水[J].进展应用化工,2012,41:2148-2153.
[4]张海云,李爱民,郑凯.水和树脂类型对磁性离子交换树脂深度处理城市污水的影响[J].水处理技术,2014,40:48-52.
[5]雷晓东,熊蓉春,魏刚.膜分离法污水处理技术[J].工业水处理,2002,22:1-3.
[6]张帆,李菁,谭建华,等.吸附法处理重金属的研究进展[J].化工学报,2013,32:2749-2756.
[7]Xiaoqi Sun,Bo Peng,Yang Ji,et al.Chitosan(chitin)/cellulose composite biosorbents prepared using ionic liquid for heavy metal ions adsorption[J].Aiche J,2009,55:2062-2069.
[8]Chingombe P,Saha B,Wakeman R J,et al.Surface modification and characterisation of a coal-based activated carbon[J].Carbon,2005,43:3132-3143.
[9]Zhenping Zhu,Zhenyu Liu,Shoujun Liu,et al.NO reduction with NH3over an activated carbon-supported copper oxide catalysts at low temperatures[J].Appl Catal B-Environ,2000,26:25-35.
[10]Ryszard D,Magdalena O.Preparation and evaluation of Ni-loaded activated carbon for enrichment of arsenic for analytical and environmental purposes[J].Micropor.Mesorpor.Mat,2013,179:1-9.
[11]Shen L C,Nguyen X T,Hankins N P,et al.Removal of heavy metal ions from dilute aqueous solutions by polymer–surfactant aggregates:A novel effluent treatment process[J].Sep Purif Technol,2015,152:101-107.
[12]Maria V,Radu A C,Luminita A,et al.Advanced treatment of wastewater with methyl orange and heavy metals on TiO2,fl y ash and their mixtures[J].Catal Today,2009,144:137-142.
[13]Shiming Wang,Hongling Li,Xiaoya Chen,et al.Selective adsorption of silver ions from aqueous solution using polystyrenesupported trimercaptotriazine resin[J].J Environ Sci-China,2012,24:2166-2177.
[14]Ru Gao,Zheng Hu,Xijun Chang,et al.Chemically modified activated carbon with 1-acylthiosemicarbazide for selective solid-phase extraction and preconcentration of trace Cu(II),Hg(II)and Pb(II)from water samples[J].J Hazard Mater,2009,172:324-329.
[15]Yantasee W,Lin Y,Fryxell G E,et al.Selective removal of copper(ii)from aqueous solutions using fine-grained activated carbon functionalized with amine[J].Ind Eng Chem Res,2004,43(11):2759-2764.
[16]Rakic V,Rac V,Krmar M,et al.The adsorption of pharmaceutically active compounds from aqueous solutions onto activated carbons[J].J Hazard Mater,2015,282:141-149.
[17]Lozano-Castello D,Lillo-Rodenas,M A,Cazorla-Amoros D.Preparation of activated carbons from Spanish anthracite I.Activation by KOH[J].Carbon,2001,39:741-749.
[18]Huanlei Wang,Gao Qiuming,Juan Hu.High hydrogen storage capacity of porous carbons prepared by using activated carbon[J].J Am Chem Soc,2009,131:7016-7022.
[19]Yan Liu,GuiJia Cui,Chao Luo,et al.Synthesis,characterization and application of amino-functionalized multi-walled carbon nanotubes for effective fast removal of methyl orange from aqueous solution[J].RSC Adv,2014,4:55162-55172.
[20]Chingombe P,Saha B,Wakeman R J.Surface modification and characterization of a coal-based activated carbon[J].Carbon,2005,43:3132-3143.
[21]Boehm H P.Surface oxides on carbon and their analysis:a critical assessment[J].Carbon,2002,40:145-149.
[22]Monser L,Adhoum M.Modified activated carbon for the removal of copper,zinc,chromium and cyanide from wastewater[J].Sep Purif Technol,2002,26:137-146.
[23]Kikuchi Y,Qian Q R,Machida M,et al.Effect of ZnO loading to activated carbon on Pb(II)adsorption from aqueous solution[J].Carbon,2006,44:195-206.
[24]Vukovic G D,Marinkovic A D,Colic M,et al.Removal of cadmium from aqueous solutions by oxidized and ethylenediaminefunctionalized multi-walled carbon nanotubes[J].Chem Eng J,2010,157:238-248.
猜你喜欢
杂志排行
新疆大学学报(自然科学版)(中英文)的其它文章
- The Absolute Ruin Risk Model with Constant Interest Investment and Linear Threshold Dividend Strategy∗
- 细菌诱导光滑鳖甲幼虫抑制差减cDNA文库的构建与分析∗
- 资源型产业与制造业集聚特征与影响因素异同分析∗
- Distance Signless Laplacian Integral Complete R-partite Graphs∗
- Finite-time Stability of Continuous-time Systems with Time-varying Delays∗
- On the Dynamical Behavior of Pest and it’s Predator Model∗
