人血白蛋白中钠离子含量对热稳定性影响的研究
2016-05-14赵朋朋靳继忠曹大伟李庆英董静
赵朋朋 靳继忠 曹大伟 李庆英 董静
【摘要】目的 采用还原光度法测定本公司生产的人血白蛋白中钠离子的含量 ,并确定人血白蛋白热稳定性的最优条件。方法 采用浊度仪对不同钠离子含量的经过热稳定性试验的人血白蛋白后进行澄清度分析。 结果 不同钠离子含量人血白蛋白热稳定存在差异。结论 压滤法生产的人血白蛋白钠离子含量维持在105~125mmol/L时,其热稳定性最好。
【关键词】人血白蛋白;热稳定性
本公司人血白蛋白的生产较之普遍采用的低温乙醇法中的Cohn6+9 法 [1,2], 改成一次性进行组分 I+Ⅱ+Ⅲ沉淀。改进后的工艺具有分离周期短、 参数易于控制,热稳定性好。国内外对于人血白蛋白的热稳定性均有报道[3,4],研究发现在蛋白浓度为20%时,pH值、辛酸钠浓度对稳定性几乎无影响[5,6],而钠离子含量影响明显,而考虑到实际生产取样量的限制,均未对钠离子含量的影响进行详细研究,同时由于热稳定性试验采用肉眼观察无法真实的反映质量指标,本试验通过用浊度计进行检测并统计100批次100个样品的浊度值,真实反映了钠离子含量对人血白蛋白热稳定性的影响,以便达到更好的质控目的。
1 仪器与试药
仪器
火焰光度计(上海傲谱分析仪器有限公司);浊度仪(上海昕瑞);CM-3型澄明度检测仪(天津药典标准仪器厂)
试药:人血白蛋白(山东泰邦生物制品有限公司)
2 方法
从100批次成品中每一批随机选一支,然后进行钠离子含量的检测,然后将100支产品进行50h 50℃加温,对加温前后浊度值进行对比。
3 结果
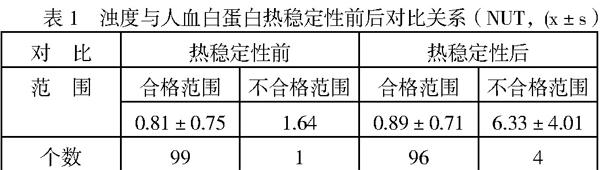
3.1 浊度为1.64 NUT的制品在灯检时发现可见异物不合格,而在热稳定试验后该制品的浊度也在不合格范围内,但由于可见异物的种类较多,不能简单的认为可见异物不合格的热稳定试验后浊度都会在不合格范围内。见表1。
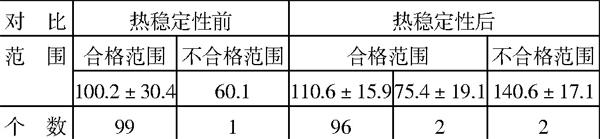
3.2 热稳定实验前后不合格品增加到4瓶,不合格品中钠离子的含量主要在高低两个范围。见表2。
4 讨论
本公司通过压滤法生产的合格的人血白蛋白浊度均小于2 NUT,而通过试验可以看出浊度值可以较为准确的反映热稳定性结果,但是考虑到可见异物的不确定性,浊度检测可以作为澄清度检测前的控制指标。
对于本公司工艺生产的制品,钠离子主要来自于组分I+Ⅱ+Ⅲ沉淀、组分Ⅴ超滤和配制中Nacl的加入,钠离子的含量对人血白蛋白的稳定性要较大影响,在较低含量56.3 mmol/L~94.5 mmol/L和较高含量133.5 mmol/L~157.7 mmol/L时稳定性较差,2015版药典对于人血白蛋白钠离子含量要求是≤160mmol/L[7],而对于本工艺来说最优的含量范围为105 mmol/L ~125 mmol/L,不同的工艺存在差异。
【参考文献】
[1]王 文,张茂宏, 徐从高.Epo和铁代谢与恶性肿瘤贫血[J].中华血液学杂志, 2 0 0 1 ; 2 2(4):2 2 2 ~3.
[2]张之南,等.血液病诊断及疗效标准[M],北京:科学出版社,1 9 9 8.3 0~2.
[3]中国生物制品标准化委员会. 中国生物制品规程[M], 北京:中国医药科技出版社,2000.187.
[4]Cohn P .Proceeding of the workshop on albumin[M]. DHEW Pubhcaion,1975.323.
[5]康建瑞. 关于白蛋白热稳定性及其影响因素的初步分析[J]. 中国输血杂志,2001,14(5):281~282.
[6]吕秀华. 人血白蛋白制品浊度与稳定性的分析[J]. 中国生物制品学杂志,2002, l 5(6):366~368.
[7]国家药典委员会. 中华人民共和国药典三部[M]. 北京:中国医药科技出版社,2015,244~245.
