正交试验设计法筛选印度块菌液体培养基
2016-05-03马欣燕王国正郭成金
马欣燕+王国正+郭成金
摘要: 为筛选出印度块菌(Tuber indicum)最适用的液体培养基,以印度块菌菌丝体生物量为测量指标,采用L9(34)正交试验方法对各配比的印度块菌液体培养基进行研究。结果表明,印度块菌最适液体培养基为20.00 g/L葡萄糖,15.00 g/L麦芽糖,1.50 g/L蛋白胨,2.50 g/L酵母浸粉,3.00 g/L KH2PO4,1.50 g/L MgSO4·7H2O,0.008 g/L维生素B1,pH值自然。25 ℃、120 r/min摇瓶培养120 h,其菌丝生物量干质量可达9.58 g/L。
关键词: 印度块菌;正交试验;液体培养基;菌丝体;生物量
中图分类号: S646.04 文献标志码: A 文章编号:1002-1302(2016)03-0200-03
印度块菌(Tuber indicum)属子囊菌门(Ascomycota)盘菌纲(Pezizomycetes)盘菌目(Pezizales)块菌科(Tuberaceae)块菌属(Tubera)[1],是一种极为珍贵的菌根食用菌。印度块菌主要分布在中国西南地区的云南省、四川省;云南省主要分布在昆明、曲靖、丽江、玉溪、保山、楚雄州、大理州、迪庆州、怒江州等地,四川省主要分布在攀枝花地区、凉山州[2]。印度块菌常生长于云南松、华山松林及高山栎下[3]。据报道,我国出产的印度块菌所含糖、蛋白质、氨基酸、矿物质、维生素等成分很高,可与黑孢块菌(Tuber melonosporum)相媲美[4]。此外,印度块菌所含有的活性成分如块菌多糖、α-雄烷醇等具有提高免疫力、抗氧化、抗肿瘤及调节女性月经等功效[5-9]。
至今,国内外对印度块菌的研究报道主要是在活性物质特性、提取纯化[5-10]、人工栽培[11-12]等方面,未见印度块菌液体培养基筛选方面的相关研究报道。笔者试图通过碳、氮源单因素试验并结合L9(34)正交试验方法的研究,筛选出印度块菌最适液体培养基,旨在为印度块菌菌种生产、原生质体融合、紫外诱变育种以及液体发酵活性物质提取等研究提供理论依据和技术支持。
1 材料与方法
1.1 菌种
印度块菌(Tuber indicum),由天津师范大学生命科学学院蕈菌研究室提供。
1.2 试验试剂
葡萄糖、蔗糖、麦芽糖、乳糖、蛋白胨、酵母浸粉、KH2PO4、 MgSO4·7H2O、维生素B1、琼脂,均为分析纯,购自生工生物工程(上海)股份有限公司。
1.3 试验仪器
YXQG02手提式压力蒸汽消毒器,山东新华医疗器械厂;Sartorius BS/BT系列电子天平,德国赛多利斯科学仪器有限公司;SW-CJ-2超净工作台,上海锦屏仪器仪表有限公司;SPX型生化培养箱,北京市永光明医疗仪器有限公司;SHB-Ⅲ循环水式多用真空泵,郑州长城科工贸有限公司;101型电热鼓风干燥箱,北京市永光明医疗仪器有限公司。
1.4 培养基
1.4.1 活化培养基 200.00 g/L马铃薯(浸提液)、20.00 g/L 葡萄糖、3.00 g/L KH2PO4、1.50 g/L MgSO4·7H2O、0.004 g/L维生素B1、20.00 g/L琼脂。
1.4.2 碳源初选培养基 分别以20.00 g/L葡萄糖、20.00 g/L 蔗糖、20.00 g/L麦芽糖、200.00 g/L马铃薯(浸提液)、2.00 g/L乳糖为供试碳源。其他成分为:2.00 g/L蛋白胨、3.00 g/L KH2PO4、1.50 g/L MgSO4·7H2O、0.004 g/L维生素B1,pH值自然。
1.4.3 氮源初选培养基 分别以2.00 g/L蛋白胨、2.00 g/L酵母浸粉、20.00 g/L麦麸(取浸提液)、2.00 g/L硫酸铵、2.00 g/L 硝酸铵为供试氮源。其他成分为:20.00 g/L葡萄糖、3.00 g/L KH2PO4、1.50 g/L MgSO4·7H2O、0.004 g/L维生素B1,pH值自然。
1.5 试验方法
1.5.1 菌种活化与提纯复壮 在无菌条件下,将菌种用活化培养基提前5 d活化,挑取强壮菌丝尖端,接种于斜面培养基上复壮,于25 ℃培养5~7 d备用。
1.5.2 转接液体培养基 采用100 mL锥形瓶,装液量为 50 mL,每瓶接种5块0.5 cm2菌块,于25 ℃静置培养48 h,然后于25 ℃、120 r/min条件下摇瓶培养120 h,每个水平设3组重复。
1.5.3 菌丝体干质量测量 滤纸分别编号后置电子天平上称质量,后将培养120 h的印度块菌菌丝体培养物分别用相对应编号滤纸抽滤,蒸馏水洗涤3次后,置于80 ℃烘箱烘干至恒质量、称量。
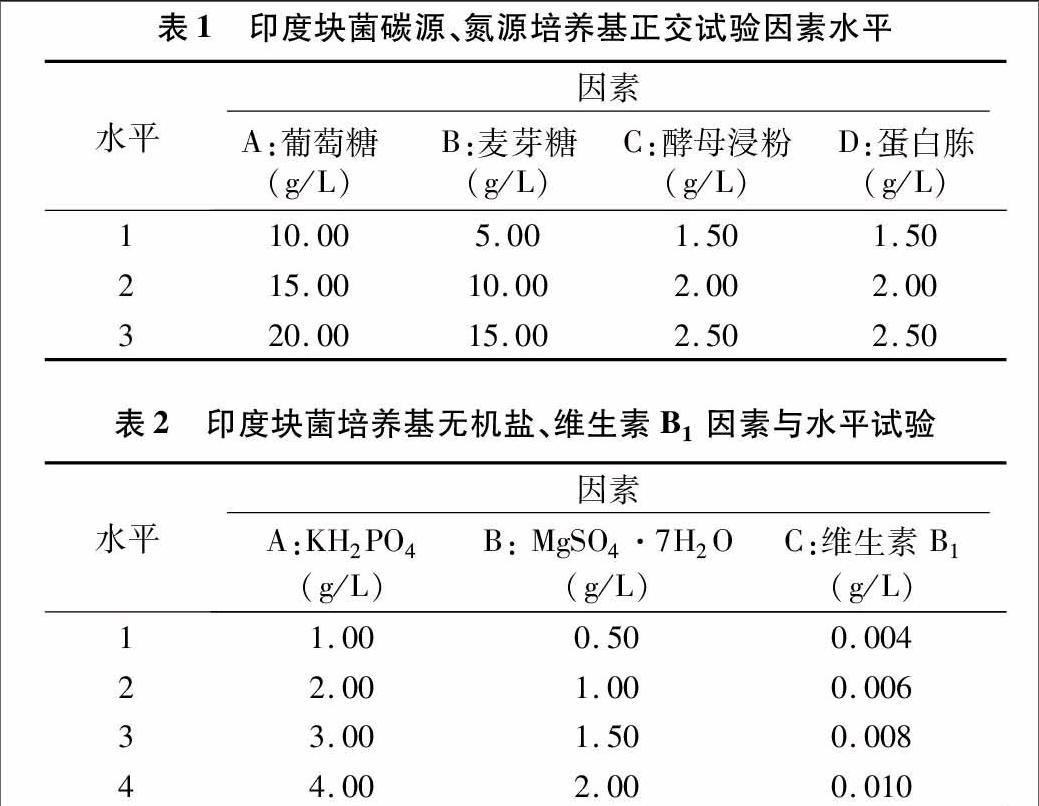
1.5.4 碳源、氮源培养基正交试验 依据碳、氮源单因素试验结果,以菌丝体干质量均值为标准,分别选择2个均值较高的碳源、氮源,按L9(34)设计4因素3水平正交试验进行复选,与3.00 g/L KH2PO4、1.50 g/L MgSO4·7H2O、0.004 g/L维生素B1 组成9组试验配方,正交试验因素与水平设计见表1。
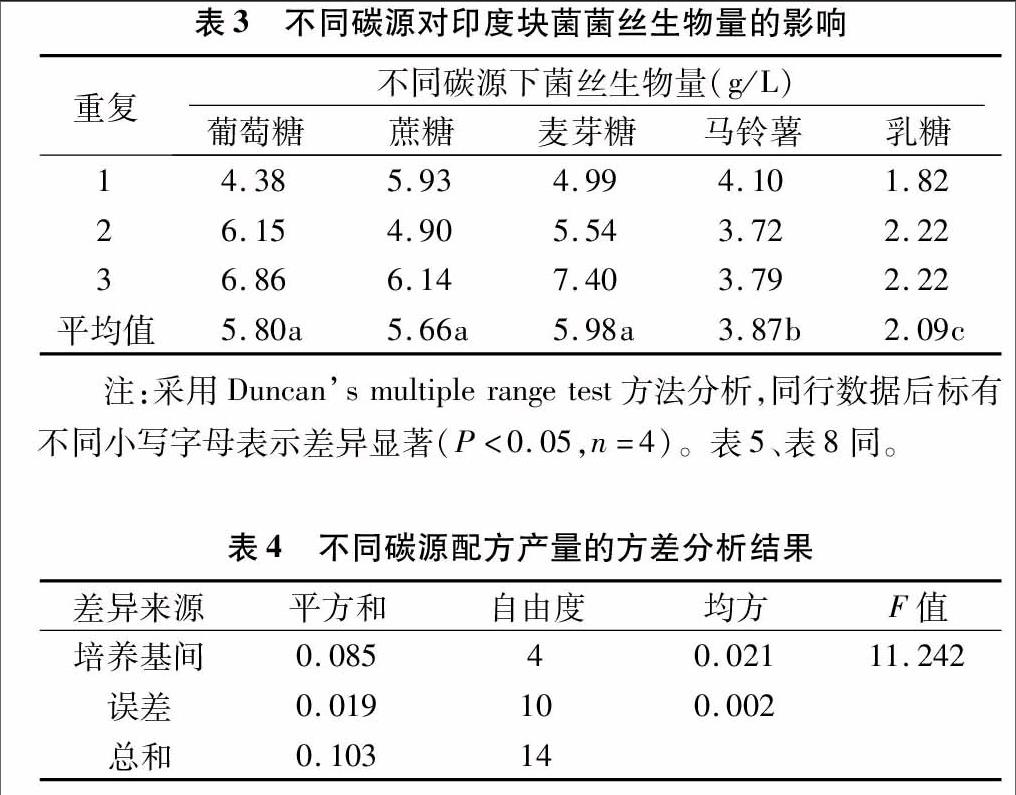
1.5.5 无机盐及维生素水平试验 根据混合碳、氮源正交试验结果,选出最佳碳源、氮源组合为基础培养基,再向其中添加不同浓度配比的KH2PO4 、 MgSO4·7H2O和维生素B1,具体处理见表2。
2 结果与分析
2.1 不同碳素营养对印度块菌菌丝体生长的影响
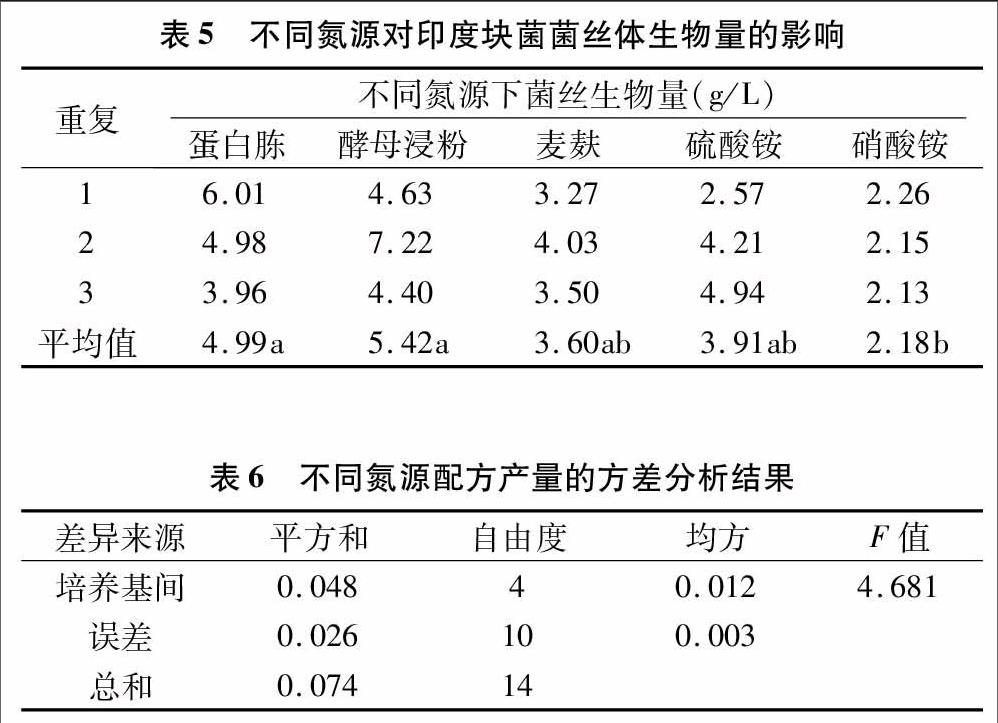
碳源是蕈菌培养基的主要营养成分之一,也是蕈菌菌丝细胞碳架结构、生长以及代谢的重要能量物质来源[13]。一些蕈菌相关研究表明,碳源主要对细胞生长和活性生物成分的合成有较大影响[14-15]。从表3可以看出,印度块菌对5种碳源均有不同程度的利用,以菌丝生物量为标准来看,其中麦芽糖的利用率最高,葡萄糖次之,乳糖最差。由表4可见,统计学方差分析F值为11.242,F>F4,10,0.01=5.994[16],表明不同碳源培养基对印度块菌菌丝体生物量的影响在α=0.01水平上差异显著,依据印度块菌菌丝生物量大小,选择麦芽糖、葡萄糖进行碳氮源正交试验。
2.2 不同氮素营养对印度块菌菌丝体生长的影响
氮源是食用菌细胞合成蛋白质和核酸必不可少的主要原料[17]。经前人试验表明,蕈菌对有机氮和无机氮均可利用且对前者的利用率高于后者[18-19]。为了全面详细地研究氮源对印度块菌菌丝体的影响,笔者对有机氮和无机氮的使用都进行了探索。试验结果表明,氮源对印度块菌菌丝体生物量的影响有一定差异。以酵母浸粉为氮源的培养基生物量最大,以硝酸铵为氮源的培养基生物量最小。有机氮源中以酵母浸粉为氮源的培养基菌丝体生物量最高,蛋白胨次之,麦麸最差;而无机氮源中以硫酸铵为氮源的培养基菌丝体生物量要高于硝酸铵氮源的。一般的NH4+盐比NO3-盐优先被利用,NO3-进入细胞后需要还原成NH4+后才能参与细胞物质合成[20]。方差分析(表5、表6)表明,印度块菌对氮源的利用存在显著差异,且酵母浸粉、蛋白胨要优于其他3种氮源,因此选择酵母浸粉、蛋白胨进行碳氮源正交试验。
2.3 正交试验结果与分析
由正交试验结果和极差分析(表7)可知,影响印度块菌菌丝生物量的大小关系为A>B>C>D。极差越大,各因素在水平变动时对生物量变化的影响就越大[21-22]。因此可知,葡萄糖是影响印度块菌菌丝生物量的主要因素。k1、k2、k3之间的差异是由因素取不同水平所引起,且k值相对较大的因素水平是较好的培养条件[23]。依据水平之间k值大小可知,印度块菌最佳液体培养基组合为A3B3C3D1,即20.00 g/L葡萄糖,15.00 g/L麦芽糖,1.50 g/L蛋白胨,2.50 g/L酵母浸粉。
2.4 不同无机盐和维生素B1浓度对印度块菌菌丝生物量的影响
无机盐中矿质元素、维生素B1的存在及浓度均对新陈代谢过程起着重要作用[13],两者比例大小会对于菌丝生长起到促进或延缓的作用[23-24]。为了完善培养基,使其营养均衡,对无机盐、维生素B1的浓度也进行了筛选,结果见表8。表9方差分析结果表明,不同处理间差异极显著。其中无机盐、维生素B1浓度的最佳组合为处理3,即 3.00 g/L KH2PO4、1.50 g/L MgSO4·7H2O、0.008 g/L维生素B1。
通过对最终所获得的印度块菌最佳液体培养基配方进行3次重复试验,结果所得菌丝平均生物量干质量为9.58 g/L。
2.5 摇瓶培养前后印度块菌菌丝量和形态对比
以最终获得的印度块菌最佳液体培养基配方进行验证试验,从图1、图2可以看出,印度块菌在摇瓶培养前后菌丝量对比差异明显。摇瓶培养前,静置48 h后的培养基清澈透亮,印度块菌菌片漂于培养上或沉于瓶底,菌片上有绒状、极短的新生菌丝(图1)。摇瓶培养120 h后,培养基浑浊,可观察到有大小不一的菌丝球和絮状菌丝,瓶壁内侧有白色绒状气生菌丝(图2)。
3 结论
通过单因素试验、正交试验相结合的研究方法得出印度
块菌最适液体培养基,为今后印度块菌液体发酵活性物质提取提供理论依据,从而更加有效地利用这一珍贵的蕈菌资源。最终获得的印度块菌最适液体培养基配方:20.00 g/L葡萄糖,15.00 g/L麦芽糖,1.50 g/L蛋白胨,2.50 g/L酵母浸粉,3.00 g/L KH2PO4、1.50 g/L MgSO4·7H2O,0.008 g/L维生素B1,pH值自然。25 ℃、120 r/min培养120 h,其生物量可达9.58 g/L。
参考文献:
[1] Kirk P M,Cannon P F,Minter D W,et al. Dictionary of the fungi[M]. 10th ed. Wallingford,UK:CABI,2008.
[2]苏开美,陈卫民,杨丽芬. 印度块菌、夏块菌、波氏块菌与锥连栎合成菌根苗技术研究[C]. 北京:第十届全国食用菌学术研讨会论文汇编,2014.
[3]陈 娟,邓晓娟,陈吉岳,等. 中国块菌属多样性[J]. 菌物研究,2011,9(4):244-254.
[4]陶 恺,刘 波. 中国块菌的生态和营养价值[J]. 山西大学学报:自然科学版,1990,13(3):319-321.
[5]胡慧娟,李佩珍,林 涛,等. 块菌多糖对小鼠肿瘤及免疫系统的影响[J]. 中国药科大学学报,1994,25(5):289-292.
[6]Kohl J V,Atzmueller M,Fink B,et al. Human pheromones:integrating neuroendocrinology and ethology[J]. Neuro Endocrinology Letters,2001,22(5):309-321.
[7]Claus R,Hoppen H O,Karg H. The secret of truffles:a steroidal pheromone?[J]. Experientia,1981,37(11):1178-1179.
[8]曹晋忠,魏 磊,苏 红,等. 印度块菌粗多糖的提取及抗氧化活性研究[J]. 山西大学学报:自然科学版,2011,34(1):137-142.
[9]罗 强,颜 亮,吴俐莎,等. 印度块菌水溶性多糖的单糖组成与抗氧化活性研究[J]. 食品科学,2010,31(23):52-56.
[10]方三平,蒲 彪,陈安均,等. 成熟度对印度块菌香气成分的影响[J]. 菌物学报,2013,32(6):1020-1027.
[11]Geng L Y,Wang X H,Yu F Q,et al. Mycorrhizal synthesis of tuber indicum with two indigenous hosts,Castanea mollissima and Pinus armandii[J]. Mycorrhiza,2009,19(7):461-467.
[12]胡炳福,远香美,余金勇,等. 印度块菌栽培在贵州首获成功[J]. 中国林副特产,2010(2):封3.
[13]刘祖同,罗信昌. 食用菌生物技术及应用[M]. 北京:清华大学出版社,2002:170-171.
[14]Zhong J J,Zhu Q X. Effect of initial phosphate concentration on cell growth and ginsenoside saponin production by suspended cultures of panax notoginseng[J]. Applied Biochemistry and Biotechnology,1995,55(3):241-247.
[15]Hwang H J,Kim S W,Xu C P,et al. Production and molecular characteristics of four groups of exopolysaccharides from submerged culture of Phellinus gilvus[J]. Journal of Applied Microbiology,2003,94(4):708-719.
[16]杜荣骞. 生物统计学[M]. 北京:高等教育出版社,2003:263-265.
[17]刘艳芳,杨 焱,贾 薇,等. 猴头菌深层发酵培养基筛选初探[J]. 食用菌学报,2003,10(3):26-31.
[18]聂建军,潘保华,李彩萍,等. 基于液态黑脉羊肚菌菌丝体培养基配方的研究[J]. 中国食用菌,2014,33(4):35-36.
[19]孙军德,鲁婷婷,温立丽,等. 樟芝液体发酵培养基配方的筛选优化[J]. 沈阳农业大学学报,2009,40(2):183-187.
[20]柏内特 J H. 真菌学基础[M]. 北京:科学出版社,1989:178-180.
[21]李春喜,姜丽娜,邵 云,等. 生物统计学[M]. 北京:科学出版社,1997:315-343.
[22]陈文强,邓百万,陈永刚,等. 用L9(34)正交试验筛选裂褶菌液体培养基[J]. 食品与生物技术学报,2005,24(4):38-41.
[23]高玉荣,卢艳明. 灵芝菌丝液体深层发酵培养基的研究[J]. 中国酿造,2006,1(1):18-20.
[24]赵桂云,律凤霞,龚振杰,等. 鸡腿蘑液体培养基配方筛选[J]. 食用菌,2004,26(6):15-16.
