酶解法制备草鱼皮蛋白水解物增殖嗜热链球菌
2016-04-15陈建康包建强上海海洋大学食品学院上海水产品加工及贮藏工程技术研究中心上海201306
陈建康,包建强(上海海洋大学食品学院,上海水产品加工及贮藏工程技术研究中心,上海 201306)
酶解法制备草鱼皮蛋白水解物增殖嗜热链球菌
陈建康,包建强*
(上海海洋大学食品学院,上海水产品加工及贮藏工程技术研究中心,上海 201306)
摘 要:嗜热链球菌被认为是一种多功能益生菌,将Neutrase 0.8L、Protease P “Amano”6、ProteAX、Alcalase 2.4L FG和风味中性蛋白酶5 种草鱼皮蛋白水解物作为培养嗜热链球菌的氮源,以水解物对嗜热链球菌的增殖效果为评价指标,选择最佳水解用酶,并利用正交试验优化酶解条件。结果表明,5 种微生物蛋白酶中,Neutrase 0.8L是水解草鱼皮蛋白的最佳用酶,最佳的酶解条件为:加酶量1%、酶解时间80 min、起始pH 6.5、料水比1∶2(m/V)。利用Neutrase 0.8L酶解法制备得到的富含胶原蛋白肽的草鱼皮蛋白水解物,是一种培养嗜热链球菌的理想氮源。
关键词:草鱼皮;蛋白酶;酶解;胶原蛋白肽;嗜热链球菌
引文格式:
陈建康,包建强.酶解法制备草鱼皮蛋白水解物增殖嗜热链球菌[J].食品科学,2016,37(5):144-148.DOI:10.7506/spkx1002-6630-201605026.http://www.spkx.net.cn
CHEN Jiankang,BAO Jianqiang.Enzymatic preparation of protein hydrolysate from grass carp skin for use as a nitrogen source for Streptococcus thermophilus growth[J].Food Science,2016,37(5):144-148.(in Chinese with English abstract)
在资源、环境和可持续发展面临的问题日益严峻的今天,作为可再生资源的胶原,备受人们的关注[1]。水产动物胶原蛋白在低过敏性、低抗原性、低热变性和酶解较容易等方面明显优于陆生动物胶原蛋白[2]。鱼类加工过程中产生的大量富含Ⅰ型胶原的鱼皮、鱼骨和鱼鳞等副产物是鱼类胶原蛋白或明胶的重要来源[3-4]。这些副产物含有的蛋白质具有优良的氨基酸平衡和蕴含生物活性肽序列[5]。活性肽序列的释放主要有体外酶法、食品加工、体内消化和发酵水解4 种途径[6],其中酶解法具有反应条件温和、减少环境不良影响、增加水解专一性、优异的产品质量和功能特性等诸多优点,成为水产品加工业发展的重要趋势[5,7-10]。酶解法制备得到的水产胶原蛋白肽具有抗氧化、抗高血压、抗疲劳、抗菌、抗肿瘤、免疫调节、降胆固醇及降血脂等生物活性,可作为功能性食品添加剂用于消化道健康和调整肠道营养吸收[5,7,10-12]。
嗜热链球菌被认为是一种多功能益生菌,与瑞士乳杆菌、保加利亚乳杆菌、嗜酸乳杆菌、干酪乳杆菌和乳链球菌相比较,其蛋白水解能力最弱[13]。嗜热链球菌体内蛋白酶的活性通常较弱,甚至缺乏必要的蛋白酶,从酸奶中分离得到的嗜热链球菌不能水解明胶进一步证实其最适培养氮源是蛋白水解物[14-15]。因此,本实验拟利用酶工程技术,以草鱼皮为利用对象,选择适宜的蛋白酶,通过正交试验确定最佳酶解工艺参数,酶解制备促进嗜热链球菌增殖的富含胶原蛋白肽的草鱼皮蛋白水解物,以期为鱼类胶原蛋白肽应用于人类的微生态领域提供实验依据。
1 材料与方法
1.1材料与试剂
草鱼皮由浙江湖州南浔新雅农产品开发有限公司提供。
草鱼皮酸溶性胶原蛋白 由食品专业加工保鲜实验室自制;Alcalase 2.4L FG(Bacillus licheniformis)、Neutrase 0.8L(Bacillus amyloliquefaciens) 丹麦诺维信(中国)投资有限公司; Protease P “Amano”6 (Aspergillus melleus)、ProteAX(Aspergillus oryzae)日本天野酶制品株式会社;风味中性蛋白酶(Aspergillus oryzae) 山东隆大生物工程有限公司;酸奶发酵剂(保加利亚乳杆菌和嗜热链球菌) 北京川秀科技有限公司;其余为国产分析纯或生化试剂。
1.2仪器与设备
TG16-WS台式高速离心机 湘仪离心机仪器有限公司;Waters e2695高效液相色谱仪(配有Waters 2996二极管阵列检测器及Empower2色谱软件) 美国Waters公司;YXQ-LS-18SI手提式压力蒸汽灭菌器 上海博讯实业有限公司;SW-CJ-2F双人双面净化工作台 苏州净化设备有限公司;ZQLY-300振荡培养箱 上海知楚仪器有限公司;T6新世纪紫外-可见分光光度计 北京普析通用仪器有限责任公司。
1.3方法
1.3.1草鱼皮成分的分析
水分含量:GB 5009.3—2010《食品中水分的测定》;蛋白质含量:GB 5009.5—2010《食品中蛋白质的测定》;脂肪含量:GB/T 5009.6—2003《食品中脂肪的测定》;灰分含量:GB 5009.4—2010《食品中灰分的测定》;总糖含量:GB/T 5009.8—2008 《食品中蔗糖的测定》。
1.3.2草鱼皮胶原蛋白肽的制备
制备流程:草鱼皮切碎物→清洗→加水混匀→调节pH值→热处理→冷却至酶解温度→加酶→酶解→灭酶→冷却→离心过滤、除脂→冻干→粉状胶原蛋白肽。
在制备过程中,考虑到草鱼蛋白分离后的肌球蛋白、肌动蛋白、肌浆蛋白及胶原蛋白的变性温度分别为50.92、74.09、59.94、59.75 ℃[16],同时避免酶解过程中的微生物污染和提高原料蛋白的酶解敏感性,故采用100 ℃、10 min热处理;另外,为了避免最终产物中的灰分含量过高,酶解过程的pH值不外加碱进行控制[17]。
1.3.3酶解产物的游离氨基酸测定
磺基水杨酸法:称取2 g样品,加入0.02 mol/L的盐酸溶液15 mL,充分均质后用0.02 mol/L的盐酸溶液定容至50 mL,在5 000 r/min离心10 min。取上清液2 mL加入8 g/100 mL磺基水杨酸溶液2 mL,在4 ℃冰箱里静置放置30 min后,在10 000 r/min离心10 min。取上清液,过0.22 μm滤膜后,进样测定(根据样品中氨基酸浓度进行适当稀释)。进样量为20 μL。
1.3.4草鱼皮胶原蛋白肽促进嗜热链球菌生长活性的测定
1.3.4.1嗜热链球菌的分离制备[18]
利用保加利亚乳杆菌和嗜热链球菌的最适pH值分别为5.0和9.0,将两者有效分离。
1.3.4.2嗜热链球菌增殖培养基的配制[19]
化学限定培养基组成(g/L):葡萄糖20.0、草鱼蛋白水解物(多肽和氨基酸添加总量)1.51、乙酸钠4.0、柠檬酸三铵1.0、磷酸二氢钾2.0、磷酸氢二钾2.0、硫酸镁0.5、硫酸锰0.05、硫酸亚铁0.02、氯化钙0.2、肌醇0.002、对氨基苯甲酸0.000 5、叶酸0.000 5、尼克酸0.002、泛酸钙0.002、生物素0.001、吡哆醇0.002、核黄素0.002、钴胺素0.001、硫胺素0.001、吐温-80 1.0。
配制过程中,维生素和无机盐用0.22 μm滤膜过滤除菌,其余溶解后115 ℃灭菌20 min。临用时再按比例混合。
1.3.4.3嗜热链球菌的增殖培养
10 mL嗜热链球菌活化试管斜面加入5 mL灭菌蒸馏水,用无菌竹签刮下菌苔,振匀制备菌悬液;250 mL三角瓶装液量为30 mL,接种量为0.3 mL菌悬液;42 ℃培养40 h;培养过程摇床转速100 r/min。
1.3.4.4嗜热链球菌培养液中嗜热链球菌增殖效果的测定
以蒸馏水为调零基准,在波长为600 nm处进行测定嗜热链球菌培养液的OD600 nm值。以OD600 nm值表示嗜热链球菌的增殖效果。
1.3.5草鱼皮蛋白质、酸溶性胶原蛋白和草鱼皮蛋白水解物氨基酸组成的测定
按照GB/T 5009.124—2003 《食品中氨基酸的测定》方法测定。
1.3.6 不同蛋白酶对草鱼皮蛋白的酶解条件
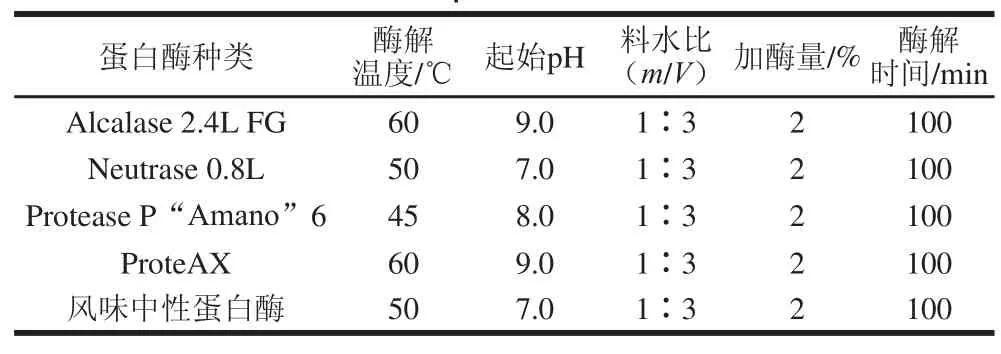
表1 5 种蛋白酶对草鱼皮蛋白的酶解条件Table 1 Hydrolysis conditions of five proteases for grass carp skin protein
1.3.7Neutrase 0.8L酶解单因素试验
由于Neutrase 0.8L中性蛋白酶的最适工作条件为:温度45~55 ℃之间,pH 5.5~7.5,因此单因素试验仅考察料水比、加酶量和酶解时间。
1.3.7.1料水比对酶解物促进嗜热链球菌增殖的影响
在50 ℃、起始pH 7.0、加酶量(以新鲜鱼皮计,下同)为2.0%、酶解时间为100 min的条件下,研究料水比(m/V)分别为1∶1、1∶2、1∶3、1∶4对酶解物促进嗜热链球菌增殖的影响。
1.3.7.2加酶量和酶解时间对酶解物促进嗜热链球菌增殖的影响
在料水比1∶2、酶解温度50 ℃、起始pH 7.0的条件下,研究加酶量分别为0.5%、1.0%、2.0%、 3.0%,酶解时间分别为60、80、100、120 min对酶解物促进嗜热链球菌增殖的影响。
1.3.8Neutrase 0.8L酶解条件正交试验
在单因素多水平分析的基础上,以酶解物促进嗜热链球菌增殖效果(OD600 nm)为指标,以起始pH值、酶解时间、料水比和加酶量为因素,通过L9(34)正交试验对影响蛋白酶Neutrase 0.8L水解的反应参数进行优化。
2 结果与分析
2.1草鱼皮基本成分
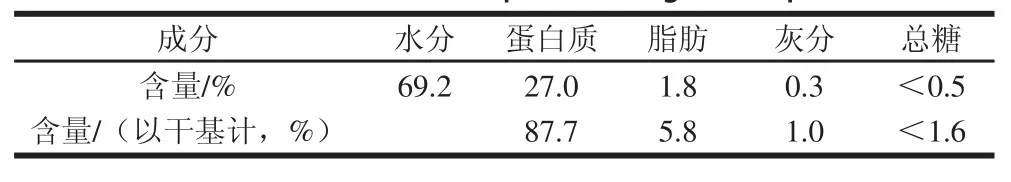
表2 草鱼鱼皮的基本成分Table 2 Proximate composition of grass carp skin
由表2可知,草鱼鱼皮具有高蛋白、低脂、低灰分、低糖的特点。检测结果与傅燕凤等[20]研究结果基本一致。本实验用鱼皮原料脂肪干基含量为5.8%,相对较低,比Wasswa[21]报道的20.1%和林琳[22]报道的20.2%低,而比张艳等[23]报道的1.9%和郭文宇等[24]报道的1.3%高。鱼皮原料的来源及其质量决定了本实验在酶解前省略去除脂肪的步骤。
2.2不同蛋白酶对草鱼皮蛋白的分解能力
从表3嗜热链球菌的OD600 nm值可知,草鱼皮蛋白水解物促进嗜热链球菌增殖效果最好的是Neutrase 0.8L,其次为风味中性蛋白酶、ProteAX、Alcalase 2.4L FG和Protease P “Amano”6。
2.3酶解产物游离氨基酸含量分析
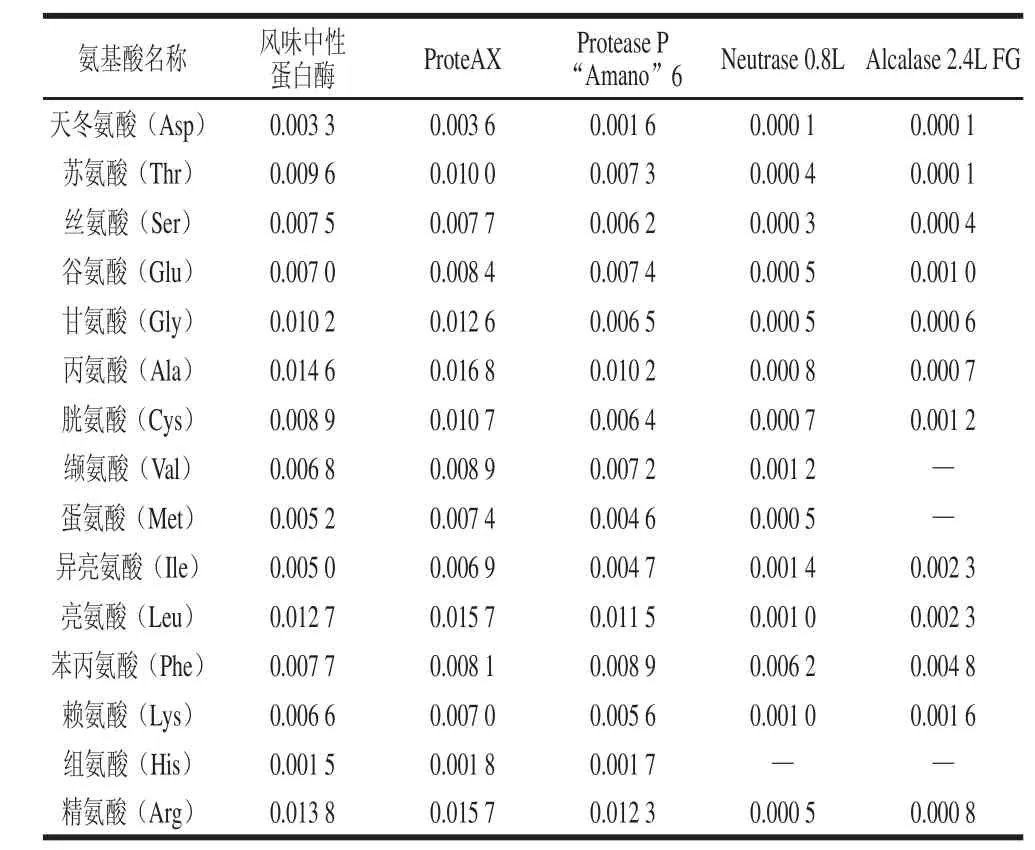
表4 5 种酶 解产物游离氨基酸含量Table 4 Free amino acid contents of five enzymatic hydrolysates %
由表4可知,Alcalase 2.4L FG和Neutrase 0.8L蛋白酶水解产生的游离氨基酸生成率明显低于风味中性蛋白酶、ProteAX和Protease P“Amano”6。Letorc[25]报道了大多数嗜热链球菌的生长都需要蛋氨酸、组氨酸、脯氨酸以及谷氨酸。由表4可知,风味中性蛋白酶、ProteAX和Protease P“Amano”6这3 种酶解产物游离谷氨酸、组氨酸和蛋氨酸含量明显比Neutrase 0.8L 和Alcalase 2.4L这两种酶解产物的相应游离氨基酸高,而且Neutrase 0.8L的游离谷氨酸含量最低,但是Neutrase 0.8L酶解产物促进嗜热链球菌增殖的效果最好,因此,酶解产物中游离氨基酸的数量并非是其促进嗜热链球菌增殖效果的决定因素。本实验侧面验证了白凤翎等[19]结果:乳酸菌生长的最佳氮源是寡肽而不是氨基酸。
2.4 Neutrase 0.8L酶解单因素试验
2.4.1料水比对酶解物促进嗜热链球菌增殖的影响
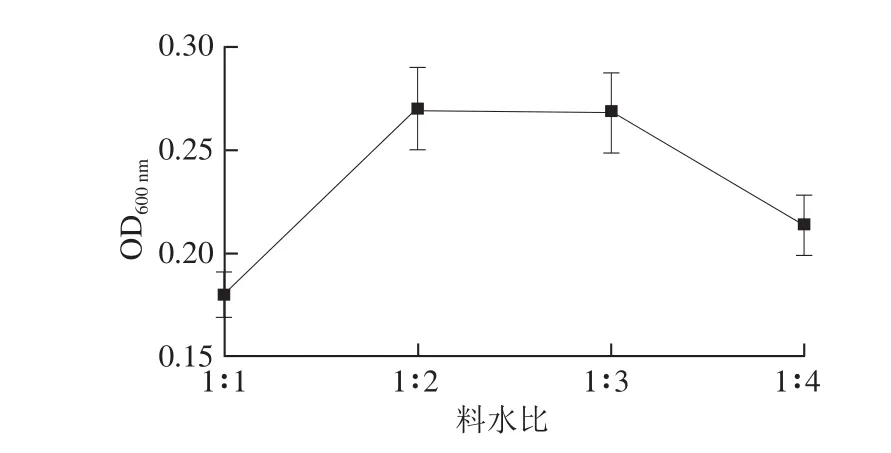
图1 料水比对酶解物促进嗜热链球菌增殖的影响Fig.1 Effect of ratio between fish skin and water on the proliferation of Streptococcus thermophilus cultured using hydrolysate as nitrogen source
由图1可知,当料水比从1∶1降至1∶2时,酶解物作为氮源得到的嗜热链球菌培养液OD600 nm值上升,当料水比继续降至1∶3后,嗜热链球菌培养液OD600 nm值有所下降,说明随着水量的增加,先有利于酶和鱼皮蛋白底物充分接触,促进寡肽的生成;随着水量的进一步增加,酶和鱼皮蛋白在水中的浓度降低,不利于酶促反应,降低了寡肽的生成率。
2.4.2加酶量和酶解时间对酶解物促进嗜热链球菌增殖的影响

图2 加酶量和酶解时间对酶解物促进嗜热链球菌增殖的影响Fig.2 Effect of Neutrase concentration and hydrolysis time on the proliferation of Streptococcus thermophilus cultured using hydrolysate as nitrogen source
由图2可知,加酶量1.0%时得到的酶解物作为氮源时,嗜热链球菌培养液OD600 nm值都是最高的,其次是加酶量3.0%,然后2.0%,最后是0.5%;同时,在酶解时间80 min内,嗜热链球菌培养液OD600 nm值上升;之后,嗜热链球菌培养液OD600 nm值下降。说明在低加酶量以及较短的酶解时间内,加酶量的增加和酶解时间的延长可促进鱼皮蛋白水解生成寡肽,然而酶过量和酶解时间过长会促进寡肽进一步生成氨基酸,导致嗜热链球菌培养液OD600 nm值下降。加酶量3.0%对应的OD600 nm值略高于加酶量2.0%对应的OD600 nm值,说明随着加酶量的进一步增加,二者寡肽处于相同较低水平时,氨基酸促进嗜热链球菌增殖的作用逐步显现。
2.5Neutrase 0.8L酶解条件正交试验
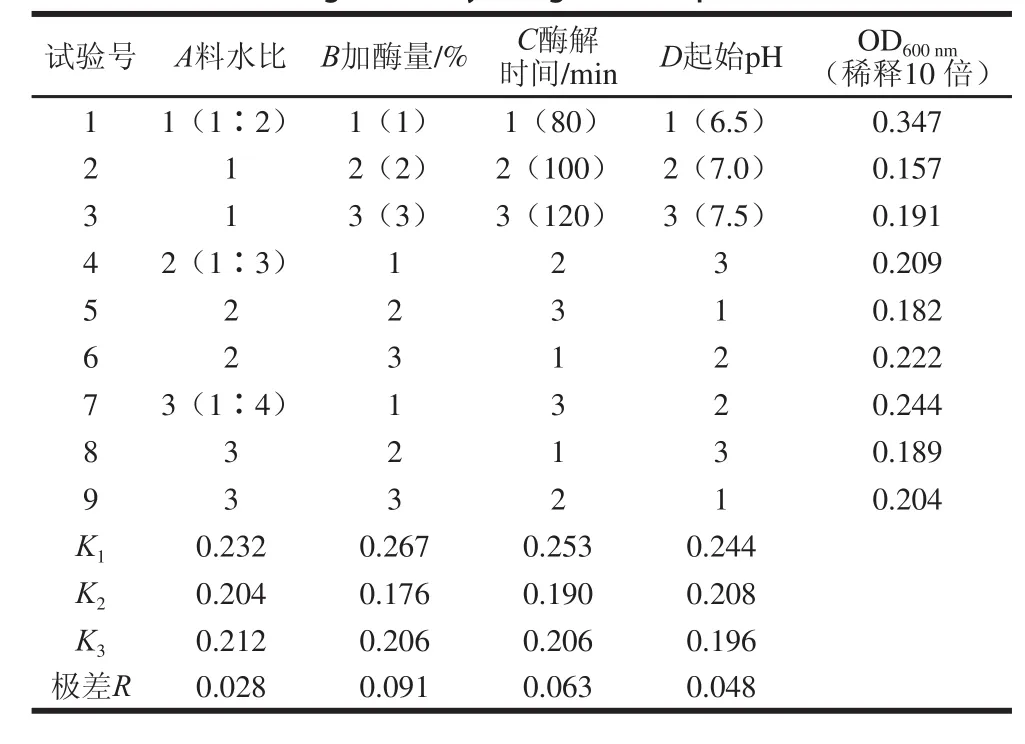
表5 Neutrase 0.8L酶解条件正交试验方案及结果Table 5 Orthogonal array design with experimental results
从表5极差R分析影响酶解物对嗜热链球菌增殖效果的各因素主次顺序为:加酶量>酶解时间>起始pH值>料水比。酶解条件最佳组合为A1B1C1D1,即加酶量1%、酶解时间80 min、起始pH 6.5、料水比1∶2。
2.6草鱼皮蛋白质、酸溶性胶原蛋白和Neutrase 0.8L酶解产物的氨基酸组成分析
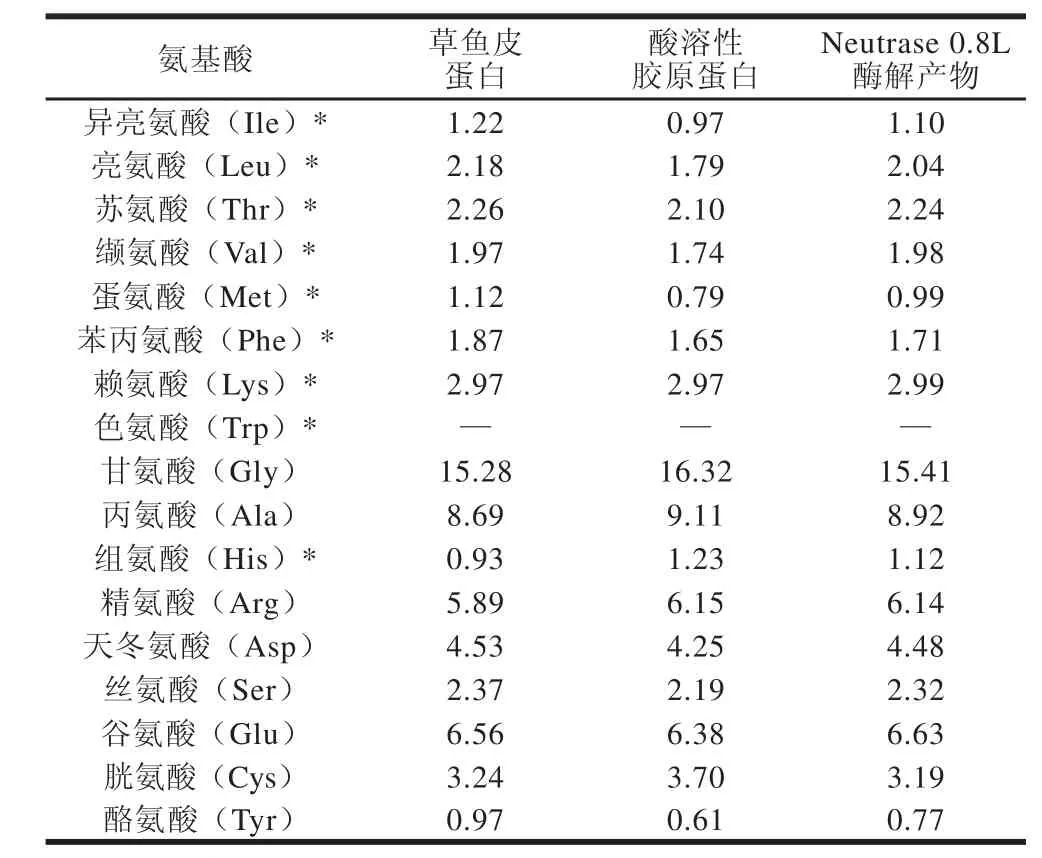
表6 草鱼皮蛋白质、酸溶性胶原蛋白和Neutrase 0.8L酶解产物的氨基酸组成分析,Table 6 Amino acid composition of native grass carp skin protein,acid-soluble collagen and Neutrase 0.8L hydrolysate %
由表6可知,草鱼皮酸溶性胶原蛋白的氨基酸中除甘氨酸、丙氨酸、组氨酸、精氨酸和半胱氨酸含量比草鱼皮蛋白中相应的氨基酸含量略高外,其余的氨基酸含量略低,二者的氨基酸组成基本相当。酶解制备草鱼皮蛋白水解物的实质就是制备胶原蛋白肽的过程。
Neutrase 0.8L制备得到的草鱼皮蛋白水解物的氨基酸组成与草鱼皮蛋白的氨基酸组成略有差异。其中,疏水性大分子氨基酸Leu、Ile、Phe的含量较草鱼皮中的对应值分别减少了6.4%、11.0%和9.2%,与中性蛋白酶的优先切点为疏水性大分子氨基酸Leu、Ile、Phe相符合。另外,Met和Tyr分别减少了11.4%和22.2%,而His、Arg 和Ala分别增加了19.1%、4.2%和2.6%。结合表5中游离氨基酸分析结果,Neutrase 0.8L草鱼皮蛋白水解物是以肽为主,游离氨基酸为次要组成部分的混合物。
草鱼皮蛋白中胶原蛋白含量约占总蛋白的86%[20],其他蛋白质,包括弹性蛋白、白蛋白、球蛋白和粘蛋白可溶性蛋白等约占14%,以草鱼皮为原料,省略提取胶原蛋白或明胶步骤,利用Neutrase 0.8L酶解制备草鱼皮蛋白水解物,不仅可以提高原料蛋白的利用率,而且含有寡肽和氨基酸的蛋白水解物对嗜热链球菌增殖具有促进作用,是一种培养嗜热链球菌的理想氮源。
3 结 论
通过比较Neutrase 0.8L、Protease P“Amano”6、ProteAX、Alcalase 2.4L FG和风味中性蛋白酶5 种微生物蛋白酶草鱼皮蛋白水解物对嗜热链球菌的增殖效果,筛选得到最佳水解用酶为中性蛋白酶Neutrase 0.8L,并且利用正交试验确定了其最佳酶解条件为加酶量1%、酶解时间80 min、起始pH 6.5、料水比1∶2。利用中性蛋白酶Neutrase 0.8L直接水解草鱼皮制备得到富含胶原蛋白肽的蛋白水解物,不仅可以省略提取胶原蛋白或明胶步骤,提高草鱼皮蛋白利用率和简化工艺,而且含有寡肽和氨基酸的蛋白水解物对嗜热链球菌增殖具有促进作用,是一种培养嗜热链球菌的理想氮源。
嗜热链球菌培养的最佳氮源是寡肽,下一步主要研究不同分子质量区间的肽对嗜热链球菌的增殖效果,并且在最佳的分子质量区间内尝试找到起增殖效果的目标肽。为鱼皮胶原蛋白肽应用到微生态领域,发挥其营养和功能特性,提供进一步的实验依据。
参考文献:
[1]汤克勇.胶原物理与化学[M].北京:科学出版社,2012:序.
[2]焦道龙,陆剑锋,张伟伟,等.水产动物胶原蛋白的研究现状及发展趋势[J].食品科学,2009,30(17):334-338.DOI:10.3321/j.issn:1002-6630.2009.17.079.
[3]中华人民共和国国家卫生和计划生育委员会.GB 6783—2013 食品安全国家标准 食品添加剂 明胶[S].北京:中国标准出版社,2013.
[4]GŁMEZ-GUILLÉN M C,GIMÉNEZ B,LŁPEZ-CABALLERO M E,et al.Functional and bioactive properties of collagen and gelatin from alternative sources:a review[J].Food Hydrocolloids,2011,25(8):1813-1827.DOI:10.1016/j.foodhyd.2011.02.007.
[5]CHALAMAIAH M,DINESH-KUMAR B,HEMALATHA R,et al.Fish protein hydrolysates:proximate composition,amino acid composition,antioxidant activities and applications:a review[J].Food Chemistry,2012,135(4):3020-3038.DOI:10.1016/j.foodchem.2012.06.100.
[6]CHANG O K,ROUX É,AWUSSI A A,et al.Use of a free form of the Streptococcus thermophilus cell envelope protease PrtS as a tool to produce bioactive peptides[J].International Dairy Journal,2014,38(2):104-115.DOI:10.1016/j.idairyj.2014.01.008.
[7]HE S,FRANCU C,ZHANG W.Functions,applications and production of protein hydrolysates from fish processing co-products(FPCP)[J].Food Research International,2013,50(1):289-297.DOI:10.1016/j.foodres.2012.10.031.
[8]TAVANO O L.Protein hydrolysis using proteases:an important tool for food biotechnology[J].Journal of Molecular Catalysis B:Enzymatic,2013,90:1-11.DOI:10.1016/j.molcatb.2013.01.011.
[9]CASTRO H C,ABREU P A,GERALDO R B,et al.Looking at the proteases from a simple perspective[J].Journal of Molecular Recognition,2011,24(2):165-181.DOI:10.1002/jmr.1091.
[10]胡晓,孙恢礼,李来好,等.我国酶解法制备水产功能性肽的研究进展[J].食品工业科技,2012,33(24):410-413.DOI:10.13386/j.issn1002-0306.2012.24.062.
[11]吴晓洒,蔡路昀,曹爱玲,等.水产品加工废弃物中的蛋白及生物活性肽的研究进展[J].食品工业科技,2014,35(23):372-376; 381.DOI:10.13386/j.issn1002-0306.2014.23.070.
[12]茅宇虹,杨文鸽.鱼皮胶原蛋白及胶原活性肽的研究[J].食品工业科技,2013,34(15):375-379.DOI:10.13386/j.issn1002-0306.2013.15.032.
[13]THOMSA T D.Role of lactic acid bacteria and their improvement for production of better fermented animal products[J].New Zealand Journal of Dairy Science and Technology,1985,2:1-10.
[14]王建芳,陈芳,靳亚平.嗜热链球菌适宜培养条件研究[J].西北农业学报,2008,17(2):56-58.DOI:10.3969/j.issn.1004-1389.2008.02.014.
[15]王俊英,张杰.酸奶中嗜热链球菌的分离和性能研究[J].周口师范学院学报,2012,29(2):89-91.DOI:10.3969/j.issn.1671-9476.2012.02.031.
[16]任娇艳.草鱼蛋白源抗疲劳生物活性肽的制备分离及鉴定技术研究[D].广州:华南理工大学,2008.
[17]李岩,班玉凤,郭洪臣,等.pH值渐变条件下双酶协同水解猪皮制备胶原蛋白寡肽的研究[J].食品科学,2003,24(7):74-79.DOI:10.3321/j.issn:1002-6630.2003.07.014.
[18]付鸿,李靖靖,岳春.酸奶中杆菌和球菌的快速分离及发酵剂的制备[J].化学与生物工程,2013,30(8):70-73.DOI:10.3969/j.issn.1672-5425.2013.08.019.
[19]白凤翎,张柏林,赵宏飞.大豆蛋白水解物促酸奶乳酸菌增殖及生长动力学[J].食品与发酵工业,2012,38(1):51-56.DOI:10.13995/j.cnki.11-1802/ts.2012.01.029.
[20]傅燕凤,沈月新,杨承刚,等.淡水鱼鱼皮胶原蛋白的提取[J].上海水产大学学报,2004,13(2):146-150.DOI:10.3969/j.issn.1004-7271.2004.02.011.
[21]WASSWA J.酶法回收淡水鱼鱼皮蛋白及其特性研究[D].无锡:江南大学,2007.
[22]林琳.胶原蛋白的制备及胶原多肽活性的研究[D].青岛:中国海洋大学,2006.
[23]张艳,李国英,缪煜清,等.草鱼皮胶原的提取及性能的初步研究[J].水产科学,2006,25(3):136-139.DOI:10.3969/j.issn.1003-1111.2006.03.008.
[24]郭文宇,边清泉,刘家琴,等.木瓜蛋白酶提取草鱼皮胶原蛋白的工艺研究[J].皮革与化工,2009,26(1):34-36.DOI:10.3969/j.issn.1674-0939.2009.01.009.
[25]LETORC C.Relation entre croissance et nutrition azotée de deux bactéries lactiques thermophiles:Streptococcus thermophilus et Lactobacillus delbrueckii subsp.bulgaricus[D].France:Université de Poitiers,2001.
Enzymatic Preparation of Protein Hydrolysate from Grass Carp Skin for Use as a Nitrogen Source for Streptococcus thermophilus Growth
CHEN Jiankang,BAO Jianqiang*
(Shanghai Engineering Research Center of Aquatic-Product Processing and Preservation,College of Food Science and Technology,Shanghai Ocean University,Shanghai 201306,China)
Abstract:Streptococcus thermophilus is regarded as a multi-functional probiotic bacterium.Five protein hydrolysates from grass carp skin were prepared using Neutrase 0.8L,Protease P “Amano” 6,ProteAX,Alcalase 2.4L FG and Flavourzyme,respectively,for use as nitrogen sources to culture Streptococcus thermophilus.Among the five proteases,Neutrase 0.8L was found to be the best enzyme to produce the optimal nitrogen source for the growth of Streptococcus thermophilus.In further investigations,we optimized hydrolysis conditions using orthogonal array experiments.The results showed that the optimal hydrolysis conditions were as follows:e nzyme dosage,1%; hydrolysis time,80 min; initial pH,6.5; and ratio between fresh skin and water,1:2(m/V).The hydrolysate obtained under these conditions was rich in collagen-derived peptides as a new optimum nitrogen source for Streptococcus thermophilus incubation.
Key words:grass carp skin; protease; hydrolysis; collagen-derived peptide; Streptococcus thermophilus
中图分类号:TS254.1;TS254.9
文献标志码:A
文章编号:1002-6630(2016)05-0144-05
DOI:10.7506/spkx1002-6630-201605026 10.7506/spkx1002-6630-201605026.http://www.spkx.net.cn
*通信作者:包建强(1963—),男,教授,硕士,研究方向为食品冷冻。E-mail:baojq@shou.edu.cn
作者简介:陈建康(1973—),男,工程师,硕士,研究方向为发酵工程。E-mail:jkchen@shou.edu.cn
基金项目:上海市科委工程中心建设项目(11DZ2280300)
收稿日期:2015-04-07
