燃煤电厂二氧化碳分解制备甲酸的催化研究
2016-04-14刘奕宁许琦陈忠陈笔
刘奕宁,许琦,陈忠,陈笔
(1.国电电力大同第二发电厂,山西大同037043;2.国电电力发展股份有限公司,北京100101; 3.国电浙江北仑第一发电有限公司,浙江宁波315800;4.清洁高效燃煤发电与污染控制国家重点实验室,江苏南京210046)
燃煤电厂二氧化碳分解制备甲酸的催化研究
刘奕宁1,4,许琦2,陈忠1,陈笔3
(1.国电电力大同第二发电厂,山西大同037043;2.国电电力发展股份有限公司,北京100101; 3.国电浙江北仑第一发电有限公司,浙江宁波315800;4.清洁高效燃煤发电与污染控制国家重点实验室,江苏南京210046)
2015年,我国CO2排放量约102亿t,占全球排放量的28.7%,全国电力行业CO2排放量约36.15亿t,合理使用CO2资源,开展CO2清洁利用技术势在必行。系统研究了CO2加氢制备甲酸的反应热力学和动力学,论证了均相催化、多相催化、低温等离子催化、电化学催化和光化学催化等催化手段,研讨了多种低能耗高效CO2加氢的反应条件,为回收燃煤电厂CO2并生成高附加值的化工产品提供了技术依据。
CO2减排;加氢;分解利用;燃煤电厂
0 引言
自工业革命以来,大气中CO2含量随着化石燃料使用的增加成比例升高[1-2],全球气温呈逐渐变暖趋势。尽管如此,为满足人口数量急剧增长的资源需求,以及随之而来的森林砍伐,大气中O2和CO2的比例已产生了显而易见的变化[3]。近年来,随着中国、印度、巴西等国家经济的迅速发展,CO2的排放问题愈发明显。我国是能源消耗大国,煤炭作为能源结构中最重要的组成部分,提供了全国大约85%的能源,同时也带来了严重的环境污染,并仍将长期使用。据统计,目前全球温室气体排放总量已达300亿t/a,其中83%来源于与能源供给有关的工业,如发电行业[4]。据预测,到2035年,由燃煤释放的CO2将达172亿t/a。
有足够的证据表明,由于CO2含量增长导致的温室效应使得生态环境被严重破坏[5]。因此,在有确凿的证据表明环境已被不可逆的破坏之前,开展可以帮助促进降低大气中CO2含量的科学研究,并在技术上得以实现,显得异常重要。
首先,从源头减少CO2的生成量,如提高生产效率并且降低能耗、运用可再生能源等[3];其次,对已产生的CO2采用减排技术,目前广泛应用的主要有2种:一是CO2捕集技术(CCS,Carbon Capture and Storage),即CO2经过捕捉和分离后直接注入地下封存[6]。该技术并不改变CO2的化学结构,存在潜在泄露的风险[7]。尽管个别国家建有小规模试点项目,但截至目前CCS仍不能作为碳减排的主流技术被广泛使用。
二是将CO2作为化工原料回收和利用。CO2不仅是温室气体的主要构成部分,也是非常有价值的资源以及潜在的可再生原料[8]。因此,对于全球CO2排放,探索和研究一切能够运用CO2作为原始化工原料合成下游高附加值产品意义重大[9]。
1 CO2 加氢制备甲酸的热力学分析
在一定的温度和压力+催化剂条件下,CO2可与氢气或含氢化合物反应生成甲酸或甲酸根:
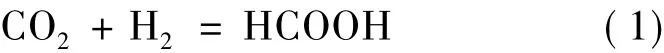
以往的研究提供了大量关于CO2加氢反应的热力学数据[10],这些反应的产物涵盖了聚碳酸酯、环氧化物、醇类、醚类、胺类和氨等,CO2分解制备CO以及化石燃料的反应工艺被大量的总结和讨论,包括电化学反应、催化反应以及光化学反应,同时提供了CO2直接加氢的多种技术,也论证了CO2作为化工原料在多类工业中的储存和应用。尽管如此,CO2加氢制备甲酸的反应机理非常复杂,在反应过程中往往伴随着一些其他的副反应见表1。

表1 CO2加氢制甲酸的主反应与副反应[10]
从表1的热力学数据可知,CO2加氢制备甲酸的反应是放热反应且反应无法自发进行,而部分副反应,如生成气态碳和液态水、生成气态甲烷和液态水以及生成气态二甲醚和液态水的反应均易自发进行,且以上反应可同时发生,因此,单一形式的甲酸难以直接获取,为了抑制副反应的发生,需要进行更多的研究来完善反应条件。
从表1可知CO2直接加氢制甲酸的反应无法自发进行,但经过研究,在液态NH3的环境下,气态CO2可通过加氢生成HCO2-(aq)和NH4+(aq),且该反应的热力学参数[11]表明该反应在此条件下可正向自发进行。
2 CO2 加氢制甲酸的均相催化
1935年,研究发现甲酸可由CO2和氢气在异象催化剂雷尼镍的催化下,在反应温度80℃、反应压力20~40MPa下直接合成[12],而使用钯(Pd)或钌(Ru)制成的复合均相催化剂,反应温度和压力的条件可大幅降低[13]。Rh及Ir的复合物等均相催化剂均可作用于以CO2为原料制备甲酸的反应。研究表明以[(P2)RhH]为催化剂,在25℃和40atm的条件下可使CO2加氢生成甲酸[14]。
当Rh复合催化剂,如“Wilkinson催化剂(RhCl (PPh3)3)”,被认为是CO2加氢制甲酸最适合的催化剂时[15],Ru-磷化氢复合催化剂被发现适用于超临界CO2合成甲酸[16]。研究发现,超临界CO2在RuH2[P(CH3)3]4或RuCl2[P(CH3)3]4的催化作用下,甲酸产量可大幅提高,并且,通过在超临界CO2中加入水和甲醇,可加速生成[17]。
以KRuIII-(EDTA-H)Cl2H2O作为催化剂,在40℃和34atm条件下甲酸和甲醛可同时生成,在同样的反应条件下,反应将继续进行,甲酸和甲醛分解的最终产物为CO和水[18]。[Ru(PnBu3)4(H)2]可作为加氢催化剂生产甲酸[19]。在使用[RuCl (O2CMe)(PMe3)4]催化剂制备三乙胺的同时CO2可被加氢,但是反应在15%的三乙胺生成的同时由于温度过低而停止[20],催化剂经过优化改良为[RuCl(PMe3)4]后,在40℃和4.1MPa条件下,可生成HCOOH/Net3。RuCl2(PTA)4均相催化剂也被用于CO2直接加氢制甲酸的反应[21]。
此外,大量研究表明:基于Ru的复合均相催化剂在不同温度和压力条件下,适用于CO2加氢制备甲酸或甲酸盐。同样,铱(Ir)的复合催化剂亦可作为甲酸制备的催化剂。图1表示了一种基于Ir III的复合催化剂(Ir III-Pincer Complex)用来研究CO2加氢制备甲酸盐的反应机理[22]。

图1 Ir III-Pincer复合催化剂反应机理[22]
对另一种相似结构的Ir III复合催化剂(imine-diphosphine ligands)制备甲酸的反应机理进行了研究(图2中“c”)[23],该催化剂同样可使CO2高效的加氢生成甲酸。

图2 Ir III-Imine-Diphosphine Ligands催化剂反应机理[23]
相比较使用Ir III-Pincer复合催化剂的反应条件,该研究同样使用THF和氢氧化钾的溶液,但压力仅需3MPa。当加入0.001mol%催化剂,反应物在140℃温度条件下,在20h后甲酸根反应生成率为81%;同样反应条件下加入0.1mol%催化剂,甲酸根反应生成率则达99%[23]。在同样温度和压力条件下,加入同样量的氢氧化钾和0.001mol%催化剂,研究不同H2和CO2的压力比对试验结果的影响。结果表明:H2∶CO2分别为40∶20和50∶10atm的条件下,20h后甲酸根的反应生成率同样可达99%。进一步的试验结果表明,提高氢氧化钾浓度可促进甲酸根的生成。
3 CO2 加氢制甲酸的多相催化
多相催化剂作为重要的催化手段,在CO2加氢研究中被广泛运用。Au作为催化剂被应用于制备HCOOH/Net3的研究,但是该催化剂在40℃、180bar的反应条件下会快速失活[24]。Ru固定于二氧化硅也被运用于此类研究,其中一项研究发现,在引入离子性液体(ILs)时,催化剂可分散于溶液中,从而导致催化系统对甲酸的生成达到好的活性和选择性,且易分离、易回收[25]。
一种Ru(III)氢氧化物加载于γ-Al2O3基的催化剂被运用于反应的研究,在反应条件为80℃、13.5MPa、环境pH为12.8时,NH3H2O作为滴定液可制备甲酸[26]。研制的(Cu(OAc)2H2O)作为CO2、水和氢化硅烷高效生产甲酸的铜催化剂,在室温条件下1h后甲酸生成率达91%;在60℃条件下,30min后甲酸生成率达95%[27]。生物催化方法也被应用于CO2直接加氢研究,如木醋杆菌是一种CO2还原酶,可用于甲酸根的制备[28]。
4 CO2 加氢制甲酸的等离子及电化学催化
CO2在电催化的作用下可转化为许多具有高附加值的产物,如反应4中的甲酸根[29]:
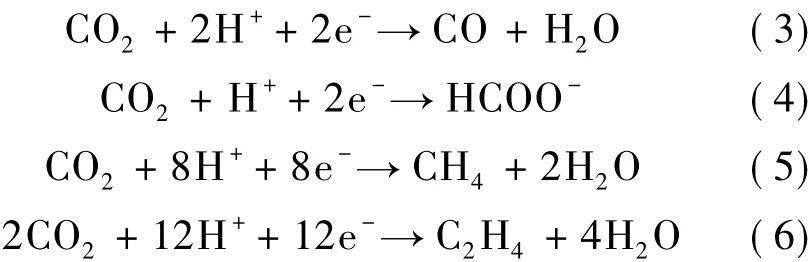
能量效率取决于反应过程中生成产物所需的总能量,同时法拉第效率(电流效率)取决于选择性的使得某种或某些特定产物生成所需要的能量,可以表示为[29]:

有研究发现,等离子催化在热力学上可不需要输入非常高的能量,即可使CO2与水反应生成甲酸[30],这也表明较低的温度或者室温即可满足反应条件。该研究也证明了氢可以直接从含氢的液态化学物质转移到CO2,从而得到甲酸。
17种基于金属酞菁的气体扩散电极用于CO2电催化的研究表明,23℃时在KHCO3水溶液环境下,使用Sn、Pd或In酞菁催化剂,生成的主要产物为甲酸[31]。另外,检测到的其他产物包括CO、甲烷、乙烯和醇类等。研究表明气体扩散电极对于CO2电催化的选择性远高于金属平面电极。对上述反应机理的深入研究发现[CO2]-可通过电子传递实现进一步的甲酸生成[32]。
Cu(内核)/CuO(外壳)纳米催化剂作为CO2电催化的一种催化方法,催化剂由纳米颗粒、水和异丙醇组成,被装载在气体扩散器的表面,铂黑被装载在阳极表面,银/氯化银作为参比电极,KHCO3在反应中作为电解液[33]。检测到的主要产物为甲酸和CO,以及少量的甲醇。
基于上述结论,深入研究发现,在水介质中使用金属电极作用于CO2电催化,可生成CO、HCOO-、CH4、C2H4,当电极的材质为Cu、Au、Ag、Zn、Pd、Ga、Ni和Pt时,CO成为反应的主要产物;而当电极的材质为Pb、Hg、In、Sn、Cd和Ti时,甲酸根成为反应的主要产物。值得一提的是,在反应过程中CO2-可以在电极表面生成,而这种自由或弱吸附CO2-可以促进甲酸根的产生[34]。相似的,运用钯碳作为催化剂同样可以使得CO2在电催化的过程中加氢生成甲酸根,在常温常压下,10%钯碳纳米粒被装载于Ti材质的电极上,以重碳酸盐水溶液为电解液,可生成HCOO-[35]。一种“固体聚合物电解质”系统被发明运用于CO2加氢电催化,可成功制成甲酸。In、Pd、Pb、Pt、Pt/Ru和Cu作为电催化剂的测试结果表明,除Pt和Pt/Ru以外,运用其他的电催化剂均可获得良好的甲酸生成率,特别是In催化剂,在特定的反应条件下甲酸生成率最高可达100%,气态氢为最主要的副产物[36]。
5 CO2 加氢制甲酸的光化学催化
光化学催化CO2加氢的方法也被大量研究。六钛酸钾(Potassium hexatitanate)被装载于Pt或Pt-K2Ti6O13所制成的光催化剂与Cu/ZnO催化剂相结合(Cu∶Zn=1∶1),被用于CO2与水的光催化还原反应[37]。在特定的光照条件下(Xe或Hg-照射灯),生成H2、CH4、HCOH和HCOOH。尽管如此,当仅使用Cu/ZnO催化剂时,使用任何光催化还原均无法获得上述产物。
CO2与水使用UV-Vis照射生成甲酸的光催化还原也被广泛研究。研究表明,TiO2结合Cu(II)酞箐染料或卟啉类化合物与单一TiO2催化剂相比,可使甲酸生成率提高62%,且Cu(II)酞箐催化剂的催化效果优于卟啉催化剂[38]。运用太阳能,在CO2和水的光合作用中引入锌元素,250~325℃温度范围内可成功获得甲酸[39]。在此过程中,锌被氧化为ZnO,而后被太阳能还原,Zn、CO2和H2O反应生成HCOOH和ZnO的焓变与吉布斯自由能分别为-114.75kJ/mol和-23.01kJ/mol。
6 结语
我国燃煤电厂的烟气排放中,CO2含量可达10%以上,每年排放的CO2总量庞大。使用烟气中的CO2作为工业原料制备高附加值的化工产品可带来可观的经济收入,并且为CO2减排做出了实际的贡献。本文就CO2直接加氢制备甲酸的反应从反应热力学、动力学、均相催化、多相催化、低温等离子催化、电催化和光化学催化等方面进行了研究和综述,充分论证了该反应的可行性,尤其是常温或较低温度、常压或较低压力、较低能耗条件下高效的生产甲酸,并且就多种催化手段对甲酸的选择性进行了讨论。
[1]Oh T H.Carbon capture and storage potential in coal-fired plant in Malaysia-A review[J].Renewable&Sustainable Energy Reviews 2010,14(9):2697-2709.
[2]Whipple D T,Kenis P J.Prospects of CO2utilization via direct heterogeneous electrochemical reduction[J].The Journal of Physical Chemistry Letters,2010,1(24):3451-3458.
[3]Srivastava M P,Kobayashi A.Carbon dioxide decomposition by plasma methods and application of high energy and high density plasmas in material processing and nanostructures[J].Transactions of JWRI,2010,39(1):11-25.
[4]王宏亮,薛建明,许月阳,等.电力领域主要温室气体排放情况及控制策略研究[J].华电技术,2014,36(10):56-58.
[5]Leonel Caetano M A,Marcolino Gherardi,Douglas-Francisco,et al.Optimal resource management control for CO2emission and reduction of the greenhouse effect[J].Ecological Modelling,2008,213 (1):119-126.
[6]钱伯章.碳捕捉与封存(CCS)技术的发展现状与前景[J].中国环保产业,2008(12):57-61.
[7]Bernstein L,Lee A,Crookshank S.Carbon dioxide capture and storage:A status report[J].Climate Policy,2006,6(2):241-246.
[8]Song C S.Global challenges and strategies for control,conversion and utilization of CO2for sustainable development involving energy,catalysis,adsorption and chemical processing[J].Catalysis Today,2006,115(1-4):2-32.
[9]Centi G,Perathoner S,Winè G,et al.Electrocatalytic conversion of CO2to long carbon-chain hydrocarbons[J].Green Chemistry,2007,9(6):671-678.
[10]Xu X D,Moulijn J A.Mitigation of CO2by chemical conversion: Plausible chemical reactions and promising products[J].Energy&Fuels 1996,10(2):305-325.
[11]Wesselbaum S,Hintermair U,Leitner W.Continuous‐flow hydrogenation of carbon dioxide to pure formic acid using an integrated scCO2process with immobilized catalyst and base[J].Angewandte Chemie International Edition,2012,51(34):8585-8588.
[12]Farlow M W,Adkins H.The hydrogenation of carbon dioxide and a correction of the reported synthesis of urethans.Journal of the American Chemical Society,1935,57(11):2222-2223.
[13]Behr A,Ebbinghaus P,Naendrup F.Process concepts for the transition metal catalyzed syntheses of formic acid and dimethylformamide based on carbon dioxide[J].Chemical Engineering&Technology,2004,27(5):495-501.
[14]Gassner F,Dinjus E,Gorls H,et al.CO2activation.7.Formation of the catalytically active intermediate in the hydrogenation of carbon dioxide to formic acid using the[{(COD)Rh(μ-H)}4]/Ph2P (CH2)4PPh2catalyst:First direct observation of hydride migration from rhodium to coordinated 1,5-cyclooctadiene[J].Organometallics,1996,15(8):2078-2082.
[15]Inoue Y,Izumida H,Sasaki Y,et al.Catalytic fixation of carbondioxide toformic-acid by transitionmetal complex undermild conditions[J].Chemistry Letters,1976(8):863-864.
[16]Jessop P G,Ikariya T,Noyori R.Homogeneous catalytic hydrogenation of supercritical carbon dioxide[J].Nature,1994(368):231-233.
[17]Jessop P G,Hsiao Y,Ikariya T,et al,Homogeneous catalysis in supercritical fluids:Hydrogenation of supercritical carbon dioxide to formic acid,alkyl formates,and formamides[J].Journal of the A-merican Chemical Society,1996,118(2):344-355.
[18]Khan M M T,Halligudi S B,Shukla S.Reduction of CO2by moleculaer-hydrogen to formic acid and formaldehyde and decomposition to CO and H2O[J].Journal of Molecular Catalysis,1989,57(1): 47-60.
[19]Schaub T,Paciello R.A Process for the synthesis of formic acid by CO2hydrogenation:Thermodynamic aspects and the role of CO[J].Angew Chem-Int Edit,2011,50(32):7278-7282.
[20]Thomas C A,Bonilla R J,Huang Y,et al.Hydrogenation of carbon dioxide catalyzed by ruthenium trimethylphosphine complexes-Effect of gas pressure and additives on rate in the liquid phase[J].Canadian Journal of Chemistry-Revue Canadienne De Chimie,2001,79(5-6):719-724.
[21]Séverine M,Paul J D,Gábor L.Direct synthesis of formic acid from carbon dioxide by hydrogenation in acidic media[J].Nature Communications,2014(5):4017.
[22]Tanaka R,Yamashita M,Nozaki K.Catalytic hydrogenation of carbon dioxide using Ir(III)-pincer complexes[J].Journal of the A-merican Chemical Society,2009,131(40):14168.
[23]Liu C,Xie J H,Tian G L,et al.Highly efficient hydrogenation of carbon dioxide to formate catalyzed by iridium[J].complexes of iminediphosphine ligands[J].Chem Sci,2015,6(5):2928-2931.
[24]Preti D,Resta C,Squarcialupi S,et al.Carbon dioxide hydrogenation to formic acid by using a heterogeneous gold catalyst[J].Angewandte Chemie-International Edition,2011,50(52):12551-12554.
[25]Zhang Z,Xie E,Li W,et al.Hydrogenation of carbon dioxide is promoted by a task-specific ionic liquid.Angew[J].Chem-Int Edit,2008,47(6):1127-1129.
[26]Hao C,Wang S,Li M S,et al.Hydrogenation of CO2to formic acid on supported ruthenium catalysts[J].Catal Today,2011,160(1): 184-190.
[27]Motokura K,Kashiwame D,Miyaji A,et al.Copper-catalyzed formic acid synthesis from CO2with hydrosilanes and H2O[J].Organic Letters,2012,14(10):2642-2645.
[28]Schuchmann K,Müller V.Direct and reversible hydrogenation of CO2to formate by a bacterial carbon dioxide reductase[J].Science,2013,342(6164):1382.
[29]Jhong H R M,Ma S,Kenis P J A.Electrochemical conversion of CO2to useful chemicals:current status,remaining challenges,and future opportunities[J].Current Opinion in Chemical Engineering,2013,2(2):191-199.
[30]Fridman A A.Plasma chemistry[D].Cambridge Univ Pr:2008.
[31]Furuya N,Matsui K.Electroreduction of carbon dioxide on gasdiffusion electrodes modified by metal phthalocyanines[J].Journal of Electroanalytical Chemistry,1989,271(1):181-191.
[32]Furuya N,Koide S.Electroreduction of carbon dioxide by metal phthalocyanines[J].Electrochimica Acta,1991,36(8):1309-1313.
[33]Lan Y,Gai C,Kenis P J A,et al.Electrochemical Reduction of Carbon Dioxide on Cu/CuO Core/Shell Catalysts[J].Chemelectrochem,2014,1(9):1577-1582.
[34]Hori Y,Wakebe H,Tsukamoto T,et al.Electrocatalytic process of CO seletivity in electrochemicalreduction of CO2at mrtal-electrodes in aqueous-media[J].Electrochimica Acta,1994,39(11-12):1833-1839.
[35]Min X,Kanan M W.Pd-Catalyzed Electrohydrogenation of Carbon Dioxide to Formate:High Mass Activity at Low Overpotential and Identification of the Deactivation Pathway[J].J Am Chem Soc,2015,137(14):4701-4708.
[36]Scott K,Cheng H,Samuel S.Reduction of carbon dioxide to formic acid in a solid polymer electrolyte(SPE)reactor[C].Energy and Electrochemical Processes for a Cleaner Environment,Proceedings 2001,2001(23),351-361.
[37]Guan G,Kida T,Harada T,et al.Photoreduction of carbon dioxide with water over K 2Ti 6O 13 photocatalyst combined with Cu/ZnO catalyst under concentrated sunlight[J].Applied Catalysis A:General,2003,249(1):11-18.
[38]Giuseppe M,Cosimo A,Lucia D,et al.Photoreduction of carbon dioxide to formic acid in aqueous suspension:A comparison between phthalocyanine/TiO2and porphyrin/TiO2catalysed processes[J].Molecules,2014,20(1):396.
[39]Jin F,Gao Y,Jin Y,et al.High-yield reduction of carbon dioxide into formic acid by zero-valent metal/metal oxide redox cycles[J].Energy Environ Sci,2011,4(3):881-884.
The research of CO2catalytical reduction and hydrogenation in coal-fired power plant
In the year of 2015,the CO2emission in China reached to 10.2 billion tons which was 28.7%of the global emission,where around 3.615 billion tons of that was contributed by the coal-fired power plant in the electrical power utilities.It gives a systematic study on the reaction thermodynamics and kinetics of the preparation of formate by CO2hydrogenation,demonstrates some catalytic methods,as the homogeneous catalysis,heterogeneous catalysis,low temperature plasma catalysis,electrochemical catalytic and optical chemical catalytic methods,etc.And explores a variety of low energy consumption and effective CO2hydrogenation reaction conditions,for the recovery of CO2from coal-fired power plants and generate high value-added chemical products provides the technical basis.
CO2reduction;hydrogenation;decomposition and utilisation;coal-fired power plant
X701.7
B
1674-8069(2016)06-010-05
2016-09-12;
2016-09-27
刘奕宁(1987-),男,山西朔州人,主要从事碳减排工作。E-mail:liuyn@600795.com.cn
