复合改性膨胀石墨的制备及对酸性艳蓝染料的吸附
2016-03-21王会丽马乐宽范鹏浩徐从斌焦春磊林爱军
王会丽,赵 越,马乐宽,范鹏浩,徐从斌,焦春磊,林爱军
( 1.北京化工大学化学工程学院,北京市环境污染控制与资源化工程研究中心,北京100029; 2.环境保护部环境规划院,北京100012)
复合改性膨胀石墨的制备及对酸性艳蓝染料的吸附
王会丽1,赵越2,马乐宽2,范鹏浩1,徐从斌1,焦春磊1,林爱军1
( 1.北京化工大学化学工程学院,北京市环境污染控制与资源化工程研究中心,北京100029; 2.环境保护部环境规划院,北京100012)
摘要采用相同反离子协同磷酸活化法,以十六烷基三甲基溴化铵( CTAB) -KBr为复合改性剂,制备了一种高效吸附剂复合改性膨胀石墨( M-EG),通过扫描电子显微镜( SEM)、傅里叶变换红外光谱( FTIR)及X射线电子能谱( XPS)等对膨胀石墨( EG)和改性膨胀石墨( M-EG)的形貌结构、组成和价态进行了表征,考察了EG和M-EG对酸性艳蓝染料废水的处理效果.结果表明,复合改性后的膨胀石墨孔隙度变大,表面含氮和溴官能团增多.吸附剂M-EG对酸性艳蓝染料废水具有较高的吸附性能,在pH= 1. 0及30℃条件下对染料的去除率达到94. 13%; EG符合二级动力学吸附模型,用Langmuir等温线方程拟合效果较好; M-EG符合二级吸附动力学方程,同时符合Langmuir和Freundlich等温吸附模型; M-EG的吸附动力学常数大于EG吸附动力学常数.
关键词复合改性膨胀石墨;酸性艳蓝;吸附性能
合成染料在纺织、颜料、造纸、塑料、化妆品及食品等行业中[1]被广泛使用,因而全球每年排放的染料废水占工业废水总量的20%[2]左右,直接排放将对生态环境和人体健康构成严重威胁.由于生产原料多为苯系、萘系、蒽醌、苯胺及联苯胺类化合物[3],且染料多数具有性质稳定、色泽度高、生态毒性大等特点,因而处理难度较大,对环境影响大[4,5],是典型的生物难降解、难处理有机工业废水之一[6],因此其有效处理和再利用是行业清洁发展的关键[7].染料废水常用的处理方法包括化学法、生物法和物理吸附法[8]等,其中吸附处理因其简单便捷而备受重视[9].吸附剂的开发和利用是吸附处理的关键因素[10],近年来发展起来的吸附剂有活性炭[11]、有机膨润土[12]、分子筛[13]、活化煤以及黏土[14]等,但存在成本高及吸附效果不佳等缺点[15,16].
碳基材料是最常用的吸附剂,除活性炭之外,比较具有发展前景的碳基材料有膨胀石墨、碳纤维、碳纳米管及石墨烯等.Chen等[17]制备了超高容量的氧化石墨烯/碳纳米管气凝胶,并用于血红蛋白的吸附分离.Yang等[18]指出石墨烯-半导体复合材料可以将太阳能转化为化学能; Zhang等[19]在石墨烯基复合材料作为光催化材料方面做出了突出贡献.但碳纳米管及石墨烯等材料的制备工艺复杂、成本较高.而膨胀石墨( EG)是以自然界广泛存在的天然鳞片石墨为原料,经插层氧化后受热膨胀而得到的蠕虫状碳材料,它保留了普通石墨吸附能力强、耐腐蚀、耐氧化及无毒等优点,其比表面积较大,具有更强的吸附能力,且其表面对非极性的染料等具有较强的吸附能力[20].人们利用EG作为载体负载催化剂[21,22]后用于环境污染治理,如Wei等[21]将钯纳米颗粒负载在EG的表面用于六价铬的还原.EG在染料废水处理中的应用得到迅速发展.Ding等[22]制备了有序孔三氧化二铟/还原氧化石墨烯纳米复合材料,并对其光催化性能进行了研究.Jiang等[22]制备了氧化锌纳米棒复合材料用于光催化降解亚甲蓝.Yue等[23]利用膨胀石墨负载ZnO后用于甲基蓝染料废水处理.Li等[24]研究了EG对于分散蓝2BLN染料废水的处理效果.但以往的研究大都存在处理时间长及吸附效果差等缺陷,因此提高EG对废水中污染物的处理速率,并改善对污染物的去除效果成为研究重点.本文采用表面活性剂十六烷基三甲基溴化铵( CTAB)及溴化钾( KBr)作为复合改性剂,对膨胀石墨进行表面改性处理,并以磷酸( H3PO4)对改性过程进行活化,得到一种含氮和溴官能团的高效吸附材料( M-EG),并用于吸附处理酸性艳蓝染料废水.对吸附材料的形貌和结构进行了表征,考察吸附材料添加量、反应温度、pH及金属化合物含量对染料吸附效果的影响,并对该吸附反应的动力学性质和等温吸附模型进行了分析.
1 实验部分
1.1试剂与仪器
天然鳞片状石墨( 32目),青岛金日来石墨有限公司;高锰酸钾、硝酸、磷酸和氢氧化钠等为分析纯,北京化工厂;盐酸,北京益利精细化学品有限公司;十六烷基三甲基溴化铵( CTAB),北京化学试剂公司;溴化钾(优级纯)和醋酸(分析纯),北京化工厂;醋酸钠(分析纯),天津市博迪化工有限公司.
低温电炉( PL-1,北京市中兴伟业仪器有限公司) ;紫外-可见分光光度计( TU-1900型,北京普析通用仪器有限责任公司) ;扫描电子显微镜( S-4700,日本Hitachi公司) ;傅里叶变换红外光谱仪( TENSOR27型,德国Bruker公司),KBr压片法; X射线光电子能谱仪( ESCALAB 250型,美国Thermo Fisher Scientific公司),Al Kα辐射.
1.2吸附材料的制备及表征
称取1. 0000 g高锰酸钾( KMnO4)研磨至粉碎状,与10. 0000 g天然鳞片石墨混合均匀,加入20. 0000 g硝酸和磷酸(质量比7∶3)的混合液,完成插层氧化过程,制得可膨胀石墨[25],备用;将可膨胀石墨置于预热至一定温度的低温电炉上,于800 W下加热膨胀至无黄烟产生后取出,得到蠕虫状膨胀石墨( EG),备用.称取2. 9156 g CTAB溶于去离子水中,与2. 0000 g KBr混合,加热搅拌至完全溶解,定容至100 mL,得到CTAB-KBr混合改性剂;取上述制备的可膨胀石墨10 g加入2 mL 50%的H3PO4,在30℃水浴条件下搅拌活化30 min,加入4 mL混合改性剂,超声混合10 min后,在60℃恒温水浴中搅拌反应5 h,水洗,烘干,膨化,得到复合改性膨胀石墨( M-EG).改变CTAB的用量以相同的方法制得不同改性剂改性的EG吸附材料.
在高真空模式下,采用扫描电子显微镜( SEM)观察样品的微观形貌和结构;用KBr压片法制样进行红外光谱扫描( 400~4000 cm-1) ;用X射线电子能谱( XPS)仪分析M-EG中C元素的价态以及元素含量.
1.3 EG与MEG对酸性艳蓝模拟染料废水的吸附
取0. 025 g酸性艳蓝染料溶于去离子水中,加入乙酸-乙酸钠缓冲溶液,定容至200 mL,配制成浓度为125 mg/L的溶液,称取一定量的M-EG置于配置好的染料溶液中,于30℃水浴条件下搅拌,在不同反应时间取样,用紫外分光光度计测定其最大吸收波长(λ= 636 nm)处的吸光度,计算染料浓度和去除率.改变吸附剂使用量、反应温度和溶液pH,测试吸附剂的最佳反应条件;在染料溶液中加入不同的金属化合物,探讨金属离子对吸附剂吸附性能的影响.去除率计算公式为R=(ρ0-ρt) /ρ0,式中,ρ0为溶液初始浓度;ρt为t时刻的染料浓度.
2 结果与讨论
2.1不同条件制备的含氮官能团的膨胀石墨对酸性艳蓝的吸附
通过改变复合改性剂中CTAB的用量,制得不同的吸附材料M-EG用于酸性艳蓝染料废水的吸附处理,结果如图1所示.其中M-EG的添加量为0. 3000 g,反应温度为30℃,溶液pH为6. 0.

Fig.1 Adsorption activities of M-EG&EG in the reduction of acid brilliant bluea.11.662 mg/g CTAB; b.17.493 mg/g CTAB; c.5.831 mg/g CTAB; d.11.662 mg/g without KBr; e.EG.
从图1可以看出,当CTAB用量为11. 662 mg/g时,采用相同反离子协同H3PO4活化法制备的M-EG对染料的去除效果最好,最大去除率为80. 944%,反应在40 min时达到吸附平衡;当CTAB用量分别为5. 831和17. 493 mg/g时,相同反应时间内,对染料的去除率均降低,最大去除率分别为71. 717%和75. 038%,反应进行1 h达到吸附平衡,这可能是由于在KBr和H3PO4的活化作用下,增加CTAB的用量,在固体EG表面所负载的表面活性剂的浓度增大,EG的表面性能得到更好的改善[26],使得染料溶液的表面张力下降[27],有利于染料与吸附材料的反应活性位点相接触.当表面活性剂的用量增加至一定程度时,溶液的表面张力降到最低,表面活性剂在固体表面的吸附量达到最大值,继续增加CTAB用量,其表面张力几乎不再变化[28].而过多CTAB大分子可能会造成石墨层间的堵塞,不利于M-EG对染料的吸附.而未使用相同反离子协同H3PO4活化法制备的M-EG对酸性艳蓝的吸附效果明显较差,但比未改性的EG对染料的去除率高,表明CTAB对EG吸附酸性艳蓝染料的反应具有促进作用,但没有与表面活性剂CTAB具有相同反离子Br·的KBr以及H3PO4的活化作用,这种促进作用比较微弱.
另外,为了考察复合改性剂M-EG在处理染料废水应用领域中的普适性,保持其它条件不变,采用吸附性能较好的M-EG( 11. 662 mg/g)对多种染料废水进行吸附处理,结果发现对亚甲基蓝、酸性大红及分散黄染料的去除率及达到吸附平衡的时间分别为64. 21%,81. 82%,90. 35%和60,50,50 min,均比未改性的EG及单纯采用CTAB(复合改性剂中不加KBr)作为改性剂制备的改性EG对染料废水的吸附效果有一定程度的提高.表明采用相同反离子协同H3PO4活化法制得的复合改性吸附剂M-EG在染料废水处理中具有普遍适用性.
2.2复合改性膨胀石墨( M-EG)的表征
对EG及吸附性能较好的M-EG( 11. 662 mg/g)材料的外观形貌进行了表征,结果如图2所示.从图2( A)中可以看出,改性前EG呈蠕虫状结构,表面具有大量的褶皱和开放型、半开放型的孔结构.将图2( A)中方框内部分继续放大得到图2( B),可以看出,EG表面的孔大多呈狭缝形和狭缝楔形[29],比较规则;图2( C)为经相同反离子协同H3PO4活化法制备的M-EG的SEM照片,表明复合改性后吸附剂的网状孔结构基本保持不变,但多边形的柱孔或楔孔数量减少甚至消失,形成连续的开放孔,孔径增大,孔容量增加[27].

Fig.2 SEM images of EG( A,B) and M-EG( C)
图3( A)给出了EG与M-EG的傅里叶变换红外光谱图.可以看出,EG的红外吸收峰主要出现在3434,1633,1120,1384. 3以及2312 cm-1处,与文献[30~33]对比,可分别与H2O,C—O,—NO2和CO特征峰相对应.其中H2O特征峰的出现是由于EG的表面吸附或制样过程中KBr吸水; N来自于制备可膨胀石墨过程中所采用的HNO3;含氧官能团来自于可膨胀石墨制备过程中的所使用的氧化剂或者高温膨化过程中的空气氧化.与EG不同,M-EG在3434和1633 cm-1处的H2O特征峰消失,可能是由于在复合改性剂及活化剂作用下,EG对H2O分子的亲和力下降;在1570和1720 cm-1处出现了CN和—COOH的特征吸收峰,而EG中由于水峰太强,这2个峰检测不到或者不存在,将1500~1800 cm-1部分谱图局部放大[图3( A)插图],可以看到,在1570和1720 cm-1处各有1个小峰,可归属为CN和—COOH,而改性后吸收峰位的偏移可归因于复合改性剂的影响; M-EG在3742 cm-1检测到分子间氢键的特征吸收,在657 cm-1处出现了C—Br键的特征吸收[34],1384与2312 cm-1处的峰强度变大,表明经混合改性剂表面处理后,EG的表面组成发生了变化.
图3( B)为M-EG中C1s的XPS能谱图,谱图用XPSPEAK Ver.4. 1进行分峰处理.其中284. 6 eV归属为C—C和C—H,285. 2 eV归属为C—N键,在291. 0 eV处还有很弱的1个峰,可能是—COOH键或者CC[35,36].而C—O,CO未能检测出来可能是由于受到了N元素的影响[10].另外,通过元素分析,改性后吸附材料表面的N元素含量由0. 84%增加到1. 29%,O和P元素含量分别由4. 11%和0. 81%减少到3. 76%和0. 7%; Br元素含量由零增加到0. 79%.表明采用相同反离子协同H3PO4活化法,制备CTAB-KBr复合改性EG吸附材料过程中,EG表面发生了化学反应,并负载了含氮和溴官能团.

Fig.3 FTIR( A) and XPS spectra( B) of M-EGa.EG ; b.M-EG.
2.3 M-EG对酸性艳蓝染料溶液的吸附性能
2.3.1反应条件对M-EG吸附酸性艳蓝染料的影响将0. 075 g M-EG添加在125 mg/L的酸性艳蓝染料废水中对染料进行吸附,其它反应条件(温度为30℃,pH为5. 5)不变,考察了吸附剂M-EG添加量对吸附效果的影响,结果见图4( A).随着吸附剂添加量的增加,对染料的去除率逐渐增大,但当加入的吸附剂量达到3. 333 mg/L时,染料的去除率反而降低;吸附剂对染料的单位吸附量却一直呈减小趋势.这可能是由于染料分子在M-EG固体表面为动态吸附过程,一定时间后吸附与脱附过程达到平衡,但当加入的吸附剂M-EG增多时,平衡向吸附的方向进行,因此染料去除率增加;但当吸附剂加入量过多时,虽然反应活性位点继续增多,受废水中染料浓度限制,吸附达到饱和.而吸附剂M-EG却由于自身机械强度缺陷在搅拌条件下破碎,释放出微小的石墨颗粒,可能影响污水处理效果.同时由于吸附剂增加,废水中的染料有限,因而M-EG未达到反应条件下的饱和吸附,呈现出单位吸附量的减小.这与文献[24]的研究结果趋势基本一致.为了研究反应温度对吸附效果的影响,分别在不同温度下以M-EG对酸性艳蓝废水进行吸附反应,其它条件(添加量为1. 25 mg/L,pH为5. 5)保持不变,结果见图4( B).当温度由10℃升高到50℃时,吸附剂对染料的去除率由81. 17%增加到94. 13%,表明在M-EG吸附酸性艳蓝染料过程中发生的是吸热反应,温度升高,反应向吸附的方向移动.废水pH是影响染料去除率的另一个重要因素,由于艳蓝染料为酸性,因此,本研究选取pH的范围为1. 0~6. 0.图4( C)表明,在酸性条件下,废水pH越小,M-EG对酸性艳蓝的吸附效果越好,去除率越高,这可能是由于随着pH减小,废水中H·数量增多,OH·数量减少,染料的结构发生变化,或者吸附剂的表面性质受到了影响[37].
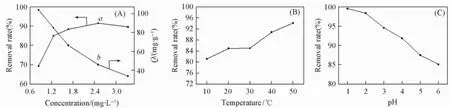
Fig.4 Effect of adding amount( A),temperature( B) and pH( C)a.Removal rate; b.equilibrium adsorption capacity.
为了考察金属离子对M-EG吸附性能的影响,分别在酸性艳蓝染料废水中加入一定量的不同金属化合物,研究染料去除率的变化,结果如表1所示.染料去除率在不同的NaCl和NaOH浓度下变化不大,表明碱金属离子对吸附剂M-EG的性能影响较小,从而验证了KBr对吸附剂性能的影响是由于Br-的存在;而当Pb( NO3)2的加入量由0增加到166. 7 mg/L时,染料的去除率由85. 06%增加到94. 66%,可能是由于重金属离子Pb2+与酸性艳蓝分子发生螯合作用,破坏了染料的显色作用[6].
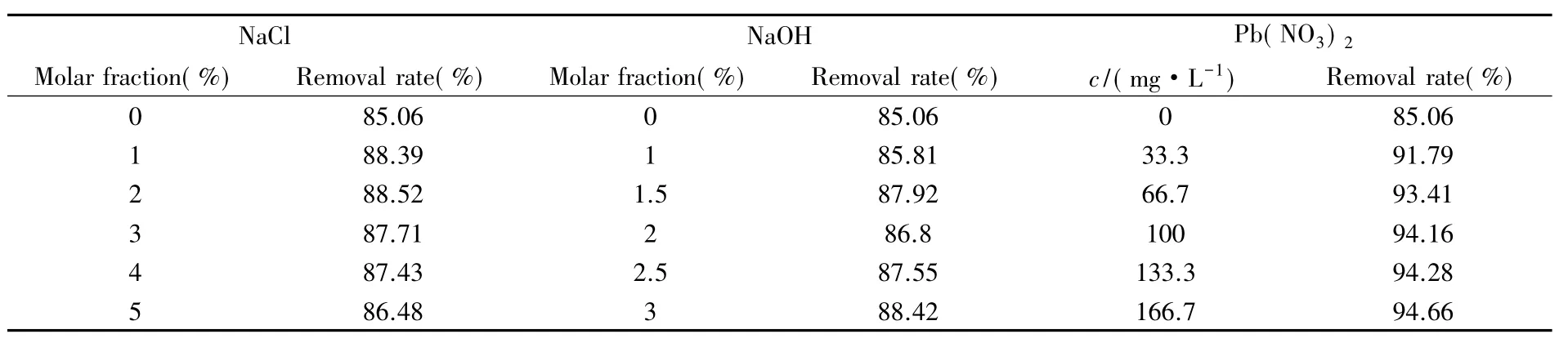
Table 1 Effects of metal compounds on reduction rate of acid brilliant blue
2.3.2 M-EG对酸性艳蓝染料的吸附动力学性质采用Lagergren准一级动力学模型和准二级动力学模型对EG和M-EG吸附酸性艳蓝染料的动力学吸附结果进行模拟,其表达式分别为[38]

式中: Qe为平衡吸附量( mg/g) ; Qt为t时刻的吸附量( mg/g) ; t为吸附时间( h) ; k1和k2分别为吸附动力学速率常数.
动力学常数拟合结果如表2所示.从表2中可以看出,与准一级动力学模型相比,准二级动力学对2种吸附剂的拟合结果能更好地与数据点重合,相关系数R2均在0. 95以上.其中M-EG比EG的拟合效果更好.而M-EG的吸附速率常数k大于EG的吸附速率常数,表明M-EG对酸性艳蓝染料的吸附比EG快[39],这与2. 1节的结果相同.
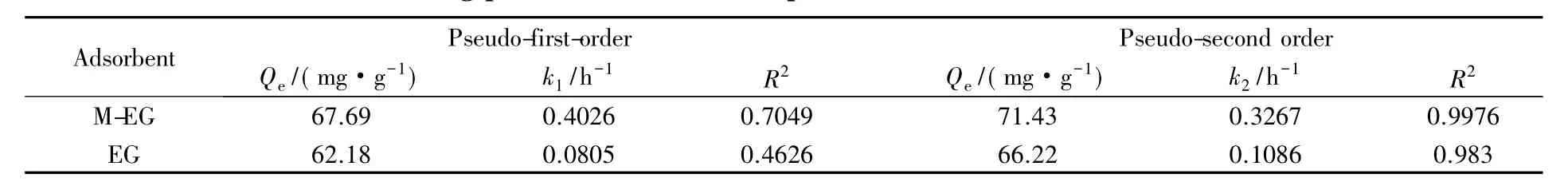
Table 2 Fitting parameters of kinetic equations for acid brilliant blue on M-EG
2.3.3 M-EG对酸性艳蓝染料的吸附等温线分别采用Langmuir和Freundlich等温吸附方程对EG和M-EG吸附酸性艳蓝染料的过程进行描述,方程式分别为[40]

式中: Qm为形成单分子层的最大吸附量( mg/g) ; Qe为吸附平衡量( mg/g) ; ce为平衡浓度( mg/L) ; LL,n分别为吸附平衡常数; KL和KF分别为吸附平衡速率常数.
吸附等温线各参数模拟结果见表3.由表3可知,EG对Langmuir模型比较符合,R2为0. 8142,而M-EG同时符合Langmuir模型和Freundlich模型,R2分别为0. 9785和0. 8311,表明M-EG对酸性艳蓝染料的吸附属于多分子层吸附,在高浓度时吸附容量会持续增加[39].

Table 3 Isotherms constants for acid brilliant blue on M-EG
综上所述,采用相同反离子协同H3PO4活化法,制得了高效复合改性膨胀石墨( M-EG).M-EG的孔径较EG变大,负载上含N和Br的官能团.相同条件下对酸性艳蓝染料的吸附速率变快,平衡去除率增大,同时单位吸附量也增加,在pH=1. 0及30℃条件下对125 mg/L的染料去除率达到94. 13%,反应进行40 min后达到吸附平衡.M-EG对酸性艳蓝染料的吸附反应符合二级动力学吸附模型,对Langmuir等温吸附模型和Freundlich等温吸附模型拟合效果均较好,但Freundlich等温吸附模型能更好地反映吸附机理.
参考文献
[1]Li F.,Wang G.Y.,Zhang Y.,Ling H.R.,Chem.J.Chinese Universities,2015,36( 7),1351—1357(李锋,王桂燕,张岩,李洪仁.高等学校化学学报,2015,36( 7),1351—1357)
[2]Li K.B.,Zhao F.,Wei H.,Zhang T.,Wang Q.Q.,Chem.J.Chinese Universities,2011,32( 8),1812—1818(李克斌,赵锋,魏红,张涛,王勤勤.高等学校化学学报,2011,32( 8),1812—1818 )
[3]Ren N.Q.,Zhou X.J.,Guo W.Q.,Yang S.S.,CIESC Journal,2013,64( 1),84—94(任南琪,周显娇,郭婉茜,杨珊珊.化工学报,2013,64( 1),84—94)
[4]McMullan G.,Meehan C.,Conneely A.,Kirby N.,Robinson T.,Nigam P.,Banat I.M.,Marchant R.,Smyth W.F.,Applied Microbiology and Biotechnology,2001,56,81—87
[5]Wang Y.Z.,Chen M.X.,Hu C.,Acta Scientiae Circumstantiae,2000,20( 6),772—775(王怡中,陈梅雪,胡春.环境科学学报,2000,20( 6),772—775)
[6]Liu Y.,Degradation of Dye Wastewater by Ccatalytic Wet Oxidation Under Room Temperature and Atmospheric Pressure,Harbin Institute of Technology,Harbin,2006(刘琰.常温常压催化湿式氧化工艺处理染料废水的研究,哈尔滨:哈尔滨工业大学,2006)
[7]Huo H.L.,Lü L.Y.,Wang H.,Chem.J.Chinese Universities,2015,36( 5),939—944(霍海玲,吕丽云,王虹.高等学校化学学报,2015,36( 5),939—944)
[8]Teng M.,Qiao J.,Li F.,Bera P.K.,Carbon,2012,50,2877—2886
[9]Bae J.H.,Song D.I.,Jeon Y.W.,Separation Science and Technology,2000,35( 3),353—365
[10]Meng F.P.,Yi H.C.,Materials Review,2009,23( 7),69—73(孟范平,易怀昌.材料导报,2009,23( 7),69—73)
[11]Liao P.,Ismael Z.M.,Zhang W.,Yuan S.,Tong M.,Wang K.,Bao J.,Chem.Eng.J.,2012,195,339—346
[12]Chen X.L.,Deng L.C.,Wang X.F.,Guan S.,Chem.J.Chinese Universities,2014,35( 12),2510—2515(陈晓磊,邓李川,王晓峰,关爽.高等学校化学学报,2014,35( 12),2510—2515)
[13]Huang C.,Chang K.,Ou H.,Chiang Y.,Wang C.,Micropor.Mesopor.Mater.,2011,141,102—109
[14]Zhou X.,Ge X.,Tang R.Z.,Chen T.,Wang G.Y.,Chin.J.Catal.,2014,35( 4),481—489(周喜,葛鑫,唐荣芝,陈彤,王公应.催化学报,2014,35( 4),481—489)
[15]Yang M.X.,Ma J.,Sun Y.R.,Chem.J.Chinese Universities,2014,35( 3),570—575(杨明轩,马杰,孙怡然.高等学校化学学报,2014,35( 3),570—575)
[16]Liu P.,Zhang L.,Sep.Purif.Technol.,2007,58,32—39
[17]Chen X.W.,Zheng X.,Wang X.F.,Wang J.H.,Chem.J.Chinese Universities,2015,36( 8),1641—1647(陈旭伟,郑旭,王晓峰,王建华.高等学校化学学报,2015,36( 8),1641—1647)
[18]Yang M.Q.,Zhang N.,Pagliaro M.,Xu Y.J.,Chem.Soc.Rev.,2014,43,8240—8254
[19]Zhang N.,Zhang Y.H.,Xu Y.J.,Nanoscale,2012,4,5792—5813
[20]Li W.,Han C.,Liu W.,Zhang M.H.,Tao K.,Catal.Today,2007,125,278—281
[21]Wei Y.X.,Tu W.X.,Chem.J.Chinese Universities,2014,35( 11),2397—2402(魏英祥,涂伟霞.高等学校化学学报,2014,35 ( 11),2397—2402)
[22]Ding M.J.,Huang H.,Yang P.,Chem.J.Chinese Universities,2015,36( 5),989—995(丁敏娟,黄徽,杨平.高等学校化学学报,2015,36( 5),989—995)
[23]Yue X.Q.,Duan W.Y.,Lu Y.,Zhang F.C.,Zhang R.J.,Bull.Mater.Sci.,2011,34,1569—1573
[24]Li J.T.,Li M.,Li J.H.,Sun H.W.,Ultrasonics Sonochemistry,2007,14,62—66
[25]Cao N.Z.,Shen W.C.,Wen S.Z.,Liu Y.J.,Material Science&Technology,1997,5( 2),121—123(曹乃珍,沈万慈,温诗铸,刘英杰.材料科学与工艺,1997,5( 2),121—123)
[26]Lu Y.,Zhong J.B.,Li J.Z.,Zeng J.,He J.J.,Chemical Research and Application,2013,25( 6),866—870(卢燕,钟俊波,李建章,曾俊,贺进进.化学研究与应用,2013,25( 6),866—870)
[27]Fu M.,Wang R.F.,Zhao X.B.,Ding J.N.,Chen Z.,Functional Materials,2009,40( 8),1322—1325(付猛,王荣飞,赵晓兵,丁建宁,陈志刚.功能材料,2009,40( 8),1322—1325)
[28]Xiao X.,Zhao Z.G.,Surfactant Application Principle,Chemical Industry Press,Beijing,2003,78—83(肖进新,赵振国.表面活性剂应用原理,北京:化学工业出版社,2003,78—83)
[29]Cao N.Z.,Shen W.C.,Wen S.Z.,Acta Physico-Chimica,1996,12( 8),766—768(曹乃珍,沈万慈,温诗铸.物理化学学报,1996,12( 8),766—768)
[30]Zhang W.H.,Yin D.,Lu N.,Li Z.Y.,Yang J.L.,Chem.J.Chinese Universities,2015,36( 11),2081—2086(张文华,殷迪,卢宁,李振宇,杨金龙.高等学校化学学报,2015,36( 11),2081—2086)
[31]Steurer P.,Wissert R.,Thomann R.,Mülhaup R.,Rapid Commun.,2009,30,316—327
[32]Han Z.D.,Wang J.Q.,Chinese Journal of Inorganic Chemistry,2003,12,1366—1370(韩志东,王建祺.无机化学学报,2003,12,1366—1370)
[33]Stankovich S.,Piner R.D.,Chen X.Q.,Wu N.Q.,Nguyen S.T.,Ruoff R.S.,J.Mater.Chem.,2006,16,155—158
[34]Weng S.F.,Fourier Transform Infrared Spectroscopy,Chemical Industry Press,Beijing,2010,377—388(翁诗甫.傅里叶变换红外光谱分析,北京:化学工业出版社,2010,377—388)
[35]Jiang B.J.,Tian C.G.,Wang L.,Xu Y.X.,Wang R.H.,Qiao Y.J.,Ma Y.G.,Fu H.G.,Chem.Commun.,2010,46,4920—4922
[36]Wang J.,Guo B.D.,Zhang X.D.,Zhang Z.H.,Ultrasonics Sonochemistry,2005,12( 5),331—337
[37]Yu G.F.,Qing C.L.,Mou S.S.,Acta Scientiae Circumstantiae,2001,21( 5),601—606(余贵芬,青长乐,牟树森.环境科学学报,2001,21( 5),601—606)
[38]Sun X.,Li L.Q.,Pan G.X.,Journal of Agro-Environment Science,2014,33( 8),1637—1643(孙璇,李恋卿,潘根兴.农业环境科学学报,2014,33( 8),1637—1643)
[39]Li R.Y.,Chen D.,Li L.Q.,Journal of Agro-Environment Science,2015,34( 5),1001—1008(李瑞月,陈德,李恋卿.农业环境科学学报,2015,34( 5),1001—1008)
[40]Sun Y.L.,Ni J.R.,Environmental Chemistry,2002,21( 1),37—44(孙玉玲,倪晋仁.环境化学,2002,21( 1),37—44)
Preparation of Composite Modified Expanded Graphite and Its Adsorption on Acid Brilliant Blue Dye†
WANG Huili1,ZHAO Yue2,MA Lekuan2,FAN Penghao1,XU Congbin1,JIAO Chunlei1,LIN Aijun1*
( 1.Beijing Environmental Pollution Control and Resource Engineering Research Center,College of Chemical Engineering,Beijing University of Chemical Technology,Beijing 100029,China; 2.Chinese Academy for Environmental Planning,Beijing 100012,China)
Abstract Modified expanded graphite( M-EG) was synthesized via same counter ion coordinated phosphate ( H3PO4) activation method,as prepared expanded graphite ( EG).M-EG was investigated by scanning electron microscopy( SEM),Fourier transform infrared spectroscopy( FTIR) and X-ray photoelectron spectroscopy( XPS).The adsorbent activities of the EG and M-EG were evaluated for the reduction of acid brilliant blue.The results indicated that the porosity of EG after composite modified expanded,the surface enlarged and the nitrogen-and bromine-containing functional groups increasing.Adsorbent M-EG in acid brilliant blue dye wastewater show high adsorbent activities with a 94. 13% reduction at pH = 1. 0 and 30℃.The adsorption reaction of EG line with second-order kinetic adsorption model,and the Langmuir isotherm equation is well fitted; M-EG conform second adsorption kinetics equation,while compliance with Langmuir isotherm model and Freundlich isotherm model,what’s more adsorption kinetics constant is greater than EG’s.
Keywords Composite modified expanded graphite; Acid brilliant blue; Adsorption property
( Ed.: V,Z)
†Supported by the National Natural Science Foundation of China( No.40901149) and the Environmental Nonprofit industry Special Research ( No.201309022).
基金项目:国家自然科学基金(批准号: 40901149)和环保公益性行业科研专项(批准号: 201309022)资助.
收稿日期:2015-07-14.网络出版日期: 2016-01-06.
doi:10.7503/cjcu20150544
中图分类号O647
文献标志码A
联系人简介:林爱军,男,博士,副教授,主要从事污水处理以及土壤污染修复研究.E-mail: ajlin@ 126.com
