聚合植物油脂表面活性剂的制备及其结构与性能
2016-03-18黄旭娟刘鹤王磊商士斌中国林业科学研究院林产化学工业研究所生物质化学利用国家工程实验室国家林业局林产化学工程重点开放性实验室江苏省生物质能源与材料重点实验室江苏南京004南京林业大学化学工程学院江苏南京004
黄旭娟,刘鹤,王磊,商士斌(中国林业科学研究院林产化学工业研究所,生物质化学利用国家工程实验室,国家林业局林产化学工程重点开放性实验室,江苏省生物质能源与材料重点实验室,江苏 南京 004;南京林业大学化学工程学院,江苏 南京 004)
聚合植物油脂表面活性剂的制备及其结构与性能
黄旭娟1,刘鹤1,王磊2,商士斌1
(1中国林业科学研究院林产化学工业研究所,生物质化学利用国家工程实验室,国家林业局林产化学工程重点开放性实验室,江苏省生物质能源与材料重点实验室,江苏 南京 210042;2南京林业大学化学工程学院,江苏 南京 210042)
摘要:采用环氧大豆油(ESO)为原料,乙酸乙酯为溶剂,四氯化锡为催化剂,通过环氧大豆油的开环自聚,制备聚合环氧大豆油(PESO);再将PESO在碱性条件下水解,洗涤纯化后得到水解聚合环氧大豆油(HPESO)。通过傅里叶红外光谱(FTIR)、核磁共振氢谱(1H NMR)和凝胶渗透色谱(GPC)对HPESO的结构及分子量分布进行了表征,并对得到的水解聚合环氧大豆油脂肪酸钾盐表面活性剂(HPESO-K)的临界胶束浓度cmc及其表面张力(γcmc)、Krafft点(KP)、液体石蜡/水体系的乳化能力(EP)与抑泡及消泡能力(FP)进行了研究。结果表明:HPESO的数均分子量范围为1056~1156g/mol,重均分子量范围为1255~1374g/mol。在水溶液pH值为9~12条件下,HPESO-K的cmc值为0.13~0.41g/L,γcmc值为25.6~31.2mN/m。在水溶液pH=9条件下测得HPESO-K的Krafft点为37℃,液体石蜡/水体系中分出10mL水的时间为130s,亲水亲油平衡(HLB)值范围为10~11。
关键词:环氧大豆油;聚合;水解;分子量分布;表面活性剂
第一作者:黄旭娟(1991—),女,硕士研究生。联系人:刘鹤,副研究员,研究领域为纤维素资源利用。E-mail liuheicifp@hotmail.com。商士斌,研究员,博士生导师,研究领域为生物质资源的化学研究与利用。E-mail shangsb@hotmail.com。
表面活性剂是在分子中同时含有亲水基和亲油基,在溶液的表面能定向排列,并能使表面张力显著下降的物质。表面活性剂是重要的精细化工产品,目前已从家用洗涤剂和个人保护用品发展到国民经济各个领域,而且在生产和生活的各个方面都起了重要的作用[1]。表面活性剂的生产最早可追溯于公元前,主要以动植物油脂为原料与草木灰或石碱等混合加热而成[2]。天然植物油脂是甘油三酸酯的多元混合物,其脂肪酸主要有油酸、亚油酸和亚麻酸等不饱和脂肪酸,具有来源广泛、价格低廉、可再生以及符合可持续发展战略要求等优点[3]。并且,随着表面活性剂的日益发展,聚合类表面活性剂成了近年来的研究热点。与小分子表面活性剂相比,聚合类表面活性剂由于分子量较大,具有较高的降低表面张力的能力,且稳定性和分散性较小分子表面活性剂更好[4]。因此,利用植物油脂为原料制备聚合植物油脂表面活性剂,不仅丰富了表面活性剂的产品种类,也提高了植物油脂的附加值。本研究以环氧大豆油(ESO)为原料,乙酸乙酯为溶剂,四氯化锡为催化剂,通过开环聚合反应得到聚合环氧大豆油,再经一步碱性水解,洗涤纯化后得到水解聚合环氧大豆油。
1 实 验
1.1 主要试剂及仪器
环氧大豆油(ESO)、蓖麻油酸、四氯化锡,阿拉丁试剂有限公司;乙酸乙酯、氢氧化钾,分析纯,南京化学试剂有限公司。
DF-101S集热式恒温加热磁力搅拌器,南京文尔仪器设备有限公司;Thermo Scientific Nicolet is10傅里叶变换红外光谱仪、Thermo Scientific orion star series pH计,美国Thermo Scientific公司;Bruker AV-300 核磁共振光谱仪,德国Bruker公司;Sigma 701表面张力仪,瑞典百欧林科技有限公司;Waters1550型凝胶渗透色谱仪,沃特世科技有限公司。
1.2 聚合植物油脂表面活性剂的制备
聚合表面活性剂的制备如图1所示。
1.2.1 聚合环氧大豆油(PESO)的制备
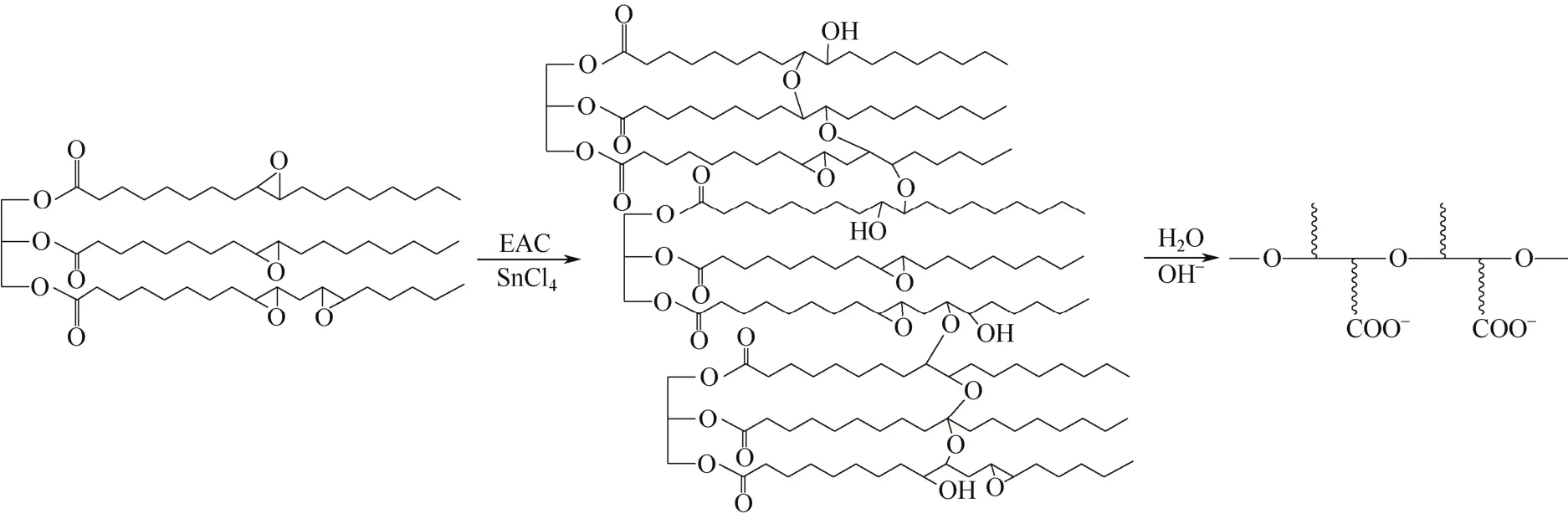
图1 水解聚合环氧大豆油的制备示意图
分别称取10g、15g和60g的环氧大豆油溶于15g乙酸乙酯溶剂并置于250mL的三口烧瓶中,在恒温水浴锅中搅拌加热至60℃。分别取50μL、150μL和600μL四氯化锡催化剂溶于5g乙酸乙酯,并通过恒压漏斗缓慢滴加进入反应体系,滴加时间为5min,反应时间为2h。反应结束后,通过减压蒸馏除去乙酸乙酯得到聚合环氧大豆油产物,产物分别记为PESO-1、PESO-2与PESO-3。
1.2.2 水解聚合环氧大豆油(HPESO)的制备
称取5g上述聚合环氧大豆油加料于250mL三口烧瓶中,加入浓度为1mol/L的氢氧化钾溶液150mL,在100℃条件下剧烈搅拌,回流反应12h;水解产物通过减压蒸馏除水后,用乙酸乙酯洗涤除去未水解的油脂及甘油。过滤后得到的固体产物重新分散于水中并调节pH值至4~6,油层通过乙酸乙酯萃取并用热蒸馏水洗涤纯化,再经减压蒸馏除去乙酸乙酯得到聚合环氧大豆油脂肪酸,产物分别记为HPESO-1、HPESO-2与HPESO-3。且通过氢氧化钾调节其pH值至9~12得到的聚合植物油脂表面活性剂分别记为HPESO-K-1、HPESO-K-2与HPESO-K-3。
1.3 产品结构表征及性能分析
1.3.1 FTIR分析
采用Thermo Scientific Nicolet is10傅里叶变换红外光谱仪对产物进行表征,采用衰减全反射(ATR)测试。
1.3.21H NMR分析
以四甲基硅烷(TMS)为内标,氘代氯仿(CD3Cl)为溶剂,利用Bruker AV-300核磁共振光谱仪对产物进行表征。
1.3.3 GPC测试
将HPESO充分溶解于四氢呋喃中,测试前,样品通过孔径为0.45μm的过滤器(Nylon,Millex-HX 13mm Syringes Filters,US)过滤,以四氢呋喃为流动相,用Waters1550型凝胶渗透色谱仪测定样品的相对分子质量,检测器为Water2487紫外检测仪和Water2414折光指数测定仪,色谱柱为Styrage HR1和HR2(300mm×7.8mm,两根串联),流动相流速为1mL/min;采用单分散聚苯乙烯(相对分子质量580~196000,分散系数为1.02~1.11)作为标准样品计算聚合物的相对分子质量及其分子量分布,相关数据由Water Breeze GPC software Verson 5.3.1.4计算获得。
1.3.4 HPECO的聚合度(DP)
环氧大豆油的结构式是脂肪酸的三甘油酯,其中单个脂肪酸链上存在一个或两个环氧基团。环氧大豆油在聚合与水解反应后,分子量减小,且根据脂肪酸分子的结构式可知单个脂肪酸的分子量范围为279~293,为方便计算取其平均值为286。因此,通过HPECO的分子量可计算出其聚合度(DP)值。
1.3.5 临界胶束浓度cmc及其表面张力(γcmc)
配置不同浓度的聚合植物油脂表面活性剂的溶液,通过Wilhelmy板(宽19.44mm;厚0.1mm;高度65mm)测试法利用Sigma 701表面张力仪测定。
1.3.6 Krafft点(KP)
配制质量分数为0.1%的水溶液,加热,记录溶液由浑浊至透明时的温度即为该聚合植物油脂表面活性剂的Krafft点,每个样品重复3次,取其平均值[5]。
1.3.7 乳化性能(EP)
室温条件下,取40mL质量分数为1%的产品水溶液与40mL液体石蜡倒入100mL的具塞量筒中,塞上塞子,剧烈振荡50次形成液体石蜡/水乳化体系,然后静置,记录乳化体系分出10mL水的时间(EP值)。每个样品重复测试3次,取其平均值[6]。
1.3.8 泡沫性能(FP)
室温条件下,取30mL质量分数为0.1%的产品水溶液倒入100mL的具塞量筒中,塞上塞子,剧烈振荡25次后,记录初始的泡沫高度及静置5min后的泡沫高度(FP值)。每个样品重复测试3次,取其平均值[7]。
1.3.9 亲水亲油平衡值(HLB值)的测定
选择一对HLB值相差较大的乳化剂:司班-80 (HLB=4.3)与吐温-60(HLB=14.9)。按不同质量比例配制一系列具有不同HLB值的混合乳化剂。用此混合乳化剂将配制的1g/L的聚合植物油脂表面活性剂制成系列乳状液,获得乳化稳定性最好的乳状液所对应乳化剂的HLB值即为产品的HLB值[8]。
2 结果与讨论
2.1 聚合反应机理
环氧大豆油开环聚合的机理如图2所示:链引发由SnCl4引发剂与环氧植物油脂本身存在的羟基或溶剂中存在的微量醇形成络合物,而后转变成离子对,提供质子。链增长为质子引发环氧基团开环,形成氧鎓离子带正电荷,其邻近的α-碳原子电子不足,导致键断裂,而后又形成离子对形式,如此增长下去。链终止时为反离子亲核性过强,容易与阳离子活性种结合而终止[9]。
2.2 FTIR分析
利用红外光谱对ESO、PESO与HPESO-K的结构进行了分析,结果如图3所示。环氧大豆油发生聚合反应之后,PESO产物中822cm−1处环氧基团特征吸收峰消失,且出现3400cm−1处羟基的特征吸收峰与1044cm−1处仲羟基的特征振动吸收峰,说明聚合反应发生后,环氧基团全部开环,且聚合反应发生的同时也生成了仲羟基。PESO在碱性条件下水解之后,HPESO−K产物中1740cm−1处酯基的伸缩振动吸收峰与1239cm−1处羧酸C—O伸缩振动吸收峰消失,出现1561cm−1处的羧酸盐的特征吸收峰,说明得到了聚合植物油脂表面活性剂。

图2 环氧大豆油开环聚合反应机理
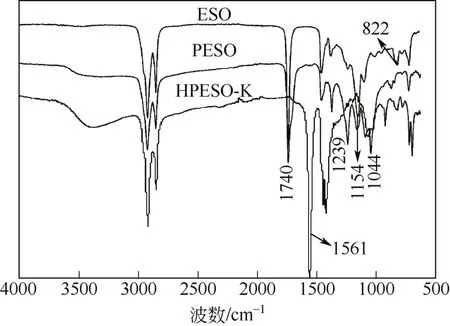
图3 环氧大豆油、聚合环氧大豆油与水解聚合环氧大豆油脂肪酸钾盐的FTIR图
2.31H NMR分析
以氘代氯仿(CD3Cl)为溶剂,对ESO与HPESO进行1H NMR分析,结果如图4所示。HPESO中5.2~5.3处油脂中甘油骨架上叔碳氢的信号峰与4.0~4.4处油脂中甘油骨架上仲碳氢的信号峰消失,表明PESO水解完全;HPESO中2.8~3.2处环氧基团上氢的特征信号峰消失,出现化学位移3.2处羟基的特征信号峰与化学位移3.8处烷烃链中与羟基相连叔碳上氢的信号峰,表明环氧大豆油经过环氧活性基团开环自聚水解之后,环氧基团完全反应,聚合的同时也生成了仲羟基,证明聚合反应的发生。

图4 环氧大豆油与水解聚合环氧大豆油的1H NMR图
2.4 GPC分子量分布分析
HPESO-1、HPESO-2和HPESO-3的分子量分布曲线图如图5所示。从图5可以看出, HPESO-1、HPESO-2与HPESO-3这3种产物的分子量分布基本一致。环氧大豆油分子结构是甘油三酸酯的多元混合物,在聚合过程中,环氧基团的开环聚合包括环氧大豆油分子内环氧基团的开环聚合与环氧大豆油分子间环氧基团的开环聚合。在聚合环氧大豆油的水解过程中,聚合环氧大豆油的甘油酯断裂,导致环氧聚合大豆油水解之后分子量的减小。GPC测试结果如表1所示,HPESO-1、HPESO-2与HPESO-3的数均分子量分别为1156、1121和1056,重均分子量分别为1358、1374和1255。通过GPC的重均分子量结果,可以算出HPECO的聚合度为4~5。结果表明:以SnCl4为催化剂,环氧大豆油的反应浓度在一定范围内,其自聚合的程度是一定的。以下表面性能测试均以HPESO-K-2产物为例。

表1 HPECO的GPC数据

图5 HPESO-1、HPESO-2和HPESO-3的分子量分布曲线
2.5 聚合植物油脂表面活性剂的表面性能
2.5.1 临界胶束浓度及其表面张力
水解聚合环氧大豆油结构中,环氧基团开环聚合生成醚键的同时,也生成了仲羟基。对于单个脂肪酸分子,蓖麻油酸结构中也存在一个羟基,与水解聚合环氧大豆油脂肪酸的重复单元结构相似,因此将蓖麻油酸钾盐与水解聚合环氧大豆油脂肪酸钾盐的表面性能作对比。图6为pH=9条件下水解聚合环氧大豆油脂肪酸钾与蓖麻油酸钾的浓度与表面张力关系曲线图。

图6 水解聚合环氧大豆油脂肪酸钾盐与蓖麻油酸钾在pH=9条件下的γ-c曲线
表面活性剂在低浓度时,溶液中的浓度越高,溶液表面的浓度也越高,表面张力下降。直至溶液表面被表面活性剂分子完全覆盖,表面张力值达到最小值。继续增加表面活性剂的浓度,溶液表面的浓度也不会改变,表面张力值也不再下降。如图6所示,平衡表面张力随着表面活性剂浓度的逐渐增加而降低,然后趋于平缓,达到一定的浓度后基本恒定。达到最小平衡表面张力所对应的第一个浓度被定义为临界胶束浓度(cmc)[10-12],所对应的最低表面张力为γcmc值。评价表面活性剂表面张力降低能力有两种方法,一种是利用表面活性剂效率,另一种则为表面活性剂的有效值[13]。在pH=9的条件下,HPESO-K-2的cmc值为0.41g/L,γcmc值为25.69mN/m;蓖麻油酸钾的cmc值为1.07g/L,γcmc值为35.2mN/m。环氧大豆油经过聚合与水解反应之后,分子结构中存在多个亲水与亲油基团,而单个脂肪酸钾盐中只存在一对亲水基与亲油基,两者相比,HPESO-K更易于在水溶液表面定向紧密排列,因此cmc值从1.07g/L下降至0.41g/L,明显提高了表面活性剂的效率。对比HPESO-K与蓖麻油酸钾的γcmc值表明,所制备的水解聚合环氧大豆油脂肪酸钾盐比单个的脂肪酸钾盐具有更强降低表面张力的能力,表面活性剂有效值显著增加。
将不同pH值条件下聚合植物油脂表面活性剂的cmc与γcmc进行对比,如表2所示。

表2 不同pH值对聚合植物油脂表面活性剂cmc值与γcmc值的影响
由表2可知,聚合植物油脂表面活性剂的cmc值随着水溶液pH值的升高而下降,γcmc值随着水溶液pH值的升高而升高。随着pH值的升高,水解聚合环氧大豆油脂肪酸中的羧酸根离子与钾正离子结合,亲水基团的量增多,使得表面活性剂形成胶束所需要的量减少,故cmc值下降[13]。在表面活性剂的分子结构中,与水分子相互排斥的非极性憎水基的部分愈大,憎水性就愈强,表面活性剂的分子也就愈聚集于表面,从而表面活性就愈强[14]。表面活性剂分子亲水基团在水溶液中以阴离子形式存在,在溶液表面排列时,随着pH值的升高,溶液中存在的亲水基团增多,而憎水基团减小,表面活性下降,故γcmc值升高。同时随着pH值的升高,电荷之间的排斥作用增大,降低了表面排列分子之间的紧密程度,降低了表面活性,γcmc值升高[15]。
2.5.2 KP、EP、FP和HLB值的测定
聚合植物油脂表面活性剂水溶液在25℃和pH=9的条件下,测定了HPESO-K-2的Krafft点、乳化性能、泡沫性能和HLB值。实验结果见表3。
Krafft点是离子型表面活性剂的重要性质之一,反映了离子型表面活性剂在水溶液中的亲水性与溶解性。在温度高于Krafft点时,表面活性剂才能更大程度的发挥其作用[5]。由表3可知,HPESO-K-2产品水溶液在25℃和pH值为9的条件下,Krafft点为37℃。结果表明,制备得到的聚合植物油脂表面活性剂具有良好的亲水性,Krafft点相对较低,符合表面活性剂使用要求。液体石蜡/水体系中分出10mL水的时间为130s,初始泡沫高度与5min后的泡沫高度分别为78mm与71mm。表明聚合植物油脂表面活性剂对液体石蜡/水体系的乳化能力较差,但其自身起泡性与稳泡性强。任何表面活性剂分子的结构中,既含有亲水基也含有亲油基,HLB值即亲水亲油平衡值,是衡量表面活性剂在溶液中性质的一个定量指标,是表明表面活性剂亲水能力的一个重要参数。聚合植物油脂表面活性剂的HLB值范围为10~11。

表3 聚合植物油脂表面活性剂的表面性能
3 结 论
(1)以环氧大豆油为原料,乙酸乙酯为溶剂,四氯化锡为催化剂,通过开环自聚反应得到聚合环氧大豆油,并将其在碱性条件下水解,洗涤纯化后得到了水解聚合环氧大豆油。
(2)通过FTIR、1H NMR和GPC对该聚合植物油脂表面活性剂的结构与分子量分布进行了表征,结果发现通过3种不同浓度聚合水解得到的聚合热植物油脂表面活性剂具有相似的分子量分布,说明以SnCl4为催化剂,环氧大豆油的反应浓度在一定范围内,其自聚合的程度是一定的。
(3)对聚合植物油脂表面活性剂在不同pH值条件下的临界胶束浓度cmc及其表面张力(γcmc)、Krafft点、对液体石蜡/水体系的乳化能力、抑泡及消泡能力进行了研究。结果表明:在水溶液pH值为9~12条件下,HPESO-K-2的cmc值为0.13~0.41g/L,γcmc值为25.6~31.2mN/m。在水溶液pH值为9条件下测得HPESO-K-2的Krafft点为37℃,液体石蜡/水体系中分出10mL水的时间为130s,HLB值范围为10~11,具有较强的泡沫稳定性。
参 考 文 献
[1] VORONOVB S,KOHUTB A,TARNAVCHYK I,et al. Advances in reactive polymeric surfactants for interface modification[J]. Current Opinion in Colloid & Interface Science,2014,19(2):95-121.
[2] LIU S Y,STEVEN P A. Recent advances in the synthesis of polymeric surfactants[J]. Current Opinion in Colloid & Interface Science,2001,6(3):249-256.
[3] PARK S J,JIN F L,LEE J R. Effect of biodegradable epoxidized castor oil on physicochemical and mechanical properties of epoxy resins[J]. Macromolecular Chemistry and Physics,2004,205(15):2048-2054.
[4] 彭子浓,岑美娇,陆建雄,等. 新型油脂基高分子表面活性剂的研究进展[J]. 广州化工,2011,39(23):9-10.
[5] WANG X G,YAN F,LI Z Q,et al. Synthesis and surface properties of several nonionic-anionic surfactants with straight chain alkyl-benzyl hydrophobic group[J]. Colloid and Surface A,2007,302:532-539.
[6] JIA W H,RAO X P,SONG Z Q,et al. Microwave-assisted synthesis and properties of a novel cationic gemini surfactant with the hydrophenanthrene structure[J]. Journal of Surfactants and Detergents,2009,12:261-267.
[7] WEGE H A, KIM S, PAUNOV V N,et al. Long-term stabilization of foams and emulsions with in-situ formed microparticles from hydrophobic cellulose[J]. Langmuir,2008,24:9245-9253.
[8] LIU W R,SUN D J,LI C F,et al. Formation and stability of paraffin oil-in-water nano-emulsions prepared by the emulsion inversion point method[J]. Journal of Colloid and Interface Science,2006,303:557-563.
[9] 潘祖仁. 高分子化学(增强版)[M]. 北京:化学工业出版社,2007:219-228.
[10] 郭珊珊,杨欠欠,袁圆,等. 双头基表面活性剂的合成、表征及其性能[J]. 化工进展,2014,33(9):2455-2458.
[11] INOUE T,YAMAKAWA H. Micelle formation of nonionic surfactants in a room temperature ionic liquid,1-butyl-3-methylimidazolium tetrafluoroborate:surfactant chain length dependence of the critical micelle concentration[J]. Journal of Colloid and Interface Science,2011,356:798-802.
[12] SLAVCHOV R I,GEORGIEV G S. Markov chain model for the critical micelle concentration of surfactant mixtures[J]. Colloid & Polymer Science,2014,292:2927-2937.
[13] CHANG C H,ELIAS I F. Adsorption dynamics of surfactants at the air/water interface:a critical review of mathematical models,data,and mechanisms[J]. Colloids and Surfaces A(Physicochemical and Engineering Aspects),1995,100(25):1-45.
[14] 金谷. 表面活性剂化学[M]. 2版. 合肥:中国科学技术大学出版社,2013:11-12.
[15] LEVITT D,JACKSON A,HEINSON C,et al. Identification and evaluation of high-performance EOR surfactants[J]. SPE Reservoir Evaluation and Engineering,2009,12(2):243-253.
研究开发
Synthesis,structure and properties of polymerized vegetable oils-based surfactants
HUANG Xujuan1,LIU He1,WANG Lei2,SHANG Shibin1
(1Institute of Chemical Industry of Forest Products,CAF;National Engineering Lab for Biomass Chemical Utilization;Key and Open Lab of Forest Chemical Engineering,SFA;Key Lab of Biomass Energy and Material,Jiangsu Province,Nanjing 210042,Jiangsu,China;2Chemical Engineering College,Nanjing Forestry University,Jiangsu Province,Nanjing 210042,Jiangsu,China)
Abstract:Polymerized epoxidized soybean oil (PESO) was firstly prepared through the ring-opening polymerization of epoxidized soybean oil in ethyl acetate using SnCl4as catalyst. The hydrolyzed PESO (HPESO) was obtained via the hydrolyzation of PESO under alkaline condition after purification. The structure of HPESO was characterized by FTIR and1H NMR. The molecular weight of HPESO was obtained by GPC. The critical micelle concentrations (cmc),the surface tensions corresponding to cmc (γcmc),the Krafft point (KP),the emulsification properties (EP),and the foam proterties (FP) of the K+counterion of HPESO (HPESO-K) were investigated. The Mnof HPESO ranged from 1056g/mol tobook=576,ebook=2411156g/mol and the Mwof HPESO ranged from 1255g/mol to 1374g/mol. Through varying the pH of HPECO-K aqueous solution from 9 to 11,the cmc of HPESO-K surfactant ranged from 0.13g/L to 0.41g/L and the γcmcof HPECO-K ranged from 25.6mN/m to 31.2mN/m,respectively. The KP of HPECO-K was 37℃ when the pH of HPECO-K solution was 9. When the surfactant was used as emulsifier,the time for 10mL water separated from the turpentine/water emulsion was 130s. The hydrophile lipophile balance (HLB) of HPECO-K was in the range of 10—11.
Key words:epoxidized soybean oil;polymerization;hydrolysis;molecular weight distribution;surfactants
基金项目:江苏省自然科学基金青年基金(BK2012063)、中央级公益性科研院所基本科研业务费专项资金(CAFINT2012C05)及国家自然科学基金青年基金(31200446)项目。
收稿日期:2015-05-21;修改稿日期:2015-08-17。
DOI:10.16085/j.issn.1000-6613.2016.02.037
中图分类号:TQ 423.11
文献标志码:A
文章编号:1000–6613(2016)02–0575–06
