拓展光催化材料光谱响应的研究进展
2016-02-26马晓娟黄柏标
荆 涛,戴 瑛,马晓娟,黄柏标
(山东大学 物理学院 晶体材料国家重点实验室,山东 济南 250100)
拓展光催化材料光谱响应的研究进展
荆涛,戴瑛*,马晓娟,黄柏标
(山东大学 物理学院 晶体材料国家重点实验室,山东 济南 250100)
摘要:光催化技术在解决能源短缺和环境污染问题方面有重要的应用前景,引起了人们的广泛关注。宽光谱响应和高量子效率是实现光催化材料大规模应用的前提。本文介绍了近年来紫外、可见和近红外光催化方面的最新进展,阐述了拓展光响应范围和促进载流子分离的有效途径,总结了光催化材料发展所面临的问题,并对其发展趋势进行了展望。
关键词:光催化;载流子分离;能带调控;氧化还原反应
1引言
石油、煤和天然气等化石燃料是当前世界使用的最主要能源。然而,化石燃料不仅是非可再生能源,不能满足人类发展的长期需求,而且其使用过程中产生废水、废气和废渣等有害物质,对环境造成极大污染。因此,寻找洁净的、可再生的新能源成为关系人类生存和可持续发展的重大课题。光催化技术不仅可以通过半导体材料直接将太阳能转化为易储存的化学能,如分解水产氢和还原二氧化碳等,而且能对环境中有机污染物实现完全矿化降解,被认为是解决能源短缺和环境污染问题最有效途径之一[1]。
半导体光催化过程通常分为3个主要阶段:(1)光催化材料吸收大于能带隙的光子产生电子-空穴对;(2)光生电子-空穴对发生分离,并迁移到半导体的表面;(3)迁移到表面的光生电子和空穴分别与吸附物发生氧化还原反应[2]。目前,光催化技术已经被应用到杀菌、处理污水和净化室内空气等方面,但很多光催化材料的太阳能转换效率仍然很低,无法实现大规模应用。这是由于TiO2、ZnO等传统光催化材料的带隙较宽(3.2 eV),只对占太阳能很小一部分(4%)的紫外光响应,而占太阳能53%比例的可见光和43%比例的近红外光却得不到有效的利用[3]。另一原因是量子效率低,有相当大比例的光生载流子在半导体的体内或者表面发生复合,以发光和发热的形式散发掉,这部分能量没有得到有效利用。
近几十年,国内外学者在拓展光催化材料的光响应范围和提高量子效率方面开展了广泛的研究,取得了巨大的进展。研究发现:金属(非金属)掺杂、固溶体、染料敏化和等离子体光催化等不同的方法可以提高光催化材料的性能。然而,半导体带隙变窄的同时其氧化还原能力也下降,从而光催化性能降低。如何在保持宽光谱响应的同时实现载流子有效分离成为近些年研究的重点和热点。另外,近些年的研究主要集中在将光响应从紫外光拓展到可见光范围,很少关注近红外光响应催化。具有近红外区域光响应的光催化研究报道甚少。因此,拓展近红外光响应材料的研究同样对提高太阳能利用率具有重要意义。本文将从紫外、可见和近红外光响应这几个方面,概述近些年来拓展光催化材料光响应范围和提高光催化效率方面的进展。
2紫外光光催化材料的研究进展
自从Fujishima和Honda发现了TiO2具有光催化分解水产氢性能后[4],大量研究集中在这一领域。但目前光催化材料的量子效率非常低 (一般低于10%),限制了其实际应用。这是因为大部分载流子在半导体的体内或者表面发生复合,从而大大降低了太阳能利用效率。因此,人们采用不同的方法对半导体光催化材料进行改性,如引入本征缺陷和掺杂;采用微结构调控手段制备高结晶度、大比表面积、高活性面暴露的光催化材料;在半导体表面沉积助催化剂;与其它半导体形成异质结等措施来抑制载流子复合,提高光催化材料的量子效率。
2.1 合成纳米粒子
由于独特的物理化学性质,光催化材料的纳米化近年来成为一个异常活跃的研究领域。纳米光催化材料的粒子尺寸一般低于100 nm,有些甚至在10 nm以内。相对于微米尺寸的材料,纳米粒子具有比表面积大,活性位点多和载流子迁移距离短等优势,这些都是光催化过程的有利因素。最近,研究者已合成多种形貌的纳米结构,如纳米线、纳米带、纳米盘、纳米管、立方结构、八面体结构、介孔结构、微球结构等[5-10]。这些纳米结构具有更大的比表面积和更多的活性位点,有利于促进光生载流子的分离和提高光催化活性。
2.2 沉积助催化剂
半导体光催化材料表面沉积助催化剂是提高其光催化活性的一种有效方法。这是因为,在助催化剂和半导体之间形成合适的异质结能够促进载流子在界面处的分离和提高总体的光催化效率。一方面,通过在半导体表面沉积Ru、Pt、Au和Ag等贵金属纳米粒子可以提高其光催化活性[11-16]。金属的费米能级一般低于半导体,由于它们之间的接触导致界面处形成肖特基势垒,使得金属成为电子的捕获中心。另一方面,一般贵金属纳米粒子具备比半导体光催化材料更小的过电位,能够降低反应动力学势垒而有利于反应过程。因此,贵金属纳米粒子能够成为还原H2或者CO2的活性位点。 Dai等人采用第一性原理密度泛函方法研究了半导体沉积Ag、Au、Pt和Cu等金属纳米团簇,发现半导体表面吸附这些金属团簇在界面处有偶极层形成,导致金属功函数的改变,这将促进光生载流子的分离[17-20]。
除了金属纳米粒子,金属氧化物如RuO2和IrO2等也被用作助催化剂以提高光催化材料的性能[21-22]。类似于金属纳米粒子,金属氧化物助催化剂和半导体间的电荷转移能够在界面处形成内建电场,驱动载流子的分离。而且这些过渡金属氧化物也能够降低氧化反应的过电位,提供氧化O2-离子的活性位点。由于金属氧化物助催化剂能够捕获光生空穴,沉积这类助催化剂能够明显提高金属硫化物和氮化物光催化材料的光稳定性。然而,贵金属元素在地球的储存量小,寻找可替代的、地球储量丰富的助催化材料成为这一领域的研究热点。最近,有研究将Co和Ni等用作光催化析氢反应的助催化剂[23-24],而将过渡金属氧化物如CoOx、NiOx和MnOx等用作析氧反应的助催化剂[25-26]。这些廉价的助催化剂具有接近甚至超过贵金属或贵金属氧化物的光催化性能。
碳基材料如石墨烯,碳纳米管等也被用作半导体光催化材料的助催化剂。石墨烯为二维单层材料,具有高的导电性,优良的电子迁移能力和大的比表面积等特性,具有较大的功函数(4.42 eV),还原势比还原氢的电位更低(-0.08 vs 0.0 eV),能够接受半导体导带上的电子[27]。因此被认为是一种高效、廉价的助催化剂,能够促进载流子的分离和提高光催化活性。例如,Yu课题组报道了一种TiO2/MoS2/graphene复合体系,能够大大提高TiO2的产氢性能,其高活性被归结于石墨烯的电子收集作用和提供高活性的吸附位点[28]。Huang等人通过水热方法制备了graphene/TiO2纳米复合体系,通过调控反应材料和反应时间来控制纳米粒子不同表面的暴露,相对于P25具有明显更高的光催化活性[29]。
2.3 半导体-半导体异质结
利用传统的半导体光催化材料与其它半导体形成异质结,也可提高载流子的分离效率和光催化活性。如果两种半导体带边相匹配,可以形成Ⅱ型异质结,光生电子从导带位置较高的半导体向导带位置较低的半导体转移,而光生空穴从价带位置较低的半导体向价带位置较高的半导体转移。同时,半导体之间的电荷转移可以在它们的界面处形成内建电场,从而抑制光生载流子的复合。近些年来,人们合成和表征了大量复合体系的光催化材料,表明异质结能够用来分离光生载流子和提高光催化活性[30-36]。
2.4 高活性的紫外光催化材料
影响光催化活性的重要因素之一是光生载流子的复合率。因此,减小载流子复合、提高分离效率是提高光催化活性的一个重要途径。内建电场广泛应用于半导体器件方面,例如,在半导体之间形成P-N结能够用来控制电子和空穴的迁移。基于这一思想,如果光催化材料的本身就具有剩余偶极矩,将在半导体的内部产生一个极化电场,而极化电场能够驱动光生电子和光生空穴沿着相反的方向迁移,从而提高其分离效率。最近,Huang课题组通过简单的水热方法合成了BiOIO3纳米盘,能够在紫外光照下10 min对甲基橙(MO)实现完全矿化降解[37]。图1给出了载流子沿内建电场迁移的示意图,BiOIO3由包含孤对电子的Bi3+和I5+阳离子的BiO6六角结构和IO3三角锥体所构成。由于BiO6单元局部的偶极矩被相互抵消,而IO3三角锥的偶极矩却相互叠加,形成了沿着c轴方向的剩余偶极矩。光生电子和空穴在极化电场的作用下沿相反的方向迁移,这将极大的提高光催化活性。其它具有极性的体系如Bi2O2[BO2(OH)]纳米面[38],K3B6O10Br[39]也被发现具有很高的紫外光光催化活性。Dai课题组的理论研究发现,K3B6O10X(X=Br,Cl)体系沿着[001]方向空穴有效质量最小,沿着这一方向存在极化电场,内建电场与载流子的迁移性质形成协同作用,从而可以增加载流子的分离效率[40]。虽然这类包含内部极性的光催化材料具有很好的光催化活性,但它们带隙一般较大,而且在材料合成中难以实现纳米化。因此,拓展光响应范围,合成纳米尺度的光催化材料,是进一步提高这类材料光催化活性的有效途径。

图1 BiOIO3中光生载流子在内建电场作用下迁移的示意图,沿着c轴方向的箭头表示极化电场的方向(来自文献[37])Fig.1 Schematic diagram of the transfer of charge carriers under the build-in electric field of BiOIO3. The electric field direction is along the c axis. Reproduced from Ref. [37] with permission. Copyright 2013 Wiley Online Library
3可见光催化材料
3.1 传统光催化材料的改性
3.1.1金属、非金属掺杂
传统的光催化材料如TiO2和ZnO等具有宽的本征带隙,只具有紫外光催化活性,而占有太阳能很大比例的可见光和近红外光得不到有效利用。通过能带结构调控减小带隙是拓展光响应范围的有效途径之一。一种办法是在半导体材料如TiO2中掺入Fe3+、Cr3+、Ru3+和V5+等金属离子[41-44]。由于离子半径接近,这些金属离子可替代TiO2中的Ti4+离子。 掺杂金属离子可引入杂质能级,使TiO2具有可见光吸收。虽然金属离子掺杂能够将光响应拓展到可见光范围,但其可见光催化活性仍然很低。主要是因为金属掺杂的浓度很低(一般小于1.5%),且掺杂通常在导带底附近引入局域的杂质能级,会降低体系的还原能力,同时还容易成为载流子的复合中心。因此,自从Asahi等人报道了N掺杂的TiO2能够在可见光下降解有机物,人们相继开展了系列非金属掺杂如C、S、B、P和F等的光催化性能调控及其机理等研究[45-48]。早些时候,在非金属掺杂拓展可见光吸收机理存在较大争议。例如Asahi等人认为是掺杂N的2p轨道与O的2p轨道杂化导致TiO2的带隙变窄[45],从而引起可见光吸收。而Irie等认为是N掺杂在TiO2的带隙中引入了孤立的杂质能级[49]。为了研究掺杂引起TiO2可见光吸收的机理,Dai课题组借助第一性原理计算开展了系列的N、P、S、C、B、Cl等掺杂TiO2的相关研究,发现非金属掺杂的TiO2受掺杂原子的位置、掺杂浓度和掺杂元素化学势等诸多因素的影响,从而导致了实验上不同的观测结果[50-55]。另外,最近N高浓度掺杂TiO2实验发现的一些新物理化学性质[56]和理论研究表明[57],N以Ti-N-Ti链方式掺杂可以更有效的改善光催化材料的性能。 传统的杂质原子间距最大化的掺杂方式中,杂质之间的耦合非常弱,仅仅在带隙中引入局域的杂质态,导致量子效率低。而Ti-N-Ti链掺杂方式的电子耦合不仅可以通过价带的上移减小TiO2带隙,同时还增加了空穴的迁移能力和降低载流子的复合率。
3.1.2固溶体结构
减小半导体的带隙可以通过降低导带,提升价带,或者在降低导带的同时提升价带位置来实现。然而,这样的调控同时也会降低光催化材料的氧化还原能力。因此,需要有效调控半导体的带隙和带边位置,固溶体方法是满足这一需求的途径之一。例如,Domen课题组2005年制备了(ZnO)x(GaN)1-x固溶体光催化材料[58],能够在可见光下完全分解水。其导带底主要由Ga的4s和4p态贡献,而价带顶主要由N2p和Zn3d态贡献,p-d态的杂化导致了其带隙的减小。Huang课题组通过层状双金属氢氧化物为前驱体制备了富Zn的(ZnO)x(GaN)1-x固溶体[59-60]。如图2所示,光吸收相对于纯的ZnO和GaN有明显的红移,而且带隙可以通过改变Zn组分进行连续调控。化学计量模型理论表明该体系N 2p和Zn 3d态之间存在的p-d强耦合能够引起带隙变窄,而且O原子的位置也对固溶体的带隙有明显的影响[61]。与(ZnO)x(GaN)1-x固溶体不同的是,Cd1-xZnxS(0 图2 (ZnO)x(GaN)1-x固溶体随着Zn浓度变化的光吸收谱和带隙(来自文献[59])Fig.2 Light absorption spectra and band gap of (ZnO)x(GaN)1-xsolid solution with the change of Zn concentration. Reproduced from Ref. [59] with permission. Copyright 2011 Royal Society of Chemistry 3.1.3窄带隙半导体和染料的敏化 窄带隙的半导体或者有机染料分子等可以作为可见光敏化剂,与宽带隙的半导体复合可以拓展光催化材料的可见光响应范围,且载流子能够在界面处发生很好的分离。例如,Ru基染料被广泛用于和过渡金属氧化物半导体形成异质结分解水产氧。这种催化材料具有很好的光吸收能力,在可见光照射下具有高的光催化活性[63]。但这种光催化材料也存在一些不足,例如在光催化过程中,氧物种如(O2)-1能够和光敏化剂发生反应,而导致敏化剂被解离。 3.1.4等离子体光催化材料 图3 AgCl、Ag-AgCl和N-TiO2的紫外-可见漫反射谱;Ag-AgCl和N-TiO2在可见光照下降解MO(来自文献[67])Fig.3 UV/Vis diffuse-reflectance spectra of AgCl, Ag-AgCl, and N-TiO2. Photo decomposition of MO dye in solution over Ag-AgCl and N-doped TiO2under visible-light irradiation. Reproduced from Ref. [67] with permission. Copyright 2008 Wiley Online Library 由于表面等离共振(SPR)效应,贵金属纳米粒子(Ag,Au,Pt)具有很强的可见光吸收能力,能够与半导体复合形成表面等离子体光催化材料。通常,等离子光催化过程可描述为金属纳米粒子在吸收光后其表面发生等离共振,随后等离子体发生衰减,把聚集的能量转移到半导体材料的导带。这个过程产生的高能电子(热电子),逃离贵金属纳米粒子而被与其接触的半导体收集,从而形成金属-半导体肖特基接触。目前实验上已合成和表征了许多具有可见光活性的等离子体光催化材料,如Ag-TiO2、Au-TiO2和Au-CeO2等离子体光催化体系[64-66]。众所周知,卤化银在吸收光子之后产生的电子易被Ag+所捕获,从而将其还原为Ag原子,因此在光照下极不稳定。然而,Huang课题组发现制备的Ag-AgCl体系却具有稳定、高效的可见光等离子体光催化性能,随后制备研究了一系列Ag-AgX(X=Cl, Br, I)等离子体光催化体系[67-75]。这一发现引发了人们对该体系光催化性能研究的热潮,为开发新型光催化材料提供了一条新的途径。研究认为,由于Ag纳米粒子与AgX之间的良好接触,促使光生载流子在界面处发生有效分离,同时沉积在AgX上Ag纳米粒子的表面等离共振效应使该材料在宽可见光区域显示出稳定、很强的光催化活性。图3为Ag-AgCl的光吸收谱和有机物降解的实验结果,显示了可见光降解MO的效率为N-TiO2的8倍,以及该体系很好的稳定性[67]。进一步的实验和理论研究表明等离子光催化材料的尺寸和形貌对其光催化性能具有很大影响,因此人们又进一步研究了各种形貌的等离子体光催化材料,包括立方、纳米球和纳米线等结构,使得其光催化性能得到进一步提高[75-81]。Dai课题组的理论研究发现AgCl空穴有效质量的大小明显依赖于迁移方向,而Ag的4d轨道在晶体场中的劈裂是导致AgCl空穴有效质量大和迁移能力低的原因,研究结果很好地解释了Ag-AgCl体系的光催化活性依赖于纳米粒子形貌的性质[82]。通过对Ag-AgCl体系能量转移机理的研究发现,Ag纳米粒子到AgCl的能量转移需要通过AgCl半导体的带隙中引入杂质态实现,表面等离共振效应能极大增强杂质态参与的光跃迁几率[83]。最近的实验发现,直接沉积Au纳米粒子到TiO2表面的光催化活性要好于光还原方法制备的Au-TiO2[84]。理论研究表明这是由于Au-TiO2等离子光催化体系氧空位能够增加热电子的迁移势垒和拓展空间电荷区,降低热电子注入效率。因此,理论建议在沉积金属纳米粒子之前,对半导体表面合适处理有利于提高热电子注入效率和光催化活性[85]。 3.2.1硫(氧)化物和氮(氧)化物 传统的光催化材料如TiO2由于本征带隙宽只能吸收紫外光,太阳能利用率低。能带结构显示其价带位置较水的氧化电位偏低。因此,通过改变阴离子提升价带位置实现带隙减小,以拓展光响应范围成为提高光催化效率的途径之一。金属硫属化合物光催化材料CdX(X=S,Se,Te)是这种策略的典型例子。 氮(氧)化物Ta3N5、TaON、LaTiO2N等也有大量的研究[86-88],它们的带隙大多处于1.6~2.4 eV范围内,而且它们之中的一部分被发现具有分解水的能力。Ta3N5为其中研究较多的一种光催化材料,带隙约为2.1 eV,导带和价带位置正好跨越水的氧化还原电位。Ta3N5一般由Ta的氧化物Ta2O5在高温NH3气下还原得到,理论上说在无偏压的情况下能够分解水。Luo等人[89]研究发现Ta3N5的角质层为一个包含Ta空位和O杂质的表面钝化层,作为载流子的复合中心而降低光催化活性。当这个角质层被剥离,Ta3N5的光电流能够极大提升,负载上Co(OH)x其光电流在1.23 VRHE下可达5.5 mA/cm2。第一性原理研究表明Ta3N5的n-型导电主要由O替位三配位的N所贡献,而碱金属掺杂能够进一步提高其n-型导电性和减小带隙[90]。但是,由于S和N具有比O更高的能级,在产氧的过程中其自身先于O2-氧化。因此,硫化物和氮化物都不大稳定,容易在光照下发生解离。 3.2.2Bi-基光催化材料 Bi-基材料如Bi2O3、BiVO4、Bi2MoO6和Bi2WO6等一般具有可见光响应,而且具有储量丰富,无毒、耐光腐蚀等优点。其中Kudo等人[91]首先合成的单斜晶系白钨矿BiVO4光催化材料被认为是一种很有前景的光解水材料,其带隙约为2.3~2.4 eV。由于载流子在其体内和表面的复合率很高导致低的光催化效率,人们采用不同方法来提高其光催化活性。Luo等人报道Mo6+和W6+掺杂能够使BiVO4在可见光下量子效率显著提高[92]。这类n-型掺杂能够使光催化活性提高的原因是载流子浓度的增加降低了BiVO4的电阻,使载流子更容易向其表面迁移。另外在BiVO4的表面沉积助催化剂也能进一步提高光催化活性。例如双层助催化剂FeOOH/NiOOH被发现能够大大提高BiVO4的光催化活性。NiOOH相对于FeOOH具有更好电催化氧化水的活性,而FeOOH能够与BiVO4形成更好的界面接触。因此,BiVO4/FeOOH/NiOOH连接能够使这些优势之间发生协同,使光催化分解水的效率得以提高[93]。 3.2.3单层碳氮化合物 2009年。Wang等人[94]发现石墨烯相氮化碳(g-C3N4) 的光催化性能,该体系引起了人们极大的研究兴趣。g-C3N4为二维框架结构,具有比表面积大,热稳定性及化学稳定性好等特性。它可以通过热凝聚单、双氰胺和三聚氰胺等前驱体获得,较小的带隙(2.7 eV)使其能够在可见光下分解水。然而,g-C3N4高的载流子复合率导致其光催化活性很低。为提高其光催化活性,人们采用了多种方法和途径如形貌调控、掺杂和构造异质节等。Zhang等人采用模板方法合成了有序介孔的g-C3N4,其表面积达到517 m2/g,在455 nm的光照下产氢的量子效率为6.77%[95]。Hong等人通过在二氧化硅颗粒存在的情况下热分解硫脲合成了S掺杂的介孔g-C3N4。S替位C使其带隙减小为2.61 eV,在440 nm光照下量子效率达到5.8%,相对于纯的g-C3N4,其活性提高了30倍[96]。Yu等人将CdS量子点沉积在g-C3N4纳米面制备了CdS/g-C3N4核/壳纳米线结构。g-C3N4和CdS形成合适的异质结构能够有效促进CdS的光空穴转移到g-C3N4,使光生电荷有效分离,这样可以提高光催化活性的同时增强体系的光稳定性[97]。 3.2.4新奇的可见光催化材料 Ye课题组新近发现的Ag3PO4间接带隙和直接带隙分别为2.43 eV和2.60 eV[98],在可见光下具有强的氧化能力,能够降解有机物和氧化水产氧,量子效率能达到90%。Bi等人采用化学沉淀法合成了(110)和(100)面暴露的单晶菱形十二面体的Ag3PO4,在降解有机物时比立方结构具有更高的活性[99]。这说明增加其高活性面暴露的比例,光催化活性可以得到提高。Umezawa等人的电子结构理论研究,认为Ag3PO4具有高光催化活性是由于坚固的PO4四面体单元增强了Ag+和(PO4)3-之间的离子键特征,从而使得Ag-O之间的共价键特征减弱,使Ag的d轨道与O的p轨道之间的杂化可以忽略,价带主要由占据的Ag的d轨道所贡献,导带主要由Ag的s态贡献。相邻Ag离子s态之间的强杂化导致Ag3PO4导带底非常离域,具有好的电子迁移能力和高的光催化活性[100]。 硅酸盐材料在自然界中储量丰富,被广泛用作工业催化剂。最近,Huang 课题组通过在AgNO3溶液中加入Na2SiO3制备了高活性光催化材料Ag6Si2O7。由于过渡金属阳离子的存在,SiO4四面体很容易扭曲而产生极化,二、三和四配位的银离子形成了AgO2、AgO3和AgO4单元。光吸收谱的测试表明,Ag6Si2O7的光响应几乎遍及整个可见光区域(<740 nm)[101]。理论研究发现,Ag6Si2O7有一个沿着c轴方向的内建电场,内建电场与不同配位阳离子之间的电荷转移的协同效应导致光生载流子更有效的分离使其具有很好的光催化活性。另外,通过一步共沉淀法制备的一系列无定型硅酸银,其能带结构可以通过改变硅离子的组分实现调控,在Ag/Si计量比值为3.2时具有最高的光催化活性[102]。此外,他们通过反应通量法制备的另一种硅酸银半导体Ag9(SiO4)2NO3,由于其极性晶体结构特征,光生载流子能够在内建电场作用下发生分离,使Ag9(SiO4)2NO3在可见光下降解有机物具有非常好的光催化活性[103]。 图4 CaGe2在HCl溶液中转化为GeH的示意图(来自文献[104])Fig.4 Schematic illustration of crystal structure transition of CaGe2to GeH in concentrated HCl. Reproduced from Ref. [104] with permission. Copyright 2014 Royal Society of Chemistry Huang 课题组以CaGe2为前驱体,通过离子交换法合成了二维材料GeH,在可见光(>420 nm)照射下能够分解水产氢和降解有机污染物。如图4所示,CaGe2中的Ca2+离子被HCl溶液中的H1+离子所取代,合成了层状的GeH[104]。紫外-可见-近红外漫反射谱表明制备的GeH在可见光范围具有强的光吸收,其带隙约为1.58 eV。理论研究表明,考虑电子-电子自能作用的GeH 带隙约为2.37 eV,大于实验测得的光学带隙,而考虑激子效应计算得到的结果与该实验值符合的很好,说明该二维体系中存在显著的激子效应[105]。当GeH与石墨烯构成GeH/graphene双层异质结构时,复合体系的界面处发生强的电荷转移,导致界面处形成肖特基势垒,有利于光生载流子的分离和其光催化性能的改进[106]。 4近红外和全光谱光催化材料 在过去的近十年中,人们的研究主要集中在拓展光催化材料的可见光响应范围,对近红外光响应光催化材料的研究很少。近红外光约占太阳光能的43%,开发近红外光响应光催化材料,对提高太阳能利用率具有重要意义。 虽然有些半导体能够吸收近红外光,但是由于近红外光的光子能量低和热效应强,大多数窄带隙半导体并不具有近红外光催化活性。上转换材料能够将近红外光转换为可见或者紫外光,一个直接的思路是将上转换材料和半导体光催化材料结合,转换近红外光为紫外或者可见光,让半导体在紫外或者可见光激发下发生光催化反应。上转换能够解决近红外光光子能量低的问题是因为需要两个或者更多的光子参与到这一过程,使发射波长比吸收波长更短,从而将宽带隙半导体价带上的电子激发到导带。例如,Qin等人报道了近红外光催化活性的Yb∶Tm∶YF3/TiO2球-壳纳米粒子,Yb和Tm共掺的YF3能够将近红外光转换为紫外光,将TiO2价带上的电子激发到导带,其在980 nm的光照射下出现了几个强的发射峰(291、347、362 nm),表明这种材料能将近红外光转换为紫外光[107]。另外,因为碳量子点具有水溶解度高,生物相容性高和无毒等优良的物理化学性质,也可以将其作为上转换材料。这一种材料能够将近红外光转化为可见光和紫外光,从而激发与之接触的半导体。它们具有接收和输运电子的性质,这使得碳量子点光催化剂在收获近红外光方面具有很大的应用前景[108-109]。目前,上转换材料仍然存在一些挑战,如光催化效率比一般的紫外或者可见光材料要低很多,而且与上转换相反的下转换同时存在,而下转换过程将会降低光催化活性。 最近,Huang课题组通过水热法制备了具有近红外光催化性能的材料 Cu2(OH)PO4[110]。这是迄今发现的第一个具有直接近红外光催化活性的光催化材料[111]。如图5所示,在近红外光照射下(<800 nm),该材料显示具有很宽的光吸收谱,拟合对应670、864、1 121和1 349 nm四个高斯峰,能量分别为1.85、1.44、1.11、0.92 eV。光催化测试表明,6 h后水溶液中2,4-DCP被降解了90%[110]。从晶体结构而言,正交相的Cu2(OH)PO4包含了CuO4(OH)三角双锥(TBP)和CuO4(OH)2八面体单元(OCT)两种配位的Cu2+离子,光生电子在这两种不同配位Cu离子之间的转移能够促进光生电子和空穴的分离,也是其具有近红外光催化活性的原因。如图5(c,d)所示,理论计算的Cu2(OH)PO4电子结构表明,对最低非占据的态贡献最大是TBP单元的铜原子,其次为OCT单元铜原子。连接两个Cu原子的桥氧(O)也对最低非占据态有明显的贡献,然而这些态在其它原子上的分布却很少。由于最高非占据态主要来自TBP单元的铜氧贡献,激发电子在弛豫过程中能够通过Cu(TBP)-O-Cu(OCT)通道发生转移。研究还表明,虽然两种不同配位的铜氧单元由于姜-泰勒效应发生扭曲,存在偶极矩,但Cu2(OH)PO4的净偶极矩为零,因此对载流子分离起主要作用的是不同配位的Cu离子之间的电荷转移[112]。随后制备的几种具有Cu-O-Cu单元的Cu基化合物Cu3(OH)4SO4、Cu4(OH)6SO4和Cu2(OH)3Cl表明,除了Cu2(OH)3Cl之外,Cu3(OH)4SO4和Cu4(OH)6SO4也均具有近红外光催化活性。导致这一差异的原因是Cu3(OH)4SO4和Cu4(OH)6SO4以及之前发现的Cu2(OH)PO4等都具有与CuOm多面体连接的受主基团(SO4,PO4),这些基团能够作为一个光生电子池,而使这些材料具有了近红外光催化活性,而Cu2(OH)3Cl不包含这样的受主基团[113]。 图5 Cu2(OH)PO4的紫外/可见/近红外吸收谱(a);近红外光照射下光催化降解2,4-DCP(0~6 h)(b); OH基中O原子的2p态(红色),八面体单元Cu的3d态(蓝色)和双三角锥单元Cu的3d态(绿色)的态密度(c);TBP-O-OC单元的部分电荷密度图(d)(来自文献[110])Fig.5 UV/Vis/NIR absorption spectrum of Cu2(OH)PO4(a); Photodegradation of 2,4-DCP with NIR irradiation(0-6 h)(b); The PDOS plots for the O 2p states of the OH groups(red), the Cu 3d states of the octahedral Cu sites(blue dots), and those of the trigonal bipyramidal Cu sites(green) (c); The band decomposed charge density for TBP-O-OCT (d). Reproduced from Ref. [110] with permission. Copyright 2013 Wiley Online Library Tian等人发现通过水热法合成了含氧空位的Bi2WO6-TiO2纳米带异质结具有全光谱的光催化活性[114]。研究认为,其近红外光催化活性主要来自于Bi2WO6纳米带,而紫外光催化活性主要来自于TiO2。由于Bi2WO6存在大量的W5+和Bi2+离子,因此推断对Bi2WO6近红外催化活性起主要贡献的是O空位。一方面,Bi2WO6和TiO2能够形成Ⅱ型异质结,有利于光生载流子在界面处的分离;另一方面,合成的纳米带结构具有大的表面积和更多的活性位点,有利于光催化反应的进行。随后的理论研究表明O空位的存在使得Bi2WO6带隙中存在杂质态,杂质态上的电子吸收近红外光跃迁到导带;而且杂质态非常的离域,空穴载流子具有很好的迁移能力。另外,Bi2WO6具有层状结构,电子和空穴能够在不同的层之间发生分离,也起到了抑制光生载流子复合和提高光催化活性的作用[115]。 5结束语 太阳能为洁净的可再生能源,是维持人类社会发展的理想能源。光催化技术的出现为实现利用太阳能这一梦想提供了一条重要途径。宽的光谱响应范围是实现高太阳能转换效率的前提。经过人们几十年的不懈努力,在拓展光响应范围和提高量子效率方面取得了巨大进展。但是从实际应用的角度来说,目前的光催化材料的太阳能利用效率仍然很低。这是因为,带隙的减小会使吸收的光子能量降低,而且同时减小其氧化还原能力,最终降低光催化材料的活性。最近报道的一些新型光催化材料,为拓展光谱响应和提高量子效率,最终实现光催化技术的应用提供了一些新的思路。如紫外光谱响应方面,BiOIO3能够利用内在的极化电场实现光生载流子的分离,从而提高光催化反应的量子效率和活性。在可见光谱响应方面,Ag3PO4中Ag离子s态之间的强耦合使光生电子具有很好的迁移能力,因此在可见光照射下具有非常高的量子效率。表面等离子体光催化材料如Ag-AgX(Cl,Br,I)等为人们提供了一种新的太阳能捕获和利用方式,不仅具有高的光吸收效率,而且光吸收范围可以通过改变贵金属纳米粒子的尺寸和形貌来调控。Ag6Si2O7的光谱响应几乎在遍及整个可见光范围,它能够利用自身的极性和不同配位阳离子之间电荷转移这两种方式的协同效应,提高载流子的分离效率和光催化活性。另外,拓展近红外光响应也是提高太阳能利用的重要途径, Cu2(OH)PO4近红外光催化材料的发现,使近红外光催化成为一个新的研究主题。尽管近红外光光子能量低和热效应明显,Cu2(OH)PO4能够利用不同配位的阳离子之间的电荷转移来实现载流子的有效分离。然而,商业应用对光催化材料的要求非常苛刻,保持宽的光谱响应的同时,还要满足高的量子效率、高稳定性,廉价和制备方法简便等要求。因此,要实现光催化材料的应用还需要人们付出更大的努力。 参考文献: [1]CHEN X,SHEN S,GUO L,etal.. Semiconductor-based photocatalytic hydrogen generation[J].ChemicalReviews,2010,110(11):6503-6570. [2]TONG H,OUYANG S,BI Y,etal.. Nano-photocatalytic materials:possibilities and challenges[J].AdvancedMaterials,2012,24(2):229-251. [3]HISATOMI T,KUBOTA J,DOMEN K. Recent advances in semiconductors for photocatalytic and photoelectrochemical water splitting[J].ChemicalSocietyReviews,2014,43(22):7520-7535. [4]FUJISHIMA A,HONDA K. Photolysis-decomposition of water at the surface of an irradiated semiconductor[J].Nature,1972,238(5385):37-38. [5]CHEN J S,TAN Y L,LI C M,etal.. Constructing hierarchical spheres from large ultrathin anatase TiO2nanosheets with nearly 100% exposed (001) facets for fast reversible lithium storage[J].J.AmericanChemicalSociety,2010,132(17):6124-6130. [6]WEN C Z,ZHOU J Z,JIANG H B,etal.. Synthesis of micro-sized titanium dioxide nanosheets wholly exposed with high-energy {001} and {100} facets[J].ChemicalCommunications,2011,47(15):4400-4402. [7]ZHU Y,DAI Y,LAI K,etal.. Synergistic Modification of Electronic and Photocatalytic Properties of TiO2Nanotubes by Implantation of Au and N Atoms[J].Chem.Phys.Chem.,2013,14(12):2800-2807. [8]WANG Z,HUANG B,DAI Y,etal.. Topotactic transformation of single-crystalline TiOF2nanocubes to ordered arranged 3D hierarchical TiO2nanoboxes[J].Cryst.Eng.Comm.,2012,14(14):4578-4581. [9]LI B,WANG Y. Facile synthesis and enhanced photocatalytic performance of flower-like ZnO hierarchical microstructures[J].TheJ.PhysicalChemistryC,2009,114(2):890-896. [10]HUANG W C,LYU L M,YANG Y C,etal.. Synthesis of Cu2O nanocrystals from cubic to rhombic dodecahedral structures and their comparative photocatalytic activity[J].J.AmericanChemicalSociety,2011,134(2):1261-1267. [11]HARA M,NUNOSHIGE J,TAKATA T,etal.. Unusual enhancement of H2evolution by Ru on TaON photocatalyst under visible light irradiation[J].ChemicalCommunications,2003(24):3000-3001. [12]MAEDA K,SAKAMOTO N,IKEDA T,etal.. Preparation of core shell-structured nanoparticles(with a noble-metal or metal oxide core and a chromia shell) and their application in water splitting by means of visible light[J].Chemistry-AEuropeanJournal,2010,16(26):7750-7759. [13]SAYED F N,JAYAKUMAR O D,SASIKALA R,etal.. Photochemical hydrogen generation using nitrogen-doped TiO2Pd nanoparticles:facile synthesis and effect of Ti3+incorporation[J].J.PhysicalChemistryC,2012,116(23):12462-12467. [14]LINGAMPALLI S R,GAUTAM U K,RAO C N R. Highly efficient photocatalytic hydrogen generation by solution-processed ZnO/Pt/CdS, ZnO/Pt/Cd1-xZnxS and ZnO/Pt/CdS1-xSexhybrid nanostructures[J].Energy&EnvironmentalScience,2013,6(12):3589-3594. [15]MURDOCH M,WATERHOUSE G I N,NADEEM M A,etal.. The effect of gold loading and particle size on photocatalytic hydrogen production from ethanol over Au/TiO2nanoparticles[J].NatureChemistry,2011,3(6):489-492. [16]AWAZU K,FUJIMAKI M,ROCKSTUHL C,etal.. A plasmonic photocatalyst consisting of silver nanoparticles embedded in titanium dioxide[J].J.AmericanChemicalSociety,2008,130(5):1676-1680. [17]WEI W,DAI Y,GUO M,etal.. Density functional theory study of Ag adsorption on SrTiO3(001) surface[J].J.PhysicalChemistryC,2010,114(24):10917-10921. [18]WEI W,DAI Y,GUO M,etal.. Au adsorption and Au-mediated charge transfer on the SrO-termination of SrTiO3(001) surface[J].AppliedSurfaceScience,2011,257(15):6607-6611. [19]WEI W,DAI Y,GUO M,etal.. Atomic Pt and molecular H2O adsorptions on SrTiO3with and without Nb-doping: Electron trapping center and mediating roles of Pt in charge transfer from semiconductor to water[J].J.SolidStateChemistry,2012,187:64-69. [20]WEI W,DAI Y,HUANG B. Role of Cu doping in SnO2sensing properties toward H2S[J].J.PhysicalChemistryC,2011,115(38):18597-18602. [21]SATO J,SAITO N,YAMADA Y,etal.. RuO2-loaded β-Ge3N4as a non-oxide photocatalyst for overall water splitting[J].J.AmericanChemicalSociety,2005,127(12):4150-4151. [22]MEEKINS B H,KAMAT P V. Role of water oxidation catalyst IrO2in shuttling photogenerated holes across TiO2interface[J].J.PhysicalChemistryLetters,2011,2(18):2304-2310. [23]AGEGNEHU A K,PAN C J,RICK J,etal.. Enhanced hydrogen generation by cocatalytic Ni and NiO nanoparticles loaded on graphene oxide sheets[J].J.MaterialsChemistry,2012,22(27):13849-13854. [24]TRAN P D,XI L,BATABYAL S K,etal.. Enhancing the photocatalytic efficiency of TiO2nanopowders for H2production by using non-noble transition metal co-catalysts[J].PhysicalChemistryChemicalPhysics,2012,14(33):11596-11599. [25]NODA Y,LEE B,DOMEN K,etal.. Synthesis of crystallized mesoporous tantalum oxide and its photocatalytic activity for overall water splitting under ultraviolet light irradiation[J].ChemistryofMaterials,2008,20(16):5361-5367. [26]LIU L,JI Z,ZOU W,etal.. In situ loading transition metal oxide clusters on TiO2nanosheets as co-catalysts for exceptional high photoactivity[J].AcsCatalysis,2013,3(9):2052-2061. [27]XIANG Q,YU J,JARONIEC M. Graphene-based semiconductor photocatalysts[J].ChemicalSocietyReviews,2012,41(2):782-796. [28]XIANG Q,YU J,JARONIEC M. Synergetic effect of MoS2and graphene as cocatalysts for enhanced photocatalytic H2production activity of TiO2nanoparticles[J].J.AmericanChemicalSociety,2012,134(15):6575-6578. [29]WANG Z,HUANG B,DAI Y,etal.. Crystal facets controlled synthesis of graphene@TiO2nanocomposites by a one-pot hydrothermal process[J].Cryst.Eng.Comm.,2012,14(5):1687-1692. [30]LIU Z,SUN D D,GUO P,etal.. An efficient bicomponent TiO2/SnO2nanofiber photocatalyst fabricated by electrospinning with a side-by-side dual spinneret method[J].NanoLetters,2007,7(4):1081-1085. [31]LONG M,CAI W,CAI J,etal.. Efficient photocatalytic degradation of phenol over Co3O4/BiVO4composite under visible light irradiation[J].J.PhysicalChemistryB,2006,110(41):20211-20216. [32]HONG S J,LEE S,JANG J S,etal.. Heterojunction BiVO4/WO3electrodes for enhanced photoactivity of water oxidation[J].Energy&EnvironmentalScience,2011,4(5):1781-1787. [33]CHENG H,HUANG B,DAI Y,etal.. One-step synthesis of the nanostructured AgI/BiOI composites with highly enhanced visible-light photocatalytic performances[J].Langmuir,2010,26(9):6618-6624. [34]WANG Z,HUANG B,DAI Y,etal.. Highly photocatalytic ZnO/In2O3heteronanostructures synthesized by a coprecipitation method[J].J.PhysicalChemistryC,2009,113(11):4612-4617. [35]WANG G,HUANG B,WANG L,etal.. CuO/CuSCN valence state heterojunctions with visible light enhanced and ultraviolet light restrained photocatalytic activity[J].ChemicalCommunications,2014,50(29):3814-3816. [36]CHENG H,HUANG B,QIN X,etal.. A controlled anion exchange strategy to synthesize Bi2S3nanocrystals/BiOCl hybrid architectures with efficient visible light photoactivity[J].ChemicalCommunications,2012,48(1):97-99. [37]WANG W,HUANG B,MA X,etal.. Efficient separation of photogenerated electron-hole pairs by the combination of a heterolayered structure and internal polar field in pyroelectric BiOIO3nanoplates[J].Chemistry-AEuropeanJournal,2013,19(44):14777-14780. [38]ZHANG R,DAI Y,LOU Z,etal.. Layered photocatalyst Bi2O2[BO2(OH)] nanosheets with internal polar field enhanced photocatalytic activity[J].Cryst.Eng.Comm.,2014,16(23):4931-4934. [39]FAN X,ZANG L,ZHANG M,etal.. A bulk boron-based photocatalyst for efficient dechlorination: K3B6O10Br[J].ChemistryofMaterials,2014,26(10):3169-3174. [40]LI M,DAI Y,MA X,etal.. The synergistic effect between effective mass and built-in electric field for the transfer of carriers in nonlinear optical materials[J].PhysicalChemistryChemicalPhysics,2015,17(27):17710-17717. [41]WANG C,BAHNEMANN D W,DOHRMANN J K. A novel preparation of iron-doped TiO2nanoparticles with enhanced photocatalytic activity[J].ChemicalCommunications,2000 (16):1539-1540. [42]IKEDA T,NOMOTO T,EDA K,etal.. Photoinduced dynamics of TiO2doped with Cr and Sb[J].J.PhysicalChemistryC,2008,112(4):1167-1173. [43]OHNO T,TANIGAWA F,FUJIHARA K,etal.. Photocatalytic oxidation of water by visible light using ruthenium-doped titanium dioxide powder[J].J.PhotochemistryandPhotobiologyA:Chemistry,1999,127(1):107-110. [44]KLOSEK S,RAFTERY D. Visible light driven V-doped TiO2photocatalyst and its photooxidation of ethanol[J].J.PhysicalChemistryB,2001,105(14):2815-2819. [45]ASAHI R,MORIKAWA T,OHWAKIT,etal.. Visible-light photocatalysis in nitrogen-doped titanium oxides[J].Science,2001,293(5528):269-271. [46]CHEN X,BURDA C. The electronic origin of the visible-light absorption properties of C-, N-and S-doped TiO2nanomaterials[J].J.AmericanChemicalSociety,2008,130(15):5018-5019. [47]YU H F. Photocatalytic abilities of gel-derived P-doped TiO2[J].J.PhysicsandChemistryofSolids,2007,68(4):600-607. [48]ZHOU J K,LV L,YU J,etal.. Synthesis of self-organized polycrystalline F-doped TiO2hollow microspheres and their photocatalytic activity under visible light[J].J.PhysicalChemistryC,2008,112(14):5316-5321. [49]IRIE H,WATANABE Y,HASHIMOTO K. Nitrogen-concentration dependence on photocatalytic activity of TiO2-xNxpowders[J].J.PhysicalChemistryB,2003,107(23):5483-5486. [50]YANG K,DAI Y,HUANG B. Study of the nitrogen concentration influence on N-doped TiO2anatase from first-principles calculations[J].J.PhysicalChemistryC,2007,111(32):12086-12090. [51]YANG K,DAI Y,HUANG B,etal.. Theoretical study of N-doped TiO2rutile crystals[J].J.PhysicalChemistryB,2006,110(47):24011-24014. [52]YANG K,DAI Y,HUANG B. Understanding photocatalytic activity of S-and P-doped TiO2under visible light from first-principles[J].J.PhysicalChemistryC,2007,111(51):18985-18994. [53]YANG K,DAI Y,HUANG B,etal.. Density functional characterization of the visible-light absorption in substitutional C-anion-and C-cation-doped TiO2[J].J.PhysicalChemistryC,2009,113(6):2624-2629. [54]YANG K,DAI Y,HUANG B. Origin of the photoactivity in boron-doped anatase and rutile TiO2calculated from first principles[J].PhysicalReviewB,2007,76(19):195201. [55]YANG K,DAI Y,HUANG B,etal.. Density functional characterization of the band edges, the band gap states, and the preferred doping sites of halogen-doped TiO2[J].ChemistryofMaterials,2008,20(20):6528-6534. [56]LIN T,YANG C,WANG Z,etal.. Effective nonmetal incorporation in black titania with enhanced solar energy utilization[J].Energy&EnvironmentalScience,2014,7(3):967-972. [57]MA X,DAI Y,HUANG B. Origin of the increased photocatalytic performance of TiO2nanocrystal composed of pure core and heavily nitrogen-doped shell:a theoretical study[J].ACSAppliedMaterials&Interfaces,2014,6(24):22815-22822. [58]MAEDA K,TAKATA T,HARA M,etal.. GaN∶ZnO solid solution as a photocatalyst for visible-light-driven overall water splitting[J].J.AmericanChemicalSociety,2005,127(23):8286-8287. [59]WANG J,HUANG B,WANG Z,etal.. Facile synthesis of Zn-rich (GaN)1-x(ZnO)xsolid solutions using layered double hydroxides as precursors[J].J.MaterialsChemistry,2011,21(12):4562-4567. [60]WANG J,YANG P,WANG Z,etal.. Effect of temperature on the transformation from Zn-Ga layered double hydroxides into (GaN)1-x(ZnO)xsolid solution[J].J.AlloysandCompounds,2015,652:205-212. [61]WEI W,DAI Y,YANG K,etal.. Origin of the visible light absorption of GaN-rich Ga1-xZnxN1-xOx(x=0.125) solid solution[J].J.PhysicalChemistryC,2008,112(40):15915-15919. [62]LU J,DAI Y,GUO M,etal.. Structure and electronic properties and phase stabilities of the Cd1-xZnxS solid solution in the range of 0≤x≤1[J].Chem.Phys.Chem.,2012,13(1):147-154. [63]ALIBABAEI L,BRENNAMAN M K,NORRIS M R,etal.. Solar water splitting in a molecular photoelectrochemical cell[J].ProceedingsoftheNationalAcademyofSciences,2013,110(50):20008-20013. [64]AWAZU K,FUJIMAKIM,ROCKSTUHL C,etal.. A plasmonic photocatalyst consisting of silver nanoparticles embedded in titanium dioxide[J].J.AmericanChemicalSociety,2008,130(5):1676-1680. [65]LI H,BIAN Z,ZHU J,etal.. Mesoporous Au/TiO2nanocomposites with enhanced photocatalytic activity[J].J.AmericanChemicalSociety,2007,129(15):4538-4539. [66]PRIMO A,MARINO T,CORMA A,etal.. Efficient visible-light photocatalytic water splitting by minute amounts of gold supported on nanoparticulate CeO2obtained by a biopolymer templating method[J].J.AmericanChemicalSociety,2011,133(18):6930-6933. [67]WANG P,HUANG B,QIN X,etal.. Ag@ AgCl: a highly efficient and stable photocatalyst active under visible light[J].AngewandteChemieInternationalEdition,2008,47(41):7931-7933. [68]WANG P,HUANG B,LOU Z,etal.. Synthesis of highly efficient Ag@AgCl plasmonic photocatalysts with various structures[J].Chemistry-aEuropeanJournal,2010,16(2):538-544. [69]WANG P,HUANG B,ZHANG X,etal.. Highly efficient visible-light plasmonic photocatalyst Ag@AgBr[J].Chemistry-AEuropeanJournal,2009,15(8):1821-1824. [70]WANG P,HUANG B,QIN X,etal.. Ag/AgBr/WO3H2O:visible-light photocatalyst for bacteria destruction[J].InorganicChemistry,2009,48(22):10697-10702. [71]CHENG H,HUANG B,WANG P,etal.. In situ ion exchange synthesis of the novel Ag/AgBr/BiOBr hybrid with highly efficient decontamination of pollutants[J].Chem.Commun.,2011,47(25):7054-7056. [72]WANG P,HUANG B,ZHANG Q,etal.. Highly efficient visible light plasmonic photocatalyst Ag@Ag(Br,I)[J].Chemistry-AEuropeanJournal,2010,16(33):10042-10047. [73]WANG P,HUANG B,ZHANG X,etal.. Highly efficient visible light plasmonic photocatalysts Ag@Ag(Cl,Br) and Ag@AgCl-AgI[J].Chem.Cat.Chem.,2011,3(2):360-364. [74]WANG P,HUANG B,ZHANG X,etal.. Highly efficient visible light plasmonic photocatalysts Ag@Ag(Cl,Br) and Ag@AgCl-AgI[J].Chem.Cat.Chem.,2011,3(2):360-364. [75]LOU Z,WANG Z,HUANG B,etal.. Synthesis and activity of plasmonic photocatalysts[J].Chem.Cat.Chem.,2014,6(9):2456-2476. [76]LOU Z,HUANG B,WANG P,etal.. The synthesis of the near-spherical AgCl crystal for visible light photocatalytic applications[J].DaltonTransactions,2011,40(16):4104-4110. [77]LOU Z,HUANG B,QIN X,etal.. One-step synthesis of AgBr microcrystals with different morphologies by ILs-assisted hydrothermal method[J].Cryst.Eng.Comm.,2011,13(6):1789-1793. [78]LOU Z,HUANG B,QIN X,etal.. One-step synthesis of AgCl concave cubes by preferential overgrowth along <111> and <110> directions[J].ChemicalCommunications,2012,48(29):3488-3490. [79]LOU Z,HUANG B,MA X,etal.. A 3D AgCl hierarchical superstructure synthesized by a wet chemical oxidation method[J].Chemistry-AEuropeanJournal,2012,18(50):16090-16096. [80]LOU Z,HUANG B,WANG Z,etal.. Interface kinetic diffusion reaction leading to fast and continuous generation of AgCl nanocubes in NaCl solution[J].DaltonTransactions,2013,42(42):15219-15225. [81]MA X,DAI Y,LU J,etal.. Tuning of the surface-exposing and photocatalytic activity for AgX(X=Cl and Br):a theoretical study[J].J.PhysicalChemistryC,2012,116(36):19372-19378. [82]MA X,DAI Y,GUO M,etal.. The role of effective mass of carrier in the photocatalytic behavior of silver halide-based Ag@AgX(X=Cl,Br,I):a theoretical study[J].Chem.Phys.Chem.,2012,13(9):2304-2309. [83]MA X,DAI Y,YU L,etal.. Electron hole pair generation of the visible-light plasmonic photocatalyst Ag@AgCl:enhanced optical transitions involving midgap defect states of AgCl[J].J.PhysicalChemistryC,2014,118(23):12133-12140. [84]BIAN Z,TACHIKAWA T,ZHANG P,etal.. Au/TiO2superstructure-based plasmonic photocatalysts exhibiting efficient charge separation and unprecedented activity[J].J.AmericanChemicalSociety,2013,136(1):458-465. [85]MA X,DAI Y,YU L,etal.. New basic insights into the low hot electron injection efficiency of gold nanoparticle photosensitized titanium dioxide[J].ACSAppliedMaterials&Interfaces,2014,6(15):12388-12394. [86]HITOKI G,ISHIKAWA A,TAKATA T,etal.. Ta3N5as a novel visible light-driven photocatalyst(.LAMBDA.<600 nm)[J].ChemistryLetters,2002(7):736-737. [87]HITOKI G,TAKATA T,KONDO J N,etal.. An oxynitride, TaON, as an efficient water oxidation photocatalyst under visible light irradiation(λ≤500 nm)[J].ChemicalCommunications,2002 (16):1698-1699. [88]KASAHARA A,NUKUMIZU K,TAKATA T,etal.. LaTiO2N as a visible-light(≤600 nm)-driven photocatalyst(2)[J].J.PhysicalChemistryB,2003,107(3):791-797. [89]LI M,LUO W,CAO D,etal.. A Co-catalyst-loaded Ta3N5photoanode with a high solar photocurrent for water splitting upon facile removal of the surface layer[J].AngewandteChemieInternationalEdition,2013,52(42):1016-11020. [90]JING T,DAI Y,MA X,etal.. Effects of intrinsic defects and extrinsic doping on the electronic and photocatalytic properties of Ta3N5[J].RSCAdvances,2015,5(73):59390-59397. [91]KUDO A,OMORIK,KATO H. A novel aqueous process for preparation of crystal form-controlled and highly crystalline BiVO4powder from layered vanadates at room temperature and its photocatalytic and photophysical properties[J].J.AmericanChemicalSociety,1999,121(49):11459-11467. [92]LUO W,YANG Z,LI Z,etal.. Solar hydrogen generation from seawater with a modified BiVO4photoanode[J].Energy&EnvironmentalScience,2011,4(10):4046-4051. [93]KIM T W,CHOI K S. Nanoporous BiVO4photoanodes with dual-layer oxygen evolution catalysts for solar water splitting[J].Science,2014,343(6174):990-994. [94]WANG X,MAEDA K,THOMAS A,etal.. A metal-free polymeric photocatalyst for hydrogen production from water under visible light[J].NatureMaterials,2009,8(1):76-80. [95]ZHANG J,GUO F,WANG X. An optimized and general synthetic strategy for fabrication of polymeric carbon nitride nanoarchitectures[J].AdvancedFunctionalMaterials,2013,23(23):3008-3014. [96]HONG J,XIA X,WANG Y,etal.. Mesoporous carbon nitride with in situ sulfur doping for enhanced photocatalytic hydrogen evolution from water under visible light[J].J.MaterialsChemistry,2012,22(30):15006-15012. [97]ZHANG J,WANG Y,JIN J,etal.. Efficient visible-light photocatalytic hydrogen evolution and enhanced photostability of core/shell CdS/g-C3N4nanowires[J].ACSAppliedMaterials&Interfaces,2013,5(20):10317-10324. [98]YI Z,YE J,KIKUGAWA N,etal.. An orthophosphate semiconductor with photooxidation properties under visible-light irradiation[J].NatureMaterials,2010,9(7):559-564. [99]BI Y,OUYANG S,UMEZAWA N,etal.. Facet effect of single-crystalline Ag3PO4sub-microcrystals on photocatalytic properties[J].J.AmericanChemicalSociety,2011,133(17):6490-6492. [100]UMEZAWA N,SHUXIN O,YE J. Theoretical study of high photocatalytic performance of Ag3PO4[J].PhysicalReviewB,2011,83(3):035202. [101]LOU Z,HUANG B,WANG Z,etal.. Ag6Si2O7:a silicate photocatalyst for the visible region[J].ChemistryofMaterials,2014,26(13):3873-3875. [102]LOU Z,WANG Z,HUANG B,etal.. One-step synthesis of amorphous silver silicates with tunable light absorption spectra and photocatalytic activities in the visible region[J].Chemistry-AEuropeanJournal,2015,5:59390-59397. [103]ZHU X,WANG Z,HUANG B,etal.. Synthesis of Ag9(SiO4)2NO3through a reactive flux method and its visible-light photocatalytic performances[J].APLMaterials,2015,3(10):104413. [104]LIU Z,LOU Z,LI Z,etal.. GeH:a novel material as a visible-light driven photocatalyst for hydrogen evolution[J].ChemicalCommunications,2014,50(75):11046-11048. [105]WEI W,DAI Y,HUANG B,etal.. Many-body effects in silicene, silicane, germanene and germanane[J].PhysicalChemistryChemicalPhysics,2013,15(22):8789-8794. [106]JIN H,DAI Y,MA X C,etal.. Enhancement of photocatalytic activity of a two-dimensional GeH/graphene heterobilayer under visible light[J].RSCAdvances,2015,5(64):52264-52268. [107]QIN W,ZHANG D,ZHAO D,etal.. Near-infrared photocatalysis based on YF3∶Yb3+, Tm3+/TiO2core/shell nanoparticles[J].ChemicalCommunications,2010,46(13):2304-2306. [108]LI H,LIU R,LIU Y,etal.. Carbon quantum dots/Cu2O composites with protruding nanostructures and their highly efficient(near) infrared photocatalytic behavior[J].J.MaterialsChemistry,2012,22(34):17470-17475. [109]LI H,LIU R,LIAN S,etal.. Near-infrared light controlled photocatalytic activity of carbon quantum dots for highly selective oxidation reaction[J].Nanoscale,2013,5(8):3289-3297. [110]WANG G,HUANG B,MA X,etal.. Cu2(OH)PO4, a near-infrared-activated photocatalyst[J].AngewandteChemieInternationalEdition,2013,125(18):4910-4913. [111]RITTER S K. Copper claims first as near-infrared photocatalyst[J].Chemical&EngineeringNews,2013,91(14):36-37. [112]LI Z,DAI Y,MA X,etal.. Tuning photocatalytic performance of the near-infrared-driven photocatalyst Cu2(OH)PO4based on effective mass and dipole moment[J].PhysicalChemistryChemicalPhysics,2014,16(7):3267-3273. [113]WANG G,HUANG B,LI Z,etal.. On structural features necessary for near-ir-light photocatalysts[J].Chemistry-AEuropeanJournal,2015,21(39):13583-13587. [114]TIAN J,SANG Y,YU G,etal.. A Bi2WO6-based hybrid photocatalyst with broad spectrum photocatalytic properties under UV, visible, and near-infrared irradiation[J].AdvancedMaterials,2013,25(36):5075-5080. [115]JING T,DAI Y,WEI W,etal.. Near-infrared photocatalytic activity induced by intrinsic defects in Bi2MO6(M=W,Mo)[J].PhysicalChemistryChemicalPhysics,2014,16(34):18596-18604. [116]SANG Y,ZHAO Z,ZHAO M,etal.. From UV to near-infrared, WS2nanosheet: a novel photocatalyst for full solar light spectrum photodegradation[J].AdvancedMaterials,2015,27(2):363-369. [117]JIANG W,WANG X,WU Z,etal.. Silver oxide as superb and stable photocatalyst under visible and near-infrared light irradiation and its photocatalytic mechanism[J].Industrial&EngineeringChemistryResearch,2015,54(3):832-841. [118]YOSHIMIZU M,KOBAYASHI R,SAEGUSA M,etal.. Photocatalytic hydrogen evolution over β-iron silicide under infrared-light irradiation[J].ChemicalCommunications,2015,51(14):2818-282. 荆涛(1981—),男,湖北荆门人,博士研究生,2010年于贵州大学获得硕士学位,主要从事光催化材料理论方面的研究。E-mail:jingtao123456@sohu.com 戴瑛(1962—),女,山东济南人,教授,博士生导师。主要从事半导体材料纳米光电性质和光催化性质及其应用方面的研究。E-mail:daiy60@sina.com Development in extending spectral response of photocatalytic materials JING Tao, DAI Ying*, MA Xiao-juan, HUANG Bai-biao (SchoolofPhysics,StateKeyLaboratoryofCrystalMaterials,ShandongUniversity,Jinan250100,China) *Correspondingauthor,E-mail:daiy60@sina.com Abstract:Photocatalysis has drawn much attention during past decades due to the potential applications in solving the current energy and environment crisis. The spectral response in wide range and high quantum efficiency are crucial to realize solar energy efficient conversion for photocatalytic materials. In the present work, we review briefly the recent progress of photocatalytic materials in responding to the UV, visible and near-infrared light. Some strategies to extend light response range and enhance the separation of charge carriers are illustrated. And challenges and prospects for further development in this field are presented. Key words:photocatalysis;carrier separation;band engineer;redox 作者简介: 中图分类号:O644.1 文献标识码:A doi:10.3788/CO.20160901.0001 文章编号2095-1531(2016)01-0001-15 基金项目:国家重点基础研究发展计划(973计划)资助项目(No.2013CB632401);国家自然科学基金资助项目(No.21333006,No.11374190);山东泰山学者项目 收稿日期:2015-09-11; 修订日期:2015-11-13 Supported by National Program on Key Basic Research Projects of China(No.2013CB632401), National Natural Science Foundation of China(No.21333006, No.11374190),Taishan Scholar Program of Shandong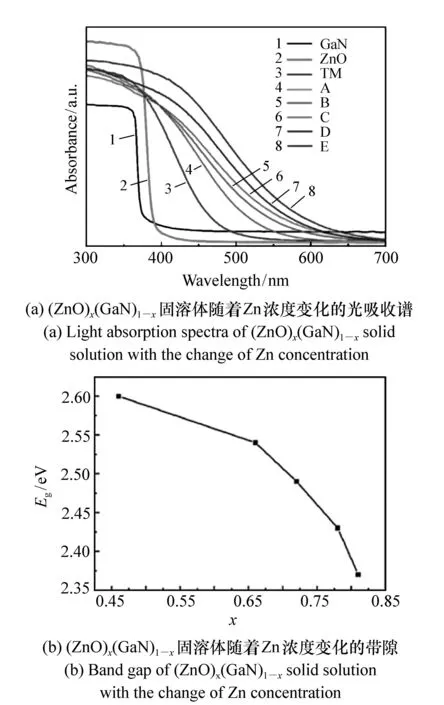

3.2 本征的窄带隙光催化材料

4.1 上转换材料
4.2 杂质态引起的近红外光催化活性

4.3 窄带隙近红外光催化材料