共价修饰法制备新型多巴胺传感器
2016-02-07窦志宇张博文吴燕英
窦志宇,张博文,吴燕英
(长春理工大学化学与环境工程学院,长春 130022)
共价修饰法制备新型多巴胺传感器
窦志宇,张博文,吴燕英
(长春理工大学化学与环境工程学院,长春 130022)
在实验中将4arm-PEG-NH2和羟基苯基铁卟啉共价修饰到玻碳电极上,成功地制备了一种新型DA传感器。由于Fe(OH)4P和4arm-PEG-NH2的协同效应,使得该传感器对多巴胺的电催化活性得到明显的提高,氧化过电位也得到了降低。在示差脉冲伏安法测定中(多巴胺的检测范围为0.2~125μmol L-1),计算获得DA的检出限为1.02×10-8M。
四臂-聚乙二醇-氨基复合物;5,10,15,20-四羟基苯基铁卟啉;两步共价修饰;多巴胺
做为单胺类神经递质中的一种,多巴胺(DA)在调节荷尔蒙的分泌、中枢神经系统及心血管系统的活动等方面发挥了巨大的作用,它的浓度过高或过低都将直接或间接地引起一些疾病的发生[1-5]。所以多巴胺自被发现伊始,便在临床应用领域获得了广泛的关注,也因此有大量检测多巴胺的方法在过去的几十年中被相继开发出来,比如荧光法[6]、化学发光法、离子色谱法[7]、毛细管电泳法等。相对比其他检查手段而言,电化学方法以其较快的检测速度,相对简单的制备过程,良好的重复性,低廉的制备成本等优点,成为该领域的研究热点[8-10]。但同时也不能忽略一个事实,那就是多巴胺的电化学检测非常容易受到其他生物活性分子的干扰,如抗坏血酸,尿酸,肾上腺素等等。从大量的研究结果中发现,人们在尝试以电极修饰的方式来解决这些问题,可以应用的修饰材料包括金属纳米粒子[11,12],导电聚合物涂覆的电极[13,14],纳米材料修饰的碳基质[15],金属卟啉等等[16]。
在对亚硝酸盐、挥发性有机物、一氧化碳和DA等生物和环境中重要分子的检测方面,金属卟啉作为电极修饰材料表现出了优异的电催化性能[17-19]。但同时也看到,单独以金属卟啉作为电极修饰材料制备的多巴胺传感器,仍会出现过电位较高的现象。而很多的研究结果证实,聚乙二醇单甲醚修饰的电极对提高DA的氧化还原活性、降低其氧化过电位起到了很好的促进性的作用。四臂-聚乙二醇-氨基复合物(4arm-PEG-NH2)作为类似的非离子型表面活性剂,同样可显著降低在电化学反应过程中电活性分子的过电位。
鉴于这两类物质对DA均具有良好的电化学催化活性,在实验中尝试将4arm-PEG-NH2和羟基苯基铁卟啉(Fe(OH)4P)共价修饰锚定到电极的表面获得一种多巴胺传感器,并对修饰电极的电催化性能进行了系统的研究。
1 实验部分
1.1 试剂和仪器
4arm-PEG-NH2和多巴胺(98%)购于Aladdin试剂公司;抗坏血酸、磷酸盐、无水乙醇、氯化钾、氢氧化钠均为分析纯;DMF(99%)购于萨思化学技术有限公司;另外,5,10,15,20-四羟基苯基铁卟啉利用文献方法制备[20]。
用CHI660D型电化学工作站(上海辰华)测试电化学,采用三电极体系,以修饰电极(GCE)或裸玻碳电极做为工作电极,饱和甘汞电极做为参比电极,对电极为铂丝;采用PBS缓冲溶液(pH=7,浓度为0.2M)做为测试溶液;使用KQ-100DE型数控超声波清洗器对样品超声清洗。
1.2 实验过程
修饰之前,需要依次用1.0μm,0.3μm和0.05μm的α-氧化铝粉末对裸GCE电极进行打磨抛光,然后再分别利用三次蒸馏水、乙醇和三次蒸馏水对电极超声处理各2分钟,最后氮气吹干。为了活化该修饰电极,还需将其放到pH=7.0的PBS溶液中进行循环伏安扫描(电位范围-0.2V~+0.2V,扫速为10mV s-1),待循环伏安曲线稳定即可停止活化。把该活化电极放到20mL溶解了40mg Fe(OH)4P的DMF溶液中,以0.1M的四丁基高氯酸铵(TBAP)做为支持电解质进行循环伏安扫描(扫速20mV s-1,电位区间-1.2V~+1.6V)。继续将该活化电极放到溶有20mL 50mg 4arm-PEG-NH2和48mg LiClO4的缓冲溶液(pH=7)中,循环伏安扫描15圈(电位区间为0~+1.0V,扫速为20mV s-1)。将修饰电极用三次蒸馏水冲洗,氮气吹干,在红外灯下烘10分钟。
2 结果与讨论
2.1 Fe(OH)4P/4arm-PEG-NH2在GCE上的电化学修饰
实验中是先后两步把羟基苯基铁卟啉(Fe(OH)4P)和四臂-聚乙二醇-氨基聚合物(4arm-PEG-NH2)依次锚定到玻碳电极上的。通过循环伏安扫描(扫描电位区间在-0.2~+0.2V)的方式活化玻碳电极,活化完成后在玻碳电极的表面将富集大量的碳正离子。然后通过亲核取代反应,将羟基苯基铁卟啉结构上的羟基与活化电极表面的碳正离子共价结合;最后仍然通过亲核取代反应,使四臂-聚乙二醇-氨基聚合物结构中的氨基与电极表面剩余的碳正离子共价键合,修饰过程如图1所示。
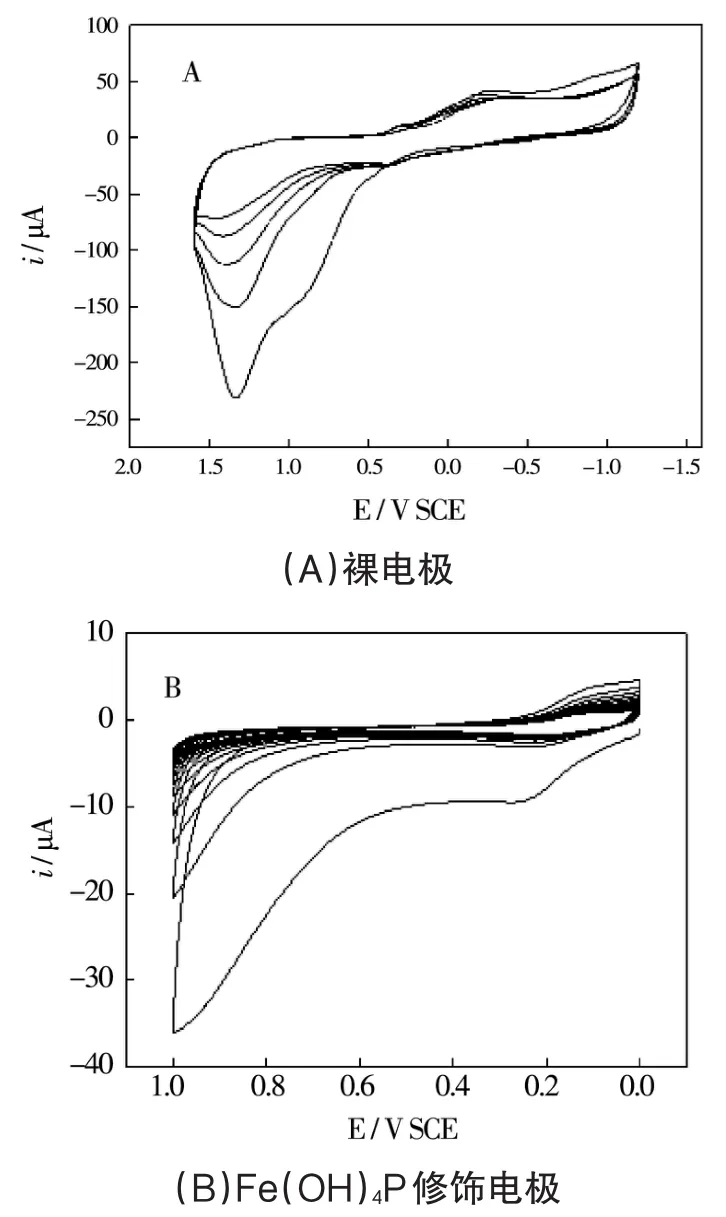
图1 循环伏安图
2.2 修饰电极催化氧化DA
图2为分别通过裸电极(电极a)、活化电极(电极b)、羟基苯基铁卟啉(Fe(OH)4P)修饰电极(电极c)、四臂-聚乙二醇-氨基聚合物(4arm-PEG-NH2)修饰电极(电极d)以及Fe(OH)4P/4arm-PEG-NH2共修饰电极(电极e)检测20μM DA缓冲溶液得到的系列循环伏安曲线。不难发现,DA对裸电极(a)几乎没有任何响应;从电极b的检测曲线中可以看出,峰电位差变小(ΔEp=177mV),电流响应仍然不强;虽然可以从单独修饰Fe(OH)4P的电极(c)的检测曲线中观察到一对明显的氧化还原峰,但却出现非常大的背景电流;四臂-聚乙二醇修饰的电极(d),峰形变尖,电流响应明显增大;而电极e较之于裸电极,氧化峰与还原峰电位差明显变小(ΔEp= 19mV),峰电流明显增强。有力地证明了羟基苯基铁卟啉和四臂-聚乙二醇-氨基聚合物复合物薄膜加快了电子转移速率,提升了电化学氧化DA反应的可逆性。
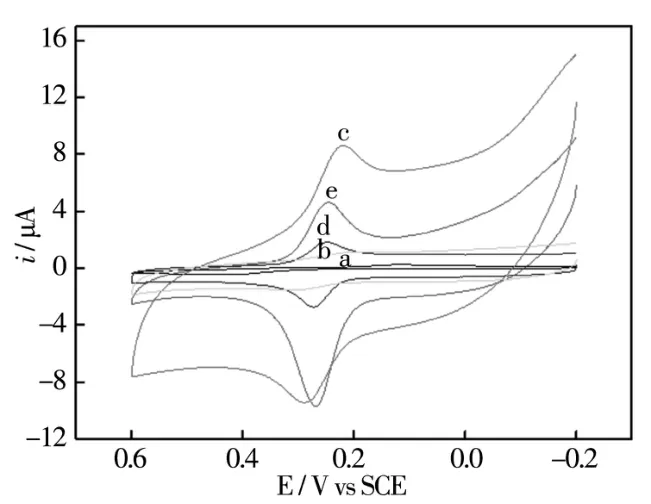
图2 五种不同电极在DA缓冲溶液的循环伏安图(20μM,pH=7,扫速50mV s-1)
2.3 扫速的影响
为了研究DA在修饰电极表面的电化学行为,在实验中固定了多巴胺浓度为20μM并改变扫描速度(从10mV s-1到500mV s-1),得到一系列循环伏安曲线,如图3-5所示)。从图可以看出,氧化和还原峰电流随着扫速的增大也相应变大,同时氧化峰电流发生正移,还原峰电流发生负移。另外,当扫速较低时(10~180mV s-1),峰电流与扫速呈现出很好的线性关系;而在较高扫速(200~500mV s-1)时,峰电流和扫速的平方根呈现很好的线性关系。这些实验结果说明:在低扫速时DA的电化学反应呈现出了受表面吸附控制的特点,而高扫速时修饰电极表面的DA反应是受扩散控制的。
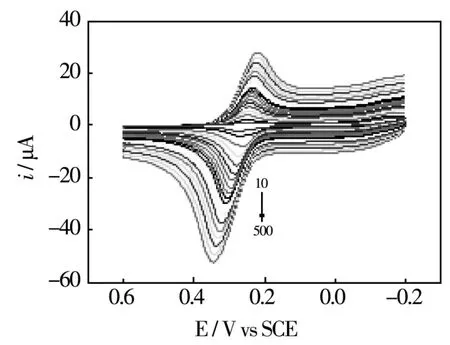
图3 共修饰电极在不同扫速下的循环伏安图
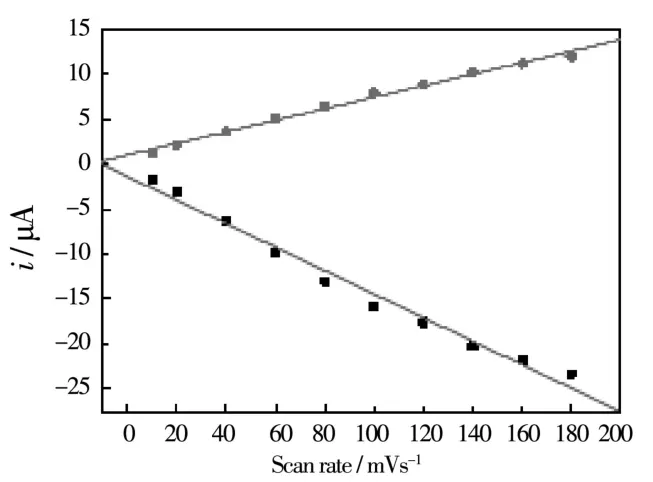
图4 Ipc和Ipa与扫速关系曲线图
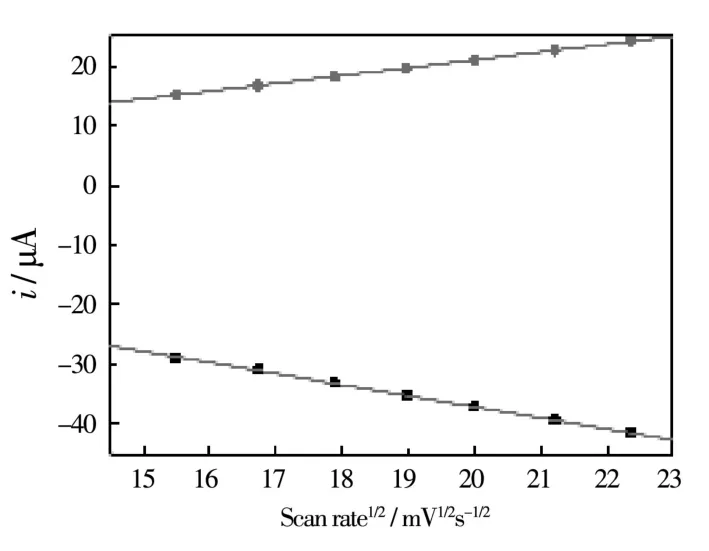
图5 Ipc和Ipa与扫速平方根关系曲线图
2.4 pH值的影响
为了进一步探讨Fe(OH)4P/4arm-PEG-NH2共修饰电极对多巴胺的电催化行为,还改变了酸碱条件(pH=3.0-9.0)对20μM的DA缓冲溶液进行循环伏安扫描,得到一系列循环伏安曲线(如图4)。从图4中可以看出,多巴胺的氧化峰电位和还原峰电位随pH值的增大而逐渐负移,所以推测在共修饰电极上有质子参与到多巴胺的氧化还原反应过程中。
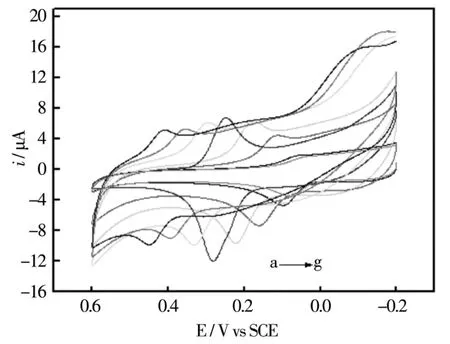
图6 不同pH值(3-9)的DA缓冲溶液在共修饰电极上的循环伏安曲线
同时也发现在pH值从3.0到9.0区间,Epa值与pH值表现出较好的线性关系(图7B),斜率值为-59.51mV pH-1(接近理论值-59mV pH-1),可以推断,Fe(OH)4P/4arm-PEG-NH2共修饰电极对多巴胺的电催化氧化是等电子等质子过程。同时,通过修饰电极所测得的多巴胺氧化峰电流值与pH值的关系曲线(图7A)不难发现,在pH=5.0的缓冲溶液中DA的氧化峰电流最大。以此为依据选择了效果最好的pH=5.0的溶液作为本实验的缓冲溶液。
2.5 干扰研究
正如前言所述,对多巴胺的检测必须要排除体液中共存的AA等其它生命基质的影响,所以在检测多巴胺时研究了共修饰电极对其他物质的抗干扰能力。选取了含AA(浓度为DA的25倍)和DA的混合溶液,对其进行DPV检测。从图8可以看出,DA和AA氧化过电位未出现重叠,且两峰差值为212mV。说明即使在含有高浓度AA的情况下,Fe(OH)4P/4arm-PEG-NH2共修饰电极仍对多巴胺表现出了很高的灵敏性、良好的选择性。
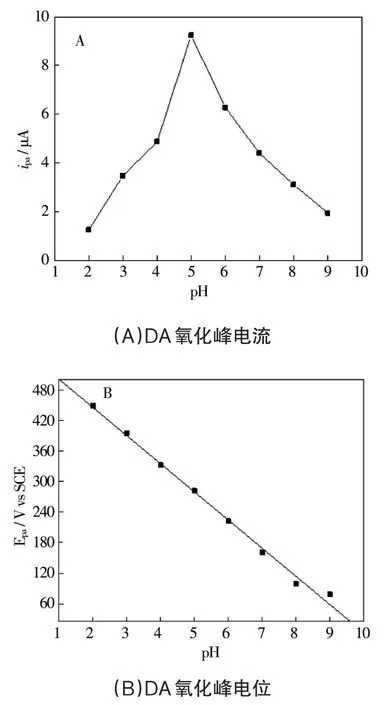
图7 DA随pH变化关系图
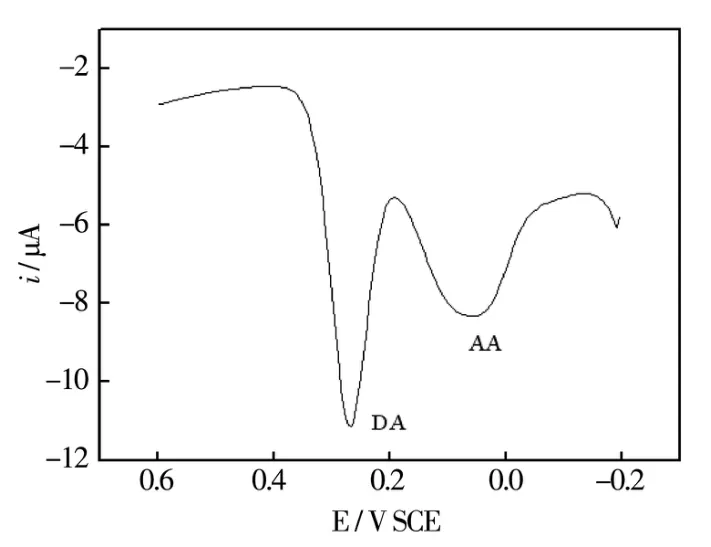
图8 修饰电极在含有50μM DA和1000μM AA的pH 5.0的缓冲溶液中的循环伏安图。
2.6 检测DA
图9是不同浓度的多巴胺缓冲溶液(pH=5.0)在Fe(OH)4P/4arm-PEG-NH2共修饰电极上的示差脉冲伏安图(DVP),发现在0.2~125μM的浓度范围内,峰电流随多巴胺浓度的增加而线性增加,得到的线性方程为:ipa(μA)=0.6041+0.2357C(μM),相关系数r为0.9990。该修饰电极通过公式Cm=3sbl/m计算得到的最低检测限为1.02×10-8M,传感器灵敏度为235.7μA mM-1。可见,由于Fe(OH)4P与4arm-PEG-NH2之间的协同作用,大大改善了修饰电极的检测限和灵敏度,拓展了其应用性。
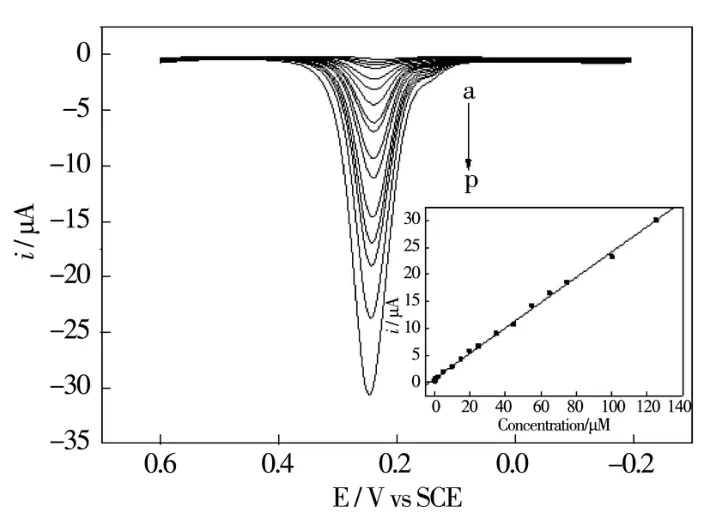
图9 不同浓度DA的缓冲溶液在Fe(OH)4P/ 4arm-PEG-NH2修饰电极上的示差脉冲伏安图
从(a)到(q)是DA浓度分别为0.2,0.6,1.0,2.0,5.0,10,15,20,25,35,45,55,65,75,100,125μM。插图为DA浓度与氧化峰电流之间的关系。
2.7 稳定性研究
为了了解共修饰电极的稳定性,将其在室温下储存3个月然后通过循环伏安法对20μM的DA缓冲溶液(pH=5.0)进行检测。从检测结果来看,DA在放置了3个月的共修饰电极中的氧化峰电流仅降低5.17%,且氧化峰电位没有发生明显变化。充分说明,Fe(OH)4P/4arm-PEG-NH2共修饰电极具有较长的使用寿命和非常好的稳定性。
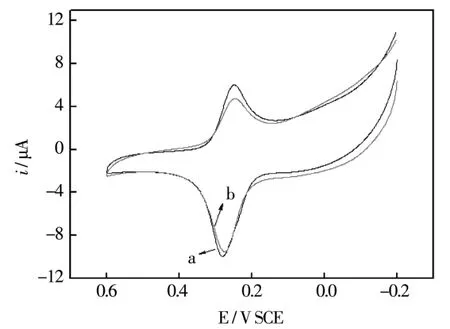
图10 DA在修饰电极上的循环伏安图
2.8 真实样品分析
利用示差脉冲伏安法对人体血液进行的检测目的在于评估共修饰电极的实际应用性(见表1)。在检测之前,将人血清样品用pH值为5.0的磷酸盐缓冲溶液稀释20倍。从表中可以看出,在盐酸多巴胺注射液中DA的回收率分别100.6%,101.7%和99.47%,相对标准偏差较低,结果比较令人满意。这也预示着通过共修饰的方法制备的多巴胺传感器有望应用于实际样本中DA的测定。
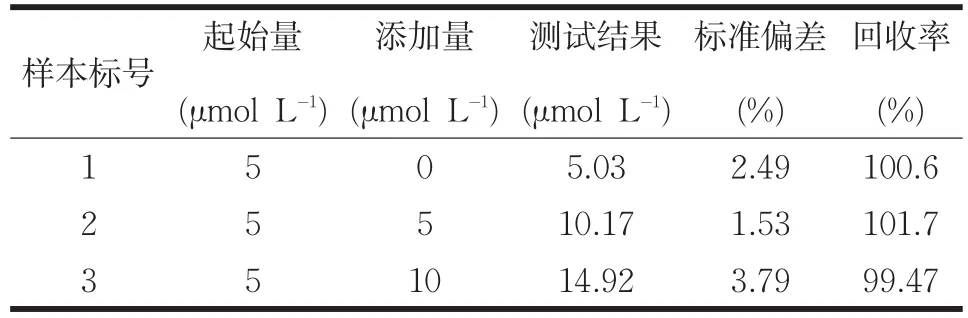
表1 在人体血清样品中测定DA的结果
3 结论
通过两步共价修饰的方法,成功地将羟基苯基铁卟啉(Fe(OH)4P)和四臂-聚乙二醇-氨基聚合物(4arm-PEG-NH2)锚定到玻碳电极表面。在随后的研究中发现,Fe(OH)4P和4arm-PEG-NH2两种物质具有很好的协同作用,使得该电极表现出了优异的电化学催化活性。主要体现在用共价修饰方法所得到的多巴胺传感器具备优异的选择性和较高的灵敏度,很好的稳定性,较低的检出限,较长的使用寿命等等,而这些都使得它具备了很好的应用前景。
[1]Chen J L,Yan X P,Meng K,et al.Graphene oxide based photoinducedcharge transfer label-free near-infrared fluorescent biosensor for dopamine[J].Analytical Chemistry,2011,83(22):8787-8793.
[2]Jaber M,Robinson S W,Missale C,et al.Dopamine receptors and brainfunction[J].Neuropharmacology,1996,35(11):1503-1519.
[3]Wang C,Yuan R,Chai Y Q,et al.Au-nanoclustersincorporated3-amino-5-mercapto-1,2,4-triazole film modified electrode forthe simultaneous determination of ascorbic acid,dopamine,uric acid andnitrite[J].Biosensors and Bioelectronics,2011,30(1):315-319.
[4]Liu J M,Wang X X,Cui M L,et al.A promising non-aggregation colorimetric sensor of AuNRs-Ag+ for determination of dopamine[J].Sensors Actuators B,2013(176):97-102.
[5]Ferreira F D P,Silva L I B,Freitas A C,et al. High performance liquid chromatography coupled to anopticalfiberdetectorcoatedwithlaccasefor screeningcatecholaminesinplasmaandurine[J]. JournalofChromatographyA,2009,1216(42):7049-7054.
[6]Wang H Y,Hui Q S,Xu L X,et al.Fluorimetric determination of dopamine in pharmaceutical products and urine using ethylene diamine as the fluorigenic reagent[J].Analytica Chimica Acta,2003,497(1-2):93-99.
[7]Guan C L,Ouyang J,Li Q L,et al.Simultaneous determination of catecholamine by ion chromatography with direct conductivity detection[J].Talanta,2000,50(6):1197-1203.
[8]Chen P Y,Vittal R,Nien P C,et al.Enhancing dopaminedetectionusingaglassycarbonelectrode modified with MWCNTs,quercetin,and Nafion[J]. Biosensors and Bioelectronics,2009,24(12):3504-3509.
[9]He M F,Zheng X H.A highly sensitive and selectivemethodfordopaminedetectionbasedonpoly(folic acid)film modified electrode[J].Journal of Molec-ular Liquids,2012(173):29-34.
[10]ArriganDWM,GhitaM,BeniV.Selective voltammetric detection of dopamine in the presence of ascorbate[J].Chemical Communications,2004,40(6):732-733.
[11]Hu G Z,Zhang D P,Wu W L,et al.Selective determination of dopamine in the presence of high concentrationofascorbicacidusingnano-Au self-assembly glassy carbon electrode[J].Colloids and Surfaces B,2008,62(2):199-205.
[12]Xue C,Han Q,Wang Y,et al.Amperometric detection of dopamine in human serum by electrochemical sensor based on gold nanoparticles doped molecularly imprinted polymers[J].Biosensors and Bioelectronics,2013,49(15):199-203.
[13]Zhang H Y,Zhou Y Z,Zhang J C,et al.Highly selectiveandsensitivedopamineanduricacid electrochemical sensor fabricated with poly(orotic acid)[J].Journal of Molecular Liquids,2013(184):43-50.
[14]Atta N F,Galal A,Ahmed R A.Poly(3,4-ethylene-dioxythiophene)electrode for the selective determination of dopamine in presence of sodium dodecyl sulfate[J].Bioelectrochemistry,2011,80(1):132-141.
[15]Yuan D H,Chen S H,Yuan R,et al.An ECL sensor for dopamine using reduced graphene oxide/ multiwallcarbonnanotubes/goldnanoparticles[J]. Sensors and Actuators B,2014,191(1):415-420.
[16]侯长军,张红英,霍丹群,等.卟啉传感器研究进展[J].传感器与微系统,2008,27(3):1-4.
[17]Guo C X,Lei Y,Li C M.Porphyrin Functionalized Graphene for Sensitive Electrochemical Detection of Ultratrace Explosives[J].Electroanalysis,2011(23):885-893.
[18]Zhang S Y,Tang Sheng,Lei J P,Dong H F,et al. FunctionalizationofGrapheneNanoribbonswith PorphyrinforElectrocatalysisandAmperometric Biosensing[J].J.Electroanal.Chem,2011(656):285-288.
[19]Wu Li,Feng L Y,Ren J S,et al.Electrochemical Detection of Dopamine Using Porphyrin-FunctionalizedGraphene[J].Biosens.Bioelectron,2012(34):57-62.
[20]Hermann High L R,Holder S J,Penfold H V. Synthesisofstarpolymersofstyreneandalkyl(meth)acrylates from a porphyrin initiator core via ATRP[J].Macromolecules,2007,40(20):7157-7165.
Construction of Novel Dopamine Sensors Based on Covalent Modification Procedure
DOU Zhiyu,ZHANG Bowen,WU Yanying
(School of Chemistry and Environmental Engineering,Changchun University of Science and Technology,Changchun 130022)
We presented a novel dopamine(DA)sensor via a two-step covalent modification approach via anchoring 5,10,15,20-tetrakis(4-hydroxyphenyl)porphyrin(Fe(OH)4P)and 4-arm-(polyethylene glycol)-aminor(4 arm-PEGNH2)onto a glassy carbon electrode(GCE).The fabricated sensor showed a pronounced electrocatalytic activity improvement toward the oxidation of DA and led to a significant decrease in the anodic overpotentials compared with bare GCE,which should be ascribed to the synergistic effect of Fe(OH)4P and 4arm-PEG-NH2-GCE.Using differential pulse voltammetry(DPV),the sensor gave a linear response to DA over the concentration range of 0.2~125μM,with a detection limit of 1.02×10-8M.
4-arm-(polyethylene glycol)-amino;5,10,15,20-tetrakis(4-hydroxyphenyl)porphyrin;two-step covalent modification;dopamine
O657
A
1672-9870(2016)06-0062-05
2016-08-02
窦志宇(1979-),女,博士,讲师,E-mail:douzhiyu79@sina.cn
