沙咪珠利对小鼠精子畸形和骨髓细胞微核的影响
2016-02-07王东亮聂巧李龙飞李宇琛陈鸿雨陈秀云卜仕金
王东亮,聂巧,李龙飞,李宇琛,陈鸿雨,陈秀云,卜仕金
(1.扬州大学兽医学院,江苏扬州 225009;2.扬州大学医学院,江苏扬州 225001)
沙咪珠利对小鼠精子畸形和骨髓细胞微核的影响
王东亮1,聂巧1,李龙飞1,李宇琛1,陈鸿雨1,陈秀云2,卜仕金1
(1.扬州大学兽医学院,江苏扬州 225009;2.扬州大学医学院,江苏扬州 225001)
为评价沙咪珠利的安全性,对其进行了小鼠精子畸形和骨髓细胞微核试验研究。选择健康ICR小鼠随机分为受试物高、中、低剂量组,阳性对照组和阴性对照组,进行精子畸形试验和骨髓细胞微核试验,计算精子畸形率和微核率。结果显示,受试物各剂量组精子畸形率与骨髓细胞微核率与阴性对照组比较,差异不显著(P>0.05),与阳性对照组比较,差异有统计学意义(P<0.01)。表明沙咪珠利对小鼠精子和骨髓细胞微核无影响,不具有遗传毒性。
沙咪珠利;精子畸形;骨髓细胞微核
三嗪类抗球虫药是一种广谱、高效、安全的化学合成药物,能有效预防和治疗鸡球虫病[1]。沙咪珠利是国内自主研发的新型三嗪类抗球虫药,难溶于水,易溶于二甲基亚砜。初步研究结果表明沙咪珠利属于低毒药物,安全性高,抗球虫效果好,抗球虫指数(ACI)达150~200,且与地克珠利、妥曲珠利等三嗪类化合物无交叉耐药现象,具有广阔的应用前景[2-3]。目前国内外对沙咪珠利的一般毒理学进行了研究报道,但关于沙咪珠利潜在的遗传毒性未见相关报道。本实验采用小鼠精子畸形试验及小鼠骨髓细胞微核试验探讨沙咪珠利对小鼠遗传毒性的影响,了解沙咪珠利作为新型抗球虫药是否具有致突变作用,以期为沙咪珠利新药的充分开发和安全应用提供毒理学资料。
1 材料与方法
1.1 试剂与器材 沙咪珠利,含量98.6%,产品批号20130308,由中国农业科学院上海兽医研究所提供;环磷酰胺(CP),山西普德药业有限公司生产,产品批号:20140703,国药准字H14023686;小牛血清:浙江天杭生物科技有限公司,批号:130919;甲醇(分析纯),1%伊红染色液,Giemsa染液。CX2型OLYMPUS显微镜、电子天平、注射器、乳头吸管、解剖剪、镊子、灌胃针头。1.2 实验动物 清洁级健康ICR小鼠,体重18~20 g,购自扬州大学比较医学中心。动物生产许可证号:SCXK(苏)2007-0001,使用许可证号:SYXK(苏)2007-0005。小鼠自由采食和饮水,饲料和饮水均符合动物饲养标准。试验前在实验动物房环境中适应性饲养1周,灌胃前停食12 h,不限制饮水。
1.3 剂量设计及分组 ICR小鼠120只,精子畸形试验组60只,全部为雄性;骨髓微核试验组60只,雌雄各半。小鼠随机分为试验高、中、低剂量组,阳性对照组和阴性对照组,每组12只。沙咪珠利对小鼠经口染毒的半数致死量(LD50)≥5000 mg/kg,依据沙咪珠利LD50,试验时设2500 mg/kg(高)、1250 mg/kg(中)、625 mg/kg(低)3个剂量组。阳性对照组选用40 mg/kg环磷酰胺,阴性对照组选用无菌水[2,4]。
1.4 小鼠精子畸形试验 各试验组每天给药1次,连续5 d,首次给药后第35天颈椎脱臼法处死小鼠,每个试验组选用10只小鼠,取附睾制片。低倍镜找到背景清晰、精子重叠较少的部位,高倍镜下检查精子形态,每只动物检查1000个精子,对畸形精子进行分类计数并统计精子畸形率[4-6]。1.5 小鼠骨髓细胞微核试验 各试验组分别连续2次给药,间隔时间24 h,第二次染毒后6 h颈椎脱臼法处死小鼠,取胸骨骨髓制片,选择细胞完整、分散均匀、染色良好的区域在油镜下计数。每只动物计数1000个嗜多染红细胞(PCE),分别计算雌、雄小鼠各试验组的PCE/RBC比值和PCE微核率[4,5,7]。
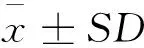
2 结果与分析
2.1 小鼠精子畸形试验 沙咪珠利的小鼠精子畸形试验结果见表1,从表中可以看出,沙咪珠利的三个剂量组的精子畸形率经统计学处理与阴性对照组比较,差异不显著(P>0.05),而阳性对照组与三个给药剂量组、阴性对照组比较,差异有统计学意义(P<0.01),差异极显著。

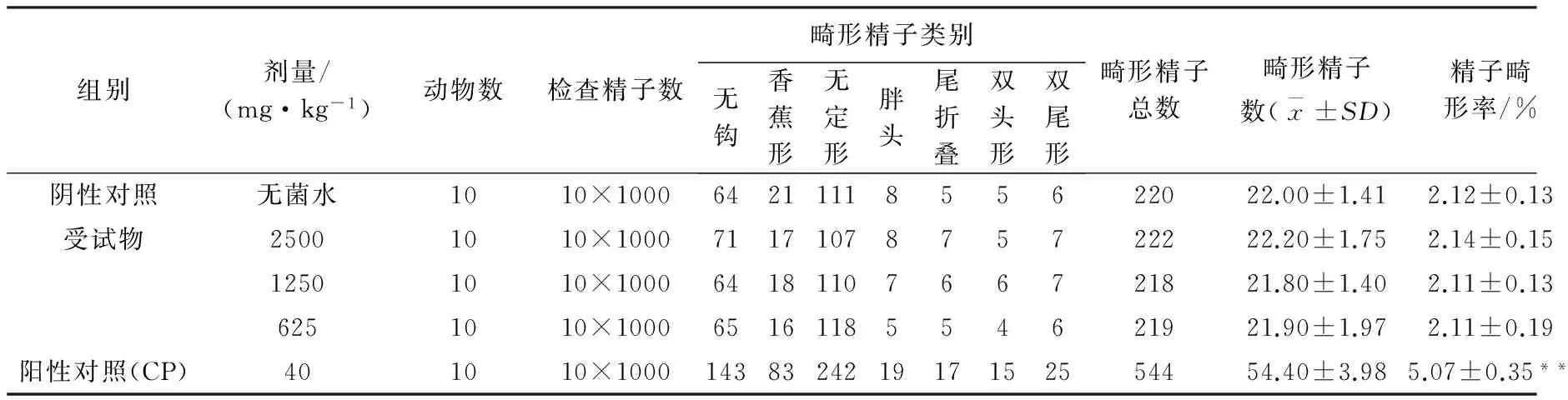
组别剂量/(mg·kg-1)动物数检查精子数畸形精子类别无钩香蕉形无定形胖头尾折叠双头形双尾形畸形精子总数畸形精子数(x±SD)精子畸形率/%阴性对照无菌水1010×10006421111855622022.00±1.412.12±0.13受试物25001010×10007117107875722222.20±1.752.14±0.1512501010×10006418110766721821.80±1.402.11±0.136251010×10006516118554621921.90±1.972.11±0.19阳性对照(CP)401010×1000143832421917152554454.40±3.985.07±0.35**
注:同列数据无肩标表示试验组与阴性对照组相比,差异不显著(P>0.05),**表示试验组与阳性对照组相比,差异极显著(P<0.01)。下同
2.2 小鼠骨髓嗜多染红细胞微核试验 实验结果见表2。各组嗜多染红细胞与成熟红细胞比值(PCE/RBC)在正常范围内。沙咪珠利三个剂量组雌、雄小鼠骨髓含微核嗜多染红细胞(PCE)率与阴性(溶剂)对照组比较,差异不显著(P>0.05),而阳性对照组与试验组、阴性对照组微核率比较(P<0.01),差异极显著,差异有统计学意义。受试物同一剂量组内雌、雄小鼠之间的微核无明显的性别差异。

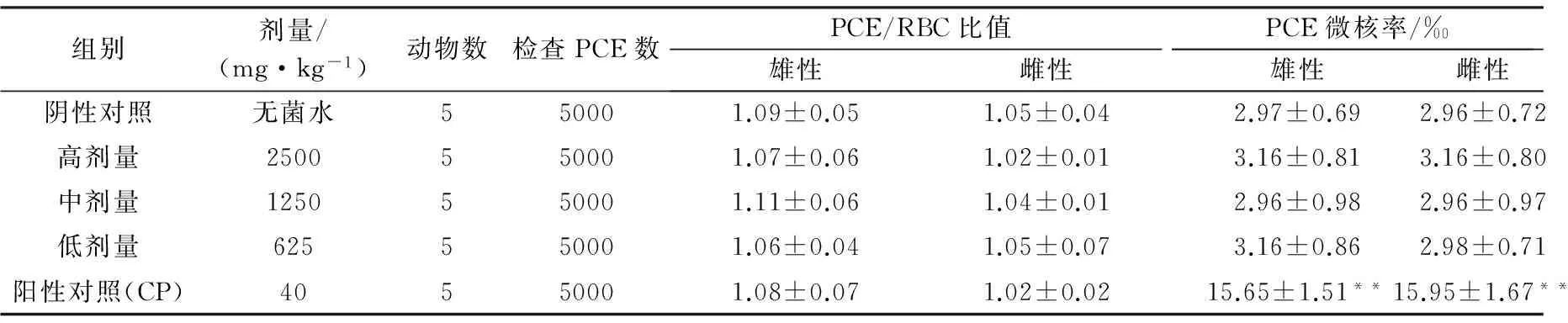
组别剂量/(mg·kg-1)动物数检查PCE数PCE/RBC比值PCE微核率/‰雄性雌性雄性雌性阴性对照无菌水550001.09±0.051.05±0.042.97±0.692.96±0.72高剂量2500550001.07±0.061.02±0.013.16±0.813.16±0.80中剂量1250550001.11±0.061.04±0.012.96±0.982.96±0.97低剂量625550001.06±0.041.05±0.073.16±0.862.98±0.71阳性对照(CP)40550001.08±0.071.02±0.0215.65±1.51**15.95±1.67**
3 讨论与小结
精子畸形是指精子的形状改变和畸形精子数量增多。正常情况下,人或哺乳动物的精液中可能存在少量畸形精子[8]。正常小鼠的精子畸变范围一般在0.8%~3.4%[9]。小鼠精子畸形试验可检测环境因子对精子畸形生成、发育的影响,而且对已知的生殖细胞致突变物有高度敏感性,故此实验适用于检测新型三嗪类抗球虫药沙咪珠利在体内对生殖细胞的致突变作用。不同品系小鼠的精子畸形率基础值差异较大,综合统计分析表明ICR小鼠自发畸变率低,更适合作为小鼠精子畸形试验材料[10]。从精子畸形实验结果可知,精子畸形主要发生在头部,类型主要是无定型和无沟型,与蒋英芝等[11]研究结果一致。沙咪珠利各剂量组的精子畸形率与阴性对照组比较差异不显著,而与阳性对照组比较差异极显著,差异有统计学意义,说明在本实验条件下,沙咪珠利对小鼠精子畸形无影响。冯秀娟[12]报道的妥曲珠利对小鼠精子畸形研究结果与本实验结果相似,张奥博等[13]报道的近年开发的新型三嗪类化合物纳川珠利对小鼠精子畸形研究也有相似结果。
微核的形成往往是受到细胞遗传毒物作用的结果,微核率的变化可反映所检测药物的遗传毒性。微核试验是新药、食品添加剂、农药、化妆品等毒理学安全性评价的必做试验[14]。余明泽等[15]研究表明胸骨骨髓的微核率高于股骨骨髓,染毒30 h的微核率高于24 h和48 h,故小鼠骨髓细胞微核试验可优先选用胸骨髓制片染毒30 h检测。从骨髓细胞微核试验结果可知,沙咪珠利各剂量组雌、雄小鼠骨髓含微核嗜多染红细胞(PCE)率与阴性(溶剂)对照组比较差异不显著,而与阳性对照组微核率比较差异极显著,且受试物同一剂量组内雌、雄小鼠之间微核无明显的性别差异。说明在本实验条件下,沙咪珠利不能引起小鼠骨髓细胞微核增加。
小鼠精子畸形和骨髓细胞微核试验均属于体内试验,遗传毒性试验同时还研究了沙咪珠利对体外中国仓鼠肺细胞染色体畸变的影响,实验结果显示受试物组与阴性对照组比较均无差异。因此可判断沙咪珠利不具有遗传毒性,此结果为沙咪珠利后续的毒理研究和临床应用研究提供了参考资料。
[1] 范 超. AC4的合成和有关物质研究[D].北京:中国农业科学院,2014.
[2] 肖文龙. 新型三嗪类抗球虫药沙咪珠利的一般毒理学研究[D]. 北京:中国农业科学院,2014.
[3] 张可煜, 李素梅, 王霄旸, 等. 大鼠粪便中抗球虫新药沙咪珠利的HPLC检测方法研究[J]. 中国动物传染病学报,2014,4:45-49.
[4] 农业部兽药评审中心. 兽药研究技术指导原则汇编 2006-2011年[M].北京:化学工业出版社,2012.
[5] 沈建忠. 动物毒理学[M]. 北京:中国农业出版社,2002.
[6] GB 15193.7-2003, 小鼠精子畸形试验[S].
[7] GB 15193.5-2003, 骨髓细胞微核试验[S].
[8] 李玖营, 沈明浩. 三氟氯氰菊酯对小鼠骨髓细胞微核及精子畸形和蓄积毒性的影响研究[J]. 中国畜牧兽医,2011,9:152-155.
[9] 欧仁福, 魏星华, 姜斌, 等. 磺胺氯吡嗪钠染毒小鼠精子畸形率及骨髓细胞微核的变化[J]. 毒理学杂志,2010,4:294-296.
[10]林健, 林蔚, 吴育文. 不同品系小鼠精子畸形基础值探讨[J]. 医学动物防制,2010,5:421-422.
[11]蒋英芝, 陈湘兵, 阎政礼, 等. 氯化镉对小鼠精子畸形的影响[J]. 湖南师范大学学报(医学版),2007,4:14-16.
[12]冯秀娟. 妥曲珠利毒性及抗鸡球虫效果研究[D].南京:南京农业大学,2005.
[13]张奥博,陈秀云,孙 庆, 等. 纳川珠利的小鼠精子畸形试验[A]. 中国毒理学会.中国毒理学会兽医毒理学与饲料毒理学学术讨论会暨兽医毒理专业委员会第4次全国代表大会会议论文集[C].中国毒理学会:,2012:1.
[14]吴占敖, 范利娟, 许华君, 等. 超细氯化钠粉的BALB/C小鼠骨髓微核实验[J]. 江苏大学学报(医学版),2013,1:9-11.
[15]余明泽, 刘以农, 蒋中仁, 等. 环磷酰胺诱导小鼠骨髓细胞微核的影响因素的研究[J]. 现代预防医学,2007,5:935-937.
(编辑:侯向辉)
Effects of Ethanamizuril on Sperm Deformity and Bone Marrow Cell Micronucleus of Mice
WANG Dong-liang1, NIE Qiao1, LI Long-fei1, LI Yu-chen1, CHEN Hong-yu1, CHEN Xiu-yun2, BU Shi-jin1
(1.VeterinaryMedicineCollege,YangzhouUniversity,Yangzhou,Jiangsu225009,China;2.MedicineCollege,YangzhouUniversity,Yangzhou,Jiangsu225001,China)
In order to evaluate the security of ethanamizuril, the sperm deformity and bone marrow cell micronucleus of ethanamizuril, healthy ICR mice were randomly divided into sample high group, sample medium group, sample low group, positive control group and negative control group, made sperm abnormality test and bone marrow micronucleus test, then calculated the sperm deformity rate and micronucleus rate. The results showed that ethanamizuril in each group was no statistical differences compared with negative control group (P>0.05). When compared with positive control group, the differences was statistically significant (P<0.01). Indicated ethanamizuril has no effect on sperm deformity and bone marrow cell micronucleus of mice, it has no genetic reproductive toxic to mice.
ethanamezuril; sperm deformity; bone marrow cell micronucleus
江苏高校优势学科建设工程(PAPD)
王东亮,硕士,从事兽医药理及毒理学研究。聂巧,硕士,从事兽医药理及毒理学研究,为共同第一作者。
卜仕金。E-mail:pushijin@aliyun.com
2016-02-24
A
1002-1280 (2016) 04-0045-03
S859.796
