多指标综合评价三七片的质量
2016-01-25吴群
吴群
(山东中医药大学附属医院, 山东 济南 250011)
多指标综合评价三七片的质量
吴群
(山东中医药大学附属医院, 山东 济南 250011)
摘要:用多指标综合评价法评价12个厂家生产的三七片的质量。采用热浸法、紫外分光光度法和高效液相色谱法,分别测定各厂家三七片的醇浸出物、总皂苷、人参皂苷Rg1、人参皂苷Rb1和三七皂苷R1的含量。获得了各样品中5个指标的测定结果,并换算出各样品的综合评价指标Y值,发现Y值存在明显差异。研究结果表明,不同厂家生产的三七片质量有差异,用多指标综合评价法,可以比较全面地评价三七片的质量。
关键词:综合评价法;三七片;醇浸出物;总皂苷;人参皂苷
三七为五加科植物三七(Panaxnotoginseng(BurK.)F.H.Chen)的干燥根和根茎,主产于云南、广西等地,野生或栽培。其性甘、微苦、温,主入肝、胃、大肠经,具有散疲止血、消肿定痛的功效[1-3],其中达玛烷型四环三萜类皂苷被认为是三七的主要生理活性成分之一。三七片以三七粉碎成细粉, 加适量辅料, 制成颗粒, 压片即得[1]。三七片生产工艺简单,其原材料的优劣严重影响制剂的疗效,市场上三七片质量和价格差异较大。目前,三七片的质量控制方法主要是采用高效液相色谱法[4-5]测定3种主要皂苷的含量,难以全面反应三七片的质量特点,有关市场上销售的三七片质量状况的相关文献未见报道。为此,本研究参照相关标准,采用热浸法、紫外分光光度法[6-7]和高效液相色谱法,选取醇浸出物、总皂苷、人参皂苷Rg1、人参皂苷Rb1和三七皂苷R15个指标来综合评价三七片的质量,并用于对12个厂家生产的三七片的质量评价,为全面控制三七片的质量提供方法和数据支持。
1 材料与仪器
1.1材料
甲醇(色谱纯,天津四友精细化学品有限公司);乙腈(色谱纯,美国天地有限公司);实验用水为Milli-Q 超纯水(18 MΩ),其余试剂为分析纯。
对照品(中国药品生物制品鉴定所):三七皂苷R1(批号110745-200415);人参皂苷Rg1(批号11703-200726);人参皂苷Rb1(批号11704-200420);三七对照药材(批号120941-200506)。样品三七片来源信息见表1。

表1 三七样品来源
1.2仪器
Waters 515-717-2487高效液相色谱仪,600自动进样器,Waters-996二极管阵列检测器,Empower工作站(美国沃特世公司);色谱柱Kromasil C18柱(200 mm×4.6 mm,5 μm),岛津UV-FW265型紫外可见分光光度计(日本岛津公司);FW-177中草药粉碎机(天津泰斯特仪器有限公司);BP211D赛多利斯十万分之一天平(德国赛多利斯集团);LC-350A超声波中药处理机(济宁市中区鲁超仪器厂)。
2 实验方法与结果
2.1醇浸出物含量测定
照醇溶性浸出物测定法[8]项下的热浸法测定,分别取样品及三七药材2.0 g,精密称定置100 mL圆底烧瓶中,加50 mL乙醇,密闭,放置1 h后,水浴微沸1 h,冷却,称定重量,用乙醇补足重量,过滤,取滤液10 mL置于干燥至恒重的蒸发皿中,挥干,放置于烘箱中,105 ℃干燥3 h,取出,置干燥器中冷却,称量。依据要求,对12个样品及三七药材进行醇浸出物含量测定,见表2。
2.2总皂苷含量测定
2.2.1试液的制备
2.2.1.1对照品溶液的制备
取三七药材,精密称定0.3 g,置于50 mL容量瓶中,准确加入乙醇20 mL,放置过夜,置80 ℃水浴上保持微沸2 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,精密量取0.6 mL,置于25 mL的容量瓶中,用乙醇定容,待测。
2.2.1.2供试品溶液的制备
取样品,精密称定0.4 g,其余步骤同2.2.1.1。
2.2.2测定波长的选择
取三七对照药材待测液,在波长400~190 nm间扫描,其最大吸收波长203 nm与文献[8]相关项下规定的203 nm一致。
2.2.3标准曲线的绘制
精密量取对照品溶液0.50、0.75、1.00、1.25、1.50 mL置蒸发皿内挥干,用乙醇定容于25 mL容量瓶中待测,在203 nm波长测定吸收度。以吸收度为纵坐标,以浓度为横坐标,绘制标准曲线,得回归方程为Y=32.118X-0.755 9,R=0.999 5。
2.2.4测定方法
取所有样品的待测液,以乙醇作为参比溶液,在波长203 nm处,以岛津UV-FW265型紫外可见分光光度计测定吸光度,并计算含量。
2.2.5精密度实验
对同一浓度的总皂苷溶液(湖北)连续测定5次,RSD=0.75%,说明该方法的精密度良好。
2.2.6稳定性实验
取1份供试品,室温放置,分别测定其在0.5、1、2、4、6 h时的含量,X=6.050%,RSD= 0.91%。结果表明,供试品溶液中总皂苷在6 h内相对稳定。
2.2.7重复性实验
随机抽取样品(湖北),精密称定6份,按照2.2项下的方法进行实验,X=6.038%,RSD=0.36%。表明本实验重复性良好。
2.2.8含量测定
经上述方法学研究表明,采用上述条件测定总皂苷的方法可行,遂对12个不同厂家的样品按上述方法进行处理、测定,结果见表2。
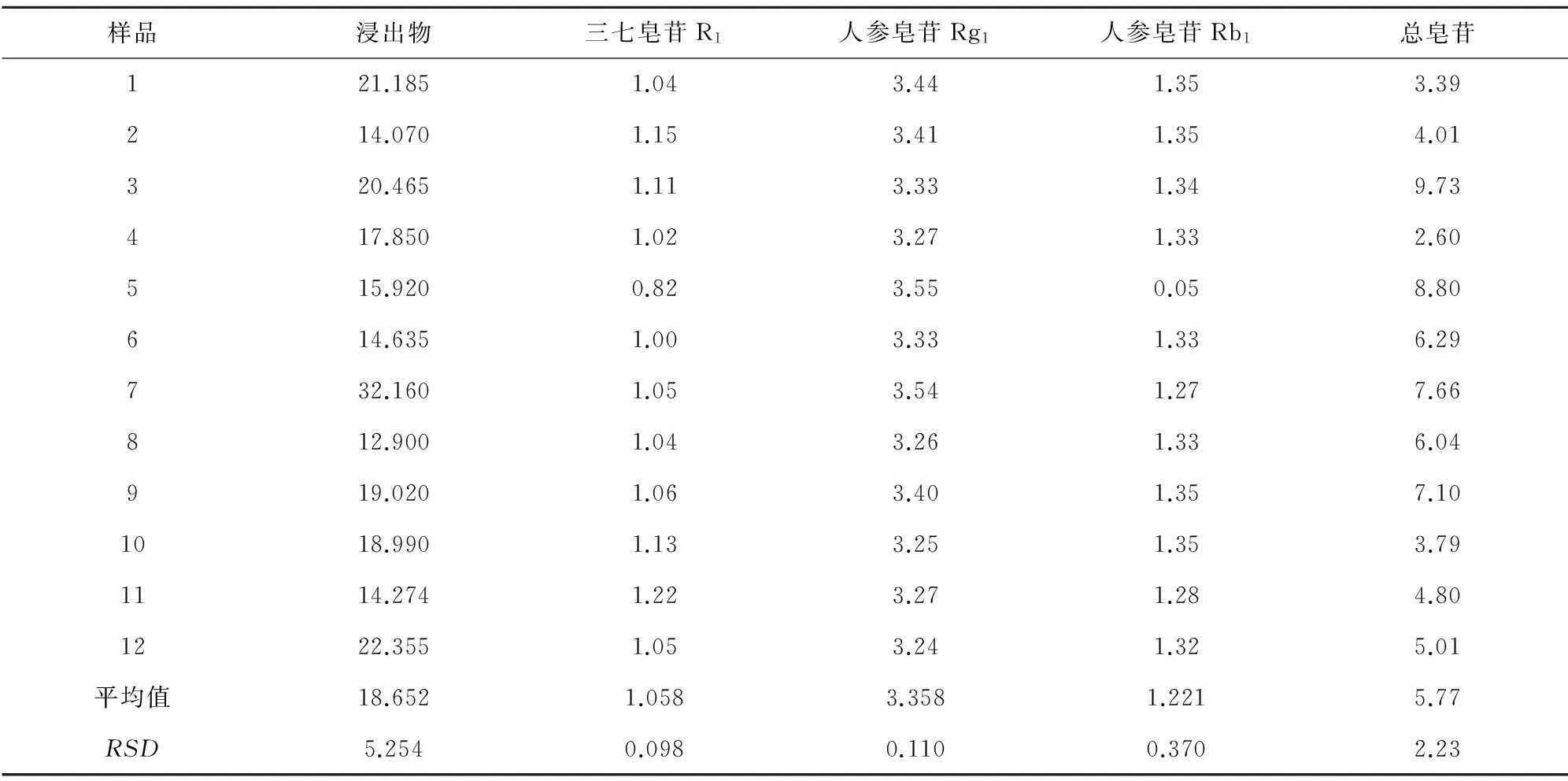
表2 5种指标的测定值(%)
2.33种皂苷类成分含量测定
2.3.1溶液的制备
2.3.1.1对照品溶液的制备
精密称取对照品适量,加甲醇制成每毫升含人参皂苷Rg10.4 mg、人参皂苷Rb10.4 mg、三七皂苷R10.1 mg的混合对照品溶液,备用。
2.3.1.2供试品溶液的制备
取各供试品粉末0.6 g,精密称定,精密加入甲醇25 mL,称定重量,放置过夜,置80 ℃水浴上保持微沸2 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3.2色谱条件
色谱柱:Kromasil ODS C18柱(250 mm×4.6 mm,5 μm),乙腈-0.05%磷酸溶液(21.5:78.5,V/V)为流动相,检测波长为203 nm,进样量20 μL,流速为1.0 mL/min,柱温32 ℃。时间(min):0~12, 12~30, 30~60;流动相A(%):19→19,19→36,36→80;流动相B(%):81→81,81→64,64→20。

1 三七皂苷R1 2 人参皂苷Rg1 3 人参皂苷Rb1图1 3种对照品的HPLC图谱Fig.1 HPLC spectra of 3 kinds of references

1 三七皂苷R1 2 人参皂苷Rg1 3 人参皂苷Rb1图2 三七片的HPLC图谱Fig.2 HPLC spectra of Sanqi tablets
2.3.3线性关系的考察
分别精密吸取混合对照品溶液1.0、2.0、3.0、4.0、5.0 mL,置10 mL容量瓶中,加甲醇至刻度,摇匀,进样量20 μL,按2.3.2色谱条件进行分析,记录各峰所对应峰面积,以对照品峰面积为纵坐标,以对照品进样量为横坐标,绘制标准曲线(表3)。从表3可以看出,3种化合物标准曲线的线性关系良好,线性范围较宽,可以满足定量测定的要求。
2.3.4精密度实验
在2.3.2色谱条件下,对同一浓度的溶液连续5次进样,记录峰面积,三七皂苷R1的RSD为0.87%,人参皂苷Rg1的RSD为0.98%,人参皂苷Rb1的RSD为1.04%,n=5。结果表明,仪器精密度良好。
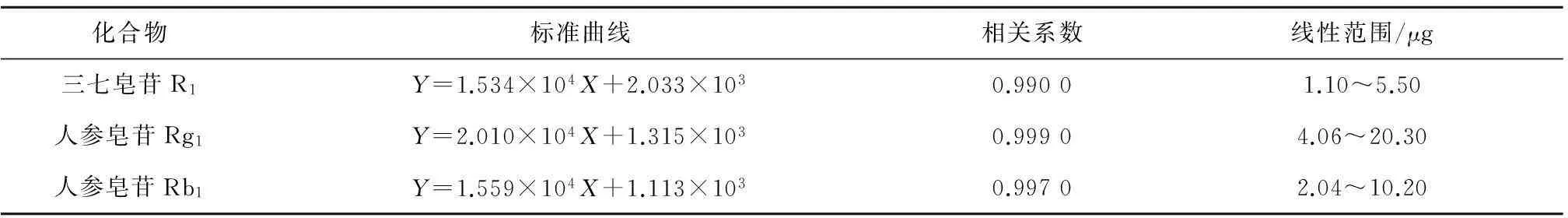
表3 标准曲线
2.3.5稳定性实验
取同一份供试品溶液,室温放置,分别在0、1、2、4、6 h进样,测定峰面积,得三七皂苷R1的RSD为0.92%,人参皂苷Rg1的RSD为0.22%,人参皂苷Rb1的RSD为1.54%,n=5。结果表明,供试品溶液在6 h内稳定。
2.3.6含量测定
以人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1为指标,测定12个厂家的三七片中皂苷的含量。分别精密吸取对照品溶液与供试品溶液各20 μL,注入液相色谱仪,测定,取平均值,即得(见表2)。
2.4综合评分值
将醇浸出物、三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1、总皂苷5个指标,按下列公式分别进行标准化处理


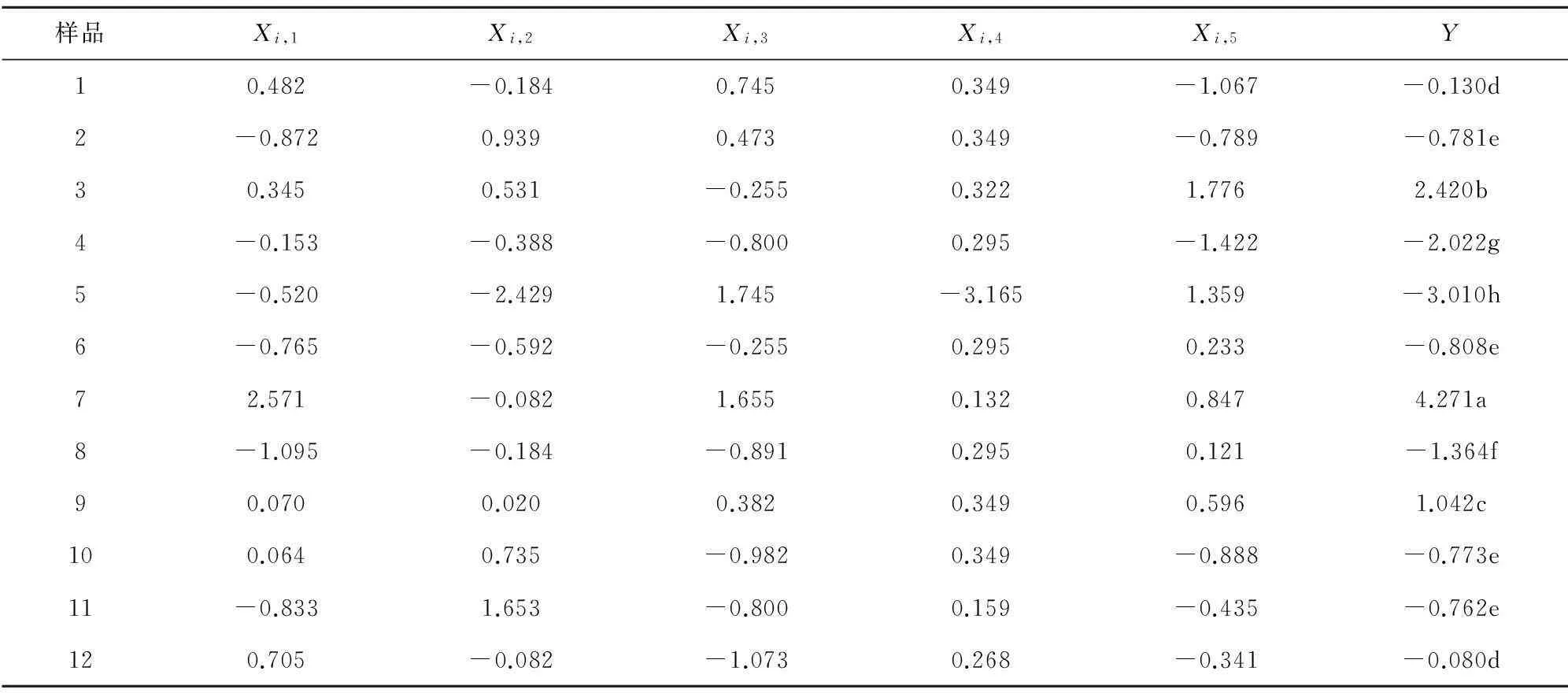
表4 5种指标的标准化值和Y值
注:不同字母间表示有显著性差异(P<0.05)。
从表4可以看出,12个厂家的三七片Y值存在明显差异,其由大到小依次为广西1、武汉1、芜湖、江苏、武汉2、四川、杭州、吉林1、广西2、湖北、吉林1和山东。
3讨论
本研究采用热浸法、紫外分光光度法和高效液相色谱法,分别测定12个厂家三七片的醇浸出物、总皂苷、人参皂苷Rg1、人参皂苷Rb1和三七皂苷R1的含量,根据各结果换算出的综合评价指标来评价各厂家生产的三七片的质量。该方法简单、准确,可以较为全面地反映三七片的质量特征,为三七片的质量评价提供了方法支持。
对12个厂家生产的三七片中5个指标的数据进行标准化处理,消除了各指标的单位和量纲的不同,以及各指标变量范围相差悬殊所造成的影响;同时根据各指标在工艺选择中的主次,给予不同的加权系数,以标准化指标加权后求和作为综合评判指标,可以更科学合理地评价三七片的质量。
另外,本实验结果表明,不同厂家生产的三七片质量有显著差异。建议各生产厂家加强三七药材原料及生产过程中的质量控制水平,以保证三七片质量稳定、可靠。
参考文献:
[1]徐冬英.三七名称及其有文字记载时间的考证[J].广西中医学院学报, 2000,17(3):91-92.
[2]黎跃东,张振国.三七临证用法概要[J].中华医学全科杂志,2003,2(6):89-90.
[3]苏雁涛.诌议三七[J].当代医学,2005,15(13):25.
[4] 宋杰,李俊,李伟琪.HPLC法测定消瘀胶囊中人参皂苷Rg1、Rb1和三七皂苷R1的含量[J].山东中医药大学学报,2014,38(5):492-494.
[5] 邹汉法,张玉奎,卢佩章.高效液相色谱法 [M].北京:科学出版社,1998:15.
[6] 刘英,曲媛,崔秀明,等.文山、红河三七花皂苷含量的比较研究[J].云南大学学报:自然科学版,2014,36(5):734-739.
[7]陈旭,党晓芳,曹飒丽,等.三七中总皂苷含量测定的对照品筛选[J].中国实验方剂学杂志,2013,19(7):66-68.
[8]国家药典委员会.中华人民共和国药典2010版一部[M].北京:中国医药科技出版社,2010:450.
【中药与天然活性产物】
Multi-index comprehensive evaluation for Sanqi tablets quality
Wu Qun
(Affiliated Hospital of Shandong University of Traditional Chinese Medicine,Jinan 250011,China)
Abstract∶We evaluate the quality of Sanqi tablets from 12 manufacturers by multi-index comprehensive evaluation method.We determine the contents of Sanqi tablets alcohol extract, total saponins, Rg1saponins, panax ginseng and panax Rb1saponins, ginsenosides R1by hot dipping, UV spectrophotometry, and HPLC.We further acquire determination results of the five indexes and comprehensive index Y.Obvious distinction exists for the index Y.Results show that the quality of Sanqi tablets different for different manufacturers.Multi-index comprehensive evaluation method can be applied to comprehensive evaluation for the quality of Sanqi tablets.
Key words∶comprehensive evaluation method;Sanqi tablets; alcohol extract; notoginseng;Panax notoginseng saponins
中图分类号:R284.1
文献标识码:A
文章编号:1002-4026(2015)04-0019-06
作者简介:吴群(1971-),女,主管药师,研究方向为中药制剂与质量控制。Email:1192685147@qq.com
基金项目:山东省中医药科技发展计划(2014094)
收稿日期:2015-05-05
DOI:10.3976/j.issn.1002-4026.2015.04.004
