钼酸盐钝化碳钢的缓蚀性能研究
2015-12-31王海峰唐昌健田仁宇
雷 霞, 王海峰, 何 玲, 唐昌健, 田仁宇, 阚 健
(贵州大学材料与冶金学院,贵州 贵阳 550025)
引 言
铬酸盐钝化因为具有成本低廉,且钝化处理后的钝化膜层具有较好的附着性和耐腐蚀性,所以长期被用于镀锌钢板以及各类合金的防腐蚀钝化处理。然而,铬具有剧毒且是“三致”物质,是世界各国都严格控制的重金属之一。因此,寻找低毒(甚至无毒)的钝化液来替代铬酸盐钝化是目前钝化技术发展的趋势。
本文以钼酸盐为主成膜剂,在有机和无机添加剂的辅助作用下对碳钢进行钝化,经过腐蚀实验及电化学实验研究钝化液pH值和温度对钝化效果的影响。
1 钼酸盐缓蚀机理
在钼酸盐中,Mo6+常以八面配位体聚合成同多酸或杂多酸离子,这些络合负离子在一定条件下具有固定的相对分子质量和结构[1]。钼酸盐钝化机理是通过在金属表面发生吸附、沉积作用,或通过膜离子的选择性及自身的氧化作用形成不溶性的物质沉积在金属的表面,以此来改变金属表面膜的性质,形成化学性非常稳定、致密且附着力好的钝化膜,从而削弱Cl-交换氧化膜中氧,以抑制金属的溶解及点蚀的扩散和蔓延,增强膜层抗腐蚀能力的作用[2-5]。MoO2-4是一种弱氧化剂,在钢铁钝化中与碳钢基体反应过程为:
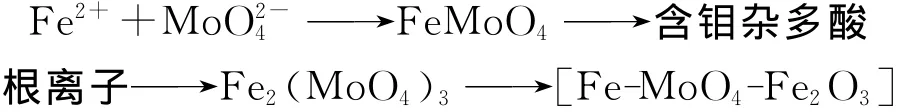
[Fe-MoO4-Fe2O3]为钼酸盐钝化钢铁最终产物,即钝化膜的主要成分。钼酸根离子不仅可吸附在活性溶解的金属表面上,而且能吸附在钝化膜的缺陷处或者进入氧化膜并与之共同作用[6-9]。
2 实验部分
2.1 原料及仪器
Q235钢,钢片规格:30mm×30mm×3mm、10mm×10mm×3mm,打磨光滑。
电化学工作站:上海华辰CHI660D、恒温水浴锅、电吹风、恒温烘干箱。
钼酸钠(分析纯),其他试剂。
2.2 实验方法
1)钝化实验:按照配方配制钝化液,将试样用酸(盐酸42mL、硫酸13mL、硝酸35mL)进行酸洗除锈,再用蒸馏水洗去残酸后,放入配制的钝化液中进行钝化。钝化完成后,取出空置、水洗、恒温烘干,以待进行腐蚀实验。
2)CuSO4点滴实验:向钝化试样上滴加几滴3g/L CuSO4溶液,记录碳钢被腐蚀的时间,并观察腐蚀情况。
3)NaCl浸泡实验:将钼酸盐钝化试样置于装有200mL 5%NaCl溶液中,室温浸泡,观察并记录腐蚀情况。
4)电化学实验操作:选择循环伏安法,在扫描电位范围-0.5V~1.6V、扫描速度2mV/s下进行伏安特性测试。
3 结果与讨论
3.1 pH值对耐腐蚀性能的影响
3.1.1 不同pH值下钼酸盐钝化碳钢的缓蚀性能
保持其他工艺条件不变,改变钝化液pH值,对碳钢进行钝化。pH值较低时,钝化过程中碳钢表面反应激烈,钝化膜颜色较深;随着pH值的升高,钝化膜的颜色加深;当pH≥5.0时,由于钝化液中存在硫酸锌,所以钝化液有沉淀产生,影响钝化效果。对不同pH值下的钝化膜进行附着力测试,结果见表1。表1表明,pH值为3.0时,膜的附着力最强。

表1 不同pH值下的附着力
CuSO4点滴实验结果如图1所示。NaCl浸泡实验结果如图2所示。

图1 硫酸铜点滴实验

图2 氯化钠浸泡实验
图1可知,随着pH值的增加,腐蚀出现时间和腐蚀变黑时间显著增加;当pH值在3.0左右时,腐蚀出现时间和腐蚀变黑时间基本达到最大值,此时缓蚀效果最好;随着pH值继续增加,腐蚀出现时间趋于平缓,腐蚀变黑时间反而缩短。图2可知,相对于其他试样,在5%NaCl中浸泡相同时间时,pH值为3.0的钝化试样腐蚀率都相对较低。
综上所述,pH值在3.0左右时,钼酸盐碳钢钝化膜易于形成,且膜层稳定,耐腐蚀能力达到最佳,缓蚀性能最好。
3.1.2 伏安特性曲线
在5%NaCl溶液腐蚀介质中,对不同pH值钝化所得到的钝化膜进行循环伏安特性测试,见图3。
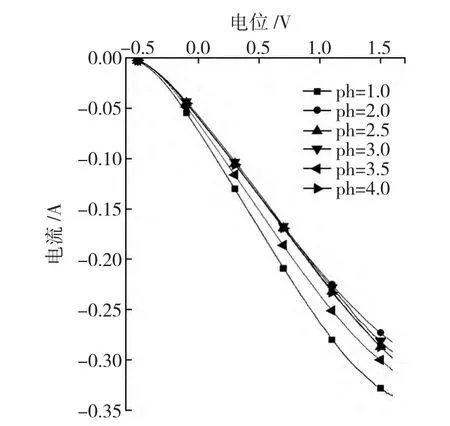
图3 电化学伏安特性曲线
从电流-电压图曲线看,钝化后的碳钢,电流随着电压的增加而降低。钝化液pH值在1.0左右时,电流降得最快;钝化液pH值在2.5~3.5时,电流下降较慢。电压的升高,不仅加快了铁的溶解速度,而且加快了钝化膜的溶解速度,破坏了钝化膜层,导致金属表层导电性能减弱,通过的电流降低。
当钝化液pH<2.0时,试样与钝化液反应剧烈,产生大量气体,反应后的碳钢表面呈暗黑色。由于此时钝化液中的磷酸含量较高,所以钝化后的表面状态与磷化处理相似。而当钝化液pH>4.0后,由于Fe会反应生成较稳定的Fe(OH)3沉积在Fe表面,阻碍Fe的溶解,从而阻碍了钝化膜的形成和生长,使钝化膜成膜困难或不能成膜,所以钝化处理效果变差。
由图3可知,pH≈3.0时,随着电压的增加,电流下降最慢,亦即其钝化膜的导电性能最好,耐腐蚀效果最好。
3.2 钝化液温度对耐腐蚀性能的影响
3.2.1 不同钝化温度下钼酸盐钝化碳钢的缓蚀性能
确定pH值为3.0及其他条件不变,改变钝化液温度,观察碳钢耐蚀性的变化。结果表明,随着温度的升高,反应加快,颜色由浅到深,附着力(见第11页表2)逐渐增强;但温度过高后,膜层会被破坏,导致附着力下降,耐腐蚀性能也随之下降。
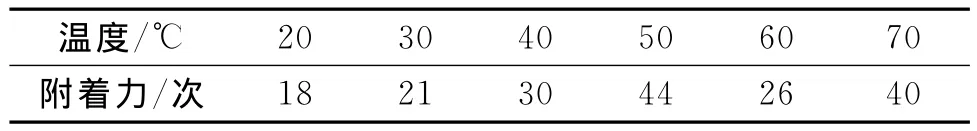
表2 不同温度下的附着力
CuSO4点滴实验和NaCl浸泡实验结果分别如图4、图5所示。
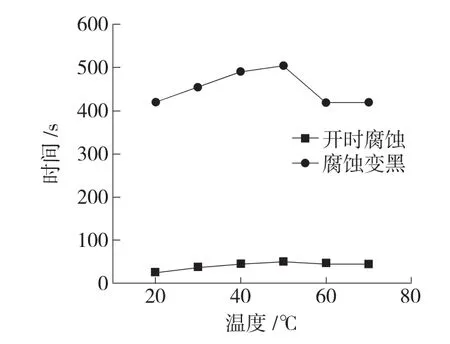
图4 硫酸铜点滴实验
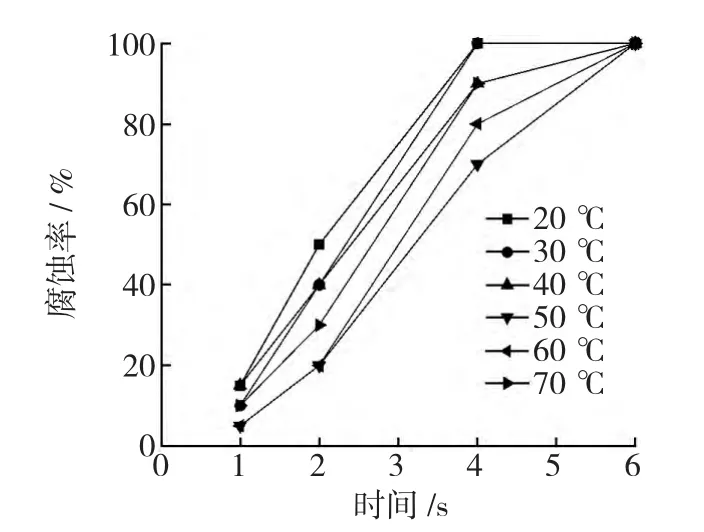
图5 氯化钠浸泡实验
由图4、图5可知,50℃下钝化的碳钢耐蚀性较好,腐蚀时间较其他试样慢。由于钼酸盐钝化膜生长到一定厚度后会出现裂纹,且钝化温度越高,钝化膜生长越快,裂纹产生和扩展也越快,所以,随着温度的继续升高,裂纹开始出现,使钝化膜耐腐蚀能力降低,钼酸盐钝化试样的缓蚀性下降。因此,50℃左右的钼酸盐碳钢钝化膜耐蚀性最强。
3.2.2 伏安特性曲线
在5%NaCl溶液腐蚀介质中,对不同温度下钝化所得到的钝化试样测试电化学伏安特性曲线,结果见图6。
从电流-电压图曲线看出,钝化后的碳钢,电流随着电压的增加而降低。当钝化温度为20℃时,电流降得最快。电压的升高,不仅加快了铁的溶解速度,而且加快了钝化膜的溶解速度,破坏了钝化膜层,导致金属表层导电性能减弱,通过的电流降低。
随着钝化温度的升高,金属表层铁的溶解速度加快,促进铁离子与钝化液中的钝化剂反应,钝化膜生长就越快。但是,温度达到临界值时,裂纹产生和扩展速度也越快。
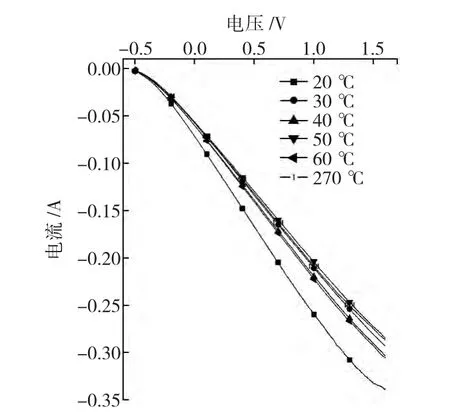
图6 电化学伏安特性曲线
当钝化温度在50℃时,随着电压的增加,电流下降最慢,其钝化膜的导电性能最好,耐腐蚀效果也最好。
4 结论
钼酸盐作为主成膜剂,添加相应的无机和有机添加剂以辅助成膜,其钝化液对碳钢的钝化效果较好,有利于提高碳钢的缓蚀性能。温度在50℃、pH=3时,钼酸盐钝化碳钢形成的膜层稳定且均匀,耐腐蚀性能较强,最有利于提高碳钢缓蚀性能。
[1] 吴水清.钼酸盐在表面处理工业中的应用[J].电镀与精饰,1994,13(3):56.
[2] 路长青.钼酸盐的缓蚀机理[J].材料保护,1996,29(10):22-23.
[3] 王瑛,柴明成,王宇友.钼酸盐与其他缓蚀剂协同缓蚀效应的研究[J].上海化工,2003(7):23-25.
[4] 李宇春.钼酸盐缓蚀剂在自来水中的电化学行为[J].材料保护,2001,34(7):10-12.
[5] 李玉明.钼酸盐缓蚀剂的机理与性能的影响因素[J].衡阳师范学院学报,2004,25(6):59-61.
[6] 郝建军,安成强,刘常升.不同添加剂对镀锌层钼酸盐钝化膜腐蚀电化学性能的影响[J].材料保护,2006,39(10):23-25.
[7] 房娟娟,许斌.钼酸盐缓蚀剂研究进展及发展趋势[J].山东化工,2008,11(37):17.
[8] 李玉明,陈志敏,蒋书怡.钼酸盐复配绿色缓蚀剂的研究[J].衡阳师范学院学报,2008,29(6):61.
[9] 叶德霖.钼酸盐缓蚀剂的性能[J].工业水处理,1995,15(4):4-5.
