罗丹明类小分子荧光探针对水中Hg2+检测的比较研究
2015-12-25吕向菲霍霄楠胡南江
吕向菲, 李 婷, 霍霄楠, 胡南江, 闫 蕾,
李国荣1, Ermelinda Bloise4
(1.陕西科技大学 资源与环境学院, 陕西 西安 710021; 2.陕西科技大学 轻工与能源学院, 陕西 西安 710021; 3.国家知识产权局专利局专利审查协作北京中心 材料工程发明审查部, 北京 100096; 4.Department of Engineering for Innovation, University of Salento, Italy Lecce 73100)
罗丹明类小分子荧光探针对水中Hg2+检测的比较研究
吕向菲1,4, 李婷1, 霍霄楠1, 胡南江2, 闫蕾3,
李国荣1, Ermelinda Bloise4
(1.陕西科技大学 资源与环境学院, 陕西 西安710021; 2.陕西科技大学 轻工与能源学院, 陕西 西安710021; 3.国家知识产权局专利局专利审查协作北京中心 材料工程发明审查部, 北京100096; 4.Department of Engineering for Innovation, University of Salento, Italy Lecce 73100)
摘要:将罗丹明B(RhB)及罗丹明6G(Rh6G)应用于水中Hg2+的荧光猝灭法测定.在KI存在时,Hg2+可与罗丹明类小分子及KI形成多元离子缔合物,故在水中可直接利用体系的荧光发射峰强度测定Hg2+.通过比较两种罗丹明类荧光探针的检测特性发现,两种罗丹明类小分子都是荧光检测特性较好的猝灭型探针,其中罗丹明6G由于其分子结构稳定性大,故灵敏性、线性范围和选择性均高于罗丹明B.
关键词:荧光猝灭; 罗丹明B; 罗丹明6G
0引言
汞离子具有持久性、易迁移性、高毒性和高度的生物富集性等,其进入水体环境后可借助细菌的作用而形成有机汞,从而进一步危害人类健康.美国国家环境保护局规定饮用水中无机汞的最高浓度为2 ppb[1]; ROHS表明欧盟自2006年7月1日起投放欧盟市场的电子电器设备中不得含有汞;我国对生活饮用水中总汞含量规定必须小于1 mg/L[2].
据《2013年上半年全国环境质量状况》报告显示:我国当前地下水源面临严重的汞污染, 12个地表水国控断面出现22次重金属超标,其中以汞的超标频次最多[3].因此,寻找高效、廉价、简洁的汞离子检测手段已成为重要的研究课题.在各种检测技术中,荧光探针检测法具有便捷、灵敏度高、样品无损、高效筛选及实时、原位检测等优点,因而成为水中汞离子检测的热点研究方法[4].
目前,用于汞离子检测的荧光探针分子主要有:香豆素、芘、萘类、双吡啶、方酸菁、氧杂蒽类(包括罗丹明类衍生物和荧光素)等[5-7].其中,罗丹明类荧光探针具有优异的光物理特性,借助其分子开环反应前后螺内酯到螺内酰胺的结构变化,显示出了极强的荧光现象和颜色变化,成为了主要的检测探针[8].
大部分用于水体汞离子检测的荧光探针是以罗丹明B和罗丹明6G为基础结构而进行的改性衍生物[9,10].从结构上对不同罗丹明类荧光探针的检测特性进行比较的研究还比较少,如果选择结构相似的罗丹明类荧光探针,分析其检测特性,并从结构角度分析其荧光差异,将有助于设计出具有更高灵敏度及选择性的探针分子.
因此,本文选择罗丹明B和罗丹明6G用于检测水体中痕量的Hg2+,并在不同条件下比较各自的检测灵敏度,得到了其分子结构与Hg2+荧光光谱的相关性,还分析了其可能的原因,这为进一步设计罗丹明类荧光探针提供了理论依据.
1实验部分
1.1试剂和药品
罗丹明B和罗丹明6G(北京百灵威科技有限公司);Tris、碘化钾(广东光华化学有限公司);磷酸、抗坏血酸、氯化汞和硝酸铅(天津市天力化学试剂有限公司);盐酸(天津市福晨化学试剂厂);氯化铜、氯化锌(分析纯,天津市科密欧化学试剂研发中心);去离子水(利用优普超纯水UPH-Ⅱ-5/10/20T系统制备得到,电导率为18.2 MΩ·cm).
1.2实验仪器
紫外-可见光谱仪Cary 300型(美国通用公司);恒温水浴箱(上海兰科股份有限公司);荧光分光光度计F4600型(日本日立高新技术公司);电子天平 BS224S型(北京赛多利斯仪器系统有限公司).
1.3实验方法
(1)Hg2+储备液:称取0.006 8 g的氯化汞用pH为7.40的tris-HCl溶液定容于50 mL的容量瓶中,得到5×10-4mol/L的HgCl2溶液.
(2)罗丹明6G储备液:称取0.24 g的罗丹明6G,用二次去离子水定容于100 mL容量瓶中,即为5×10-4mol/L的罗丹明6G溶液.
(3)碘化钾-抗坏血酸( KI-VC )混合溶液:取分析纯碘化钾20 g、抗坏血酸2 g溶解后,定容至100 mL容量瓶中.
(4)1.33 mol/L H3PO4溶液:用移液管移取9.1 mL浓磷酸用二次去离子水定容于100 mL容量瓶.
(5)罗丹明6G对Hg2+的检测:在25 mL容量瓶中,首先加入适量汞离子储备液,再加入5 mL 1.33 mol/L磷酸溶液, 稀释至10 mL,依次加入1 mL碘化钾-抗坏血酸( KI-VC )混合溶液、0.5 mL 5×10-4mol/L 罗丹明6G溶液,混合均匀用tris-HCl溶液稀释至25 mL,于发射波长处测其荧光强度.
罗丹明B检测汞离子方法与上述步骤类似.
(6)干扰离子的检测:于25 ℃下罗丹明6G(罗丹B)-Hg2+(10-6mol/L)体系中加入Zn2+、Cu2+、Cd2+、Pb2+等作为干扰离子,考察两种探针的抗干扰能力.配制方法为(以罗丹明6G为例,罗丹明B类似):在25 mL容量瓶中依次加入罗丹明6G溶液、5 mL 1.33 mol/L磷酸溶液、1 mL碘化钾-抗坏血酸( KI-VC )混合溶液、HgCl2溶液,摇匀后再加入干扰离子(干扰离子浓度为:Cu2+,10-5mol/L;Zn2+,10-4mol/L;Cd2+,10-4mol/L;Pb2+,10-4mol/L ),用蒸馏水稀释至刻度,摇匀后检测体系荧光光谱.
实际水体中Hg2+的检测,与上述方法类似,不同的地方是将HgCl2换成实际水样.
2结果与讨论
2.1罗丹明B与罗丹明6G的光谱特性
图1与图2分别是25 ℃下1×10-5mol/L 罗丹明B与罗丹明6G的紫外可见吸收和荧光发射检测图.由图1~2可知,罗丹明B的紫外-可见最大吸收峰位于483 nm;罗丹明6G的紫外-可见最大吸收峰位于526.5 nm.在荧光检测过程中,为了比较两者的光谱特性,选择400 nm 的紫外光作为激发光,得到了两种探针的荧光发射光谱.罗丹明B的荧光发射特征峰为591.2 nm;罗丹明6G的荧光发射特征峰为558.2 nm.经比较发现,相同条件下罗丹明6G的荧光发射峰强度明显高于罗丹明B,这表明在后续的检测过程中,罗丹明6G荧光探针更灵敏.且两种探针的紫外-可见吸收光谱与荧光发射光谱呈镜像,说明它们均具有很好的荧光检测特性.

图1 罗丹明B的紫外可见吸收与荧光发射光谱图

图2 罗丹明6G的紫外可见吸收与荧光发射光谱图
2.2不同温度下荧光探针对Hg2+的检测比较
文献[11]表明,温度会影响罗丹明荧光检测体系的荧光强度.因此,选择了1×10-5mol/L罗丹明探针检测1×10-6mol/L Hg2+体系作为对象,分别测定了该系统在水浴温度为15 ℃、20 ℃、25 ℃和30 ℃下,两种不同体系荧光发射峰的强度变化,分别如图3和图4所示.由图3~4可知,罗丹明B-Hg2+体系荧光强度先降低后升高,在25 ℃时的荧光强度最低;而罗丹明6G-Hg2+体系的荧光强度随温度一直降低,在30 ℃时的荧光强度最低.该结果说明,在研究者所在的西安地区全年大部分温度范围内都可利用罗丹明类分子进行Hg2+的检测,对于罗丹明B分子在夏季具有更灵敏的检测特性,而对罗丹明6G分子在春秋两季的检测性更高.

图3 温度对罗丹明B检测Hg2+荧光强度的影响
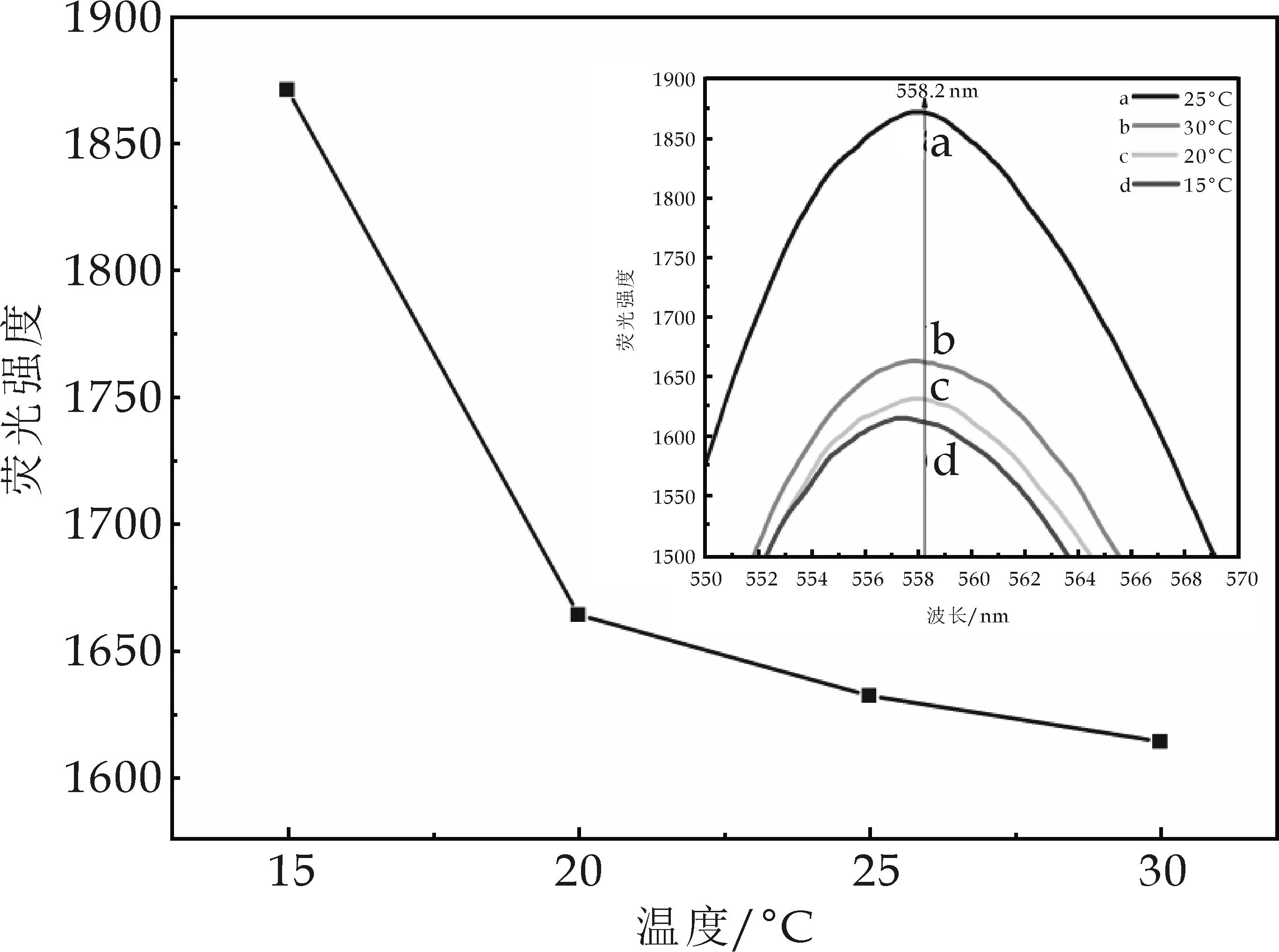
图4 温度对罗丹明6G检测Hg2+荧光强度的影响
2.3检出限及线性范围比较
选择在25 ℃下,绘制汞离子标准曲线,测定了Hg2+浓度从1×10-8mol/L到1×10-5mol/L范围内,罗丹明B及罗丹明6G识别体系荧光强度的变化图,其结果见图5及图6所示.
由图5可知,在25 ℃下,Hg2+浓度在0~0.000 001 mol/L范围内,罗丹明B的荧光强度均与Hg2+浓度呈现良好的线性关系,R2为0.983 1;由图6可知,在25 ℃下,Hg2+浓度在0~0.000 01 mol/L范围内,罗丹明6G的荧光强度均与Hg2+浓度呈现良好的线性关系,R2为0.991 9.这表明两种探针都可用于水体痕量Hg2+的检测,且罗丹明6G的检测精度更高.
同时,通过拟合直线斜率发现,两种探针都属荧光猝灭型探针,根据文献[12]的计算方法,可知罗丹明B和罗丹明6G对Hg2+的检出下限分别为6.9×10-8mol/L 和1.2×10-9mol/L.
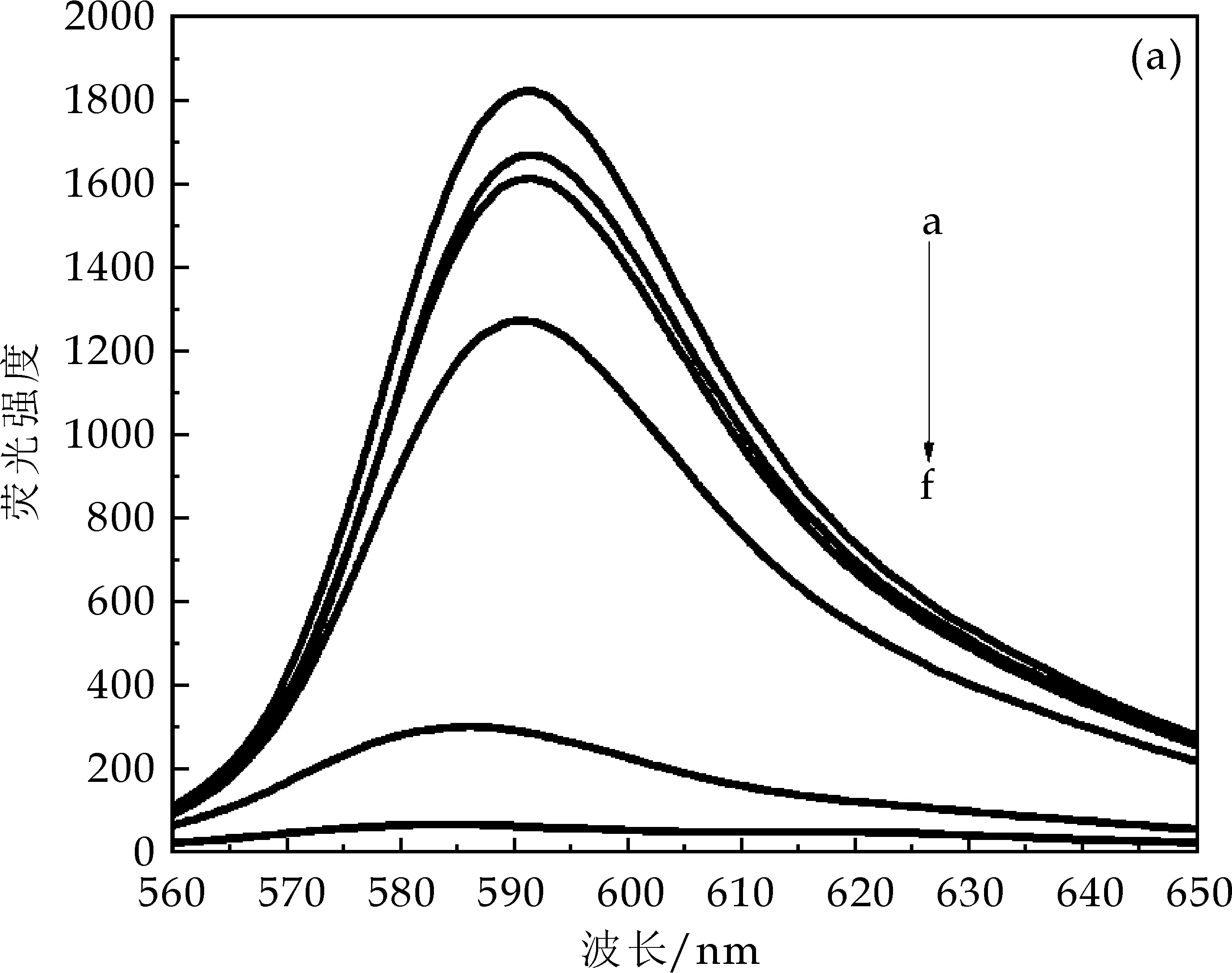
(a)Hg2+浓度(沿箭头方向依次是a:0 mol/L;b:10-8 mol/L;c:10-7 mol/L;d:10-6 mol/L;e:10-5 mol/L;f:10-4 mol/L)

(b)罗丹明B检测Hg2+拟合直线图图5 罗丹明B检测Hg2+体系的荧光强度变化图

(a)Hg2+浓度(沿箭头方向依次是a:0 mol/L;b:10-8 mol/L;c:10-7 mol/L;d:10-6 mol/L;e:10-5 mol/L;f:10-4 mol/L)

(b)罗丹明6G检测Hg2+拟合直线图图6 罗丹明6G检测Hg2+体系的荧光强度变化图
2.4干扰离子对不同体系荧光检测结果比较
为了比较两种探针对Hg2+识别的选择性,选择了Zn2+、 Cu2+、Pb2+及Cd2+等作为干扰离子,测试了25 ℃下两种探针对混合体系中Hg2+的荧光检测图.在测试体系中,罗丹明B(罗丹明6G)浓度为1×10-5mol/L、Hg2+浓度为1×10-6mol/L、干扰离子浓度为1×10-5mol/L,其检测结果分别如图7和图8所示.
由图7~8可知,两种探针对Hg2+的响应性均较好,当体系中仅有Hg2+存在时,罗丹明B检测体系荧光强度为1 271;而罗丹明6G检测体系荧光强度为1 871.当体系中引入干扰离子后,罗丹明B检测体系荧光强度迅速下降,仅为619;而罗丹明6G检测体系荧光强度变化不大,仍高达1 854,这说明罗丹明6G比罗丹明B的抗干扰能力强,即罗丹明6G的选择性更高.
比较两者的分子结构(如图9所示)可发现,罗丹明6G与罗丹明B分子中的苯环之间有附加的氧桥,分子结构刚性均较强,两者均具有一定的荧光检测特性.从外围取代基结构分析,与罗丹明6G相比,罗丹明B分子中多出了一个羧基,羧基是强极性基团,提高了整个分子在水中的溶解性及与金属阳离子的作用位点,同时,也增加了罗丹明B与阳离子间的结合机会,因此,其在水中的抗干扰能力较差;从探针分子的结构稳定性分析,与罗丹明B相比,罗丹明6G分子的苯环外围存在给电子的甲基,在检测过程中使苯环活化,能量升高更易与目标分子发生开环反应,因此,其分子检测的准确性更高.

图7 罗丹明B对混合体系中Hg2+的荧光检测图
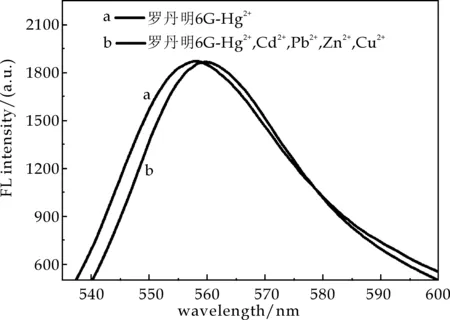
图8 罗丹明6G对混合体系中Hg2+的荧光检测图
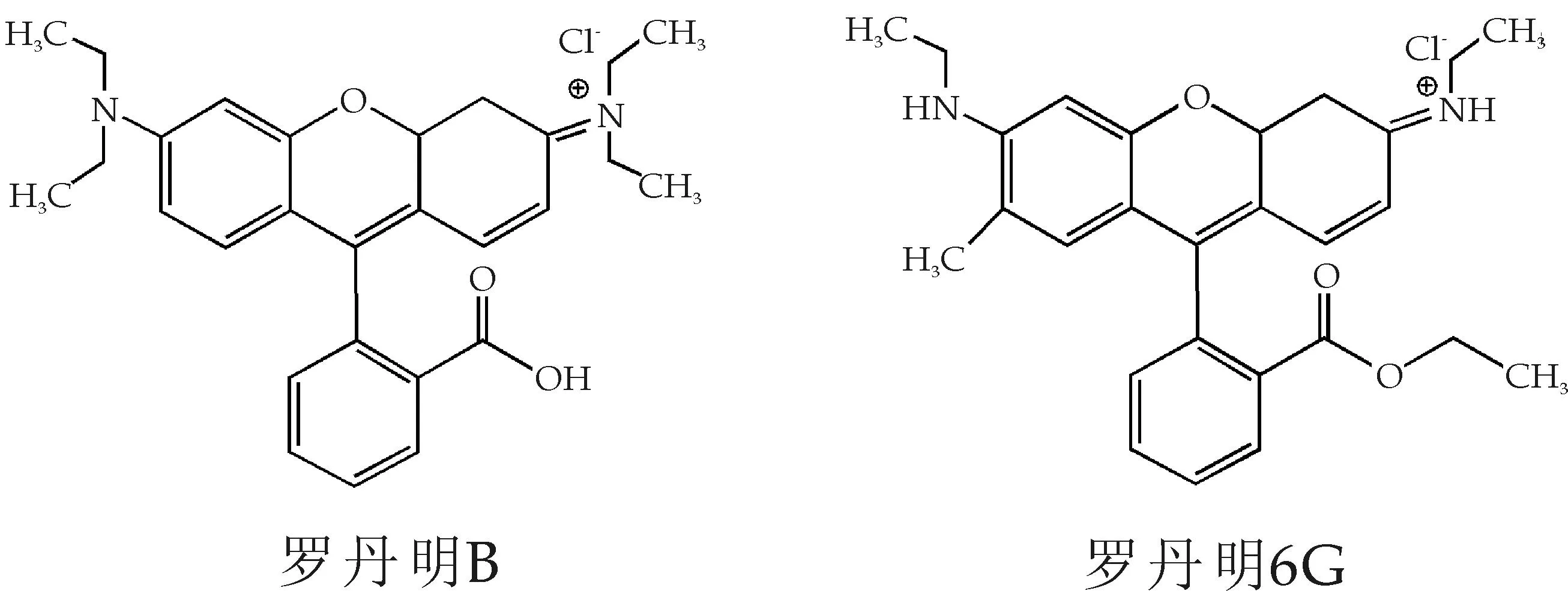
图9 罗丹明B及罗丹明6G的分子结构图
2.5实际水样中Hg2+测量结果比较
在25 ℃下,利用两种探针检测自来水样中的Hg2+,其结果如图10所示.由图10可知,罗丹明B 和罗丹明6G检测体系的最大荧光发射峰处的强度分别为890.6和885.5.根据25 ℃条件下两种探针荧光发射峰强度与汞离子浓度变化的线性关系,将其带入拟合直线方程中,乘以稀释倍数后,分别求得自来水中Hg2+浓度分别为9.69×10-6mol/L和3.25×10-5mol/L.
从上面的计算可知,两种罗丹明类荧光探针检测出的汞离子浓度不同,但是从前述的讨论可知,罗丹明6G具有较高的灵敏性和选择性及线性范围.所以,可认为罗丹明6G检测汞离子的浓度为3.25×10-5mol/L是较准确的.由于罗丹明B在实际检测中易受到其它离子的干扰,其选择性较差,故其检测结果比实际值小.
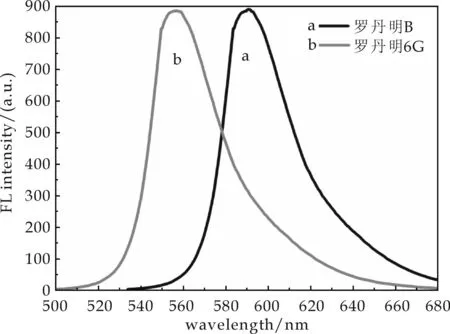
图10 两种探针分子对自来水中Hg2+的检测图
3结论
罗丹明B与罗丹明6G对水中Hg2+都具有极好的荧光检测特性.两种探针都属荧光猝灭型探针,受温度影响较大.其中,罗丹明6G对Hg2+检测的线性范围、检出限及选择性均高于罗丹明B.因此,在实际水样Hg2+的荧光检测中,罗丹明6G探针的准确性更高.
从其结构上分析可知,罗丹明6G分子中存在给电子的甲基,在检测过程中使苯环活化,能量升高更易与检测离子发生开环反应.所以,在今后的探针改性中,为了提高探针分子的准确性,要适当控制探针分子的极性,尽量减少羧基、羟基等强极性基团对罗丹明类分子的取代,而应选择在其外围修饰给电子基团.
参考文献
[1] Evert Nieboer,David H.S.Riehardson.The replacement of the nondescript term“heavy metals” by a biologically and chemically significant classification of metal ions[J].Enviormnental Pollution (Seiries B),1980,1(1):3-26.
[2] Estela Climent,M.Dolores Marcos,Ramón Martínez-Mez, et al.The determination of methylmercury in real samples using organically capped mesoporous inorganic materials capable of signal amplification[J].Angewandte Chemie International Edition,2009,48(45):8 519-8 522.
[3] 国家环境保护部.2013年上半年全国环境质量状况[R].北京:中华人民共和国环境保护部,2013:30-31.
[4] 史慧芳,赵强,安众福,等.基于小分子的汞离子荧光探针[J].化学进展,2010,22(9):1 741-1 752.
[5] Knut Rurack.Flipping the light switch ‘ON’-the design of sensor molecules that showed cation-induced fluorescence enhancement with heavy and transition metal ions[J].Spectrochimica Actan Part A,2001,57(11):2 161-2 195.
[6] Roberto Purrello,Sergio Gurrieri,Rosaria Lauceri.Porphyrin assemblies as chemical sensors[J].Coordination Chemistry Reviews,1999,190-192(9):683-706.
[7] Zsolt Valicsek,Ottó Horvth.Application of the electronic spectra of porphyrins for analytical purposes:The effects of metal ions and structural distortions[J].Microchemical Journal,2013,107(3):47-62.
[8] Xiaoqiang Chen,Kyung Hwa Baek,Youngmee Kim,et al.A selenolactone-based fluorescent chemodosimeter to monitor mecury/methylmercury species in vitro and in vivo[J].Tetrahedron, 2010,66(23):4 016-4 021.
[9] Young Keun Yang,Sung Kyun Ko,Injae Shin,et al.Fluorescent detection of methylmercury by desulfurization reaction of rhodamine hydrazide derivatives[J].Organic and Biomolecular Chemistry,2009,7(22):4 590-4 593.
[10] Young Keun Yang,Keun Jeong Yook,Jinsung Tae.A rhodamine based fluorescent and colorimetric chemodosimeter for the rapid detection of Hg2+Ions in aqueous media[J].Journal of American Chemistry Society,2005,127(48):16 760-16 761.
[11] Xiande Zhao,Wengang Zheng,Daming Dong,et al.Temperature effect on fluorescence of PtOEP embedded in sol-gel membrane used in oxygen sensor[J].Optik-International Journal for Light and Electron Optics,2013,124(24):6 799-6 802.
[12] Michael Shortreed,Raoul Kopelman,Michael Kuhn,et al.Fluorescent fiber-optic calcium sensor for physiological measurements[J].Analytical Chemistry,1996,68(8):1 414-1 418.

Comparison of detection for Hg2+in water
by rhodamine fluorescence probes
LV Xiang-fei1,4, LI Ting1, HUO Xiao-nan1, HU Nan-jiang2, YAN Lei3,
LI Guo-rong1, Ermelinda Bloise4
(1.College of Resources and Environment, Shaanxi University of Science & Technology, Xi′an 710021, China; 2.College of Light Industry and Energy, Shaanxi University of Science & Technology, Xi′an 710021, China; 3.Material Engineering Invention Examination Department, Patent Examination Cooperation Center of the Patent Office, SIPO, Beijing 100096, China; 4.Department of Engineering for Innovation, University of Salento, Lecce 73100, Italy)
Abstract:The rhodamine B and rhodamine 6G were applied to the determine of Hg2+in water by quenching-fluorescence.After the addition of KI,Hg2+could produce multi-ionic associated substance with rhodamine probes,which was used to detect the Hg2+in water solution through the intensity of fluorescence emission peak in system.By comparision of the detection performance based two probes,the results indicated that two rhodamine moleculers were quenching fluorescence probes and the rhodamine 6G showed higher sensitivity,linearity and selectivity than rhodamine B,due to its steady structure.
Key words:fluorescence quenching; rhodamine B; rhodamine 6G
中图分类号:O657.3
文献标志码:A
文章编号:1000-5811(2015)05-0034-06
作者简介:吕向菲(1984-),女,陕西临潼人,讲师,博士,研究方向:荧光探针对水中重金属离子的检测
基金项目:陕西省科技厅自然科学基金项目(2013JQ2026); 国家级大学生创新创业训练计划项目(201310708013); 陕西科技大学学术骨干培育计划项目(XSG(4)012)
收稿日期:*2015-06-18
