浅析高考理综化学选择题解题攻略
2015-12-18郑欣佳,衷明华
浅析高考理综化学选择题解题攻略
郑欣佳衷明华
(韩山师范学院化学系,广东 潮州 521041)
摘要:近几年来高考理综化学中的选择题,考查的方式和内容都较为稳定,六道单选,两道双选,共计三十六分。分值不低,所以一直是习题训练的重点部分,也有些知识点是必考的。重点考查了化学科的主干知识、基础理论和基本技能。选择题的各个选项从不同知识范围立意,这样既可以考查学生掌握基础知识的广度,也可以考查学生对知识掌握的。
关键词:高考选择题高考化学解题方法基础知识标准状况
对于高考理综的选择题来说,一般有两种解题顺序,一般都强调一个小时内完成。第一类是:先单科单科完成,即先写好一个科目的选择题,再写另一个科目的选择题。第二类是:按出题顺序,一般按照生物化学物理的出题顺序,先完成单选的,再完成双选,这种方法则需要考生在答题时很快速地转换解题思路,所以一般建议考生选择第一种解题顺序。而一个小时内要完成理综三科的选择,按化学的题量,八道选择题,用时大概二十分钟左右,考生在解题时要注意时间的分配,不可花费过多时间,也不可以花费时间过少。在高考化学中,选择题是基础,选择题得分的高低一定程度上决定着高考化学成绩的高低。
近年高考中,选择题也突出了思维能力的考查。选择题的考查功能主要有使试卷有较大的知识点覆盖面,其中少量的“基础题”增加考生的保底分,保留某些类型的“常见题”调控总难度。考查的知识容量较大,最热的考点主要有:以物质的量为中心的相关概念分析计算、周期表和周期律、原子结构的判断、化学反应速率和化学平衡、电化学、离子共存和离子方程式正误判断、氧化还原反应、化学实验基本操作、简单计算等等。总之,在选择题的部分,就要求学生扎扎实实地打好基础,认真审题、分析题、解题。接下来,我们就从两个常考知识点的例题讲解中,总结出一种化学选择题的答题策略。
一、阿伏加德罗常数
阿伏伽德罗常数是历年高考的热点,常常在考题中有意设置一些极易疏忽的干扰因素。在分析解答这类问题时,要特别注意以下几点:
(1)状态问题:如水在标况下是为液体或固体;SO3在标况下是固体,通常状况下是液体;
(2)用到22.4L/mol时,要注意是否处于标况下;
(3)对类型题目可以归纳熟记。
下面通过例题,举例分析。
例题一:设阿伏加德罗常数(NA)的数值为nA,下列说法正确的是()。
A、0.1mol过氧化钠与足量水反应生成的O2分子数为0.1nA
B、标准状况下,11.2L四氯化碳含有的分子数为0.5nA
C、1mol S在足量O2中燃烧,转移电子数为6nA
D、常温常压下,16g的O2和O3混合气体含有的原子数为nA
解析:A、方程式为
2Na2O2+2H2O=4NaOH+O2↑,由方程式可以知道Na2O2:O2=2:1,可以得出A选项错误;
B、常温下,11.2L四氯化碳含有的分子数确实为0.5nA,通过下面的公式可以算出结果,N=n×NA=V/Vm×NA=0.5nA。但是值得注意的是题干为标况下,所以B选项错误;
C、写出题目要求的方程式S+O2=SO2,所以在方程式中硫元素的单价从硫单质的0单价升到二氧化硫中的+4价,可知转移电子数为4nA,因此C选项也错误;
D、常温常压下,16g的O2和O3混合气体含有的原子数为nA,由下面的公式可以得出D正确,N(O)=n(O)×NA。
例题二:(2010广东高考)设NA为阿伏加德罗常数的数值,下列说法正确的是()。
A、16g CH4中含有4NA个C-H键
B、1mol/L NaCl溶液含有NA个Na离子
C、1mol Cu和足量稀硝酸反应产生NA个NO分子
D、常温常压下,22.4L CO2中含有NA个CO2分子
解析:A、每个CH4中含有4个C-H键,故16g CH4(1mol)中含有4NA个C-H键,A正确;
B、没有告诉溶液的体积,无法知道NaCl的物质的量,故B错;
C、根据化学方程式知1mol Cu~2mol NO,故C错;
D、常温常压下,22.4L CO2不是1mol,故D错,注意此选项就是标况下类型题,做这类题时就应该注意这些字眼。
我们可以从例题中总结易错点,归类对比得出解题规律:
例题一的D选项:常温常压下,16g的O2和O3混合气体含有的原子数为nA。
例题二的A选项:16g CH4中含有4NA个C-H键。
这两个选项都是由质量m求物质的量n,不需要考虑是否是标况下,标况下是体积的换算,这里是质量,这个地方是容易混淆的知识点。
例题一的A选项:0.1mol过氧化钠与足量水反应生成的O2分子数为0.1nA。
例题二的C选项:1mol Cu和足量稀硝酸反应产生NA个NO分子。
这两个选项都是要通过书写方程式,确立比值来解题,这里则要求考生熟悉方程式的书写。
例题一的B选项:标准状况下,11.2L四氯化碳含有的分子数为0.5nA。
例题二的D选项:常温常压下,22.4L CO2中含有 NA个CO2分子。
这两个选项,则应该注意题目里的条件,标准状况下,四氯化碳为液体,无法用气体体积进行计算,常温常压下,22.4L CO2不是1mol。
二、化学反应速率、化学平衡
此知识点,有难有易,但是常考知识点,遇到容易的题目,有些考生会大意,而选错选项,而遇到难得题目,则会有瓶颈,不知如何解题。总之,不论难易,都应该仔细思考各个选项,逐个分析。而我们可以通过一两道例题的归纳类比,总结做题规律,就能在下次看见同类题型的时候,有清晰的思路去解题,虽然有时过程比较繁琐,但却是很有益的方法。化学反应进行的快慢对应的即化学反应速率,化学反应的限度对应的即化学平衡。常见的有图形题,以及考察增大或减小反应速率的措施的类型题。
下面通过例题,举例分析:
例题三:针对平衡2SO2(g)+O2(g)2SO3(g),采用下列措施一段时间后,能增大正反应速率的是()。
A、通入大量O2
B、增大容器容积
C、移去部分SO3
D、降低体系温度
思路点拨:解答本题需要掌握以下几个关键的知识点。
增大任一反应物或生成物的浓度,一段时间后,正、逆反应速率都能加快。
(2)升高反应体系的温度,正、逆反应速率都加快。
(3)对反应体系加压,正、逆反应速率都加快。
答案:A。
解析:增加O2的浓度,这一瞬间正反应速率加快,逆反应不变,但随着反应,生成物的浓度增大,逆反应反应速率随之加快,A项正确;增大容器容积、移去部分SO3,即减小浓度,而减小物质的浓度、降低温度均减小反应速率,B、C、D项错误。
例题四:下图反应A2(g)+3B2(g)2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是()。
A、升高温度,同时加压
B、降低温度,同时减压
C、增大反应物浓度,同时使用催化剂
D、增大反应物浓度,同时减小生成物浓度
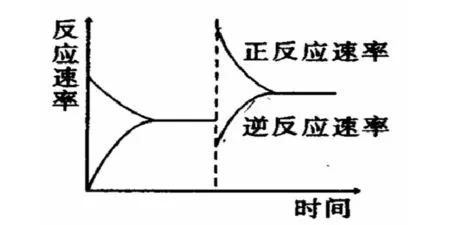
图 平衡移动
解析:看到图形题,千万不可以大意,先看图再一一看选项,不能看到一个选项以为是对的就立刻选下来,而不去看其他的选项,这样很容易失分。就此道题的图来看,看两个点,即可逆反应平衡后,变化的两个点,从图中可以看出,正反应速率增大,逆反应速率降低了,下面进行分选项分析。
A、升高温度,正逆反应速率都会增大,故A错;
B、降低温度,正逆反应速率都会降低,故B错;
C、增大反应物浓度,正逆反应速率会增大,但这一瞬间逆反应速率是不变的,注意使用催化剂不能改变正逆反应速率,故C错;
D、增大反应物浓度,正反应速率会增大,同时减小生成物浓度,逆反应速率会降低,故D正确。
对于化学反应速率、化学平衡是考试的热点,需要多练习题,提高做题的效率以及正确率。在看到题目时,应该清楚地知道所考知识点,同样地也要总结题目规律,这样才有利于解题。
总之,在做高考化学选择题时,要求考生认真仔细地审题,分析题目后再作答,平时的做题积累总结也是很重要的一个部分,需要考生多练多积累多作总结。
