微纳米气泡基本特性及溶解氧的研究
2015-12-13潘习习徐建平
潘习习,徐建平
(安徽工程大学 生物与化学工程学院,安徽 芜湖 241000)
微纳米气泡的相关研究已经成为近些年研究的热点.微纳米气泡具有普通气泡所不具有的特点,如:气泡体积小、上升速度慢以及具有较强的氧化性等特点.相关文献指出由于气泡细小,受空气在水中溶解度的影响较小,气泡在污水中停留时间较长,具有良好的气浮处理效果[1-2].在水体增氧、浮选技术、治理污水等领域也有着重要的应用价值[3].与其他水处理方法相比,微纳米气泡还具有操作简便、功耗小、无二次污染等特点,具有很好的可推广性.但是,目前对微纳米气泡的形成规律以及特性等问题,还处在继续研究的过程中,微纳米气泡的一些特性和用途还有待于开发和利用[4].
在微纳米气泡与普通气泡的不同特性中,研究者对其在水中溶解氧的影响因素持有不同看法.总体体现在两方面:一方面研究者认为,微纳米气泡的溶解现象与普通气泡的相同,受到温度、压力等因素的影响[5-6];另一方面研究者认为,由于气泡尺寸极小,使得其比表面积相当大,因而受空气在水中溶解度的影响不大.
此次实验将探究部分影响因素(温度、p H和转速等)对微纳米气泡在水中溶解氧的影响.在此基础上,利用正交试验对反应条件进行优化,为下一步研究微纳米气泡在工业废水中的应用提供基础.
1 材料与方法
1.1 材料与试剂
硫酸锰溶液,碱性碘化钾溶液,浓硫酸,淀粉溶液(1%),硫代硫酸钠溶液(0.025 mol/L).
1.2 仪器与设备
卷尺,烧杯,量筒,搅拌器,水浴锅,定制实验用PVC透明水槽(长150 cm、宽50 cm、高120 cm),云南夏之春环保公司的XZCP-K-0.75,该装置原理是使水与气高度相溶混合,超声波空化弥散释放出高密度的、均匀的超微米气泡.
1.3 溶解氧的测量方法
溶解氧的测定采用-碘量法(GB 7489-87)进行测量.
1.4 实验方法
(1)微纳米气泡悬浮时间.用1 L的量筒获取在微纳米气泡发生装置稳定条件下水槽中制备得到的乳白状水气混合液1 L,将量筒静置在水平桌面上,测量该乳白状水气混合液从浑浊状态到澄清时所用的时间.为减少实验带来的误差,实验采取多次测量求平均值的方法,最终得出微纳米气泡在水中悬浮时间为252 s,实验数据如表1所示.
(2)有效气液混合比.为测量微纳米气泡在水中实际产气量的效率,实验选用250 m L,500 m L,1 000 m L的量筒量,获取在稳定条件下水槽中制备得到的乳白色水气混合液,放置在水平桌面上,测量澄清前后量筒内液体体积,并计算出混合液中微纳米气泡的实际有效比例.有效气液混合比η=(v1-v2)/v1.计算时进行3次测量取平均值,最终计算得出混合气液比为2.12%,即微纳米发生装置产生的气水混合液中有效气液混合比至少为2.12%.

表1 微纳米气泡悬浮时间测量

表2 有效气液混合比测量
(3)将微纳米气泡发生器、臭氧发生器、机械搅拌机以及水槽组合成一个实验装置.实验前检查装置运转是否正常.测量水样时,用250 m L溶解氧瓶获取实验后的水样进行研究.实验装置示意图如图1所示.
在上述装置条件下,依次改变反应体系的p H值(4~10)、时间(0~45 min)、温度(20~45℃)、转速(500~3 000 r/min),分别测定溶解氧的含量,考察单因素对微纳米气泡的溶解氧的影响.
2 结果与分析
2.1 反应时间对溶解氧的影响
时间对溶解氧的影响结果如图2所示.由图2可知,反应时间对溶解氧的含量有显著影响.在一定时间内,溶解氧随时间的增加而不断升高,反应时间达到10 min时达到最大值;此后随着反应时间的增加,溶解氧的含量呈现出下降趋势.因此,分析微纳米气泡在水中溶解氧的较佳时间应该是在10 min附近.反应开始时,随着微纳米气泡的不断产生,溶解氧含量不断升高,当到达一定时间后,随着时间增加溶解氧呈下降趋势.根据分析是由于微纳米气泡在水中破裂时,会产生大量的热,使得水中的温度上升,加强了分子的热运动,使得气泡破裂排出水面从而使得溶解氧下降.
2.2 p H对溶解氧的影响
p H对溶解氧的影响如图3所示.由图3可知,p H对溶解氧的影响较明显.根据图3中曲线可以得出,当p H在6~7之间时,微纳米气泡在水中的溶解氧达到最大值,其他p H值条件下都较低.根据相关文献的分析,微纳米气泡在水中上升的过程中,由于其比表面积小,在气泡表面会形成双电子层结构,界面上存在着高浓度离子,在微气泡破裂瞬间,由于剧烈变化界面上将释放出化学能,从而产生大量的羟基自由基[7].不同的p H带来水中不同离子含量,对双电子层起到了不同程度的影响[8].同时,实验前后p H值没有发生改变,也能说明微纳米气泡对溶液的p H没有影响.当p H在6~7之间时,微纳米气泡在水中的含量较高.这一规律与严伟[9]的观点一致,研究指出水和废水呈中性时,气浮法处理效果良好,p H值如大于或小于7,都会降低气浮法的处理效果.
2.3 温度对溶解氧的影响
温度对溶解氧的影响如图4所示.由图4可知,温度对微纳米气泡的影响比较显著.随着温度的增加,溶解氧不断升高.当达到25℃左右时,溶解氧含量达到最大值;此后,继续升高温度,溶解氧含量呈下降趋势,最终曲线平缓溶解氧稳定.据分析当温度相对较低时,能够使得少量微纳米气泡破裂,产生的氧溶解到水中,从而使溶解氧含量增加,随着温度的持续升高,较高的温度会使得水中气泡的界面发生变化,使大量气泡破裂,溶解氧流失较大,进而产生溶解氧降低的现象.
2.4 转速对溶解氧的影响
搅拌对溶解氧的影响如图5所示.由图5可知,随着搅拌程度的不断增加,微纳米气泡在水中的溶解氧含量随之升高,当搅拌程度达到1500 r/min时,溶解氧含量达到最大;此后,继续增加转速,溶解氧含量逐渐下降.转速对溶解氧的影响,据分析应是由于适当的转速可以使得溶解氧更好地与水均匀混合,有利于水中溶解氧的增加,但当转速增大到一定程度时,水中的剪切力增大,使得气泡破裂,破坏了气液混合的平衡条件,进而使得溶解氧下降.
2.5 正交优化
根据单因素实验结果,确定各因素的较优取值范围后,设计正交试验,进行实验并优化反应条件.实验设计因素及水平如表3所示.根据单因素实验结果,选取时间、温度、p H、转速4因素进行正交试验设计,结果如表4所示.
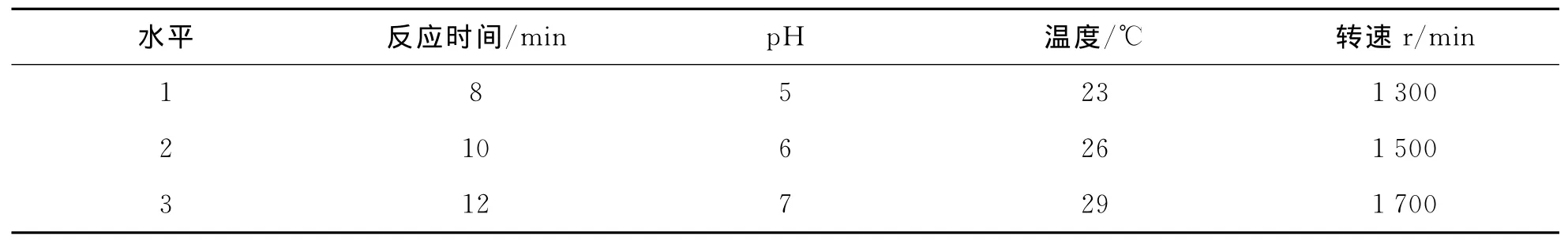
表3 溶解氧正交试验因素与水平设计

表4 L9(34)正交试验结果
根据正交实验得出优化组合,即p H值7、时间8 min、温度23℃、转速1 300 r/min,在此条件下进行平行验证性实验,得出溶解氧为14.7 mg/L.
3 结论
研究表明,微纳米气泡在水中悬浮时间为252 s.微纳米发生装置产生的气水混合液中有效气液混合比至少为2.12%.由实验可以看出,微纳米气泡在水中的停留时间相对于普通气泡的停留时间有较大差异.微纳米气泡的这一特性,可用于传统曝气方法的改进.又由于其气泡体积较小,具有较强的氧化性,可大大提高曝气方法在水体供氧和对有机物的氧化处理,有助于开发拓展新型环保的污水处理方法.
本实验以空气微纳米气泡为基础,研究了温度、时间、p H值等影响因素对微纳米气泡在水中的溶解氧的影响.实验证明得出温度、时间、p H值等影响因素对微纳米气泡在水中的溶解氧具有一定的影响效果.其单因素的影响程度顺序为:温度、转速、p H、时间.正交试验结果表明,在一定时间内,溶解氧随时间的增加而不断升高,反应时间达到10 min时达到最大值,此后随着反应时间的增加,溶解氧的含量呈现出下降趋势.当p H在6~7之间时,微纳米气泡在水中的溶解氧达到最大值,其他p H值条件下都较低.随着温度的增加,溶解氧不断升高,当达到25℃左右时,溶解氧含量达到最大值,此后,继续升高温度,溶解氧含量呈下降趋势,最终曲线平缓溶解氧稳定.随着搅拌程度的不断增加,微纳米气泡在水中的溶解氧含量随之升高,当搅拌程度达到1 500 r/min时,溶解氧含量达到最大,此后,继续增加转速,溶解氧含量逐渐下降.以空气为载体的微纳米气泡优化条件为p H值7、时间8 min、温度23℃、转速1 300 r/min时,溶解氧含量较高.在此优化条件下进行平行验证性实验,得到溶解氧平均值为14.7 mg/L.
[1]陈冀孙,胡斌.气浮净水技术的研究与应用[M].上海:上海科学出版社,1985:1-9.
[2]王毅力,汤鸿霄.气浮净水技术研究及进展[J].环境科学进展,1999,7:94-103.
[3]Takahashi Masayoshi,Chiba Kaneo,L Pani.Free-radical generation from collapsing microbubbles in the absence of a dynamic stimulus[J].J.PHys.Chem.B,2007,111(6):1343-1347.
[4]吕宙.微纳米气泡曝气在污水处理中的应用研究[D].合肥:合肥工业大学,2014.
[5]邓超,杨丽,陈海军,等.微纳米气泡发生装置及其应用的研究进展[J].石油化工,2014,10:1 206-1 213.
[6]郑最胜,李南方.纳米气泡简介[J].化学教学,2008,3:41-43.
[7]洪涛,叶春,李春华,等.微米气泡曝气技术处理黑臭河水的效果研究[J].环境工程技术学报,2011,1:20-25.
[8]宋滔,杜筱兰,董亚明,等.溶解气体和纳米气泡对固-液溶胶电导率的影响[J].上海师范大学学报,2009,38(1):68-69.
[9]严伟.p H 值对气浮法净水的影响[J].化工环保,1986,6:76-77.
