氧化锆-活性炭纤维复合材料的制备及其对F-吸附性能
2015-12-05刘景亮宗恩敏许昭怡
刘景亮 宗恩敏 陈 欢 许昭怡
(1南京晓庄学院环境科学学院,南京 211171) (2台州学院生命科学学院,台州 317000) (3南京理工大学环境与生物工程学院,南京 210094) (4污染控制与资源化研究国家重点实验室,南京大学环境学院,南京 210046)
氧化锆-活性炭纤维复合材料的制备及其对F-吸附性能
刘景亮*,1宗恩敏2陈欢3许昭怡4
(1南京晓庄学院环境科学学院,南京211171) (2台州学院生命科学学院,台州317000) (3南京理工大学环境与生物工程学院,南京210094) (4污染控制与资源化研究国家重点实验室,南京大学环境学院,南京210046)
采用水热合成法成功制备了氧化锆-活性炭纤维复合材料,并研究了其对F-的吸附行为。表征结果表明,复合材料中氧化锆粒子成功负载于活性炭纤维上。吸附实验结果表明,负载了氧化锆的活性炭纤维对F-有高效的去除效率,其吸附机理包括离子交换和静电作用力,吸附等温线符合Langmuir等温吸附模式,吸附动力学可用拟二级动力学模型拟合。吸附量随着溶液pH的升高而降低,共存离子Cl-、NO3-和SO42-对F-在氧化锆-活性炭纤维复合材料上的吸附几乎没有影响。
活性炭纤维;氟;吸附;氧化锆
氟是人体必需的微量元素之一,适量的氟能促进人体健康,然而过量的摄入氟则会导致氟斑牙和氟骨症等症状[1]。氟化物是重要的化工原料,广泛应用于半导体制造、金属冶炼、玻璃和陶瓷制造业。据统计钢铁企业冶炼过程中以萤石(CaF2)作为助熔剂,有11.33%左右的氟元素通过废水排入自然环境中[2];同样在玻璃、陶瓷、搪瓷以及水泥合成工业中,通过添加萤石、冰晶石来提高产品质量,也产生了大量的含氟污染物,加剧了水环境中F-的污染[3]。我国生活饮用水规定氟化物含量的限值为1.0 mg· L-1。水体中F-的去除方法有沉淀法、电渗析,离子交换和吸附法[4-8]。其中吸附法因吸附效率高、操作简单等优点而受到广泛关注。活性氧化铝,活性炭和金属氧化物复合材料吸附剂被广泛的应用于水体中氟离子的去除[9-11]。
近年来稀土元素复合吸附剂得到广泛的关注。姚瑞华等[12]研究表明负载金属镧的壳聚糖对氟离子有很高的吸附效率;Wasay等[13]的研究表明,稀土元素镧对水体中的众多阴离子具有亲和力;刘瑞霞等[14]制备的镧纤维吸附剂对氟离子吸附显示了较好的吸附动力学;马刚平等[15]用镧氧化膜处理微污染水源中的F-,具有较好的吸附效果;Evans等[16]的研究则表明锆金属可有效吸附去除F-;Liao等[17]制备含锆吸附剂处理含氟废水,去除率高达97.4%。
以上的研究表明,通过负载作用,有利于将稀土元素分散到载体中,进而增加金属元素活性位点,因此通过载体本身的特性能提高和拓宽这类材料的吸附性能。作为第三代炭基材料,活性炭纤维拥有良好的化学稳定性、较高的比表面积和较窄的孔径分布[18-20],备受人们的关注。 已有研究者[21-22]将金属镧嫁接在氧化的活性炭纤维上,并应用于磷酸盐的吸附,取得了一定的吸附效果。然而将金属锆负载在活性炭纤维上,并应用于水体中氟离子的研究未见报道。
本研究采用水热法合成氧化锆负载的活性炭纤维复合材料,并系统研究了该复合材料对F-的吸附行为,旨在揭示其吸附机理,同时考察水化学条件的影响,为开发高效的除氟吸附材料提供一定的理论依据和技术支持。
1 实验部分
1.1实验材料与试剂
活性炭纤维购于江苏苏通炭纤维有限责任公司;正丙醇锆购于Aldrich公司;氟化钠、硝酸钠、二水合柠檬酸三钠离、双氧水、盐酸、氢氧化钠、氯化钠、无水甲苯以及无水乙醇购自南京化学试剂有限公司。
1.2氧化锆-活性炭纤维复合材料的制备
活性炭纤维预处理:将活性炭纤维在去离子水中浸渍24 h后烘干,沸水煮2 h;然后用蒸馏水多次洗涤去除残留的水溶性和挥发性的杂质,烘干备用。
活性炭纤维的氧化:称取5 g预处理后的活性炭纤维置于100 mL 30wt%的双氧水中,回流反应6 h,冷却后蒸馏水洗至中性,干燥后得到氧化后的活性炭纤维,记为ACF-O。
氧化锆-活性炭纤维复合材料的制备:按照水热合成方法[23],称取3 g氧化后的活性炭纤维(ACFO),加入60 mL的无水甲苯中,通氮气30 min;然后逐滴加入6 mL 70wt%的正丙醇锆于上述溶液中,回流反应3 h;冷却后依次用甲苯、无水乙醇和去离子水洗涤,真空干燥得到氧化锆-活性炭纤维复合材料,记为ACF-Zr。
1.3吸附剂的表征
ACF-O以及ACF-Zr样品形貌、晶体结构分别用扫描电子显微镜(SEM)和X射线衍射仪(XRD)进行分析。SEM分析采用日本 Hitachi公司 S-3400N II型扫描电子显微镜。XRD分析采用瑞士ARL公司的X′TRA型X射线衍射仪(Cu靶Kα线,λ=1.540 562 nm,40 kV,40 mA,2θ=10°~70°)。N2吸附-脱附等温线由Micromeritics ASAP 2020(Micrimetitics,USA)型物理吸附仪上操作完成,在-196℃(77 K)条件下测定。元素分析采用ARL-9800型(Arl,Switzerland)X射线荧光光谱仪进行测定。XPS测定采用PHI 5000 Versa Probe型(UIVAC-PHI,Japan)电子能谱仪。红外光谱采用NEXUS870型(Nicllet,USA)傅立叶变换红外光谱仪进行测定。
1.4吸附实验
吸附等温线:准确称取10 mg ACF-Zr吸附剂置于50 mL比色管中,加入初始浓度为1、2、4、8、16、32、64、100 mg·L-1的F-溶液。恒温25℃避光条件下振荡24 h,实验采用2组平行样。根据动力学实验结果选取24 h作为吸附平衡时间。吸附平衡后,经0.45 μm的水相针式滤头过滤后,测定滤液中F-浓度,F-浓度测定采用氟离子选择电极法,同时测定吸附平衡时溶液的pH值。以Qe~Ce作图,得到ACF-Zr对F-的吸附等温线。

式中,C0和Ce分别为初始磷浓度和吸附平衡后的磷浓度,mg·L-1;V为溶液的体积,L;m为吸附剂的质量,g。
吸附动力学:准确称取80 mg吸附剂ACF-Zr于500 mL广口瓶中,分别加入到初始浓度为15 mg·L-1和30 mg·L-1的F-水溶液中,其初始pH值为6.8±0.2,温度为25℃。避光条件下进行吸附,磁力搅拌器快速搅拌以确保体系混合均匀,于不同时间间隔取样。样品用0.45 μm滤膜过滤,测定滤液中F-浓度。
pH值对吸附的影响:实验初始pH值用0.1 mol·L-1HCl和0.1 mol·L-1NaOH溶液调节至2~11,F-初始浓度为16 mg·L-1,按前述吸附等温线方法进行吸附实验,采用2组平行样,并测定吸附平衡时的溶液pH值。
共存离子对吸附的影响:选取的共存离子为Cl-、NO3-和SO42-,其浓度范围为0~200 mg·L-1,F-初始浓度为16 mg·L-1,按前述吸附等温线方法进行吸附实验,采用两组平行样。
2 结果与讨论
2.1表征结果
氧化后的活性炭纤维(ACF-O)和氧化锆-活性炭纤维复合材料(ACF-Zr)扫描电镜图(SEM)如图1所示。图1a显示ACF-O为直纤维状(棒状)结构,图2b与图2a对照可知负载在ACF-O上的氧化锆不影响ACF-O的形态分布,通过图2可以得知氧化锆能比较均匀的分散在ACF-O的表面上。图2为活性炭纤维负载氧化锆前后的XRD图。从图中可以得知,ACF-O在2θ角为24°和43°有2个衍射宽峰,分别对应于类石墨微晶结构的(002)面和(100)面[24-25];负载氧化锆后ACF-Zr后材料的(002)峰和(100)峰变宽变矮,且(002)峰发生明显右移,表明类石墨微晶结构发生了细晶化,这是因为经后水热处理后,活性炭纤维的微晶层面与负载成分发生了一定的作用,使微晶成分有一定程度的损失,导致微晶尺度的下降。另外,在2θ角为30°附近出现无定形态氧化锆的衍射峰[26],表明氧化锆成功负载于活性炭纤维上。

图1 ACF-O(a)和ACF-Zr(b)的扫描电镜图Fig.1 SEM images of ACF-O(a)and ACF-Zr(b)
图3为氧化锆改性前后的活性炭纤维的FTIR图谱。从图中可以看出,ACF-O在900~1 300 cm-1之间出现一个宽的吸收峰,此处为醇羟基、酚羟基和羧基官能团中的-C-O伸缩振动峰和-OH的弯曲振动峰[27];1 714 cm-1处为羧基官能团中的C=O伸缩振动峰[28],1 570 cm-1处为碳骨架的吸收峰[29]。改性后的ACF-Zr在1 370 cm-1和3 400 cm-1左右出各出现新的吸收峰,分别归属于为Zr-OH的振动峰[30]和Zr-OH-Zr的对称伸缩振动峰[31]。此外,C=O伸缩振动峰、-C-O伸缩振动峰和-OH的弯曲振动峰的峰强都显著下降,表明氧化锆通过与表面含氧官能团发生相互作用成功负载于活性炭纤维上。
图4是活性炭纤维改性前后的XPS全谱图结果。对比改性前后的XPS谱图发现,ACF-O表面仅出现C1s和O1s的特征峰,而ACF-ZR还出现了Zr3d和Zr3p的特征峰,且C1s的特征峰峰减弱了。改性前后材料的比表面积以及ACF-Zr上氧化锆在体相中的含量结果列于表1。从表1中可知,氧化锆在ACF-Zr体相含量为12.73wt%,且负载氧化锆后材料的比表面积由837 m2·g-1降为497 m2·g-1,这可能是由于氧化锆堵塞了部分活性炭纤维表面或者端口开口的微孔结构,进而导致比表面积的下降。

图2 材料ACF-O(a)和ACF-Zr(b)的XRD图Fig.2 XRD patterns of ACF-O(a)and ACF-Zr(b)

图3 材料ACF-O(a)和ACF-Zr(b)的FT-IR图谱Fig.3 FTIR spectra of ACF-O(a)and ACF-Zr(b)

图4 材料ACF-O(a)和ACF-Zr(b)的XPS全谱图Fig.4 XPS wide spectra of ACF-O(a)and ACF-Zr(b)

表1 材料的结构性质Table1 Structural properties of the samples
2.2吸附等温线
图5为氧化后的活性炭纤维 (ACF-O)和氧化锆-活性炭纤维复合材料(ACF-Zr)对F-的吸附等温线结果,从图中可以看出,ACF-O对F-的吸附很低,而ACF-Zr对F-的吸附量显著增加,说明材料表面的氧化锆是F-的有效活性吸附位点。主要原因是活性炭纤维经氧化处理后表面产生较为丰富的含氧官能团,有机锆源(正丙醇锆)则利用这些含氧官能团作为其活性作用位点从而被固定下来,并进一步发生水解反应,在表面多以Zr-OH的形式存在;与此同时,由于活性炭纤维表面的含氧官能团的分布位置不同,从而促进了锆在表面的高度分散,有效的减小了团聚的发生,能暴露出更多可供F-吸附的活性位点,从而大大提高了吸附量。F-离子是通过离子交换机制得以被去除,表面羟基的存在可能是去除水体中F-的关键,这与之前的报道结果一致[15,32],其除氟的机理可简单表示为:


图5 F-在ACF-O和ACF-Zr吸附等温线Fig.5 Adsorption isotherms for F-on ACF-O and ACF-Zr
此外静电作用力也是F-在ACF-Zr上的吸附作用力之一,为了进一步的验证,我们考察了pH值对吸附的影响(见2.4)。
吸附等温线结果分别用 Langmuir方程和Freundlich方程模型拟合,拟合参数如表2所示。通过表2中的拟合参数可以看出,Langmuir模型可很好地对吸附数据进行拟合,说明F-在ACF-Zr上的吸附为表面的单层吸附。
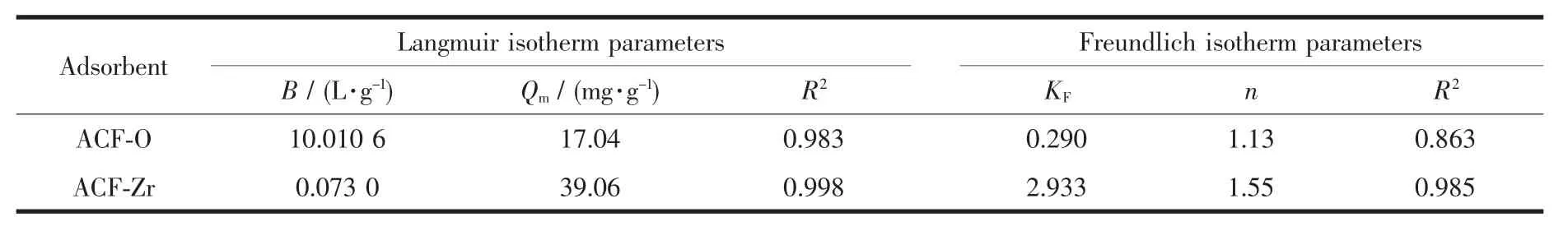
表2 Langmuir和Freundlich模型拟合参数:Qm,b,KF与n和R2Table2 Langmuir and Freundlich Model Parameters,Qm,b,KFand n and R2
2.3吸附动力学
ACF-Zr对F-吸附动力学曲线如图6所示。由图可见,在吸附初期,F-的吸附量随吸附时间推移而快速增加,随着时间的延长,吸附量增加缓慢。从图6可以看出,当初始浓度为15 mg·L-1时,吸附在100 min左右趋于平衡;初始浓度为30 mg·L-1时,吸附在200 min左右趋于平衡。吸附过程分别用拟一级动力学方程(式3)和拟二级动力学方程(式4)进行拟合,

式中,Qexp为平衡吸附量的实验值,mg·g-1;Qt是t时间时的吸附量,mg·g-1;Qe为平衡吸附量的拟合值,mg·g-1;t为时间,min;k1和k2分别为拟一级动力学和拟二级动力学速率常数。

图6 ACF-Zr对F-的吸附动力学Fig.6 Adsorption kinetics of F-on ACF-Zr plotted as solid-phase concentration vs time
按上述两式拟合结果列于表3。通过拟合发现,按照拟一级动力学方程拟合得到的相关系数R2较低,且计算得到的平衡吸附量与实验所得平衡吸附量相差甚远;而按照拟二级动力学拟合得到的相关系数R2>0.999,且拟合得到的平衡吸附量与实验数值非常接近,表明ACF-Zr对F-吸附符合拟二级动力学。根据表3的结果,当F-初始浓度分别为15 mg·L-1和30 mg·L-1时,ACF-Zr对F-的平衡吸附量分别为22.8 mg·g-1和48.03 mg·g-1,拟二级动力学吸附速率常数分别为 1.30×10-3g·mg-1·min-1和2.75×10-3g·mg-1·min-1,即平衡吸附量随着初始浓度的增加而增加,吸附速率也是随着初始浓度的增加而增加。

表3 不同初始浓度下的F-在ACF-Zr拟一级和拟二级动力学拟合结果Table3 Comparison of the pseudo-first-order and pseudo-second-order rate constants at different initial concentrations for F-adsorption onto ACF-Zr
2.4pH值对吸附的影响

图7 pH值对ACF-Zr吸附F-的影响Fig.7 Adsorption of F-on ACF-Zr as a function pH
不同pH值条件下ACF-Zr对F-吸附结果如图7所示,pH值为吸附平衡时的pH值。从图7可见,ACF-Zr对F-的吸附量随着pH的增加而降低;这与F-在ACF-Zr上的吸附机理密切有关。当pH值较低时,吸附剂表面因质子化而带正电,溶液中的F-因为静电吸引作用力被吸附于材料的表面[33],导致了比较高的吸附量。当pH增加时,吸附剂表面因去质子化而带负电,使得静电作用力减弱,吸附量下降,但由于溶液中的F-可以通过离子交换作用与吸附剂表面的Zr-OH发生配体交换,因而仍可吸附部分F-;当pH值进一步增加,溶液中的OH-浓度逐渐增加,与F-形成了强竞争吸附[34],导致ACF-Zr对F-吸附量的进一步下降。pH值影响结果很好的验证了静电相互作用力也是F-在ACF-Zr上吸附的重要作用力之一。
2.5离子强度的影响
阴离子广泛存在各种水体中,研究各种阴离子对ACF-Zr吸附F-吸附效果的影响具有重要的现实意义。3种阴离子离子Cl-、NO3-和SO42-分别对F-在ACF-Zr上的吸附影响如图8所示。从图8可以看出,3种阴离子对ACF-Zr吸附F-几乎没有影响,并且随着3种阴离子的浓度从0 mg·L-1增加到100 mg·L-1,其对F-吸附影响仍然比较小,这与文献的研究结果是相同的[13]。实验结果说明,ACF-Zr可以应用于存在高浓度上述离子的废水溶液中,用以实现F-的吸附去除。

图8 共存离子对F-在ACF-Zr吸附上影响Fig.8 Effect of coexisting ions for F-adsorption on ACF-Zr
3 结 论
本文采用水热合成法制备了氧化锆负载的活性炭纤维ACF-Zr,表征结果表明氧化锆成功负载与活性炭纤维表面上,并且高度分散在活性炭纤维表面。ACF-Zr对水体中的F-具有较高的吸附容量,吸附量远高于活性炭纤维,吸附等温线符合Langmuir等温吸附模式,其吸附机理包括离子交换和静电作用力;ACF-Zr对F-具有较快的吸附速率,吸附动力学符合拟二级动力学模型。溶液的pH值能显著影响ACF-Zr对F-的吸附效果,酸性、中性条件有利于F-的去除,共存阴离子Cl-、NO3-和SO42-对F-的去除效果几乎没有影响。由于氧化锆和活性炭纤维都具有良好的耐受力,因此可以广泛地使用于不同pH值和各种高浓度的阴离子存在下的废水中。本研究所得复合材料易于合成,吸附容量高,在水处理去除F-方面有很好的应用潜力,亦可为新型除氟材料的合成提供参考。
[1]GU Hao(顾浩),XU Zhao-Yi(许昭怡),ZHENG Shou-Rong(郑寿荣),et al.Acta Scientiae Circumstantiae(环境科学学报), 2009,29(3):589-593
[2]ZHANG Qiang-Guo(张强国),XIE Guo(谢果).J.Chongqing University Sci.Technol.(重庆科技学院学报),2005,7(4):17-19
[3]YANG Hong-Xiao(杨红晓),ZHOU Ai-Dong(周爱东).Non-Ferrous Min.Metall.(有色矿冶),2005,21(1):46-49
[4]Amor Z,Bariou B,Mameri N,et al.Desalination,2001,133: 215-223
[5]Zeni M,Riveros R,Melo K,et al.Desalination,2005,185: 241-244
[6]Yang M,Zhang Y,Shao B,et al.J.Environ.Eng.,2001,127: 902-907
[7]Ku Y,Chiou H M,Wang W.Sep.Sci.Technol.,2002,133: 349-360
[8]Ku Y,Chiou,H M.Water Air Soil Pollut.,2002,133:349-360
[9]LIU Xue-Yan(刘雪岩),JIANG Xin(姜鑫),LU Yi(逯义), et al.Acta Scientiae Circumstantiae(环境科学学报),2012, 32(8):1833-1841
[10]WANG Shu-Guang(王曙光),LI Yan-Hui(李延辉),ZHAO Dan(赵丹),et al.Chem.J.Chinese Universities(高等学校化学学报),2003,24(1):95-99
[11]FAN Jie(范杰),XU Zhao-Yi(许昭怡),ZHENG Shou-Rong (郑寿荣)et al.Environmental Chemistry(环境化学),2006, 25(4):425-428
[12]YAO Rui-Hua(姚瑞华),MENG Fan-Ping(孟范平),ZHANG Long-Jun(张龙军)et al.Ion Exch.Adsorpt.(离子交换与吸附),2009,25(4):319-326
[13]Wasay S A,Haron M J,Tokunaga S.Water Environ.Res., 1996,68:295-300
[14]LIU Rui-Xia(刘瑞霞),TANG Hong-Xiao(汤鸿霄).Chinese J.Environ.Sci.(环境科学),2000,21(4):34-37
[15]MA Gang-Ping(马刚平),LIU Zhen-Ru(刘振儒),ZHAO Chun-Lu(赵春禄).China Environ.Sci.(中国环境科学),1999,19(4):345-348
[16]Zhao Y P,Li X Y,Liu L,et al.Carbohydr.Polym.,2008,72: 144-150
[17]Liao X P,Shi B.Environ.Sci.Technol.,2005,39:4628-4632 [18]Zhang S,Li X,Chen J P.Carbon,2010,48:60-67
[19]Mochida I,Korai Y,Shirahama M,et al.Carbon,2000,38: 227-239
[20]Shen W Z,Wang H,Guan,R G,et al.Colloids Surf.A, 2008,331:263-267
[21]Zhang L,Wan L H,Chang N,et al.J.Hazard.Mater.,2011, 190:848-855
[22]Zhang L,Zhou Q,Liu J Y,et al.Chem.Eng.J.,2012,185: 160-167
[23]Tang Y Q,Zong E M,Wan H Q,et al.Microporous Mesoporous Mater.,2012,155:192-200
[24]Park S J,Jang Y S.J.Colloid Interface Sci.,2003,261:238-243
[25]Ganr V,Sharma A,Verma N.Chem.Eng.Process.,2006,45: 1-13
[26]Chitrakar R,Tezuka S,Sonoda A,et al.J.Colloid Interface Sci.,2007,313:53-63
[27]Gaur V,Sharma A,Verma N.Chem.Eng.Process.,2006, 45:1-13
[28]Szabo T,Berkesi O,Dekany I.Carbon,2005,43:3186-3189
[29]Liu M H,Yang Y L,Zhu T,et al.Carbon,2005,43:1470-1478
[30]Seredych M,Bandosz T J.J.Phys.Chem.C,2010,114:14552 -14560
[31]Kytokivi A,Lakomaa E L,Root A,et al.Langmuir,1997, 13:2717-2725
[32]Wu X M,Zhang Y,Dou X M,Yang M.Chemosphere,2007, 69:1758-1764
[33]Alagumuthu G,Rajan M.Chem.Eng.J.,2010,158:451-457
[34]Raichu A M,Basu M J.Sep.Purif.Technol.,2001,24:121-127
Adsorption of Fluoride Ion by Zirconia Functionalized Activated Carbon Fiber
LIU Jing-Liang*,1ZONG En-Min3CHEN Huan2XU Zhao-Yi4
(1School of Environmental Science,Nanjing XiaoZhuang University,Nanjing 211171,China) (2School of Life Science,Taizhou University,Taizhou,Zhejiang,317000,China)
(3School of Environmental and Biological Engineering, Nanjing University of Science and Technology,Nanjing 210094,China) (4State Key Laboratory of Pollution Control and Resource Reuse, School of the Environment,Nanjing University,Nanjing 210046,China)
Zirconia functionalized activated carbon fiber(ACF-Zr)adsorbent was successfully prepared using the post-grafting method and its adsorptions for fluoride ion(F-)uptake were investigated in details.Characterized results demonstrated that zirconia was highly dispersed on the surface of active carbon fiber.Adsorption experiment indicated ACF-Zr has high removal efficiency of F-,because of ion exchange andelectrostatic interaction.The adsorption isotherm could be well described by the Langmuir adsorption model and adsorption kinetics on ACF-Zr followed by pseudo-second-order kinetics.The adsorption capacity decreased with the increase of solution pH value.Nearly no influence was observed by solution coexisting ions Cl-,NO3-and SO42-.
active carbon fiber;F-;adsorption;zirconia
O647.3;TB333
A
1001-4861(2015)06-1105-07
10.11862/CJIC.2015.152
2015-01-19。收修改稿日期:2015-04-03。
国家自然科学基金(No.31471699,21407074,51208257),江苏省生态学“十二五”省重点建设学科项目和南京晓庄学院项目(No.2012NJX103)资助。
*通讯联系人。E-mail:liujingliangnju@163.com