腹腔镜手术治疗肝良性肿瘤18 例体会
2015-11-22折占飞张俊斌
王 亮,折占飞,张俊斌,齐 鑫
(鄂尔多斯市中心医院康巴什部,内蒙古 鄂尔多斯,017100)
1991 年Reich 等[1]首次报道了肝良性病变的腹腔镜局部切除术。1996 年Azagra 等[2]发表了腹腔镜解剖性肝左外叶切除术,自此,腹腔镜肝脏切除术的报道逐渐增多,随着腹腔镜技术的成熟、器械的改进,腹腔镜技术治疗肝良性肿瘤获得迅猛发展。与开腹手术相比,腹腔镜肝切除术在创伤程度、恢复时间等方面具有明显优势。本文旨在通过对比我院所行的完全腹腔镜及开放肝良性肿瘤切除术,总结腹腔镜肝良性肿瘤切除术的手术体会,探讨此术式在基层医院开展的可行性。
1 资料与方法
1.1 临床资料选取2013 年9 月至2015 年5 月于我院行腹腔镜与开放肝良性肿瘤切除手术的病例各18 例,均由病理确诊为肝脏实性良性肿瘤。经我院伦理委员会审批,患者或家属签署知情同意书。腹腔镜组男10 例,女8 例;31 ~58岁,平均(38.65±3.78)岁。开放组男12 例,女6 例;34 ~71岁,平均(42.34±5.65)岁。腹腔镜组入选标准:不合并其他肝脏及胆道疾病的肝良性肿瘤患者,肿瘤位于肝脏第Ⅱ、Ⅲ、Ⅴ、Ⅵ段,肿瘤为单一病灶,肿瘤大小及位置不影响第一、第二肝门的解剖,肝功能Child 分级均为A 级。排除标准:既往有腹部手术史;多发病灶;肝功能失代偿;重要脏器功能障碍者无法耐受麻醉。开放组:适合腹腔镜手术标准,自愿选择传统开腹手术。
1.2 手术方法腹腔镜、开腹肝脏切除术均常规消毒铺巾,气管插管,采用静脉复合麻醉,开放手术遵循常规手术方法应用多功能手术解剖器施术。腔镜手术步骤如下:患者取头高脚低位(术中可根据病灶位置调整体位)。行腹腔镜肝脏切除术时,于脐上缘0.5 cm 处穿刺10 mm Trocar,常规建立气腹,压力为12 ~13 mmHg,脐孔套管内置腹腔镜观察腹腔,分别于剑突下、右锁骨中线、腋前线肋缘下2 ~3 cm 处穿刺Trocar,穿刺点按常规开腹手术切口排列,以便于中转开腹手术。切除肝脏实性结构时采用超声刀与LigaSure,分为不规则肝切除与规则性肝切除。手术第一步是肝周韧带的游离,游离程度为完全显露所切除肝段、瘤体。较传统开腹肝切除术肝游离程度范围、程度减小。因为腹腔镜切肝为从前向后,从浅入深逐步推进,肝脏整体原位不动,直视下断肝,仔细处理肝内脉管结构。常规第一肝门Pringle 法预置肝门阻断带(图1),视术中情况必要时行肝血流阻断,两段以上的肝切除、肝功较差时行选择性肝叶血流阻断。应用电钩及超声刀、LigaSure 分离囊肿壁、肝组织(图2、图3),较大血管(直径>3 mm)预先Hem-o-lok 夹闭。最后冲洗肝脏创面,充分彻底止血,常规于膈下放置腹腔引流管,用自制标本袋取出标本。

图1 预留肝门阻断带(箭头所示)

图2 超声刀切开肝表面

图3 LigaSure 断肝,瘤体牵引电钩止血
1.3 观察指标分别记录两组患者手术时间、术中出血量、术后住院时间及胆漏、出血等术后并发症发生情况。术后随访24 个月,随访患者术后恢复及复发情况。
1.4 统计学处理应用SPSS 15.0 软件进行统计学分析,本实验计数资料用χ2检验,计量数据采用均数±标准差(±s)表示,采用t 检验。P <0.05 为差异有统计学意义。
2 结 果
两组患者性别、年龄、肿瘤大小、肿瘤位置间差异无统计学意义(P >0.05)。见表1。两组患者病理结果包括:肝脏血管瘤(腹腔镜组13 例,开腹组14 例)、肝脏局灶结节性增生(2/2)、炎性肉芽肿(3/1)、肝脏腺瘤(0/1)。经术后观察及院外随访,两组患者术后恢复良好,均未出现胆漏、出血、感染等并发症。两组手术时间、术中出血量、术后住院时间、术后第1 天引流量差异有统计学意义。见表2。
表1 两组患者术前情况的比较(±s)

表1 两组患者术前情况的比较(±s)
?
表2 两组患者手术情况的比较(±s)
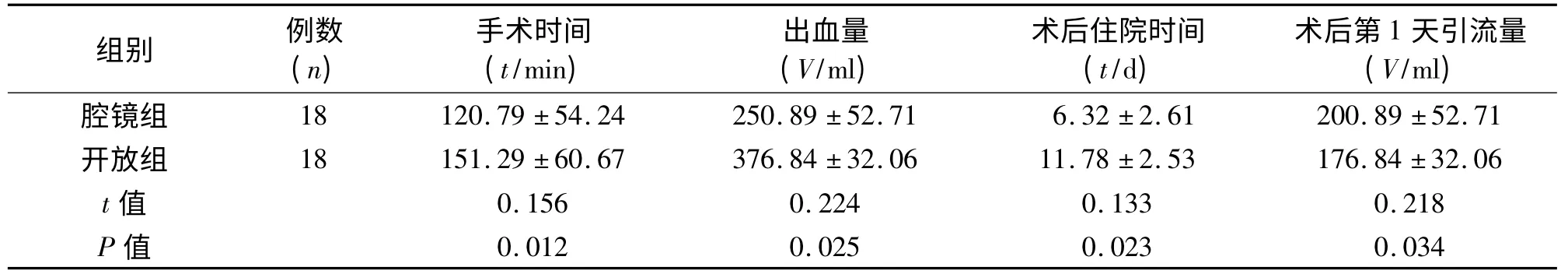
表2 两组患者手术情况的比较(±s)
?
3 讨 论
自1991 年国内开展第1 例腹腔镜胆囊切除术以来,在外科的每一个领域,微创外科手术无论是技术抑或理论都取得了迅速、广泛的发展。腹腔镜肝切除术已不再是梦想,已成为现实,国外Nguyen等[3]已报道2 804 例腹腔镜肝切除术,深入分析国际上用英语发表的腹腔镜肝切除文献,共2 804 例报道,以楔形切除及肝段切除最多,占45%;围手术期病死率为0.3%,肝细胞癌切除术后的5 年存活率及5 年无癌存活率分别为50%~75%及31%~38%。至2008 年国内已施行单纯腹腔镜肝切除术735 例,其中50%为恶性病变。因此,可以认为微创肝脏外科已走向成熟,但也不可否认单独腹腔镜手术仍然有不少困难、限制。
由于肝脏解剖及功能的复杂性,腹腔镜肝切除术是风险较高、难度较大的手术,专家一致认为应由经过系统培训、熟练掌握肝切除术、腹腔镜技术的外科医师实施[4]。同时,腹腔镜肝切除术的适应证相对要求严格,主要受到肝脏病变部位、范围、肝功能的限制。尤其肝脏病变的部位对腹腔镜手术而言要求较高。因此,要严格把握手术指征,病变位于Couinaud Ⅱ、Ⅲ、Ⅳa、Ⅴ、Ⅵ段,病变大小不影响第一、第二肝门的解剖为准,瘤体直径<15 cm,病变太大会影响暴露,操作空间小,且创面大,止血困难,渗血较多,患者肝功能要求在B 级以上,其他脏器无严重器质性病变,能够耐受腹腔镜手术[5],我们体会,由于基层医院缺少腔镜超声的术中指示,我们通常通过术前影像学检查,选择腔镜下可以看见的肿瘤,腹腔镜肝切除术的适应证并不是绝对的,术者可以根据自己的经验、技术特点,通过改变体位、加用器械辅助等方法扩大手术适应证。
我们总结了以下手术要点:首先,腹腔镜操作孔的位置一般根据切除的肝脏病变部位而定,以便于术中操作,器械可互不影响。我们的腹腔镜肝叶切除术一般应用四孔法,病变在右肝者主操作孔位于剑突下,病变在左肝者主操作孔位于左锁骨中线肋缘下,副操作孔、主操作孔及腹腔镜孔应保持一定的距离,以免影响主刀的操作。两个副操作孔也不宜太近,一般取5 cm,以免操作时互相干扰。取标本时,切口可选择绕脐切口。其次,术区的暴露除采用适合的体位外,术中可使用金手指、扇形拉钩等器械协助手术视野的暴露。术中腔镜下操作应轻柔,避免抓、捅等粗暴动作,或者因止血打乱手术的节奏。此外,对创面的处理主要是止血、防止胆漏。了解并选择合适的腹腔镜下止血设备,超声刀可处理直径3 mm 以下血管,LigaSure 可处理直径7 mm 的血管;生物夹、Hem-o-lok 可夹闭较粗的血管,Endo-GIA 可直接切割闭合肝蒂,不受血管管径的限制。确认断面无出血及胆漏后,可用生物蛋白胶涂抹,但使用生物蛋白胶的患者有3 例,术后1 个月复查肝脏超声可见创面处的包裹性积液。本实验中2 组手术病例均未出现出血、胆漏等并发症发生,可见腹腔镜肝切除术的手术效果较好。
与传统开放手术相比,腹腔镜肝良性肿瘤切除术手术时间短,出血量较少,患者术后康复快。只要合理选择符合手术适应证的病例,把握手术要点,在基层医院开展腹腔镜肝良性肿瘤切除术是可行的。
[1] Reich H,McGlynn F,DeCaprio J,et al.Laparoscopic excision of benign liver lesions[J].Obstet Gynecol,1991,78(5 Pt 2):956-958.
[2] Azagra JS,Goergen M,Gilbart E,et al.Laparoscopic anatomical(hepatic)left lateral segmentectomy-technical aspects[J].Surg Endosc,1996,10(7):758-761.
[3] Nguyen KT,Gamblin TC,Geller DA.World review of laparoscopic liver resection-2,804 patients[J].Ann Surg,2009,250(5):831-841.
[4] Buell JF,Cherqui D,Geller DA,et al.The international position on laparoscopic liver surgery:The Louisville Statement,2008[J].Ann Surg,2009,250(5):825-830.
[5] 刘荣.腹腔镜肝脏外科手术操作要领与技巧[M].北京:人民卫生出版社,2014:33.
