第二相碳对LiFePO4/C正极材料性能的影响
2015-11-21孙文仙王红强张经济郑锋华李庆余
孙文仙, 王红强, 张经济,郑锋华,李庆余
(广西师范大学化学与药学学院,广西桂林541004)
锂离子电池以其比能量高、循环寿命长等优点,成为较理想的高容量电池[1]。正极材料是限制锂离子电池发展的关键因素,它将直接影响到电池的能量密度、比功率、温度特性以及安全特性。其中橄榄石型结构的LiFePO4由于具有较高的电位(Li/Li+为3.4 V)[2]、较高的理论比容量(170 mAh/g)[3]以及优良的循环和安全性能等优点在动力型电池应用方面具有非常诱人的前景,成为锂离子电池正极材料的研究热点之一。
然而,由于磷酸铁锂较低的电导率及Li+在两相界面间的迁移速率限制了材料在较高倍率下容量的发挥[3-6]。为解决上述问题,碳包覆、金属离子或粒子掺杂以及纳米化[7-10]等工艺已被广泛应用于LiFePO4改性研究。其中,碳包覆工艺是研究较多、价格低廉有效、较易产业化的方法,然而大量地包覆碳又会大大降低材料的质量密度和电池的体积比能量,因此选择合适的碳源达到提高材料的电子电导率尤为重要。本文采用两步固相烧结法,第一步采用有机碳源经高温裂解后形成均匀的碳层包覆在LiFePO4表面,第二步采用无机碳源,期望使之分散于LiFePO4颗粒间形成连续的导电层以提高材料的电子电导性,着重探讨了第二步烧结过程中加入无机碳源对其电化学性能的影响。
1 实验
1.1 材料制备
将FeC2O4、LiH2PO4、C6H12O6·H2O(有机碳源)按化学计量比1∶1∶0.08准确称量,以水为分散剂球磨8 h后于120℃烘干,放入氮气保护的管式炉中于400℃高温处理12 h,得到初烧料。在初烧料中加入一定量的乙炔黑(无机碳源),球磨混料1.5 h,将得到的混合物放入氮气保护的管式炉中,于600℃高温处理8 h。得到二相复合碳源LiFePO4/C正极材料,记为样品A。作为对比,用相同的方法制备未加入乙炔黑的单一有机碳源LiFePO4/C正极材料,记为样品B。
1.2 材料表征
采用X射线粉末衍射仪 (Cu-Kα靶)对样品进行晶相分析,分析条件为波长λ=0.154 06 nm,管电压40 kV,管电流30 mA,扫描范围10°~90°,扫描速度为10(°)/min。采用FEI Quanta200场发射扫描电镜观察样品表面形貌、颗粒大小及分布状态。采用invia激光拉曼光谱仪对样品进行包覆碳结构分析,扫描范围为800~1 900 cm-1。用HCS-140型高频红外碳硫分析仪对样品中的碳含量进行分析。用SDY-5四探针电阻测试仪测定样品的电子电导率。
1.3 电池组装及测试
将LiFePO4/C样品、导电剂乙炔黑和粘接剂PVDF按质量比90∶5∶5称量并混合,加入适量NMP,搅拌均匀后涂覆于0.016 mm厚的铝箔上,在80℃下真空干燥4 h,轧膜后冲成直径13.5 mm的圆片,即为正极片。以金属锂片为负极,以Celgard2400聚丙烯微孔膜为隔膜,1 mol/L LiPF6/(EC+DMC+ EMC)(体积比1∶1∶1)溶液为电解液,在充满氩气的手套箱中组装成CR2032型扣式电池。在LAND电池测试系统上对实验电池进行恒流充放电测试,电压范围2.5~4.2 V。
2 结果与讨论
2.1 物相分析
图1为样品A和B的X射线衍射图谱(XRD),两种样品的衍射峰与橄榄石型晶体结构(JCPDS卡40-1499)相对应,属于正交晶系(Pnmb空间群),且无杂相生成。从XRD衍射图中并未发现碳的衍射峰,可能与碳含量低或碳以非晶态存在有关,这也说明碳的加入并没有影响到磷酸铁锂的橄榄石结构。表1为利用JADE软件对两种样品的XRD数据进行精修所获得的晶胞参数,与文献报道[11]基本吻合。
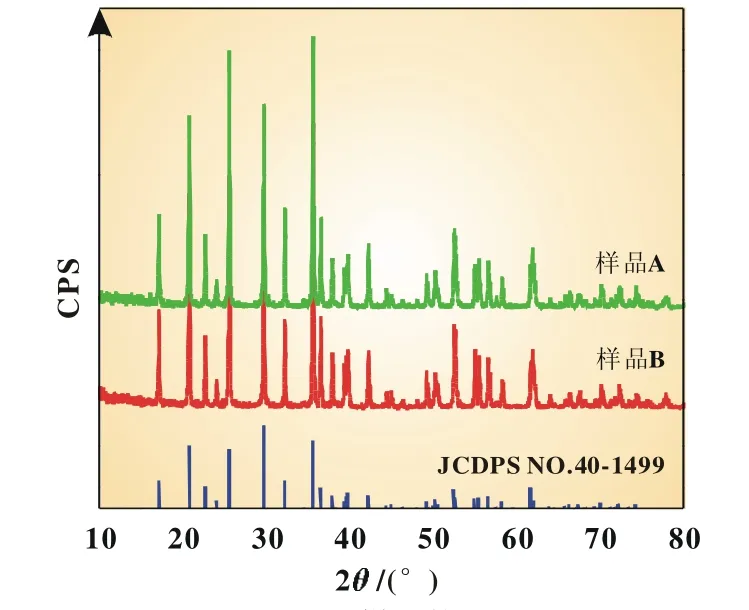
图1 样品的XRD
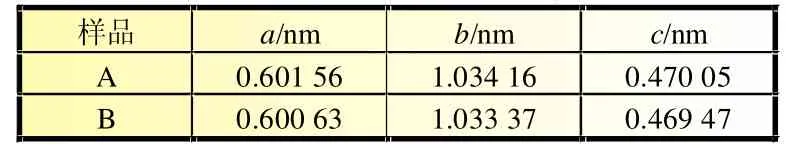
表1 样品材料的晶胞参数
2.2 形貌分析
图2为所得样品的扫描电子显微镜(SEM)图像,通过样品A和B对比初烧料可知,经过第二次烧结后,材料的粒径都有所增大,这与固相反应特征有关[12];样品A的LiFePO4颗粒粒径分布均匀,在100~300 nm之间,形貌规则,基本没有团聚现象,这可能是由于葡萄糖热分解产生的导电碳微粒和乙炔黑粉末包覆在LiFePO4晶粒表面或分布晶粒之间,有效抑制了LiFePO4晶粒的长大;样品B的LiFePO4颗粒呈团聚现象,颗粒大小很不均匀。在合成过程中,LiFePO4/C颗粒粒径较小以及团聚现象的减少有利于电解液的渗透和提高Li+的扩散速率,提高活性物质利用率,并提高材料的电化学性能。

图2 样品的SEM图像
2.3 拉曼分析
图3为LiFePO4/C样品的拉曼图谱,940、1 350和1 600 cm-1处分别出峰,其中,940 cm-1为LiFePO4中PO43-的伸缩振动峰,1 350和1 600 cm-1是碳的两个特征峰D峰和G峰,G峰来源于sp2碳原子键的伸缩振动,是石墨的特征峰;D峰来源于碳环的呼吸振动,与石墨片边缘的晶格对称性破缺、缺陷,晶型的不完整性,石墨片层间堆垛的无序化有关[13]。ID/IG的值大致上反映了无定形碳中和石墨结构的碳的比例,ID/IG比值越小,则表现出导电性能会越好[14]。
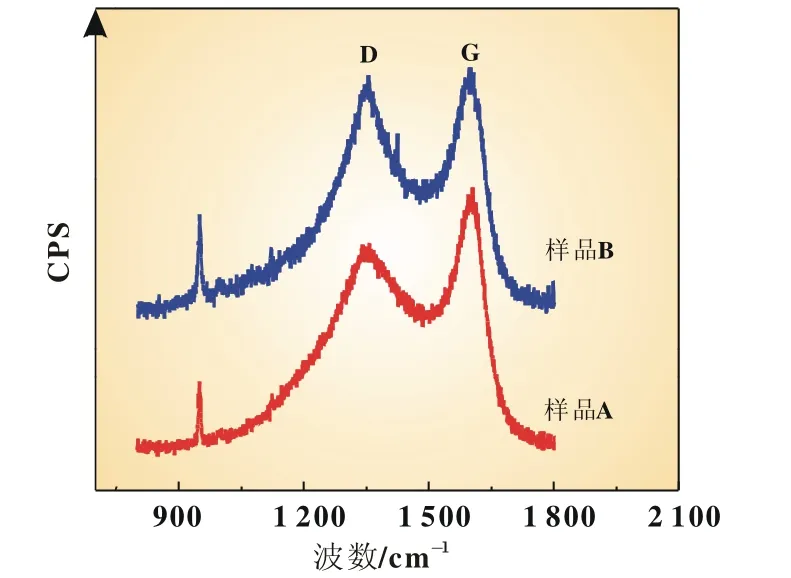
图3 样品的拉曼图谱
样品的ID/IG比值,碳含量以及材料的电导率见表2。根据红外碳硫仪的分析结果,样品A和B的含碳量分别为1.43%,和1.27%。加入第二相碳后,碳含量有所增加,ID/IG值也相应的减小,说明石墨化结构的碳含量增加,此值与样品所测的电子电导率的趋势保持一致,即加有二相复合碳源的LiFePO4/C的电子电导率明显提高。

表2 LiFePO /C样品的性能参数
2.4 电化学性能分析
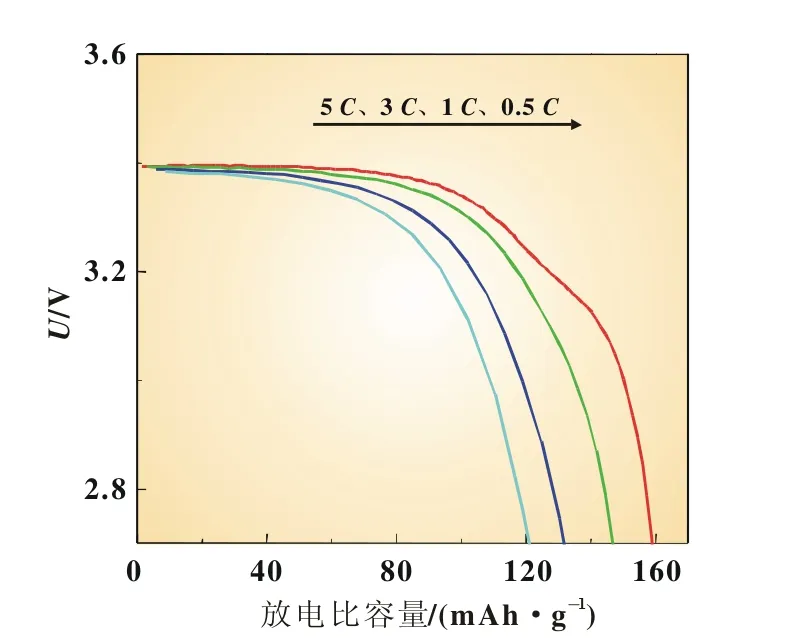
图4 样品A在各倍率下的放电曲线
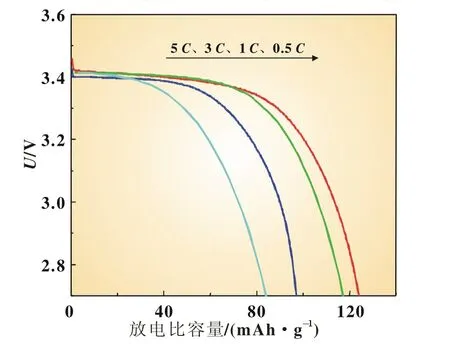
图5 样品B在各倍率下的放电曲线
图4、图5分别为样品A和样品B在放电倍率为0.5C、1 C、3C、5C下的放电曲线,测试温度为25℃,两种LiFePO4/C正极材料样品的放电电压平台均在3.4 V左右。二相复合碳源LiFePO4/C正极材料电池在0.5C、1C、3C、5C下放电比容量分别达到161、149.3、133.9、122.7 mAh/g,分别为理论容量的94.71%、87.82%、78.41%、72.18%。相比之下,单一有机碳源LiFePO4/C正极材料电池在0.5C、1C、3C、5C下放电比容量分别达到127.2、121.4、99.1、88 mAh/g,分别为理论容量的74.82%、71.41%、58.29%、51.76%。对比数据表明:二相复合碳源LiFePO4/C正极材料在各个倍率下的放电比容量均比单一有机碳源LiFePO4/C正极材料的高,前者的放电比容量更接近理论容量,说明加入乙炔黑使材料的放电比容量显著提高,可能是在加入第二相碳的情况下,乙炔黑分散在高温处理后得到的LiFePO4/C材料的颗粒中间使电子电导率增加,影响到了其放电容量。
图6为LiFePO4/C材料的两种样品在3C下的循环性能曲线,测试温度为25℃。在3C下,二相复合碳源LiFePO4/C正极材料初始放电比容量为133.9 mAh/g,循环30次后为128.5 mAh/g,保持率为95.97%;单一有机碳源LiFePO4/C正极材料初始放电比容量为99.1 mAh/g,循环30次后为85.2 mAh/g,保持率为85.97%。由此可知,加入乙炔黑提高了LiFePO4/C的循环性能。这可能是乙炔黑作为一种絮状连续碳源分布于颗粒间,架构出一个连续的导电桥,进一步促进了颗粒间的电子传导,由此提高了LiFePO4/C的循环性能。
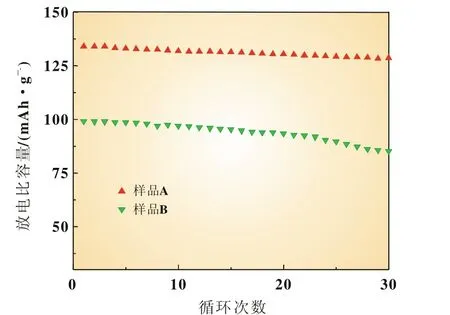
图6 样品在3C下的循环性能曲线
3 结论
采用高温固相法制备了复合碳源LiFePO4/C正极材料,研究发现:(1)加入第二相碳对材料的橄榄石型结构没有影响;(2)制备材料的颗粒较小,分布在100~300 nm之间;(3)通过拉曼光谱以及电子电导率的分析,加入第二相碳后材料中残余碳的石墨化程度提高,从而使电子电导率提高;(4)电化学性能测试结果表明加入乙炔黑的材料表现出较好的倍率性能和循环性能,在0.5C、1C、3C、5C下首次放电比容量分别为161、149.3、133.9、122.7 mAh/g,在3C下循环30次后,容量保持率为95.97%。
[1] TARASCON J M,ARMAND M.Issues and challenges facing rechargeable lithium batteries[J].Nature,2001,414:359-367.
[2]FRANGER S,CRAS F L,BOURBON C,et al.LiFePO4synthesis routes for enhanced electrochemical performance[J].Electrochem Solid-State Lett,2002,5(10):A231-A233.
[3]HUANG H,YIN S C,NAZAR L F.Approaching theoretical capacity of LiFePO4at room temperature at high rates[J].Electrochem Solid-State Lett,2001,4(10):A170-A172.
[4]CHUNG S Y,BLOKING J Y,CHIANG Y M.Electronical conductive phosphor-olivines as lithium storage electrodes[J].Nat Mater,2002,1(2):123-128.
[5]YAMADA A Z,CHUNG S C,HINOKUMA K.Optimized LiFePO4for lithium battery cathodes[J].Journal of the Electrochemical Society,2001,148(3):A224-A229.
[6]ISLAM M S,DRISCOLL D J,FISHER C A J,et al.Atomic-scale investigation of defects,dopants,and lithium transport in the LiFe-PO4olivine-type battery material[J].Chem Mater,2005,17(20): 5085-5092.
[7] AHMET Ö,EMRAH B,MAHMUT Ö.Effects of different carbon sources on a particle size of LiFePO4/C nanocomposite cathode active material for lithium-ion batteries[J].Advanced Science,2011 (3):108-112.
[8] CHEN Z Y,ZHU H L,JI S.Influence of carbon sources on electrochemical performances of LiFePO4/C composites[J].Solid State Ionics,2008,179:1810-1815.
[9] LI C F,HUA N,WANG C Y.Effect of Mn2+-doping in LiFePO4and the low temperature electrochemical performances[J].Journal of Alloys and Compounds,2011,509:1897-1900.
[10]DELACOURT C,POIZOT P,LEVASSEUR S,et al.Size effects on carbon-free LiFePO4powders-the key to superior energy density [J].Electrochemical and Solid-State Letters,2006,9(7):A352-A355.
[11] 朱令之,韩恩山,曹吉林,等.LiFePO4/C正极材料改进固相法优化合成[J].电源技术,2011,35(4):378-381.
[12] 胡国荣,童汇,张新龙,等.磷酸铁锂正极材料制备与电性能研究[J].电源技术,2007,31(3):233-235.
[13] LU C Z,FEY G T K.Study of LiFePO4cathode materials coated with high surface area carbon[J].Journal of Power Sources,2009,189:155-162.
[14] WANG D Y,LI H,WANG Z X,et al.New solid-state synthesis routine and mechanism for LiFePO4using LiF as lithium precursor [J].Journal of Solid Stae Chemistry,2004,177:4582-4587.
