柴油微乳体系对生物油增溶性能研究
2015-11-18李闪星袁兴中冷立健王雪丽付丽欢曾光明湖南大学环境科学与工程学院湖南长沙410082湖南大学环境生物与控制教育部重点实验室湖南长沙410082
李闪星,袁兴中*,冷立健,王雪丽,朱 仁,付丽欢,李 辉,曾光明(1.湖南大学环境科学与工程学院,湖南 长沙 410082;2.湖南大学环境生物与控制教育部重点实验室,湖南 长沙 410082)
柴油微乳体系对生物油增溶性能研究
李闪星1,2,袁兴中1,2*,冷立健1,2,王雪丽1,2,朱 仁1,2,付丽欢1,2,李 辉1,2,曾光明1,2(1.湖南大学环境科学与工程学院,湖南 长沙 410082;2.湖南大学环境生物与控制教育部重点实验室,湖南 长沙 410082)
利用鼠李糖脂(RL)为表面活性剂,不同碳链长度正构醇为助表面活性剂构建柴油逆胶束体系,进而研究了该体系对模拟生物油的增溶性能.以单位柴油逆胶束增溶生物油的量为评价指标,研究了生物油和柴油的体积比B/D、醇的种类、醇与表面活性剂的质量比C/R及表面活性剂的浓度对生物油增溶性能的影响,并对最佳增溶条件下获得的生物油/柴油微乳体系进行了性能分析,包括元素分析、傅里叶红外分析、热稳定性和燃料产品指标分析等.当生物油与柴油的体积比B/D为3:7,RL浓度为15g/L,助表面活性剂选用正庚醇且醇与表面活性剂的质量比C/R为2.0时,柴油微乳体系增溶生物油的量最大,性能较佳.
鼠李糖脂;模拟生物油;柴油微乳体系;正构醇
近年来,全球性的能源危机、化石能源的日益枯竭及其大规模使用所导致的环境污染,对社会和环境造成了严重的负担.各种生物质能、太阳能等可再生能源将逐步取代化石能源,成为未来的主导能源[1].生物质衍生生物油(以下简称:“生物油”)是生物质能的一种,是指通过热化学转化技术,如低温热解液化和热化学直接液化,处理生物质转化形成的液态生物能源[2].研究表明生物油的组成和结构非常复杂,已被确认的化合物多达数百种,如酮、酯、酚、醇、醛和有机酸等[3-5].然而,生物油的燃料特性较差,存在含水率大、氧含量高、热稳定性差和有腐蚀性等缺点,导致其应用受限[6].为了使生物油可以直接作为内燃机燃料使用,借助柴油乳化或微乳燃料来精制生物油是一种行之有效的手段[4,7-13].
柴油微乳燃料,是由表面活性剂、助表面活性剂、柴油和水组成的透明均一、热力学稳定的分散体系[14].研究证明柴油微乳液在燃烧过程中可减少烟尘、氮氧化物和碳氢化合物的排放,是一种应用前景非常广阔的节能降污产品[15].当表面活性剂在非极性有机溶剂中超过临界胶束浓度(CMC)时,会形成逆胶束[16].将生物油增溶进柴油逆胶束体系可形成稳定的柴油-生物油微乳液体系(亦可称之为“生物柴油”),从而达到生物油与柴油混合乳化的目的.
表面活性剂是构成逆胶束油包水结构的关键因素,而目前柴油微乳体系大多使用化学表面活性剂来研究[15,17].然而产生于微生物发酵过程中的生物表面活性剂,其低毒性、可降解性、生态相容性和高效性等优势使柴油-生物油微乳液燃料具有“环境可持续性”的优点[18].鼠李糖脂(RL)作为生物表面活性剂的代表,在构建逆胶束体系中取得了难以比拟的效果[18-19],但却很少用于生物油与柴油混合乳化的研究.
本文以RL为表面活性剂,以中长碳链正构醇(正丁醇、正戊醇、正己醇、正庚醇及正辛醇)为助表面活性剂,考察生物油与柴油体积比(B/D)、助表面活性剂醇的种类、醇与表面活性剂质量比(C/R)和表面活性剂的浓度对柴油逆胶束体系增溶生物油的性能的影响.通过筛选得出柴油微乳体系增溶生物油所需的最佳状态,并对体系的性能进行分析研究,从而为通过柴油逆胶束体系来精制生物油的应用提供有价值的参考.
1 实验部分
1.1 试剂与仪器
表面活性剂:鼠李糖脂(RL),纯度>90%(wt.%),平均相对分子质量601,湖州紫金生物科技有限公司;助表面活性剂:正丁醇、正戊醇、正己醇、正庚醇及正辛醇,中国医药集团上海化学试剂公司;柴油(0#):市售0#柴油,中国石油化工集团公司加油站;超纯水:RO超纯水机,上海和泰仪器有限公司;罗丹明B(RB):天津市大贸化学试剂厂.除柴油和超纯水外,其他所用试剂均为分析纯.
生物油是一种高氧含量、组分复杂的化合物,利用模拟生物油研究增溶性能具有典型性,可为生物油原油的增溶提供理论指导.根据热解油中主要化合物的类型和含量,本实验室按照一定的配方制备了模拟生物油样品,见表1[20].具体方法如下:在25℃下,将葡萄糖和香兰素混合于水中2小时,待完全澄清后再加入甲醇、乙酸、乙二醛、丙酮醇、糠醛、愈创木酚,最后加入易挥发的乙醛[21].所得生物油样品pH值为2.20.所用试剂均购买于中国医药集团上海化学试剂公司.

表1 模拟生物油样品的成分[20]Table 1 Main compositions of synthetic bio-oil[20]
主要仪器:LS55型荧光分析仪,IKA RT 5型高效5点加热磁力搅拌器,TGL-16G型离心机,EL III型元素分析仪,傅里叶变换红外分光光度计(Nicolet 5700,USA),SDACM500型热值测定仪,PHSJ-5型PH值测定仪,SYD-260A水分测定仪,KD-R0515运动粘度测定仪,石油产品硫含量测定器,SL602型全自动酸值测定仪.
1.2 实验方法
1.2.1 荧光光度法测定RL在柴油微乳液的CMC 以超纯水为溶剂,配置浓度0.001mol/L的RB溶液备用.改变RL的用量,配制一系列浓度不同的柴油逆胶束体系.通过荧光光谱仪测量各体系中RB的荧光发射强度,根据RB荧光强度的变化规律确定油相中RL的CMC.相关参数为:最大激发波长564nm,激发狭缝宽度2.5nm,发射狭缝宽度8nm,扫描速度500nm/min.
1.2.2 生物油/柴油微乳体系的制备 以RL为表面活性剂,正丁醇、正戊醇、正己醇、正庚醇和正辛醇为助表面活性剂,制备生物油/柴油微乳体系.具体方法:
(1) 在50mL的锥形瓶中加入一定数量的柴油,然后加入一定浓度的RL,搅拌至溶解;
(2) 按与RL的质量比(0.2, 0.4, 0.6, 0.8, 1.0,2.0, 3.0)加入相应的正构醇,再按与柴油的体积比(9:1, 8:2,…… 1:9)加入一定数量的生物油,搅拌15分钟后转移至10mL的刻度容器中静置,随时记录分层.对于所有混合样品,在5~10分钟内会迅速分层,待3小时分层完全固定后,取上层生物油/柴油微乳溶液进行后续实验.根据具体实验数据,测量微乳条件对生物油的增溶性能S(V/V)和E(L/mol)的影响.参数S(V/V)和E(L/mol)分别代表单位体积的柴油所增溶生物油的体积量、单位摩尔表面活性剂所增溶生物油的体积量,其中Emax(L/mol)代表C/R固定条件下某种醇获得的最大E(L/mol)值.
1.2.3 生物油/柴油微乳体系的燃料性能 稳定性测定 用自然静置和离心法测量生物油/柴油微乳液的稳定性.首先将上述实验制备的微乳液在室温下静置一个月,然后观察其状态(颜色、透明度)随时间的变化,再将其置于离心试管中于5000r/min条件下离心30min,观察微乳液状态,判断其是否分层或浑浊.
分析方法 对0#柴油、生物油和研究构建的生物油/柴油微乳体系的部分燃料特性指标进行测定,并进行对比,分析生物油/柴油微乳液作为石油产品燃料的可行性和优越性.根据JY/T 017-1996 元素分析仪方法通则测定了燃料样品中的C、H、N元素的含量.通过傅里叶红外光谱分析,分析了样品中的主要有机成分.按照全自动酸值测定仪的使用方法测量了样品的酸值.参照ASTM D240-02 测量样品的热值,GB/T3535测量倾点,GB/T6986测量浊点,ASTM D130测量腐蚀性,GB/T265测量运动粘度,GB/T1884测量密度,GB/T380测量硫含量[22-28].
热稳定性测定 采用日本TG/DTA 7300热重分析仪在氮气气氛下对燃料样品进行热稳定分析,考查样品的热稳定特性,计算热分析特性参数.实验过程燃油样品质量约为25~45mg,采用10℃/min的加热速率,温度范围30~600℃.
2 结果与讨论
2.1 荧光探针法测定RL在柴油微乳液中CMC
逆胶束(又称“反胶束”或“反胶团”),是表面活性剂两性分子在非极性有机溶剂中超过其CMC时自发形成的聚集体.目前RL在水相中的CMC已被测得,但柴油逆胶束中的溶剂为油相,油相中CMC还未知.在本实验中,以RB为探针,利用荧光法测量RL在油相中的CMC.在油相中,当RL的浓度达到CMC时,其疏水的非极性尾部指向油相,亲水的极性头部指向聚集体内部,构成一个纳米大小的极性核(polar core).由于表面活性剂对RB有着增溶作用,在CMC附近时,RB水溶液分子插入到了聚集体核内,导致其荧光发射强度发生了一个突变,根据这种变化规律从而得到了体系的CMC[29].
由图1可知,不同RL浓度下柴油微乳体系的荧光发射强度有个突出的拐点,而拐点位置对应的浓度即RL在柴油微乳液中的CMC.以CMC为分界,荧光发射强度分为两个过程.当RL浓度小于CMC时,逆胶束胶团尚未形成,染料探针RB主要以分子状态存在于水溶液体系中,随着RL浓度的增大,荧光发射强度逐渐加强.当RL浓度接近CMC时,逆胶束胶团逐步形成,此时染料分子逐渐在胶团的亲水端吸附富集形成染料分子聚集体,因而荧光减弱,发射强度突然下降,直至浓度完全达到CMC时出现一个最低值.当RL浓度大于CMC时,逆胶束胶团也会逐渐增多,且溶液中可能存在未插入胶团核的游离RB单体,荧光发射强度出现缓慢增长[30].

图1 不同RL浓度下的荧光发射强度Fig.1 Fluorescence intensity of different RL concentrations
经测量,RL在油相中的CMC为4g/L或6.66×10-3M/L,此数值略高于其在水相中的CMC(1-2×10-4M/L)[19].RL属于一种偏向于亲水性的表面活性剂,用来制备柴油微乳液具有一定的可行性.
2.2 微乳因素对生物油增溶性能的影响
生物油/柴油的体积比B/D、助表面活性剂醇/表面活性剂RL的质量比C/R及醇的类型对生物油增溶性能的影响见图2.RL固定0.1g(CMC为4g/L),B/D变化范围为1:9到9:1(V/V),C/R变化范围为0到3.0(M/M).当B/D从5:5变化到9:1时,发现柴油增溶到了生物油中,其增溶机制与本研究不符合,所以未予以考虑.由图2可知,随着B/D的变化,S和Emax值都有明显的变化,且不同的B/D比例下,S和Emax的增长趋势类似,其中Emax对应正庚醇.根据实验数据,当助表面活性剂为正庚醇时,柴油微乳液体系对生物油的增溶达到最大,其最大S值(0.083)和Emax值(4.64L/mol)在B/D为3:7和C/R为2.0时获得.

图2 不同B/D比例、C/R比例和醇的类型对生物油增溶性能的影响Fig.2 Effect of initial B/D ratio,C/R ratio and cosurfactant type on the bio-oil solubilization capacity
2.2.1 B/D比例的影响 如图2所示,不加醇时,随着B/D的增大,S值和Emax值先缓慢增加,当B/D达到3:7时,所有S值和Emax值趋于最大,当B/D超过3:7时,S值和Emax值增长速度缓慢甚至部分出现下降的趋势.当B/D为1:9时,S值和Emax值明显低于其他3个比例,其最大的S值0.044和Emax值2.40L/mol在正庚醇为助表面活性剂时获得.B/D为2:8时,S值0.069略高于0.044,Emax值3.33L/mol也稍高于2.40L/mol.当B/D达到3:7时,S值和Emax值得到最大极值0.083和4.64L/mol,稍高于4:6时获得的0.079和2.85L/mol.所有比例下最大S值和Emax值都是在正庚醇为助表面活性剂时获得.比较4种比例的增溶值,S值先增加后降低的原因可能是:随着B/D的增加,在一定的范围内意味着能被增溶进入柴油中的生物油的量增多,但单位生物油对应的柴油量却在减少,因此单位体积柴油增溶的生物油量超过一定的临界值后,在B/D为4:6时会趋于稳定或略微降低.而由于表面活性剂的量固定不变,生物油增溶量随着B/D比例先增大后降低,故单位摩尔表面活性剂增溶的生物油量也随着B/D比例先增大后降低,即Emax值先增大后在B/D为4:6时又趋于降低.因此,B/D为3:7时S值和Emax值最大,此时的比例定义为最佳B/D比例. 2.2.2 醇种类的影响 由图2可知,以5种正构醇为助表面活性剂时柴油微乳体系对生物油的增溶具有明显增高.不加醇时,S值随B/D增大而逐渐增加,在4:6时达到最大0.035;加入醇后,体系的S值先增大后降低,在3:7时达到最大0.083.其原因可能是:醇作为助表面活性剂,在油水界面上与表面活性剂构成了混合膜或者吸附在油水界面上,进一步降低了界面张力,扩大了界面层面积,使界面膜更加柔韧,易于弯曲,促进微乳液的形成,从而改善了体系对生物油的增溶性能[31].
比较4种B/D比例,每种比例不同种类的醇S值变化的情况类似,当碳链长度达到正庚醇和正辛醇时,S值明显大于另外3种醇.当助剂醇为正丁醇、正戊醇和正己醇时,增溶效果不明显,部分S值甚至低于不添加醇的情况.从图2可以看出,当C/R为2.0,助剂醇为正庚醇时所构建的微乳体系的S值和其他醇相比最大.这很可能跟助剂醇的结构有关.微乳液结构的稳定性很大程度上取决于表面活性剂和助表面活性剂碳链长度的对称性[32],RL结构中一般包含两个长度相同的 C8脂肪酸链, 因此,相对于正庚醇来说,正辛醇结构与RL会更加匹配对称,但因正辛醇的亲油性较强,与表面活性剂对称结合之后将较多的溶解于油相中,从而使分配到界面上的表面活性剂数量减少,导致形成胶束的数量减少,所以正辛醇体系的S值反而比正庚醇小.另外,对于脂肪醇,随醇的碳链长度增加,疏水性也会逐渐增强,由于RL具有亲水性的结构,所以它与越疏水的助剂醇混合后更容易降低界面张力,从而微乳液结构更稳定[19].因此,正庚醇较比正丁醇、正戊醇、正己醇,增溶性能S值最大.其中,正丁醇不理想的增溶效果很可能跟其高亲水性相关[32].
2.2.3 C/R比例的影响 由图2可知,随着醇用量的增加,5种醇所构建柴油微乳体系对生物油增溶的S和Emax值都是先增加到达一个极值后又缓慢减少.每个B/D比例的Emax都对应正庚醇作为助剂醇时获得.当B/D为3:7,助剂醇为正庚醇时,随着C/R的增大,S和Emax值都先逐渐增加到C/R为2.0时达到最大,分别为0.083(V/V)和4.64(L/mol),然后在C/R为3.0时,又逐渐趋于下降.其原因可能是:RL属于阴离子表面活性剂,在形成胶束时,亲水基之间存在静电斥力,相互之间不易靠近并缔合成胶束,加入醇后,由于醇分子较小的结构容易插入表面活性剂分子间,使亲水基之间的距离增大,静电斥力变小,表面活性剂的疏水链和醇的碳氢链可最紧密靠拢,当C/R比例越大时,这种紧密结合的机会就更多,从而使得CMC降低,胶束更容易生成,有利于生物油的增溶.当界面上醇达到饱和,过量的醇远远多于表明活性剂时,它们会隔开表面活性剂分子,使得表面活性剂分子不易相互靠近缔合形成胶束,反而使CMC升高,不利于生物油的增溶[33],所以S值和Emax值在C/R为2.0时增大到最大后又逐渐趋于下降,此时的比例定义为最佳C/R比例.
2.3 RL浓度对生物油增溶性能的影响
表面活性剂在柴油微乳液增溶生物油的过程中起着至关重要的作用,当其浓度超过CMC时会形成逆胶束,促进微乳液的形成,从而增溶生物油.以RB为探针采用荧光法测得柴油中RL的CMC约为4g/L,研究以大于CMC为准,固定C/R为2.0和B/D为3:7,选择9种RL在柴油中不同的浓度(5,7.5,10,12.5,15,17.5,20,22.5,25g/L)进行测量(图3).随着RL用量的增加,S值随着浓度增大持续增高,而E值却随着浓度的增大持续降低.

图3 RL浓度对生物油增溶性能的影响Fig.3 Effect of RL concentration on the bio-oil solubilization capacity
柴油微乳液增溶生物油的增溶机制基于相似相溶的原则,极性分子更易溶于极性溶剂,而非极性分子更易溶于非极性溶剂,因此,生物油的非极性成分易溶于非极性的柴油中,而极性成分易溶于微乳液的极性核中[34].生物油是一种非常复杂的混合物,主要成分有酮、酯、酚、醇、醛和有机酸等,研究假设生物油按成分的不同分别增溶进入微乳液逆胶束体系的不同位置.微乳液通常被看作是一种“被溶胀的胶束溶液”或“胶束乳液”,单位微乳粒子则被看作是一个胶束,分为球形胶束和反向胶束[35-37].在反胶束中,表面活性剂的非极性基团尾部指向非极性的有机溶剂,而极性基团头部则排列在内形成一个纳米极性核(polar core),构成了一种透明的、热力学稳定的W/O体系.此极性核具有溶解极性物质的能力,极性核溶解水后,形成了“水池”(water pool)[35].以RL为表面活性剂构建的柴油微乳W/O体系,将生物油增溶进入了油相或者逆胶束体系的“水池”.被增溶物在胶束中的增溶位置很大程度跟其化学结构相关,生物油被增溶进入柴油微乳体系的位置根据分析主要包括4种形式[38](图4):水和乙酸等极性物质被增溶进入胶束内部(图4a);长链脂肪酸和醇类、酯类、酰胺等弱极性物质被增溶于胶束的栅栏层中,它们的极性基团插入胶束的内部,非极性基团则伸出胶束与表面活性剂分子的疏水基团相间地分布在胶束的表面(图4b);被疏水链卷曲包裹,使其缠绕束缚于链上(图4c);吸附于胶束表面(图4d).

图4 被增溶物在胶束中的增溶位置Fig.4 Location for the solubilization of additives in micelles
由于RL的羧酸盐基团带负电,在形成胶束时,亲水基之间存在静电斥力,所以RL构建的柴油微乳液体系属于阴离子表面活性剂体系,而这种头部带电的阴离子体系使被增溶物更易进入胶束内部或栅栏层中[39](图4a和4b),因此随着RL浓度的增加,形成的胶束也会增多,所以被增溶的生物油量越来越多,即S值越来越大.但是单位摩尔表面活性剂增溶的生物油量会越来越少,所以E值会逐渐降低.综合考虑S值和E值,实验选取15g/L为RL的最佳浓度.
2.4 体系的性质分析
以RL为表面活性剂,正庚醇为助表面活性剂,固定RL浓度为15g/L,B/D为3:7,C/R为2.0构建柴油微乳体系增溶生物油.根据实验,待样品分层固定后,下层很可能是未增溶进入柴油的生物油大颗粒分子,而上层柴油过量区则形成了一个W/O微乳系统(WII)[40-41].通过自然静置和离心法测试,实验所得的微乳液样品均无分层或浑浊现象出现,证明微乳液性能稳定.选取生物油/柴油微乳液、生物油、0#柴油3种样品作燃料特性分析比较.
2.4.1 元素分析 由表2可知,生物油/柴油微乳液的元素组成跟0#柴油的元素组成非常相似,但生物油的氧含量远高于0#柴油.对于热值,三者之中0#柴油最高,而生物油/柴油微乳液因增溶了生物油,其热值在36~37MJ/kg之间,稍低于0#柴油.

表2 生物油、0#柴油和生物油/柴油的元素成分和热值Table 2 Composition and energy content of bio-oil, diesel and bio-oil/diesel microemulsion
2.4.2 傅里叶红外光谱分析 对模拟生物油、0#柴油、容器中分层后上层样品(B上)和下层样品(B下)进行了傅里叶红外光谱分析,结果如图5所示.由图5可知,0#柴油和生物油的红外光谱吸收峰的分布情况存在很大的差异性,但0#柴油和生物油的所有吸收峰基本在B上样品的光谱图中都有出现,且B下样品和生物油的光谱图非常类似.
比较0#柴油和B上样品的光谱图,二者在频率为2950~2850cm-1(-CH2,-CH3)、1450cm-1(CH)、1380cm-1(C-H) 和 818~742cm-1(O-H)处均有很强的吸收峰.比较生物油和B上样品的光谱图,B上样品图谱比0#柴油多出的吸收峰在生物油图谱中都能找到,证明B上样品除了包含有柴油的成分,也增溶进入了生物油.在B上样品的光谱图中,频率为1730cm-1和 1600cm-1处的吸收峰代表 C=O 伸缩振动,证明样品内存在酮、醛、酯、酸等;在频率1500cm-1处吸收峰也较明显,此处对应C-H伸缩振动,代表烷烃含量较高;频率为1260~1030cm-1处的吸收峰代表C-O伸缩振动,证明B上样品中有脂肪酸或醇的存在;吸收峰在频率为943~742cm-1处也较明显,对应O-H伸缩振动,表明B上样品中存在酚类、酯类和芳香族化合物[42].从图5还可看出,B下样品的光谱图非常类似于生物油的光谱图,而且频率为3390cm-1(O-H)的吸收峰仅在它们光谱图中出现,在B上样品的光谱图中不明显.频率3390cm-1的吸收峰对应O-H的伸缩振动,是由水或醇类物质引起的,由此可以推断生物油中的大部分水可能未被增溶入B上样品的微乳液.另外,在B下样品的光谱图中同样可以看到频率为2950~2850cm-1(-CH)特征吸收峰,说明实验过程中也存在少量柴油组分溶入下层生物油的现象.根据上述分析结果可以推断:生物油中大部分的酮、酯、酚、醇、醛和有机酸都被增溶进入了柴油,故依靠柴油微乳液增溶生物油的技术具有一定的可行性.

图5 不同油产品的傅里叶红外光谱Fig.5 FTIR spectra for different oil products
2.4.3 燃料特性分析 对所构建的生物油/柴油微乳体系与普通0#柴油、生物油做比较,结果如表3所示.由表3可知,生物油/柴油微乳液的密度比0#柴油略大,很可能是因为增溶了生物油的缘故(生物油1.089g/cm3).生物油/柴油微乳液的运动黏度比0#柴油和生物油都大,很可能是受RL和正庚醇的影响,但仍在GB252-2011[43]规定的3.0~8.0mm2/s(20℃)范围之内.生物油/柴油微乳液的浊点和倾点分别为-2℃和-25℃,跟0#柴油的-5℃和-21℃相差不大.生物油/柴油微乳液含水率远低于生物油,其结果与傅里叶红外光谱分析一致,证明生物油中的大部分的水未被增溶入微乳液.生物油/柴油微乳液的pH值低于0#柴油,但略高于生物油.生物油/柴油微乳液的铜片腐蚀度为1a,跟柴油同属于轻度腐蚀.由于实验所配样品除了柴油含有微量硫,其他样品均不含硫,但生物油/柴油微乳液因为增溶了生物油,硫含量相较于柴油略微降低.生物油原油pH值一般为2~4,总酸含量通常在7%~30%[44],而实验室配制生物油pH值为2.20,主要由于其中乙酸含量就为14%,故生物油的酸值可高达131.70mgKOH/100mL,其跟腐蚀性测量结果相吻合,而由于生物油酸值过高,导致生物油/柴油微乳液的酸值也高达77.00mgKOH/100mL,尚达不到GB252-2011[43]中关于柴油酸值指标的规定(<7mgKOH/100mL).
2.4.4 热稳定性分析 热重数据可以用来分析燃油产品的热力学性质和能量转换的动力学性质.运用阿伦尼乌斯模型来分析处理热重数据已被得到广泛应用[45],参照模型公式:

式中:x表示重量损失分数;A和R是阿伦尼乌斯公式中的参数,A为指前因子(也称阿伦尼乌斯常数),min-1;R为摩尔气体常数,J/mol.K; T为热力学温度,K; Ea为表观活化能,kJ/mol; B表示升温速率,K/min.从公式可以看出ln[-ln(1-x)]和1/T成直线线性关系,斜率为-Ea/R,从热重分析曲线中计算出ln[-ln(1-x)]和1/T的值,然后作图可得到表观活化能Ea.
Ea反应物质有效碰撞的能量,从图6可以看出生物油的Ea为17.97kJ/mol,明显低于柴油的53.57kJ/mol,而生物油/柴油微乳液的Ea为44.77kJ/mol,低于柴油,说明生物油的增溶对柴油热稳定有影响,但是影响不是特别明显.
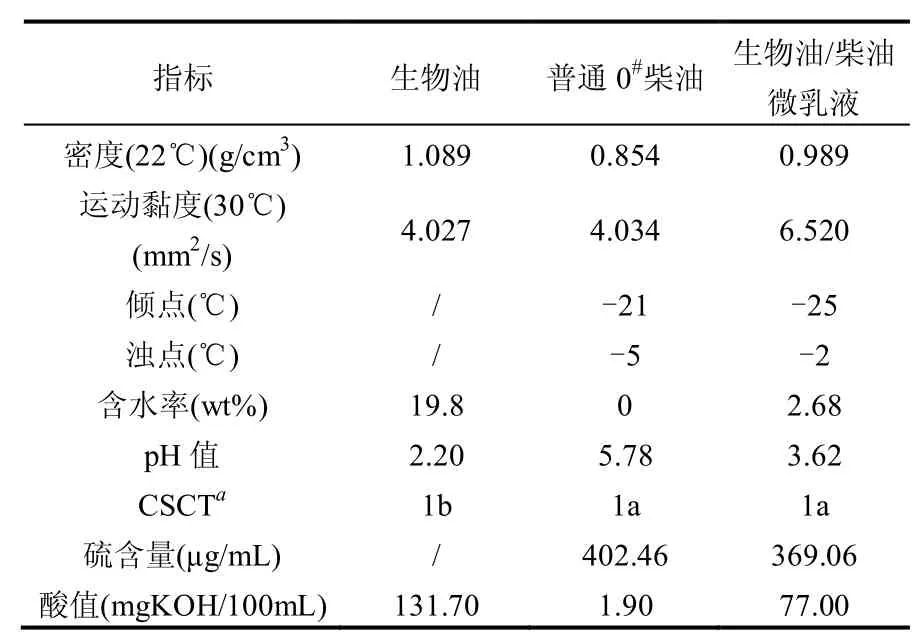
表3 生物油/柴油微乳液、生物油和0#柴油的性能Table 3 Properties of the bio-oil, diesel and bio-oil/diesel microemulsion

图6 不同油产品的积分Fig.6 Integral plot for different oil products
3 结论
3.1 根据相似相溶的增溶原理和胶束理论,使用RL作为生物表面活性剂构建柴油微乳体系来增溶模拟生物油,不同条件下构建的微乳体系对生物油的增溶性能有影响.考虑微乳体系的增溶性能,生物油/柴油体积比B/D为3:7时,增溶效果最好,比例过高或过低增溶效果都不是很理想.
3.2 助表面活性剂的加入可以使微乳体系的增溶量增大,且加入量过高或过低都会降低增溶量.相比其他4种醇,采用正庚醇作为助表面活性剂,与RL质量比C/R为2.0时,生物油的增溶量最大.
3.3 RL浓度对微乳体系增溶性能也有影响,随RL用量增加,S值增大,E值减小,综合考虑两项指标,RL浓度选择15g/L最为合适.
3.4 所构建的生物油/柴油微乳体系跟0#柴油相比,部分指标仅有微小差别,但由于生物油中酸含量过高,仍存在类似酸值等不符合标准的指标.
[1]Demirbas A. Progress and recent trends in biofuels [J]. Progress in Energy and Combustion Science, 2007,33:1-18.
[2]Zhang L, Xu C, Champagne P. Overview of recent advances in thermo-chemical conversion of biomass [J]. Energy Conversion and Management, 2010,51:969-982.
[3]Al-Sabawi M, Chen J. Hydroprocessing of biomass-derived oils and their blends with petroleum feedstocks: a review [J]. Energy and Fuels, 2012,26:5373-5399.
[4]Zhang Q, Chang J, Wang T J, et al. Review of biomass pyrolysis oil properties and upgrading research [J]. Energy Conversion and Management, 2007,48:87-92.
[5]Isahak W N R W, Hisham M W M, Yarmo M A,et al. A review on bio-oil production from biomass by using pyrolysis method [J]. Renewable and Sustainable Energy Reviews, 2012,16:5910-5923.
[6]Lu Q, Li W, Zhu X. Overview of fuel properties of biomass fast pyrolysis oils [J]. Energy Conversion and Management, 2009,50:1376-1383.
[7]Chiaramonti D, Bonini M, Fratini E, et al. Development of emulsions from biomass pyrolysis liquid and diesel and their use in engines-Part 1:emulsion production [J]. Biomass Bioenergy,2003,25:85-99.
[8]Ikura M, Stanciulescu M, Hogan E. Emulsification of pyrolysis derived bio-oil in diesel fuel [J]. Biomass Bioenergy, 2003,24:221-232.
[9]Ikura M, Mirmiran S, Stanciulescu M, et al. Pyrolysis liquidin-diesel oil microemulsions [J]. U. S. Patent, 1998,5,820,640.
[10]Xu Y F, Wang Q J, Hu X G, et al. Characterization of the lubricity of bio-oil/diesel fuel blends by high frequency reciprocating test rig [J]. Energy, 2010,35:283-28.
[11]Jiang X X, Ellis N. Upgrading bio-oil through emulsification with biodiesel: mixture production [J]. Energy Fuels, 2009,24:1358-1364.
[12]Jiang X X, Ellis N. Upgrading bio-oil through emulsification with biodiesel: thermal stability [J]. Energy Fuels, 2010,24:2699-2706.
[13]He R H, Ye X P, Harte F, et al. Effects of high-pressure homogenization on physico chemical properties and storage stability of switchgrass bio-oil [J]. Fuel Processing Technology,2009,90:415-421.
[14]Balcan M, Mihăilescu F C, Anghel D F, et al. Microemulsion systems containing diesel and colza oil as alternative fuels: Phase studies, interfacial tension and solubilization [J]. Fuel, 2014,117:251-258.
[15]崔 英,龚华碧,胡才仲,等.柴油微乳液的制备及性能研究 [J].应用化工, 2010,39(3):393-396.
[16]彭 馨,袁兴中,黄华军,等.漆酶的逆胶束萃取条件优化的研究[J]. 中国环境科学, 2013,33(5):904-909.
[17]李建彤,韩萍芳,吕效平.乳化柴油研究及其应用进展 [J]. 化工进展, 2004,23(4):364-369.
[18]Mulligan C N. Environmental applications for biosurfactants [J]. Environmental Pollution, 2005,133:183-198.
[19]Nguyen T L, Edelen A, Neighbors B, et al. Biocompatible lecithin-based microemulsions with rhamnolipid and sophorolipid biosurfactants: formulation and potential applications [J]. Journal of Colloid and Interface Science, 2010,348:498-504.
[20]Fisk C A, Morgan T, Ji Y, et al. Bio-oil upgrading over platinum catalysts using in situ generated hydrogen [J]. Applied Cataysis A:General, 2009,358:150-156.
[21]Tripathi M M, Hassan El B M, Yueh F Y, et al. Study of the effect of ultraviolet exposure on bio-oil by laser-induced fluorescence[J]. Energy Fuels, 2010,24:6187-6192.
[22]ASTM D 240-2009 用弹式量热计测定液烃燃料燃烧热的试验方法 [S].
[23]GB/T3535-2006 石油产品倾点测定法 [S].
[24]GB/T6986-2014 石油产品浊点测定法 [S].
[25]ASTM D 130-2004 用铜条试验检测石油产品对铜腐蚀性的标准试验方法 [S].
[26]GB/T265-1988 石油产品运动粘度测定法和动力粘度计算法[S].
[27]GB/T1884-2000 原油和液体石油产品密度实验室测定法(密度计法) [S].
[28]GB/T380-1977 石油产品硫含量测定法(燃灯法) [S].
[29]Thangamanit S, Shreve G S. Effect of anionic biosurfactant on hexadecane partitioning in multiphase [J]. Environ Sci Technol,1994,28(12):1993-2000.
[30]崔凯龙,袁兴中,曾光明,等.生物表面活性剂用于逆胶束体系的构建及微水相条件优化 [J]. 中国环境科学, 2011,31(9):1444-1450.
[31]Mitra R K, Paul B K, Moulik S P. Phase behavior, interfacial composition and thermodynamic properties of mixed surfactant(CTAB and Brij-58) derived w/o microemulsions with 1-butanol and 1-pentanol as cosurfactants and n-heptane and n-decane as oils [J]. Journal of Colloid Interface Science, 2006,300:755-764.
[32]Paul S, Panda A K. Physico-chemical studies on microemulsion:effect of cosurfactant chain length on the phase behavior, formation dynamics, structural parameters and viscosity of water/(polysorbate-20+ n-alkanol)/n-heptane water-in-oil microemulsion [J]. J Surfact Deterg, 2011,14:473-486.
[33]Do L D, Singh V, Chen L, et al. Algae, canola, or palm oils—diesel microemulsion fuels phase behaviors, viscosity, and combustion properties [J]. International Journal of Green Energy,2011,8:748-767.
[34]Nguyen T, Do L, Sabatini D A. Biodiesel production via peanut oil extraction using diesel-based reverse-micellar microemulsions [J]. Fuel, 2010,89:2285-2291.
[35]Emin S M, Denkova P S, Papazova K I, et al. Study of reverse micelles of di-isobutyl-phenoxy-ethoxy-ethyl- dimethyl-benzyl ammonium methacrylate in benzene by nuclear magnetic resonance spectroscopy [J]. Journal of Colloid Interface Science,2007,305:133-141.
[36]Kaur G, Chiappisi L, Prévost S, et al. Probing the microstructure of nonionic microemulsions with ethyl oleate by viscosity,ROESY, DLS, SANS, and cyclic voltammetry [J]. Langmuir,2012,28:10640-10652.
[37]Spernath A, Aserin A, Sintov A C, et al. Phosphatidylcholine embedded micellar systems: enhanced permeability through rat skin [J]. Journal of Colloid Interface Science, 2008,318:421-429.
[38]Wang X L, Yuan X Z, Huang H J, et al. Study on the solubilization capacity of bio-oil in diesel by microemulsion technology with Span80as surfactant [J]. Fuel Processing Technology, 2014,118:141-147.
[39]Myers D. Surfactant science and technology [M]. Thirded., John Wiley and Sons, Inc., Hoboken, NJ, 2006.
[40]Khomane R B, Manna A, Mandale A B, et al. Synthesis and characterization of dodecanethiol-capped cadmium sulfide nanoparticles in a winsor II microemulsion of diethyl ether/AOT/water [J]. Langmuir, 2002,18:8237-8240.
[41]Pan T, Wang Z L, Xu J H, et al. Stripping of nonionic surfactants from the coacervate phase of cloud point system for lipase separation by Winsor II microemulsion extraction with the direct addition of alcohols [J]. Process Biochem, 2010,45:771-776.
[42]孙青亮,吴昌永,胡 翔,等.石化污水厂二级出水溶解性有机物分级解析研究 [J]. 中国环境科学, 2012,32(11):2017-2022.
[43]GB252-2011 普通柴油 [S].
[44]崔洪友,王景华,魏书芹,等.酸碱电位滴定法测定生物油中总酸含量 [J]. 可再生能源, 2010,28(6):36-39.
[45]Wan Nik W B, Ani F N, Masjuki H H. Thermal stability evaluation of palm oil as energy transport media [J]. Energy Conversion and Management, 2005,46:2198-2215.
Study on the solubilization capacity of bio-oil in diesel by microemulsion technology.
LI Shan-xing1,2, YUAN Xing-zhong1,2*, LENG Li-jian1,2, WANG Xue-li1,2, ZHU Ren1,2, FU Li-huan1,2, LI Hui1,2, ZENG Guang-ming1,2(1.College of Environmental Science and Engineering, Changsha 410082, China;2.Key Laboratory of Environmental Biology and Pollution Control, Hunan University, Changsha 410082, China). China Environmental Science, 2015,35(3):783~791
Synthetic bio-oil was upgraded by solubilizing bio-oil in diesel by microemulsion technology. Diesel microemulsions were formed with rhamnolipid (RL) as surfactant and different kinds of normal alcohols with varying carbon chain length as cosurfactants. The effects of different microemulsion parameters on the solubilization capacity of bio-oil in diesel were investigated, which include initial bio-oil/diesel volume ratio (B/D ratio), surfactant concentration,cosurfactant type, and the mass ratio of cosurfactant/surfactant (C/R ratio). Meanwhile, fuel properties of bio-oil/diesel microemulsion were examined, which include elemental analysis, FT-IR analysis, thermogravimetric analysis, and other common fuel properties. Experimental results indicated that the proper bio-oil/diesel volume ratio was 3:7, the optimal concentration of RL was 15g/L, and the ideal cosurfactant was heptanol with C/R ratio of 2.0. Bio-oil/diesel microemulsion formed under the optimal solubilization conditions was proven to have fuel properties comparable to diesel.
rhamnolipid;synthetic bio-oil;diesel microemulsion;n-alcohol
X382
A
1000-6923(2015)03-0783-09
李闪星(1989-),女,湖南娄底人,硕士研究生,主要从事表面活性剂应用的研究.
2014-07-15
国家自然科学基金资助项目(21276069)
* 责任作者, 教授, yxz@hnu.edu.cn
