Cu2O/Ag复合催化剂的合成及红外光激发下的光催化性能研究
2015-11-02铁绍龙
简 蓝, 万 霞, 铁绍龙
(华南师范大学化学与环境学院,广州 510006)
Cu2O/Ag复合催化剂的合成及红外光激发下的光催化性能研究
简蓝, 万霞*, 铁绍龙
(华南师范大学化学与环境学院,广州 510006)
采用液相还原法合成不同摩尔比的Cu2O/Ag(x)复合型催化剂,应用X-射线粉末衍射(XRD)、扫描电子显微镜(SEM)、紫外可见漫反射(DRS)等分析手段对样品进行表征.结果显示,纳米金属Ag的存在使得Cu2O/Ag(x)样品对光的吸收扩展到了整个可见和近红外区,且随样品中Ag含量的增加,该区域的吸收逐渐增强,证明Cu2O/Ag(x)复合催化剂对太阳光具有高的吸收能力.以甲基橙(MO)为目标降解物,研究催化剂在黑暗条件下的降解性能,结果表明Cu2O/Ag(0.05)催化剂具有最高的降解能力,在120 min内黑暗条件下MO(30 mg/L) 降解率达到89.2%.另外对Cu2O/Ag(x)复合催化剂的降解机理进行了探讨.
Cu2O/Ag(x)复合催化剂; 光吸收; 光催化; 降解甲基橙
光催化技术近年来越来越受到关注,开发利用新型、无毒、可重复使用、能高效吸收太阳光的光催化剂成为环境污染控制和可持续发展的重要课题[1-3].自1998年,Ikeda等[4]在太阳光照射下以氧化亚铜(Cu2O)为光催化剂将水分解成氢气和氧气以来,对其光催化性能的研究成为热点.Cu2O是一种p型半导体材料,具有窄的禁带宽度(Eg=2.0~2.2 eV),能够被可见光诱导激活,具有很好的应用前景.但氧化亚铜带隙窄,导致光生电子和空穴的复合率高,而且活性粒子在其内部的迁移率较低,这些因素导致其光催化效率偏低.为了提高光催化性能,将Cu2O与其他催化剂复合组成新的催化剂是一种有效的方法. Wang等[5]采用还原氧化石墨烯(rGO)吸附醋酸铜为前驱体,在乙二醇存在下还原得到Cu2O/rGO催化剂,光催化降解罗丹明B,降解率提高了53%. Chen等[6]通过电化学沉积法获得了具有不规则形貌的Cu2O/CS(壳聚糖)催化剂,发现其在可见光照射下降解活性艳红X-3B有更强的催化能力.Hu等[7]通过浸渍还原法合成了异质结催化剂Cu2O/CeO2,在可见光照射下降解酸性橙7,发现复合后光催化效率提升了20%.另外,Gao等[8]发现在Cu2O微晶表面沉积银,可以增强拉曼散射.对于氧化亚铜复合银的研究,Lin等[9]通过一步合成法获得了Ag/Cu2O纳米粒子,研究了它在可见光照射下降解甲基橙的行为,其降解性能优于单一催化剂.
虽然报道的这些催化剂均能有效地降解污染物,但都需要在额外光源(可发射紫外光或可见光)照射下才能持续、有效地进行降解[10-12].因为Ag与Cu2O晶体均属立方晶系,通过液相还原-沉淀法,使用葡萄糖做还原剂,一步即可获得Cu2O/Ag(x)复合催化剂.该催化剂能够高效地吸收紫外、可见和近红外波长范围的光,由此可实现在黑暗条件下有效降解有机污染物,例如甲基橙(MO).迄今为止,不通过额外光源有效进行光催化降解的研究鲜有报道,因此研究Cu2O/Ag(x)复合催化剂在黑暗下降解甲基橙具有重要研究价值.因为该复合型催化剂能高效地吸收太阳光,可在无需架设光源的条件下实现24 h不间断地催化降解,具有非常好的应用前景.
1 实验部分
1.1Cu2O/Ag(x)催化剂的合成
采用常压液相还原法合成复合Cu2O/Ag(x)样品.称取0.024(1-x) mol CuSO4·5H2O和0.014 mol葡萄糖溶于1 500 mL去离子水中,溶液转入2 L三颈烧瓶,进行水浴加热.待溶液温度达到75 ℃时,同时滴加200 mL 0.4 mol/L的NaOH溶液和含AgNO3为0.024xmol (x=0、0.01、0.03、0.05、0.07、0.10)的硝酸银溶液100 mL,待反应液的pH达到11时停止加碱,继续保温1 h.沉淀减压过滤,用去离子水洗涤多次,在烘箱中60 ℃干燥24 h,即获得系列不同Ag含量的Cu2O/Ag(x)复合催化剂.用符号Cu2O表示无Ag样品,Cu2O/Ag(x)表示催化剂中Ag含量分别为0.01、0.03、0.05、0.07、0.10的样品.
1.2降解甲基橙实验
向50 mL 30 mg/L的甲基橙溶液中加入0.05 g催化剂样品,在黑暗下超声分散10 min后置于恒温水浴(30±0.2 ℃)中,在磁力搅拌下于黑暗 (避光黑箱内)中进行催化降解反应.每隔一定时间取样1次,用直径为0.45 μm的过滤膜分离除去样品,滤液按一定比例稀释后在紫外可见分光光度仪(UV-1700, 日本岛津公司)上测定滤液在max=464 nm处(MO最大吸收波长)的吸光度值At.MO的降解率计算公式如下:
式中,C0和Ct分别表示MO在初始和反应时间t时的浓度,A0和At分别表示初始和反应时间t时MO在=464 nm处的吸光度值.
1.3样品分析与测试
通过德国Carl Zeiss NTS GmbH 公司的Zeiss Ultra 55 型热场发射扫描电子显微镜观察样品的形貌和大小;采用丹东通达公司的TD-3000型X射线粉末衍射仪对样品的物相和晶体结构进行表征;样品的漫反射光谱通过澳大利亚Varian Inc.公司的Cary 5000型UV-Vis-NIR光谱仪获得;采用日本岛津公司的UV-1700型紫外-可见分光光度计测定甲基橙溶液的吸收光谱.
2 结果与讨论
2.1Cu2O/Ag(x)样品的物相特性
2θ分别位于36.5°(110)、42.4°(111)、61.5°(200)和73.6°(311)的衍射峰与JCPDS卡中78-2076号的标准Cu2O完全相同(图1),表明合成的所有样品中含有Cu2O晶体,属立方晶系,简单立方晶格,Pn3m[224]点群, 晶胞参数a=4.267.
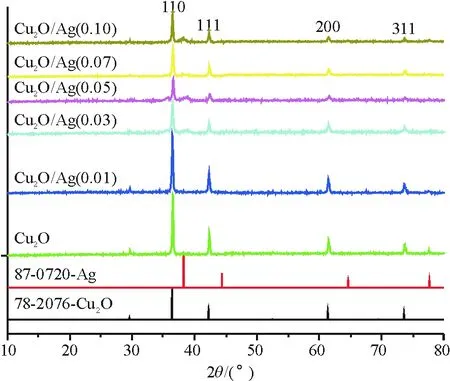
图1 Cu2O/Ag(x)样品的X-射线粉末衍射谱
当有Ag存在时,样品在2θ分别为38.25°(111)和44.4°(200)处出现了与JCPDS卡中87-0720号金属单质Ag完全相同的衍射峰,也属立方晶系,面心立方晶格,Pm3m[225],晶胞参数a=4.077,证明在Cu2O/Ag样品中Ag以金属单质形式存在.由于Cu2O晶体与单质Ag均属立方晶系,晶胞参数也接近,所以容易形成共生晶体.合成时,Cu2+和Ag+同时存在于溶液中,均具有氧化性,与还原剂葡萄糖发生氧化还原反应,最终转化为Cu2O和Ag,因此本文合成的Cu2O/Ag复合型催化剂是由均属立方晶系的Cu2O和单质Ag复合而成.由图1看出,随着金属Ag含量的增加,Cu2O/Ag(x)样品的晶化度逐渐减弱,因为有序性在逐渐减弱.
2.2Cu2O/Ag(x)样品的形貌和大小
图2A表明,纯Cu2O样品为切角立方体构型(插图a),均匀性与分散性好.Cu2O样品粒径主要分布在0.9~1.1 μm之间(插图b).复合Ag的Cu2O/Ag(x)样品为立方体,其粒径大幅减小至200 nm,且表面有无数小晶粒附着(图2C内嵌图),样品表面粗糙度大幅增加,比表面积明显增大,有利于样品更好地吸收辐射光和吸附污染物,提高样品光催化降解污染物的能力.另外,由图3中Cu2O/Ag(0.03)样品的透射电镜图表明,金属Ag与Cu2O共生在一起(图3A椭圆框所示),也有部分附着在由Cu2O和Ag共同形成的立方体表面(图3A中矩形框所示).图3B进一步证明Ag的存在.由于Cu2O和Ag的共生,虽然均属立方晶体,但复合晶体的晶化度和紧实度均下降,该结论也被图1的XRD数据证实.随着Ag含量的增加,样品的晶化度减小.而催化剂晶化度的减弱有利于活性的电子或空穴迁移速率的提高,进而提高催化剂的催化活性.
2.3样品的紫外-可见-近红外漫反射光谱
Cu2O的带边吸收波长为627 nm(图4),由公式求算出Eg=1 239.8/=1 239.8/627=1.98(eV),即Cu2O样品只能吸收波长低于630 nm的可见和紫外光.而复合了金属Ag的Cu2O/Ag(x)样品不仅其吸收扩展到了全部可见区,并延伸到了近红外区,并且在紫外区的吸收也明显强于纯Cu2O.随着金属银含量的增加,样品在可见和近红外区的吸收也增加.这是由样品表面的Ag纳米粒子表面等离子体共振吸收所引起[13-14].表明Cu2O/Ag(x)样品能实现紫外、可见和近红外全光谱吸收.

图2 Cu2O和Cu2O/Ag(x)样品的SEM
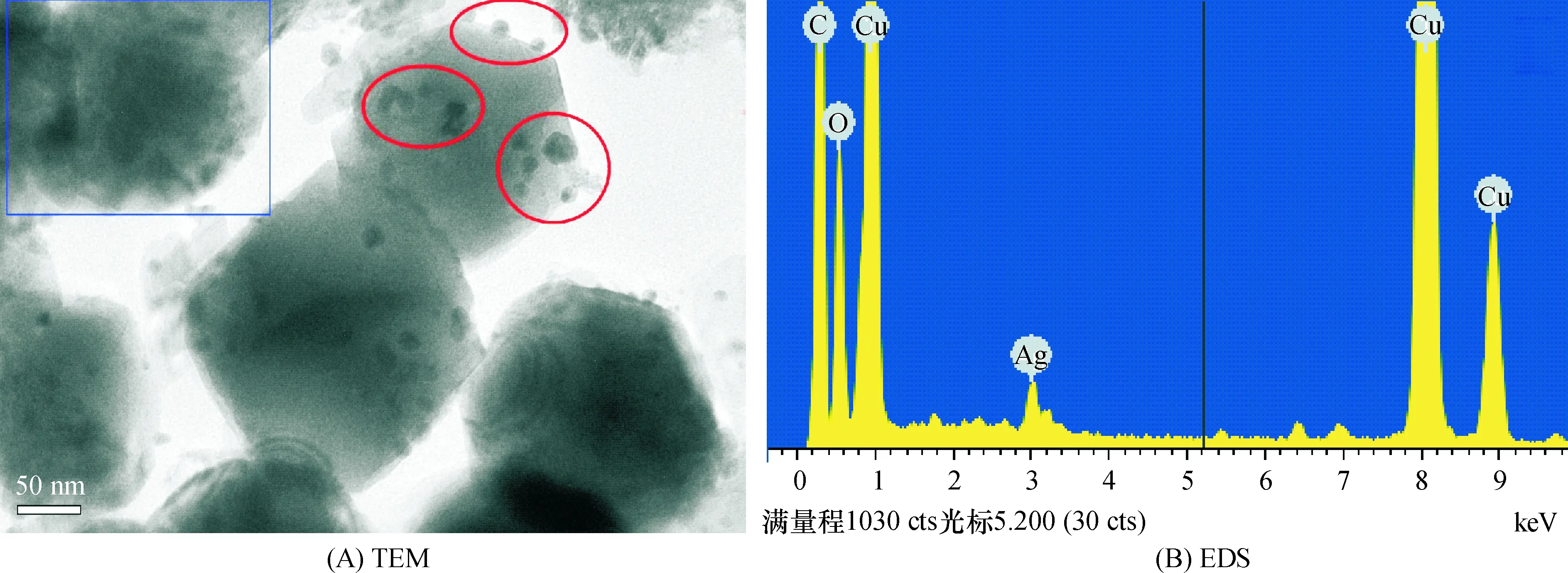
图3 Cu2O/Ag(0.03)样品的TEM及其EDS能谱
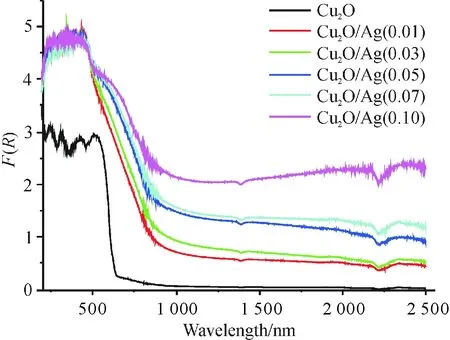
图4 Cu2O和Cu2O/Ag(x)样品的UV-Vis-NIR漫反射光谱
Figure 4Diffuse reflection spectra of Cu2O and Cu2O/Ag(x) samples in UV-Vis-NIR wavelength region
2.4Cu2O/Ag(x)复合催化剂在黑暗条件下降解甲基橙的性质
在黑暗条件下Cu2O降解MO很弱(图5曲线1),因为Cu2O不能有效地吸收近红外光.随着催化剂中复合Ag含量的增加,对MO的降解逐渐增大,在Ag含量为0.05 mol时,复合催化剂的降解效率最高,反应2 h后,MO的降解率达到约89.2%(图5曲线4).继续增加Ag的含量,催化剂的降解效率减弱.这是因为随着Ag的增加,催化剂在近红外区域的吸收逐渐增强,即光子的吸收效率得到显著提高,被激活的光生电子或空穴数量增加.Ag与Cu2O之间形成的肖特基势[15]可使Ag晶体中被低能量光子(近红外光)激活的电子转移到Cu2O的表面,同时进行降解反应而被不断消耗,导致Cu2O内部的电子不断迁移到表面进行补充,因此有效抑制了电子-空穴对的复合,提高了样品的催化活性,因此Cu2O/Ag(x)催化剂在黑暗条件下也能有效地降解MO.当Ag添加量超过0.05 mol后,虽然样品吸收近红外光的能力不断增强,但Ag含量的进一步增大导致Ag原子之间的距离缩短,电子容易形成无数小的闭合回路而被灭活,导致电子从内部迁移到样品表面以及电子在Ag与Cu2O之间的转移几率均减少,所以最终降解MO的能力反而减弱.
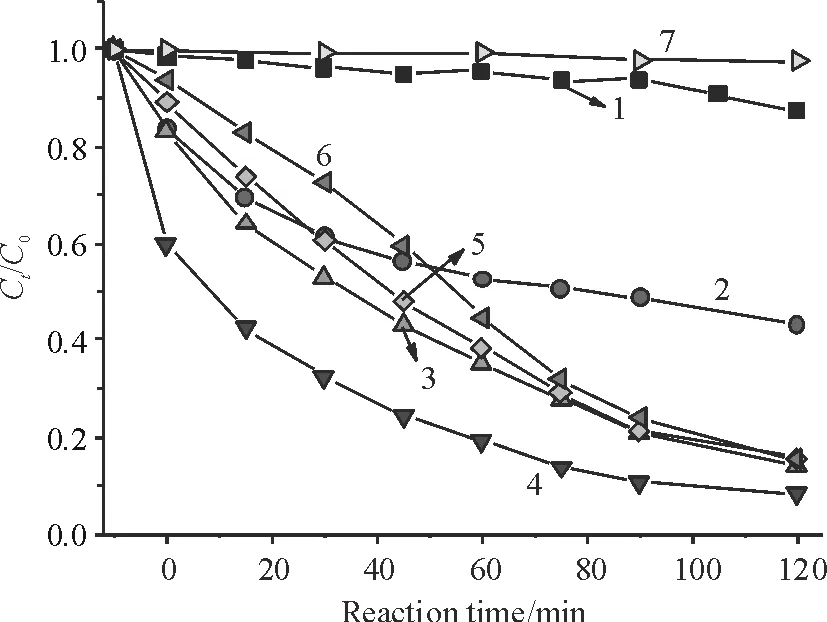
1:Cu2O; 2:Cu2O/Ag(0.01); 3:Cu2O/Ag(0.03); 4:Cu2O/Ag(0.05); 5:Cu2O/Ag(0.07); 6:Cu2O/Ag(0.10); 7:空白.
图5Cu2O/Ag(x)样品在黑暗下降解MO的Ct/C0-t曲线
Figure 5Ct/C0of MO as a function of time (t) in Cu2O/Ag(x) systems in the darkness

图7描述了Cu2O/Ag(0.05)催化剂在黑暗下循环使用4次的Ct/C0-t曲线,结果显示,催化剂的催化效率基本不变,说明该催化剂稳定性好,防中毒能力强,因此具有很好的应用前景.
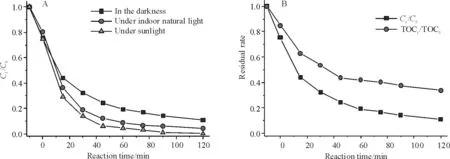
图6 Cu2O/Ag(0.05)在不同光源下降解MO的Ct/C0-t曲线(A)及在黑暗下MO降解的TOC曲线(B)
Figure 6Ct/C0of MO as a function of time in Cu2O/Ag(0.05) system under different light sources (A) and TOC of MO in the darkness (B)
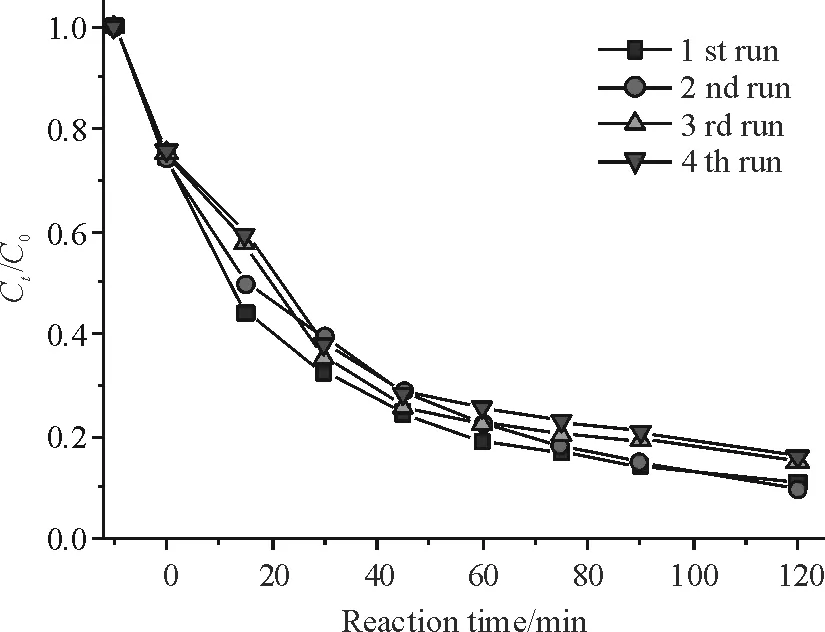
图7Cu2O/Ag(0.05)催化剂不同回收次数下的Ct/C0-t曲线(黑暗下)
Figure 7Comparison ofCt/C0of MO in cycling runs in Cu2O/Ag(0.05) system in the darkness
2.5Cu2O/Ag(x)复合催化剂在黑暗下降解甲基橙的机理
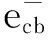
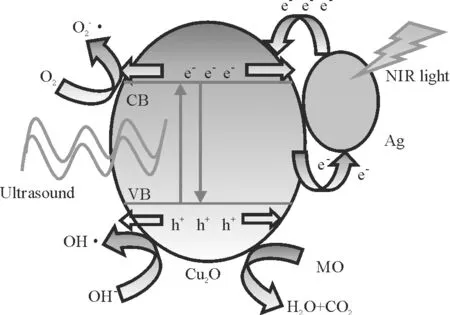
图8 Cu2O/Ag(x) 复合催化剂的光催化降解有机物的机理
Figure 8Mechanism for the degradation of organism in Cu2O/Ag(x) composite catalyst system
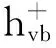
3 结论
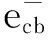
[1]孟楠, 张爱茜, 吴海锁. TiO2与Cu2O光催化降解对硝基苯酚比较研究[J] 环境化学, 2005, 24(6):659-661.
Meng L, Zhang A Q, Wu H S. Comparison study on photocatalytic degradation ofp-nitrophenol assisted by titanium dioxide and cuprousoxide[J]. Environmental Chemistry, 2005, 24(6): 659-661.
[2]Hara M, Kondo T, Komoda M, et al. Cu2O as a photocatalyst for overall water splitting under visible light radiation[J]. Chemical Communications, 1998, 29(3): 357-358.
[3]Ramirez-Ortiza T, Ogura J, Medina-Valtierra J, et al. A catalytic application of Cu2O and CuO films deposited over fiber glass[J]. Applied Surface Science, 2001, 174(3/4):177-184.
[4]Ikeda S, Takata T, Kondo T, et al. Meehano-catalytic over all water splitting[J]. Chemical Communications, 1998(20):2185-2186.
[5]Wang A L, Li X S, Zhao Y B. Preparation and characterizations of Cu2O/reduced graphene oxide nanocomposites with high photocatalytic performances[J]. Powder Technology, 2014, 261(7):42-48.
[6]Chen J Y, Zhou P J, Yang Z. Studies on the photocatalytic performance of cuprous oxide/chitosan nanocomposites activated by visible light[J]. Carbohydrate Polymers, 2008, 72(1):128-132.
[7]Hu S C, Zhou F, Wang L Z, et al. Preparation of Cu2O/CeO2heterojunction photocatalyst for the degradation of Acid Orange 7 under visible light irradiation[J]. Catalysis Communications, 2011, 12(9):794-797.
[8]Gao H, Zhang J Y, Li M,et al. Evaluating the electric property of different crystal faces and enhancing the Raman scattering of Cu2O microcrystal by depositing Ag on the surface[J]. Current Applied Physics, 2013, 13(5):935-939.
[9]Lin X F, Zhou R M, Zhang J Q, et al. A novel one-step electron beam irradiation method for synthesis of Ag/Cu2O nanocomposites[J]. Applied Surface Science, 2009, 256(3):889-893.
[10]Liang Z H, Zhu Y J. Synthesis of uniformly sized Cu2O crystals with star-like and flower-like morphologies[J]. Materials Letters, 2005, 59(19/20):2423-2425.
[11]Huang L, Peng F, Yu H, et al, Preparation of cuprous oxides with different sizes and their behaviors of adsorption, visible-light driven photocatalysis and photocorrosion[J]. Solid State Science, 2009, 11(1):129-138.
[12]袁梦,万霞,铁绍龙. 纳米NiO光催化剂性质对降解亚甲基蓝染料的影响[J]. 华南师范大学学报:自然科学版, 2013, 45(1):62-67.
Yuan M, Wan X, Tie S L. Effects of catalyst characters on the photocatalytic activities of NiO nanoparticles in the degradation of methylene blue[J]. Journal of South China Normal University: Natural Science Edition, 2013, 45(1): 62-67.
[13]Matsubara K, Tatsuma T. Morphological changes and multicolor photochromism of Ag nanoparticles deposited on single-crystalline TiO2surfaces[J]. Advanced Materials, 2007, 19(19):2802-2806.
[14]Xiang Q J, Yu J G, Cheng B, et al. Microwave-hydrothermal preparation and visible-light photoactivity of plasmonic photocatalyst Ag-TiO2nanocomposite hollow spheres[J]. Chemistry-An Asian Journal, 2010, 5(6):1466-1474.
[15]Wei S Q, Shi J, Ren H G, et al. Fabrication of Ag/Cu2O composite films with a facile method and their photocatalytic activity[J]. Journal of Molecular Catalysis A: Chemical, 2013, 378(11):109-114.
【中文责编:谭春林英文责编:李海航】
Synthesis of Cu2O/Ag Composite Catalysts and Their Photocatalytic Property under Infrared Light Irradiation
Jian Lan, Wan Xia*, Tie Shaolong
(School of Chemistry and Environment, South China Normal University, Guangzhou 510006, China)
A series of Cu2O/Ag(x) composite catalysts with different molar ratios were synthesized by a liquid phase reduction method. The properties of Cu2O/Ag(x) samples were characterized by SEM, XRD and DRS (UV-Vis-NIR) analyzing methods. The results indicated that in the presence of nanometre metallic Ag, the light absorption of Cu2O/Ag(x) sample was greatly extended to visible and near infrared wavelength regions. With increasing molar ratio of Ag, the absorption intensities of samples enhanced. This implies that Cu2O/Ag(x) composite catalysts exhibit strong absorption of sunlight. The photocatalytic performances of Cu2O/Ag(x) catalysts in the darkness were evaluated using methyl orange (MO) as a degradation target. The results showed that Cu2O/Ag(0.05) sample exhibited the highest photocatalytic activity, while the degradation rate of MO (30 mg/L) reached 89.2% in 120 min. Inaddition, the photocatalytic mechanism of the Cu2O/Ag(x) composite catalyst system was proposed.
Cu2O/Ag(x) composite catalysts; light absorption; photocatalysis; degradation of methyl orange
2014-11-10《华南师范大学学报(自然科学版)》网址:http://journal.scnu.edu.cn/n
国家自然科学基金项目(11374109)
万霞,副教授,Email: wanxia@scnu.edu.cn.
O611.6
A
1000-5463(2015)05-0044-06
