双环醇片防治抗癌药物所致肝损害临床研究
2015-10-24唐静
唐静
(四川省凉山彝族自治州第一人民医院,四川西昌615000)
双环醇片防治抗癌药物所致肝损害临床研究
唐静
(四川省凉山彝族自治州第一人民医院,四川西昌615000)
目的观察双环醇片防治抗癌药物所致肝损害的临床疗效。方法选取医院2013年6月至2014年6月收治的确诊恶性肿瘤拟行化学治疗(简称化疗)的患者120例,按照随机数字表法分为治疗组和对照组,各60例。两组患者均接受常规化疗,治疗组加服双环醇片25mg,3次/天,治疗3个周期。出现化疗药物性肝损害的患者暂停化疗,给予双环醇片25mg口服,3次/天,肝功能指标恢复正常后再按照原方案和剂量继续完成2个周期化疗,共5个周期。结果治疗3个周期内,治疗组药物性肝损害发生率为28.33%,明显低于对照组的66.67%(P<0.05);治疗组不良反应各分度发生率明显低于对照组(P<0.05);治疗3个周期后,对照组肝功能指标明显较治疗前升高(P<0.05),而治疗组较治疗前升高不明显(P>0.05),且升高程度明显低于对照组(P<0.05);肝功能损害患者接受双环醇片治疗后,各肝功能指标均较治疗前明显下降(P<0.05)。结论双环醇片预防性保肝治疗,可降低抗癌药物所致药物性肝损害的发生率,减轻肝功能损害程度,且对药物性肝损害有良好的治疗效果,值得临床推广。
双环醇;抗癌药物;化学治疗;药物性肝损害
全身化学治疗(简称化疗)是治疗恶性肿瘤的常用手段。药物性肝损害是指在药物治疗过程中,由于药物或其代谢产物引起的肝细胞毒性损害或肝脏对药物及代谢产物的变态反应所致疾病[1]。目前,临床使用的大多数化疗药物均在肝脏内进行代谢,化疗药物所致肝损害是常见的不良反应,若不及时给予保肝治疗,可能会导致肝损害进一步加重,影响抗癌疗效[2]。双环醇是新型保肝护肝药物,能通过清除自由基、保护肝细胞膜和线粒体,减少肝细胞核DNA损伤及细胞凋亡,使肝细胞核DNA免受损伤及减少细胞凋亡的发生,从而降低血清氨基酸转移酶、减轻肝组织的炎性反应坏死,防止肝纤维化,从而起到保肝护肝的作用[3],近年来在临床应用广泛。笔者观察了双环醇片对抗癌药物所致肝损害患者的治疗和预防作用,现报道如下。
1 资料与方法
1.1一般资料
选取医院2013年6月至2014年6月收治的确诊恶性肿瘤拟行化疗的患者120例,均经细胞学或组织学病理检查明确诊断,年龄0~40岁;男61例,女59例;肺癌39例,结肠癌31例,淋巴瘤8例,胃癌13例,直肠癌18例,乳腺癌9例,胰腺癌2例。排除标准:肿瘤肝脏转移;合并病毒性肝炎所致肝功能异常;肝功能失代偿;合并心、肝、肾等重要器官慢性基础疾病和造血功能障碍;过敏体质或对多种药物过敏。本研究经过我院伦理委员会批准,并征得患者及其家属知情同意。按随机数字表法将120例患者分为治疗组和对照组,各60例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。详见表1。
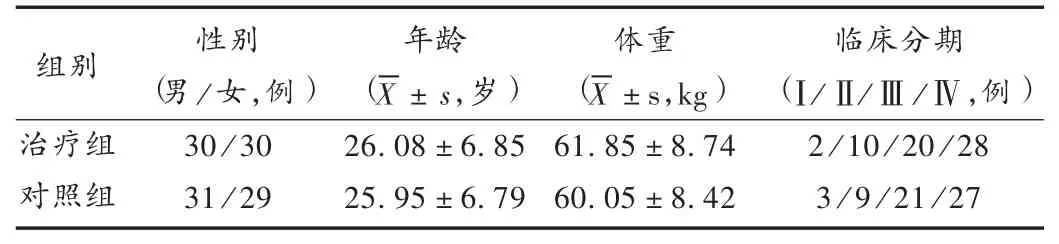
表1 两组患者一般资料比较(n=60)
1.2治疗方法
两组化疗用药剂量:顺铂75mg/m2,每3周1次或分为2~3次;卡铂按AUC=6 mg/(mL·min)给药,每3周1次;草酸铂130 mg/m2,每3周1次,或85 mg/m2,每2周1次;环磷酰胺750mg/m2,每3周1次;异环磷酰胺1300mg/m2,每3周连用3 d;盐酸伊立替康180mg/m2,每2周1次;卡培他滨每日2000mg/m2,每3周连用2周;紫杉醇135~175mg/m2,每3周1次;多西紫杉醇60mg/m2,每3周1次;足叶乙苷60mg/m2,连用5 d;长春新碱1.4mg/m2,每周1次,每3周连用2周;丝裂霉素6~8mg/m2,每3周1次;表阿霉素80mg/m2,每3周1次;吉西他滨1000mg/m2,每周1次,连用2周;长春瑞滨25mg/m2,每周1次,每3周连用2周;甲氨蝶呤40 mg/m2,每周1次,连用2周;5-氟尿嘧啶1 000mg/m2,连用2 d,每2周1次。化疗方案选用上述2~3种药物联合治疗,每3周或4周为1个周期。治疗组患者在化疗基础上同时给予双环醇片(北京协和药厂,国药准字H20040467,规格为每片25 mg)25mg,口服,3次/天,从化疗第1天开始服用,对照组患者不给予预防性保肝治疗,治疗3个周期,治疗期间不使用其他保肝药物。治疗期间每周随访1次;如出现肝损害则暂停化疗,给予双环醇片25mg口服、每日3次,肝功能指标恢复正常后再按照原方案和剂量继续完成2个周期化疗,共5个周期。
1.3观察指标及疗效判定标准[4]
记录治疗期间抗癌药物不良反应发生情况,计算药物性肝损害发生率;记录患者肝损害症状和体征发生情况,包括乏力、纳差、黄疸、肝区疼痛、肝肿大等;每周复查肝功能,包括丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)及总胆红素(TBIL)等。化疗后,经排除其他活动性肝炎及肿瘤肝脏转移等因素所致的肝功能异常,方可诊断为化疗药物性肝损害,损伤程度根据世界卫生组织(WHO)抗癌药物毒副作用分度标准进行评价。
1.4统计学处理
2 结果
结果见表2至表4。两组共有57例药物性肝损害患者,采用双环醇片治疗后,肝功能指标均较治疗前明显下降(P<0.05),表明双环醇片对药物性肝损害具有良好疗效。
3 讨论
常用化疗药物如环磷酰胺、甲氨蝶呤等主要在肝脏进行代谢,易直接或间接引起肝功能损害[5]。联合化疗用药时,肝损害作用更强[6]。在肿瘤治疗过程中,其他辅助用药(如抗生素、解热镇痛药、免疫抑制剂及营养支持治疗、激素类等)也可引起不同程度的肝损害,或加重化疗药物引起的肝损害[7]。化疗药物所致肝损害的治疗及预防性保肝药物已成为研究热点[8]。
保肝药是指具有改善肝脏功能、促进肝细胞再生、增强肝脏解毒功能等作用的药物,广泛应用于临床肝病患者,主要包括:抗肝炎病毒药,如干扰素;治疗肝炎辅助用药,如促肝细胞生长素、联苯双酯、甘草酸二铵、水飞蓟宾、硫普罗宁等;核苷类似物,如阿德福韦酯、拉米夫定、利巴韦林等[9]。双环醇作为我国自主研制的新型保肝护肝药,其在联苯双酯药物的基础上,经调整药物结构和筛选后被国家批准为Ⅰ类保肝护肝新药。双环醇对多种动物和细胞性肝损伤均有明显的肝保护作用,其机理可能是:抑制药物和化学毒物引起的脂质过氧化,抑制细胞调亡,加速化学毒物、致癌物的代谢清除,提高肝内抗氧化物巯基转移酶水平,维持线粒体膜流动性等[10]。

表2 两组患者肝损害分度情况比较[例(%),n=60]
表3 两组患者肝功能指标比较(±s,n=60)

表3 两组患者肝功能指标比较(±s,n=60)
注:与本组治疗前相比,*P<0.05;与对照组治疗后相比,#P<0.05。
组别治疗组对照组时间治疗前治疗后治疗前治疗后ALT(U/L)28.13±12.16 31.12±8.02#26.87±10.12 64.12±14.07*AST(U/L)26.11±9.03 28.05±10.13#25.06±8.12 77.11±18.03*TBIL(μmol/L)19.06±5.13 21.10±4.26#18.99±7.57 43.47±10.64*
表4 57例药物性肝损害患者肝功能比较(±s,n=57)

表4 57例药物性肝损害患者肝功能比较(±s,n=57)
注:与治疗前相比,*P<0.05。
时间治疗前治疗后ALT(U/L)108.13±62.15 34.12±4.06*AST(U/L)98.15±69.13 37.12±8.02*TBIL(μmol/L)33.06±12.15 13.43±1.64*
本研究结果显示,治疗3个周期内,治疗组药物性肝损害发生率明显低于对照组(P<0.05);治疗组不良反应各分度发生率明显低于对照组(P<0.05),表明加用双环醇片可降低药物性肝损害发生率,且肝损害程度较轻;治疗3个周期后,对照组肝功能各指标明显较治疗前升高(P<0.05),而治疗组较治疗前升高不明显(P>0.05),治疗组升高程度明显低于对照组(P<0.05);肝功能损害患者接受双环醇片治疗后,各肝功能指标均较双环醇治疗前明显下降(P<0.05),表明双环醇片对药物性肝功能损害具有良好疗效。
综上所述,双环醇片预防性保肝治疗可降低抗癌药物所致药物性肝损害的发生率,减轻肝功能损害程度,且对药物性肝损害有良好疗效,值得临床推广。
[1]杨佼,吕文良.药物性肝损伤临床研究及治疗进展[J].现代中西医结合杂志,2012,21(12):1 359-1 363.
[2]崔成旭,杜春霞,张雯,等.双环醇片预防肿瘤化疗药物性肝损害的研究[J].癌症进展,2008,6(6):555-557.
[3]郝立群,林海弘.双环醇片防治化疗药物性肝损害的研究[J].首都医药,2009(12):48-49.
[4]孙燕,周际昌.临床肿瘤内科手册[M].第3版.北京:人民卫生出版社,1996:30-32.
[5]Malhi H,Annamaneni P,Slehria S,et al.Cyclophosphamide disrupts hep
aticsinusoidal endothelium and improves transp lante sell engraftment in ratlive[J].Hepatology,2002,36(1):112-121.
[6]Castaneda F,Kinne RK.Effects of doxorubicin,mitomycin C,and ethanol on HSPG2 cellsin vitro[J].JCancerResClinOneol,2009,125(1):1-8.
[7]Nanarro VJ,Senior JR.Drug-related Hepatoloxicity[J].N Engl JMed,2006,354(7):731-739.
[8]Solary E,Droin N,Bettaieb A,et al.Positive and negative regulation Of apoptotic pathways by cytotoxic agents in hematologicalmalignaneies[J]. Leukem ia(Baltmore),2000,14(10):1 833-1 849.
[9]郑乐.双环醇联合阿霉素对人淋巴瘤Raji细胞的影响[D].长沙:中南大学,2012.
[10]Jiang S,Song MJ,Shin EC,et al.Apoptosis in human hepatoma cell lines by chemotherapeutic drugs via Fas-dependent and Fas-independent pathways[J].Hepatology,1999,29(1):101-110.
Clinical Research on Bicyclol Tablet for Preventing and Treating Anti-Cancer Drug Induced Liver Dam age
Tang Jing
(Liangshan Yi Autonomous Prefecture First People′s Hospital,Xichang,Sichuan,China 615000)
Objective To observe the clinical effect of Bicyclol Tablet for preventing and treating the anti-cancer drug induced liver damage.M ethods 120 patients with malignant tumor undergoing chemotherapy in the hospital from June 2013 to June 2014 were selected and divided into the treatment group and the control group according to the random number table,60 cases in each group.The two groups all accepted the conventional chemotherapy.The treatment group was added with oral Bicyclol Tablet 25 mg,3 times daily for 3 cycles of treatment,after appearance of the chemotherapeutic drugs caused liver damage,the chemotherapy was stopped and oral Bicyclol Tablet 25 mg was given,3 times daily,after the liver function indexes recovered to the normal levels,other 2 cycles of chemotherapy was continuously completed according to the original regimen and dosage.The chemotherapy lasted for 5 cycles.Results The occurrence rate of drug induced liver injury within 3 cycles of treatment in the treatment group was 28.33%,which was significantly lower than 66.67%in the control group(P<0.05);each indexing of adverse reactions in the treatment group was significantly lower than that in the control group(P<0.05);the liver function level after 3-cycle treatment in the control group was significantly increased compared with before treatment(P<0.05),while the increase after treatment in the treatment group was not obvious compared with before treatment(P>0.05),the increase degree in the treatment group was significantly lower than that in the control group(P<0.05);after the treatment of Bicyclol Tablet,the various liver function indexes in the patients with liver damage were significantly decreased compared with before treatment(P<0.05).Conclusion Bicyclol Tablet for preventive liver-protecting therapy can decrease the occurrence rate of anti-cancer drug induced liver damage,alleviates the liver damage degree,has better effect for treating drug induced liver damage and deserves clinical promotion.
bicyclol;anti-cancer drugs;chemotherapy;drug-induced liver damage
R969.4;R975+.5
A
1006-4931(2015)16-0043-03
2015-02-09)
