电感耦合等离子体质谱法和原子荧光法测定植物性食品中硒含量的对比分析
2015-10-21江永红
摘要[目的]运用电感耦合等离子體质谱法和原子荧光法对植物性食品中的硒含量进行测定。[方法]试验采用密闭高压消解技术和湿法消解对样品进行前处理,分别采用电感耦合等离子体质谱法和原子荧光法测定植物性食品中痕量硒的含量,并对2种方法进行了对比分析。[结果]研究表明,2种方法的线性回归方程的相关系数均大于0.999,其方法检出限分别为0.01、0.04 μg/L,加标回收率在95.6%~103.0%,相对标准偏差均小于5%,2种方法均具有良好的准确度和灵敏度。[结论]试验表明,电感耦合等离子体质谱法简单快速、线性范围宽,更加省时,效率更高。
关键词 电感耦合等离子体质谱法;原子荧光法;植物性食品;硒
中图分类号S609.9文献标识码
A文章编号0517-6611(2015)05-228-03
Comparative of Determination of Selenium in Plant Food by Inductively Coupled Plasma Mass Spectrometry and Atomic Fluorescence Spectrometry
JIANG Yong-hong (Guangxi Center for Disease Prevention and Control,Nanning,Guangxi 530028)
Abstract [Objective] Selenium content in plant food was determined by using Inductively Coupled Plasma Mass Spectrometry (ICP-MS) and Atomic Fluorescence Spectrometry (AFS).[Method] The methods of Inductively Coupled Plasma Mass Spectrometry (ICP-MS) and Atomic Fluorescence Spectrometry (AFS) for determination of selenium in plant food were developed and compared.The samples were digested by sealed high pressure digestion and wet digestion.The good veracity and precision were obtained in the comparison study on the two methods.[Result] The correlation coefficients for the standard curves of two methods were greater than 0.999,and the detection limits were 0.01 and 0.04 μg/L respectively.The recoveries varied from 95.6% to 103.0%,and the relative standard deviations were less than 5%.[Conclusion] The experimental results show that ICP-MS is simple,rapid,and which has a wide linear range and the precision and recovery are better than AFS.
Key words Inductively Coupled Plasma Mass Spectrometry; Atomic Fluorescence Spectrometry; Plant food; Selenium
作者简介江永红(1968- ),女,广西融安人,主管技师,从事理化检验工作。
收稿日期2014-12-26
硒是人体必需的15种微量元素之一,参与体内许多重要的代谢过程,被称为生命元素。它能清除生物体内的活性氧自由基,提高机体免疫功能,有效防止心血管疾病、肿瘤、癌症等疾病的发生,但摄入过量的硒会导致体内的血红蛋白和谷丙转氨酶升高,血糖、谷胱甘肽降低,从而对人体造成伤害[1]。因而对食品中硒含量进行检测具有重要的意义。
目前测定硒的主要方法有:分光光度法[2-3]、原子吸收光谱法[4-6]、电化学法[7-8]、原子荧光法[9-10]和电感耦合等离子体质谱法[11-13]。国家标准中以微波消解氢化物-原子荧光法测定蔬菜中的硒,胡兰基等用微波消解法对样品进行前处理使用原子荧光法对鲜黄蘑菇中的硒含量进行了测定[14],但该方法对酸度和温度要求较为苛刻,操作繁琐。电感耦合等离子体质谱法[15]作为一种新兴的痕量分析技术,由于具有高效快速、灵敏度和准确度较高等优点,自20世纪80年代发展至今,在金属测定方面已得到广泛的应用。笔者运用这2种方法对植物性食品中的硒含量进行了测定,并加以对比研究。
1材料与方法
1.1材料国家有证标准物质大米(GBW10010)和圆白菜(GBW10014),中国地球物理地球化学勘察研究所。
主要仪器:Nexion 300D电感耦合等离子体质谱仪,美国PE公司;SA-10型原子荧光形态分析仪,北京吉天仪器有限公司;硒空心阴极灯,北京有色金属研究总院;Milli-Q Academic超纯水系统,美国Millipore公司。主要试剂:硝酸(优级纯),德国Merck公司;过氧化氢(优级纯),国药集团;质谱调谐液,1.0 μg/L:Li、Be、Mg、In和U。硒标准溶液[GBW(E)080215]:100 μg/ml,中国计量科学研究院;Ge标准溶液(GSB 041728):1 000 μg/ml。超纯水:电阻率18.2 MΩ·cm。
试验用水均为超纯水,所用的器皿均在体积分数为20%的硝酸溶液中浸泡24 h以上,并用超纯水冲洗干净备用;所有试验均在室温(25 ℃)下完成。
1.2试验原理
1.2.1电感耦合等离子体质谱法。样品经密闭高压酸消解转化为溶液,样品溶液经雾化由载气送入等离子体炬管中,经过蒸发、解离、原子化和离子化等过程,转化为带正电荷的离子,经离子采集系统进入质谱仪,质谱仪根据质荷比进行分离。对于一定的质荷比,质谱的信号强度与进入质谱仪的离子数成正比,即样品浓度与质谱信号强度成正比。通过测量质谱的信号强度来测定试样溶液的元素浓度。
1.2.2原子荧光法。试样经酸加热消解后,在6 mol/L盐酸介质中,将试样中的六价硒还原成四价硒,用硼氢化钾作还原剂,将四价硒在盐酸中还原成硒化氢(H2Se),由载气带入原子化器中进行原子化,在硒空心阴极灯照射下,基态硒原子被激发至高能态,在去活化回到基态时,发射出特征波长的荧光,其荧光强度与硒含量成正比。
1.3试验方法
1.3.1标准曲线与内标溶液的配制。电感耦合等离子体质谱法(ICP-MS):用硝酸溶液(5%)将100 μg/ml的硒元素标准溶液逐级稀释成0、0.5、1.0、2.0、4.0、8.0、12.0、20、40、50 μg/L的标准使用液。Ge内标使用液(1.0 μg/ml):用硝酸溶液(5%)将1 000 μg/ml Ge标准溶液逐级稀释配得。
原子荧光光谱法(AFS):0.1 μg/ml Se标准使用液为用10%的盐酸溶液将硒标准溶液(100 μg/ml)逐级稀释得到,现配现用。标准曲线:分别移取0、0.25、0.50、1.25、2.50、5.00、10.00 ml 0.1 μg/ml Se标准使用液于25 ml容量瓶中,各加入2.50 ml浓盐酸和1.00 ml 100 g/L铁氰化钾溶液用纯水定容至25 ml,摇匀待用。
1.3.2样品预处理
1.3.2.1电感耦合等离子体质谱法。
称取样品约2.0 g于100 ml高压密闭消解内罐中,加入8.0 ml硝酸在60~90 ℃下预消解2 h后(或放置过夜),加入2.0 ml H2O2后盖好内盖,旋紧不锈钢外套,放入恒温干燥箱中,120~170 ℃保持4~6 h,在箱内自然冷却至室温,缓慢旋松不锈钢外套,将消解内罐取出,放在控温电热板上140 ℃赶酸,待溶液约剩1.0 ml 时,用水洗涤消解罐3~5次,洗液合并于25 ml塑料容量瓶中,用水定容至刻度,混匀备用。同时做试剂空白试验和质控样。
1.3.2.2氢化物-原子荧光光谱法。称取样品约2.0 g于三角烧瓶中,加10.0 ml的混合酸(V硝酸∶V高氯酸=9∶1)盖上表面皿冷消化过夜。次日于电热板上加热,并及时补加硝酸。当溶液变为清亮无色并伴有白烟时,再继续加热至剩余2.0 ml,放冷,加入5.0 ml(1+1)HCl继续加热至冒白烟后全量转移,加1.00 ml 100 g/L铁氰化钾用纯水定容至25 ml,混匀备用。同时做空白试验和质控样。
1.3.3电感耦合等离子体质谱法测定。仪器开机预热20 min后,用质谱调谐液对仪器进行最优化选择,使仪器的灵敏度、氧化物、双电荷和分辨率等各项指标达到测定要求。具体参数如下:射频功率1 100 W;采样深度2.5 mm;雾化器流量0.96 L/min;等离子体气流量15 L/min;辅助气流量1.2 L/min;雾室温度2 ℃;取样速率0.5 L/min;获取点数30;扫描方式为跳峰;重复测定次数为3次;Be>3 000 cps;Mg>20 000 cps;In>50 000 cps;U>40 000 cps;CeO/Ce<2.5%;Ce++/Ce<3.0%。
1.3.4原子荧光法测定。預热后确定仪器最佳工作状态,参考工作条件如下:负高压270 V;灯电流60 mA;原子化器高度8 mm;载气流量300 ml/min;屏蔽气流量800 ml/min;测量方法为校准曲线;读数方式为峰面积;读数时间10 s;延迟时间1.0 s。
2结果与分析
2.1电感耦合等离子体质谱法
2.1.1酸的种类和用量的选择。
预处理试验中用于分解样品的试剂主要有:硝酸、盐酸、高氯酸和过氧化氢等。由于使用盐酸和高氯酸消解试样会产生大量的氯离子影响电感耦合等离子体质谱法测定,而单一使用硝酸来处理样品,其产生的大量氮氧化物又会干扰试验的测定,过氧化氢是一种强氧化剂,与硝酸共用不但能够增强消解能力将有机物完全破坏而且消解完成后易于分解除去;所以试验选用“硝酸+过氧化氢”作为消解试剂。同时为了使样品消解彻底、试验空白值低等,试验选择“8.0 ml HNO3+2.0 mlH2O2”。
2.1.2硝酸浓度对测定结果的影响。
当混合标准使用液的浓度为2.0 μg/L时,考察了硝酸浓度对测定信号相对强度的影响。试验结果表明,当硝酸浓度在0.5%~15.0%范围内时,随着硝酸酸度的增加,试验的测定结果基本没有变化,同时为了减少酸对采样锥和截取锥的腐蚀和降低试剂空白值,该试验选择硝酸浓度为5%。
2.1.3干扰的消除。
使用ICP-MS测定食品中的Se时受到的干扰除了非质谱干扰外,还有质谱干扰(如Kr、BrH、Ar2H、Ho++、Dy++、Er++)。对于这些同量异位素、多原子、双电荷离子等质谱干扰,使用普通模式采用数学校正方程来校正往往不太可靠,为此该试验采用最优化仪器条件(降低氧化物和双电荷的产生)和动态反应池(NH3模式下对可能出现的各类干扰能有效地消除)等方法来消除。非质谱干扰主要源于样品基体,克服基体效应最有效的方法是稀释样品、内标校正。试验通过在线加入74Ge内标溶液监测信号变动情况,用内标法定量,有效地克服了仪器的漂移,保证了测量的准确性。
2.2氢化物-原子荧光光谱法
2.2.1负高压与灯电流的选择。
考察了不同负高压和灯电流对体系的荧光强度的影响。试验显示,当负高压为 270 V,灯电流为 60 mA。此时体系的灵敏度较高,噪声小,校准曲线的线性较好。
2.2.2载气与屏蔽气流量的选择。
改变载气流量,测定硒标准溶液的荧光强度。结果表明,过小的载气流量易导致硒化氢的传输效率较低,从而降低荧光信号;而过大的载气流量则容易冲稀硒原子蒸汽的浓度,造成荧光信号降低。屏蔽气流量为800 ml/min时,体系的荧光强度最大且变化较小,为达到最佳效果,试验选择载气流量300 ml/min;屏蔽气流量800 ml/min。
2.2.3酸度的选择。
合适的酸度有利于氢化物的生成。试验考察了酸度在1%~15%范围内,荧光信号的变化情况。试验表明,随着酸度的增加,产物的荧光强度不断增强,当酸度在1%~15%时荧光强度达到最大,所以试验选用10%的盐酸作介质。
2.2.4硼氢化钾浓度的选择。
硼氢化钾的浓度大小直接影响硒化氢的生成。用量较小时,由于还原能力比较弱,所以灵敏度很低;而当用量过大时,由于生成大量氢气产生稀释作用,灵敏度也降低。试验固定其他条件不变,改变硼氢化钾的浓度,对硒的荧光强度进行测试。结果表明,当硼氢化钾浓度为 25 g/L时,荧光强度最大,效果较佳。
2.3校准曲线、线性范围及检出限
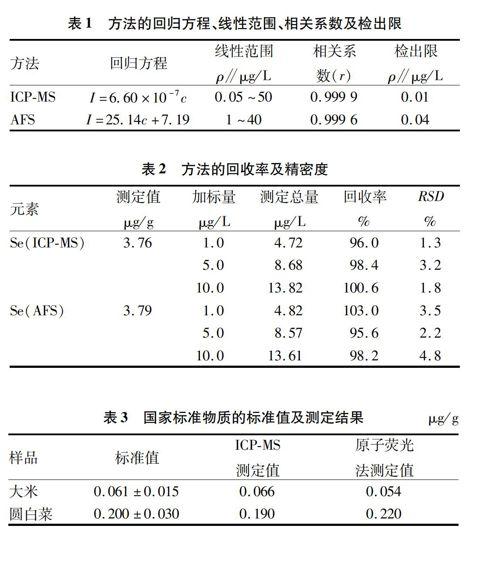
在最佳试验条件下,以硒的质谱信号强度(cps)与Ge的质谱信号强度(cps)的比值为纵坐标,硒浓度为横坐标绘制标准曲线;荧光法则测定不同浓度硒标准溶液对应的荧光强度,绘制硒浓度与荧光强度的工作曲线。2种方法的检出限均按空白溶液平行测定11次所得的标准偏差的3倍计算,如表1所示。
2.4方法的精密度和准确度
取待检食品的消化液,分别添加高、中、低3种不同浓度的硒元素标准液,连续重复测定3次,样品的回收率及精密度如表2所示。由表2可以看出,2种方法的准确度和精密度都较好,符合痕量分析的要求。
2.5样品测定结果
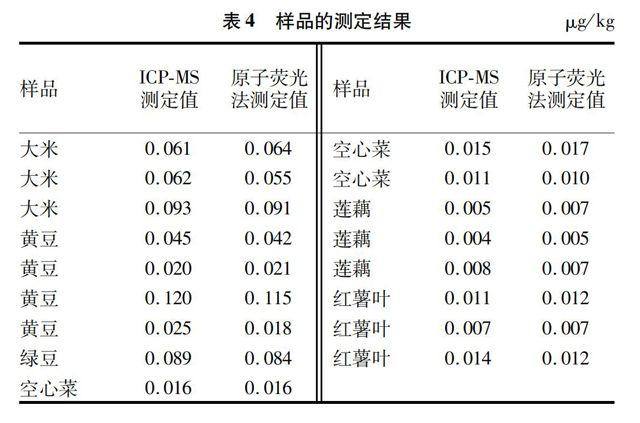
采用试验方法对样品进行处理,平行测定3次并计算其平均值,结果如表4所示。
3结论
试验分别采用电感耦合等离子体质谱法与原子荧光法对植物性食品中的硒含量进行了检测,并在样品处理及结果影响方面对2种方法进行了对比分析。结果表明,2种方法用于蔬菜中硒的测定均具有较好的准确度与灵敏度。但与原子荧光法相比,电感耦合等离子体质谱法用于食品中硒的测定操作更为简单,分析更快速,检出限更低,更有推广应用价值。
参考文献
[1]
王夔.生物科学中的微量元素(上册)[M].北京:中国计量出版社,1992.
[2] REVANASIDDAPPA H D,KIRAN KUMAR T N.Spectrophotometric determination of selenium by use of thionin[J].Analytical and Bioanalytical Chemistry,2002,374:1121-1124.
[3] 朱鸭梅,崔群,王海燕.紫外分光光度法测定硒氧化过程中二氧化硒[J].分析试验室,2010,9(10):60-63.
[4] 舒永红,牟德海.石墨炉原子吸收法测定麦芽粉中的锗和硒[J].光谱学与光谱分析,1998,18(6):703-706.
[5] 哈婧,康维钧,孙汉文,等.流动注射-氢化物发生-导数原子吸收光谱法测定水中痕量硒[J].冶金分析,2007,27(5):14-19.
[6] 弓巧娟,杨海英.石墨炉原子吸收法测定黑花生中的硒[J].分析测试学报,2011,30(2):218-221.
[7] LANGE B,VAN DEN BERG,C M G.Determination of selenium by catalytic cathodic stripping voltammertry[J].Analytica Chimica Acta,2000,418:33-42.
[8] 楊志明,李方实,江涛.阴极溶出伏安法测定硒酵母中微量硒[J].广东微量元素科学,2001,11(8):62-65.
[9] 薛超群,郭敏.氢化物发生-原子荧光光谱法测定土壤样品中不同价态的硒[J].岩矿测试,2012,31(6):980-984.
[10] 倪迎瑞,李中玺,李海涛,等.氢化物发生-四通道无色散原子荧光光谱法同时测定纯铜中的痕量砷锑硒碲[J].冶金分析,2012,32(9):26-29.
[11] LABAT L,DEHON B,LHERMITTE M.Rapid and simple determination of selenium in blood serum by inductively coupled plasma-mass spectrometry (ICP-MS)[J].Analytical and Bioanalytical Chemistry,2003,376:270-273.
[12] 刘军,陈建平.微波消解-电感耦合等离子体质谱法测定灵芝孢子粉中锗和硒[J].食品科学,2008,29(12):531-532.
[13] 墨淑敏.微波消解-电感耦合等离子体质谱法测定大米中痕量硒和锶[J].分析试验室,2013,32(10):84-86.
[14] 胡兰基,杨娜,王洪桂,等.氢化物发生-原子荧光光谱法测定鲜黄蘑菇中的硒[J].安徽农业科学,2014,42(19):6387-6480.
[15] 王小如.电感耦合等离子体质谱应用实例[M].北京:化学工业出版社,2005.
安徽农业科学2015年
责任编辑李菲菲责任校对李岩
