辣椒CaMAPK7启动子顺式作用元件及其表达分析
2015-10-21杨明星申磊文嘉瑜唐倩石兰平刘艳艳杨晟胡炯刘彩玲吴杨何水林
杨明星 申磊 文嘉瑜 唐倩 石兰平 刘艳艳 杨晟 胡炯 刘彩玲 吴杨 何水林

摘 要 促分裂原活化蛋白激酶(MAPK)在植物生长、发育和适应环境中起着十分重要的作用,但对该家族多数成员的表达调控机制认识仍十分有限。前期实验已分离获得辣椒一个MAPK家族成员CaMAPK7,并发现该基因的表达受病原菌、高温等逆境的诱导,但其表达调控机制仍不清楚。本研究进一步分离了CaMAPK7的启动子序列(pCaMAPK7),发现其TATA框位于-165 bp与-170 bp之间,此外还发现W-box,HSE,TCA,LTR,ERE等多种与生物及非生物逆境胁迫应答相关的顺式作用元件。通过构建该启动子与报告基因GUS融合表达载体pCaMAPK7::GUS,利用农杆菌介导的本氏烟草叶片瞬间表达系统分析发现pCaMAPK7可应答青枯菌接种及水杨酸(SA)、茉莉酸甲酯(MeJA)、油菜素内酯(BR)、脱落酸(ABA)和乙烯(ET)等外源激素处理,表明CaMAPK7应答青枯菌、外源激素处理主要是通过该启动子介导的转录调节实现的。
关键词 辣椒;启动子;烟草瞬间表达系统
中图分类号 S641 文献标识码 A
MAPK(促分裂原活化蛋白激酶)联结一般由MAPKKK、MAPKK 和MAPK组成,广泛存在于真核生物中,参与介导细胞的生长、发育、分裂、分化及凋亡等多种生物学过程的调节,并与生长素、脱落酸、乙烯和细胞分裂素等信号通路有关,在植物生长、发育和适应生物胁迫及非生物胁迫的信号传导中起重要的调节作用,但其表达调节和作用机制仍不清楚。
拟南芥[1]、小麦[2]、水稻[3]、辣椒[4]和短柄草[5]等大量的植物或作物基因组测序的完成和公布,为植物MAPK信号联结成员的鉴定、表达调节和功能分析奠定了重要的基础。已经在多种植物基因组中发现20个左右的MAPK成员,并对部分成员的表达和功能及其作用机制进行了分析。例如,研究表明棉花GhMPK2可以受到病原菌侵染的诱导表达并且其在烟草超表达可以明显提高转基因烟草对病原菌的抗性[6],GhMPK17在棉花應答高盐中起着重要的作用[7],水稻MAPK家族成员IBR5在水稻耐干旱中起着负调控的作用[8],这些结果表明MAPK通路在植物适应各类逆境胁迫过程中起着重要作用。本实验室前期研究发现辣椒基因组中CaMAPK7在根、茎和叶中均有不同程度的组成型表达,其中以根部的表达最高,这种组成型表达可能与该基因参与植物的生长发育有关,另外,在叶片中则受到青枯菌侵染、高温等逆境及水杨酸、茉莉酸甲酯和乙烯等外源激素处理的诱导,但脱落酸处理使其表达下调,暗示CaMAPK7可能在辣椒应答青枯病和高温等逆境胁迫中起一定作用[9],但其应答逆境或外源激素表达的分子机制还不太清楚。本研究利用GUS报告基因分析启动子在生物与非生物逆境处理下的转录表达情况,不仅有利于阐明CaMAPK7应答几种外源激素的分子机制,为进一步鉴定CaMAPK7功能奠定基础,还可望为作物的遗传改良提供有利用价值的诱导型启动子或者顺式作用元件。
1 材料与方法
1.1 材料
辣椒基因型CM334、本氏烟草、大肠杆菌(Escherichia coli)菌株DH10B、根癌农杆菌(Agrobacterium tumefaciens)菌株GV3101、Gateway入门载体pDNOR-207及GUS融合载体pMDC163均由本实验室提供。KOD高保真聚合酶购自北京百奥莱博科技有限公司,Gateway试剂盒购自Invitrogen公司,质粒提取试剂盒、凝胶回收试剂盒均购自泰京有限公司,各种抗生素购自上海生工生物有限公司,引物合成和测序均委托上海Invitrogen公司。其他常规试剂均为国产分析纯产品。
1.2 方法
1.2.1 CaMAPK7启动子的克隆 利用CTAB法提取的辣椒CM334基因组DNA为模板,利用premier primer 5.0生物信息学软件设计用于扩增该启动子的上下游引物(F5′-GGGGACAAGTTTGTA
CAAAAAAGCAGGCTTCACCAATTTAAATAATGTAA
TAGAAA-3′R:5′-GGGGACCACTTTGTACAAGAAA
GCTGGGTCTTCTCTGTTATTTTCAATATTCA-3′),采用KOD高保真酶进行PCR反应(程序:94 ℃,5 min;94 ℃,30 s;56 ℃,30 s;68 ℃,90 s,30 cycles,68 ℃,10 min),用1%琼脂糖凝胶电泳检测后,将扩增得到的PCR产物进行回收。
1.2.2 CaMAPK7启动子转化载体的构建 用Gateway法的BP反应将PCR产物连接到入门载体pDNOR-207,命名为pCaMAPK7-207,挑取经PCR验证的阳性克隆送往英俊生物公司进行测序,测序确认无误后使用Gateway的LR反应构建pCaMAPK7::GUS目的表达载体,并命名为pCaMAPK7-163。PCR检测为阳性的再使用冻融法转化到农杆菌GV3101菌株中保存备用。
1.2.3 对CaMAPK7启动子序列进行顺式作用元件分析 把公司发回的测序结果与GenBank公布的辣椒(CM334)的启动子序列在DNAMAN上进行比对,确定两者之间的同源序列,比对结果无误之后在PlantCARE网站(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)上对获得的启动子序列进行顺式作用元件分析。
1.2.4 农杆菌介导的瞬间表达 将含有重组质粒的农杆菌在含75 μg/mL抗生素利福平、50 μg/mL卡那霉素和0.2 μg/mL LB固体(10 g Tryptone,5 g Yeast extract,10 g NaCl,15 g agar/L),培养基上划线,28 ℃下培养2 d。挑取单克隆接种于2 mL含有相应抗生素的液体LB培养基中,28 ℃下以220 r/min震荡培养过夜后,转移至50 mL新鲜配制不加抗生素的LB液体培养基扩大培养,3 500 r/min离心15 min并收集菌液,用侵染液(10 mmol/L MgCl2,
10 mmol/L MES,200 mmol/L acetosyringone,pH5.1~5.4)重悬,终浓度为OD600=0.6~0.8。用不带针头的针管将菌液注射进事先用水拭擦干净的生长健康且均匀一致的本氏烟草叶片中。将注射完渗透液的烟草移至25 ℃光照培养箱中(L ∶ D=16 h ∶ 8 h)。培养2 d后对烟草进行各种逆境处理。
1.2.5 烟草植株的几种逆境处理 烟草植株的烟草青枯菌(R. solanacearum)接种:首先将-80 ℃保存的青枯菌FJC100301于4 ℃下溶化并在含有TTC的SPA固体培养基中划线,28 ℃培养2~3 d,从SPA固体培养基中挑取单克隆接种于100 mL SPA液体培养基中,28 ℃摇床震荡约24 h,摇至菌液OD600值达到1.0。菌液在3 500 r/min下离心10 min,去除上清,用10 mmol/L MgCl2重悬至终浓度为OD600=0.6,接着把调好OD600值的悬浮液用去掉针头的注射器针筒注射先前已渗入含启动子渗透液的各个烟草叶片中,同时以注射MgCl2的烟草叶片作为对照。处理后的烟草放回光照培养箱正常培养12 h和24 h后,分别采样做GUS酶活性的测定。
烟草植株外源激素处理:对先前已注射启动子渗透液的本氏烟草叶片分别进行外源激素处理。具体方法是将茉莉酸甲酯100 μmol/L、水杨酸1 mmol/L、脱落酸100 μmol/L、乙烯100 μmol/L和油菜素内酯10 μmol/L直接喷洒在已注射含启动子渗透液的烟草叶片并保湿,置于25 ℃光照培养箱中(L ∶ D=16 h ∶ 8 h)处理12 h和24 h后分别采样提取蛋白用于GUS定量分析,同时设置喷洒蒸馏水为对照。所有的处理均做6个重复。
1.2.6 CaMAPK7启动子酶活性的测定 GUS酶活性的测定采用分光光度计法进行,具体步骤参考曾凡锁[10]等的方法。酶活力单位为每分钟水解PNPG生成1 nmol/L对硝基苯酚的酶量为一个单位。GUS活性以每mg蛋白的酶活力表示,实验设置6次重复。
2 结果与分析
2.1 CaMAPK7基因的启动子克隆及序列分析
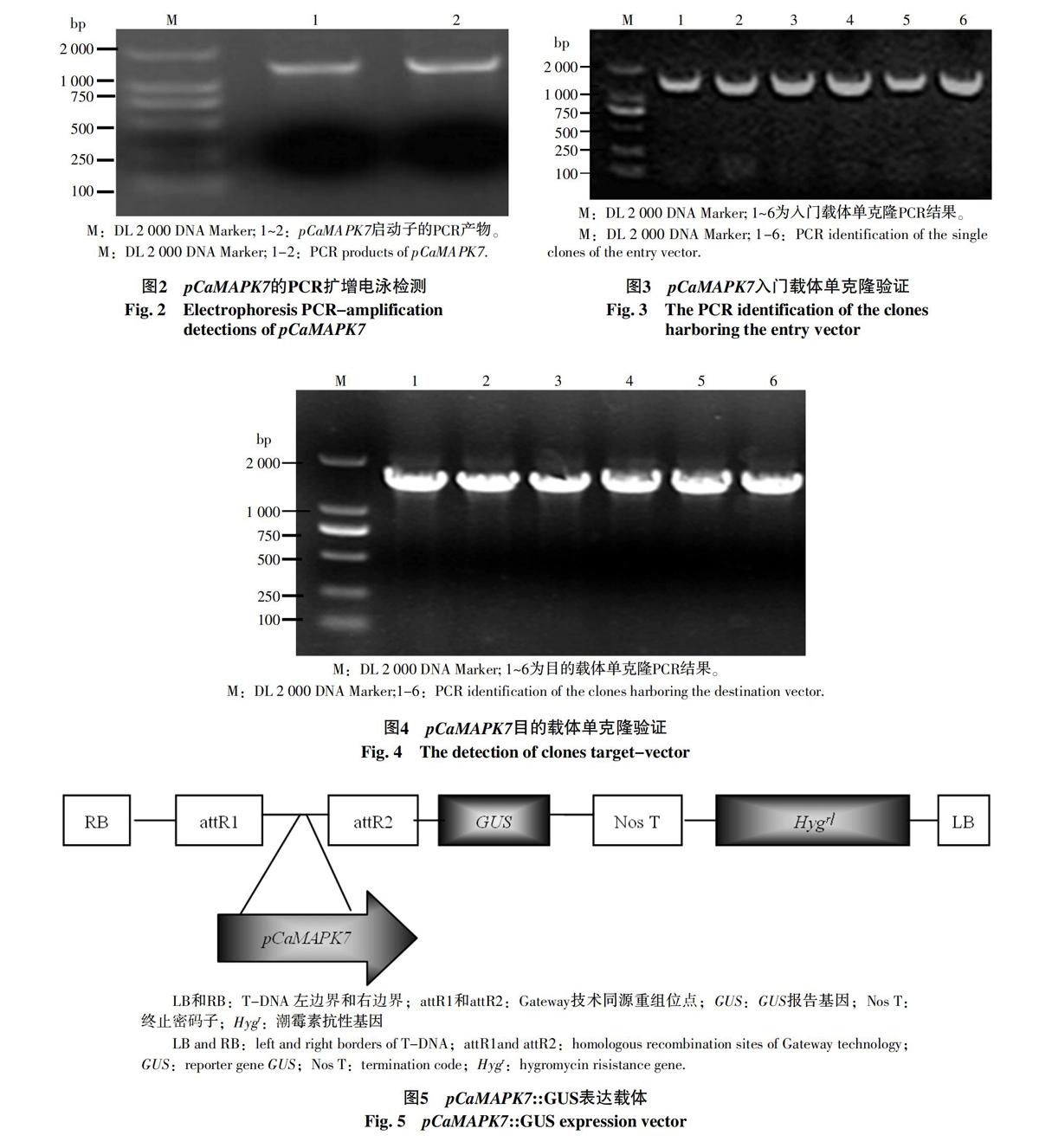
通过PCR反应扩增出一条大小约为1 500的PCR产物,将该产物连接到入门载体pDNOR-207并测序,得到的测序序列与Genbank公布的辣椒CM334该启动子序列比对,在顺式作用元件分析网站plantCARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)对获得的序列进行分析,预测到多个与植物逆境相关元件,如高温相关元件HSE、WRKY转录因子结合元件W-box、乙烯应答元件ERE、低温应答元件LTR等(图1)。
2.2 启动子GUS融合载体的构建
通过特异性引物PCR的扩增,获得了CaMAPK7启动子PCR扩增片段(pCaMAPK7)(图2),将该片段通过Gateway技术通过过渡载体pDONR-207进一步克隆到目的载体pMDC163中并验证(图3),最后将含pCaMAPK7::GUS 的目的载体转化到农杆菌GV3101并验证(图4),最终构建的融合表达载体(图5)。
2.3 启动子不同逆境和激素处理下的表达分析
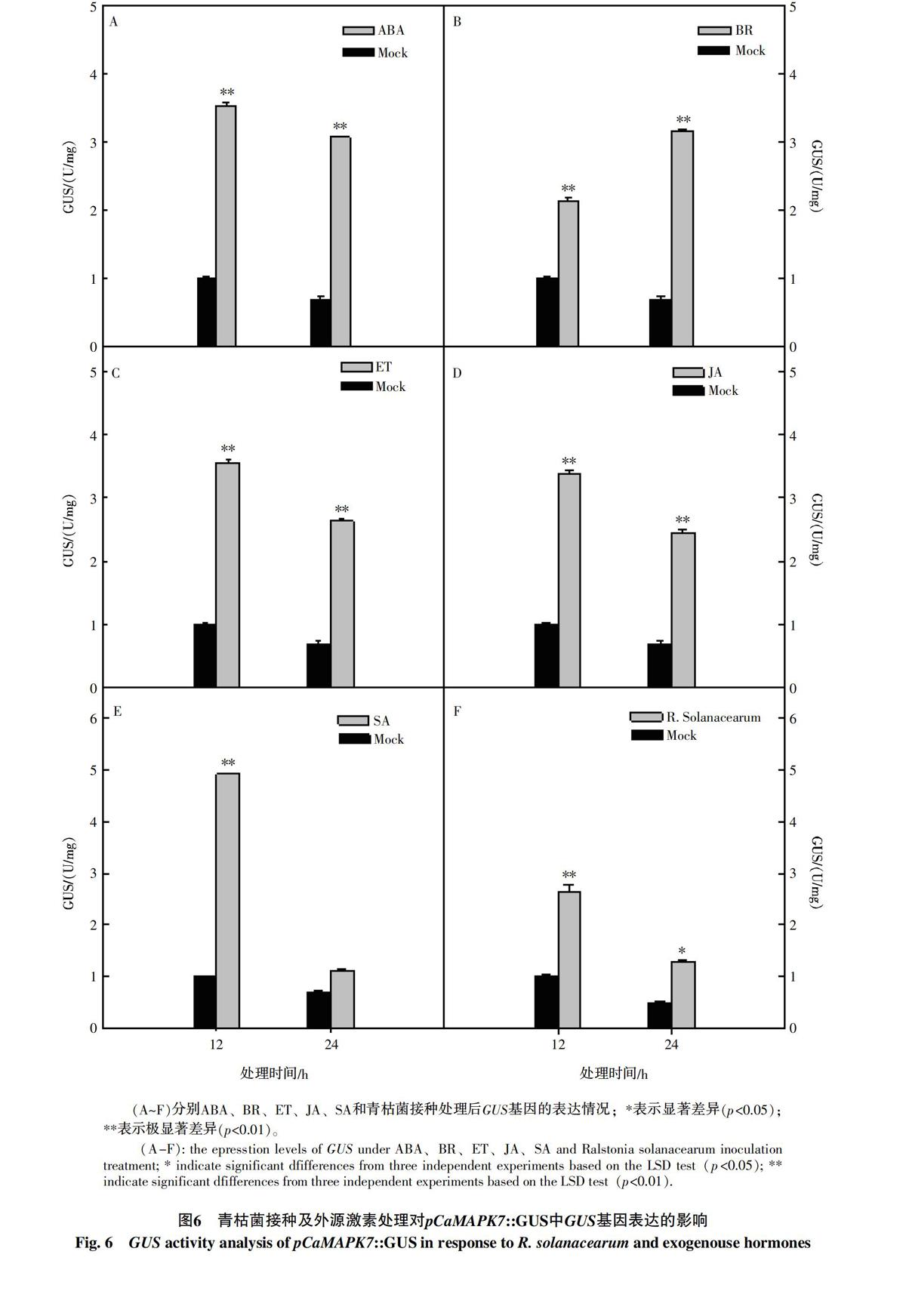
在ABA、BR、ET、JA激素处理下,12 h和24 h时,GUS活性都出现了极显著性差异(p<0.01),在12 h,分别为对照的3.53、2.12、3.55、3.37倍;在24 h,分别为对照的4.37、4.48、3.74、3.48倍;而在SA处理下,在12 h出现极显著性差异,为对照的4.9倍,随后在24 h又恢复到与对照没有显著差异;在接种青枯病处理后,在12 h出现极显著性差异,为对照的2.63倍,24 h则有显著性差异(p<0.05),为对照的2.56倍。在ABA、BR、ET、JA、SA和青枯菌接种处理下,pCaMAPK7驱动的GUS活性都出现不同程度的增强(图6)。这些结果说明CaMAPK7启动子能够响应青枯菌和多种外源激素处理。
3 讨论与结论
植物在其自然生境中总是不可避免地遭受到各种生物和非生物逆境胁迫,長期的进化也使植物形成了复杂的防御反应机制,包括对各种逆境的感知和信号传递,最终达到细胞核调节相关基因的表达以实现在生理生化水平上应对逆境的调节。植物的耐(抗)逆反应在很大程度上受到信号通路的调控,其中MAPKKK-MAPKK-MAPK级联是植物应答逆境信号通路的重要组成成员,均由多基因家族编码。大量研究表明,参与应答逆境的植物MAPK家族成员往往表现出对逆境胁迫的转录应答。本研究发现,辣椒CaMAPK7的启动子区域中含有5个W-box、1个HSE、1个LTR和1个TCA等与生物以及非生物胁迫相关的顺式作用元。其中W-box是可和特定WRKY转录因子相结合,而WRKY转录因子的不同成员可参与包括病害、高温、干旱、高盐等,还与SA、JA、ET等信号通路相关[11-16]。LTR元件是与低温胁迫相关的元件[17-21]。ERE元件是一个与乙烯应答相关的元件[22]。HSE则可通过与HSF结合,介导目标基因对高温胁迫的应答[23]。TCA在目标基因应答外源SA处理中起作用[24]。这些原件的存在与本实验室前期研究发现该基因可受到青枯菌接种和高温处理的诱导结合较为吻合。基于农杆菌注射的烟草外源基因瞬间表达分析方法已经在植物功能基因组学研究中得到了成功的应用[25]。本研究利用该方法分析了pCaMAPK7::GUS中GUS报告基因对青枯菌接种以及外源激素处理的应答,结果发现pCaMAPK7驱动的GUS基因表达受到青枯菌接种和外源SA,JA,ET,BR 和ABA等激素处理的诱导,进一步表明CaMAPK7应答青枯菌接种和各种外源激素处理与其启动子顺式作用原件结合特地的转录因子在转录水平上调节所致。由于pCaMAPK7可协同应答SA,JA,ET,BR 和ABA等外源激素处理,暗示CaMAPK7可能参与了上述激素介导的信号通路,在辣椒耐高温和抗病等反应中起重要的调节作用。未来进一步分离CaMAPK7的底物,将有助于进一步 解析CaMAPK7的作用辣椒的抗逆机制。
参考文献
[1] Kerk D, Bulgrien J, Smith D W, et al. The complement of protein phosphatase catalytic subunits encoded in the genome of Arabidopsis [J]. Plant Physiol, 2002, 129(2): 908-925.
[2] Kong X, Lv W, Zhang D, et al. Genome-wide identification and analysis of expression profiles of maize mitogen-activated protein kinase kinase kinase[J]. PLoS One, 2013, 8(2): e57 714.
[3] Kumar K, Sinha A K. Genome-wide transcriptome modulation in rice transgenic lines expressing engineered mitogen activated protein kinase kinase 6[J]. Plant Signal Behav, 2014, 9: e28 502.
[4] Kim S, Park M, Yeom S I, et al. Genome sequence of the hot pepper provides insights into the evolution of pungency in Capsicum species[J]. Nat Genet, 2014, 46(3): 270-278.
[5] Chen L, Hu W, Tan S, et al. Genome-wide identification and analysis of MAPK and MAPKK gene families in Brachypodium distachyon[J]. PLoS One, 2012, 7(10): e46 744.
[6] Zhang L, Xi D, Luo L, et al. Cotton GhMPK2 is involved in multiple signaling pathways and mediates defense responses to pathogen infection and oxidative stress[J]. FEBS J, 2011, 278(8): 1 367-1 378.
[7] Li Y, Feng D, Zhang D, et al. Rice MAPK phosphatase IBR5 negatively regulates drought stress tolerance in transgenic Nicotiana tabacum[J]. Plant Sci, 2012, 188-189: 10-18.
[8] Zhang J, Zou D, Li Y, et al. GhMPK17, a cotton mitogen-activated protein kinase, is involved in plant response to high salinity and osmotic stresses and ABA signaling[J]. PLoS One, 2014, 9(4): e95 642.
[9] 石蘭平, 杨 晟, 申 磊, 等. 辣椒CaMAPK7的全长cDNA克隆及其表达分析[J]. 亚热带农业研究, 2014(3): 181-186.
[10] 曾凡锁, 钱晶晶, 康 军, 等. 转基因白桦中GUS基因表达的定量分析[J]. 植物学报, 2009, 44(4): 484-490.
[11] Dang F, Wang Y, She J, et al. Overexpression of CaWRKY27, a subgroup IIe WRKY transcription factor of Capsicum annuum, positively regulates tobacco resistance to Ralstonia solanacearum infection[J]. Physiol Plant, 2014, 150(3): 397-411.
[12] Dang F F, Wang Y N, Yu L, et al. CaWRKY40, a WRKY protein of pepper, plays an important role in the regulation of tolerance to heat stress and resistance to Ralstonia solanacearum infection[J]. Plant Cell Environ, 2013, 36(4): 757-774.
[13] Eulgem T. Dissecting the WRKY web of plant defense regulators[J]. PLoS Pathog, 2006, 2(11): e126.
[14] Eulgem T, Somssich I E. Networks of WRKY transcription factors in defense signaling[J]. Curr Opin Plant Biol, 2007, 10(4): 366-371.
[15] Knoth C, Ringler J, Dangl J L. Arabidopsis WRKY70 is required for full RPP4-mediated disease resistance and basal defense against Hyaloperonospora parasitica[J]. Mol Plant Microbe Interact, 2007, 20(2): 120-128.
[16] Wang Y, Dang F, Liu Z, et al. CaWRKY58, encoding a group I WRKY transcription factor of Capsicum annuum, negatively regulates resistance to Ralstonia solanacearum infection[J]. Mol Plant Pathol, 2013, 14(2): 131-144.
[17] Bahn S C, Bae M S, Park Y B, et al. Molecular cloning and characterization of a novel low temperature-induced gene, blti2, from barley(Hordeum vulgare L.)[J]. Biochim Biophys Acta, 2001, 1522(2): 134-137.
[18] Chen A, Gusta LV, Brule-Babel A, et al. Varietal and chromosome 2H locus-specific frost tolerance in reproductive tissues of barley(Hordeum vulgare L.)detected using a frost simulation chamber[J]. Theor Appl Genet, 2009a, 119(4): 685-694.
[19] Chen A, Reinheimer J, Brule-Babel A, et al. Genes and traits associated with chromosome 2H and 5H regions controlling sensitivity of reproductive tissues to frost in barley[J]. Theor Appl Genet, 2009b, 118(8): 1 465-1 476.
[20] Dunn M A, Goddard N J, Zhang L, et al. Low-temperature-responsive barley genes have different control mechanisms[J]. Plant Mol Biol, 1994, 24(6): 879-888.
[21] Ivashuta S, Naumkina M, Gau M, et al. Genotype-dependent transcriptional activation of novel repetitive elements during cold acclimation of alfalfa(Medicago sativa)[J]. Plant J, 31(5): 615-627.
[22] Mahajan N S, Dewangan V. Structural features of diverse Pin-II proteinase inhibitor genes from Capsicum annuum[J]. Planta, 2014, 12(4): 119-128.
[23] 李 冰, 劉宏涛, 孙大业, 等. 植物热激反应的信号转导机理[J]. 植物生理与分子生物学学报, 2002, 28(1): 1-10.
[24] Bowler C, Alliote T, De Loose M, et al. Effects of salicylic acid on oxidative stress and t hermotolerance in tobacco[J]. Plant Physiol, 2000, 156: 659-665
[25] Choi D S, Hwang I S, Hwang B K. Requirement of the cytosolic interaction between PATHOGENESIS-RELATED PROTEIN10 and LEUCINE-RICH REPEAT PROTEIN1 for cell death and defense signaling in pepper[J]. Plant Cell, 2012, 24(4): 1 675-1 690.
