聚L-精氨酸/石墨烯修饰电极对日落黄的测定
2015-10-19胡晴晴朱庆仁孙登明
胡晴晴,朱庆仁,孙登明
(淮北师范大学化学与材料科学学院,安徽淮北235000)
0 引言
石墨烯是一种新型的二维结构材料,其中碳原子sp2杂化成的单层片堆叠成一个二维蜂巢状点阵结构,并被称为“宇宙中最薄的材料”[1-3]。石墨烯固有的大π键是其具有很强导电性的原因[4]。此外石墨烯有较高的比表面积[5],良好的导电性及稳定的化学性能,是一种良好的电化学传感材料[6]。石墨烯修饰在玻碳电极上能大大增加峰电流、提高催化性能和降低过电位。以石墨烯为基础的传感器不仅可以用于药物和生物小分子的检测,对色素类物质的研究也有重要作用。
日落黄(SY)是一种人工合成的偶氮类色素,该色素色艳、稳定、价廉[7],常用作果蔬、饮品、糖果的食用添加剂。由于分子中含有偶氮官能团(N=N)和芳环结构[8],对人体可导致慢性毒性,也有一定的致癌性[9],因此对其含量测定有重要的现实意义。目前,对合成色素测定的方法主要有荧光光谱法[10]和分光光度法[11]等。这些方法需要复杂的预处理,且过程繁琐。该文制备了PLAERGO/GCE复合膜修饰电极,研究了SY在修饰电极上的电化学响应,建立了电化学测定SY的新方法,该方法简单,修饰电极稳定性和重现性好,测定SY灵敏度高,用于样品中SY的测定,结果令人满意。
1 实验部分
1.1 仪器和试剂
BAS100/W电化学分析系统 (美国BAS公司);pHS-3C型酸度计(上海康仪仪器有限公司)。
GO分散液:2 mg/mL(南京先锋纳米材料科技有限公司);SY 贮备液:5.00×10-3mol/L(避光冷存),LA 贮备液:5.0×10-3mol/L, 使用时逐级稀释至所需浓度; 磷酸盐缓冲溶液 (PBS):pH2.0~pH8.0, 用 0.1 mol/L 磷酸盐按常规方法配制,pH计校准。
1.2 修饰电极的制备
玻碳电极(φ=3 mm)按文献[12]中的方法进行预处理。在 1.00 mg/mL GO,1.00×10-3mol/L LA,酸度为pH5.5的聚合底液中,以玻碳电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极,扫描电位:2.3~-1.1 V,扫描速率:120 mV/s,扫描循环周次:8周。由于在较负的电位下,GO能被电化学还原成石墨烯[13-14], 因此把修饰到GCE表面的GO记作ERGO。取出电极用水冲洗干净,室温干燥,即制得PLA-ERGO/GCE。
1.3 实验方法
在10 mL容量瓶中,准确加入一定量的SY,5.0 mL pH 为 3.5 的 PBS,用水定容,摇匀后转移到石英电解池中。以修饰电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极。进行循环伏安或示差脉冲扫描,记录电化学参数。扫描结束后,在空白液中将电极进行扫描,至SY的峰消失,即可进行下一次测定。所有实验均在室温下进行。
2 结果与讨论
2.1 SY的循环伏安行为
图1为1.00×10-5mol/L SY在不同电极上的循环伏安图。可以看出SY在GCE上几乎看不到氧化峰,在PLA/GCE和PLA-ERGO/GCE上峰电流增大,说明PLA/GCE和PLA-ERGO/GCE对SY有较明显的催化作用,其中PLA-ERGO/GCE的催化效果最强,这可能是ERGO提供了较大的比表面积,并与PLA协同催化作用的结果。

图1 SY 在 GCE(a),PLA/GCE(b)和 PLA-ERGO/GCE(c)上的循环伏安曲线Fig.1 CVs of SY on GCE(a),PLA/GCE(b)and PLAERGO/GCE(c)at a scan rate of 0.10 V/s in PBS(pH3.5)
2.2 pH的影响
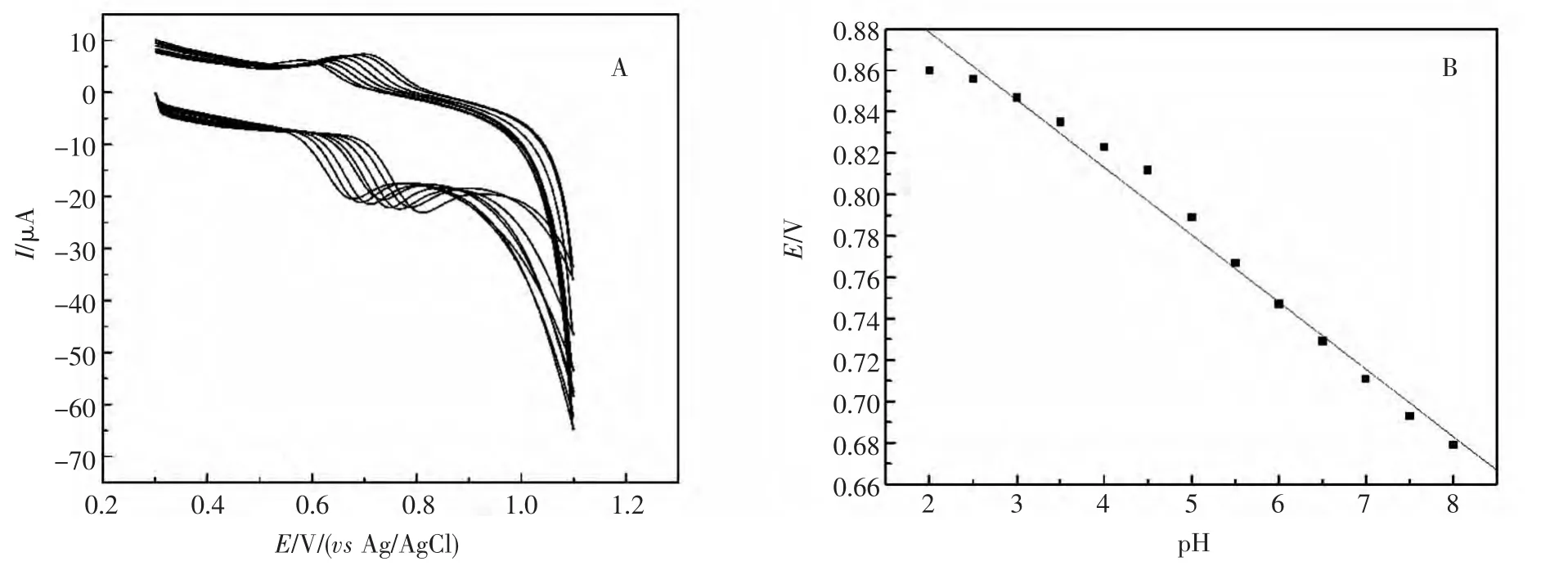
图2 SY在不同pH下的CV曲线(A)和E与pH的关系曲线(B)Fig.2 CVs of SY with different pH(A)and the corresponding relationship curve between the peak potential and pH(B)pH1~8:4.5,5.0,5.5,6.0,6.5,7.0,7.5,8.0;Scan rate of 0.10 V/s
酸度的影响如图2所示,随着pH增加,SY的峰位置均负移,在 pH2.0~pH8.0 范围内,峰电位与pH呈线性关系,其线性回归方程为E=0.94325-0.03253 pH,r=0.9909。说明 SY 的氧化过程有质子参与,SY在pH3.5时峰电流最大,该实验选择pH3.5作为测定SY的最佳酸度。
2.3 扫速与峰电流、峰电位的关系
扫速的影响见图3,随着扫速的增加,SY的响应电流逐渐增大,氧化峰正移,还原峰负移。在0.04~0.40 V/s 范围内, 峰电流与扫速成线性关系 , 其 回 归 方 程 为 :Ia=-9.8599-0.07028 v,r=0.9905,说明SY在修饰电极上主要受吸附控制。扫速在 0.02~0.40 V/s范围内,电位与扫速的对数也呈线性关系,其回归方程为:Epa=0.68332+0.03221lnv,r=0.9901, 说明扫速增加时,SY 在修饰电极上的氧化还原反应速率降低,电极反应可逆性变差。
2.4 电极表面吸附量的计算
采用计时电量法,仪器参数设置如下,初始电位 0.4 V,阶跃电位 0.9 V,等待时间 10 s,采样间隔时间 0.5 s,采样点数 500,在 pH3.5 的底液中, 对1.00×10-5mol/L SY和空白溶液测定,测得计时电量结果见图4。SY在电极表面的吸附量由式(1)计算,式中,n为得失电子数,F为法拉第常数,τ为吸附量 (mol/cm2),A 为电极表面积(cm2),Qdl为电容电量(c)。

图3 SY在不同扫速下的CV图Fig.3 Cyclic voltammetric curves for SY with different scan ratefrom 1 to 20:0.02,0.04,0.06,0.08,0.10,0.12,0.14,0.16,0.18,0.20,0.22,0.24,0.26,0.28,0.30,0.32,0.34,0.36,0.38,0.40
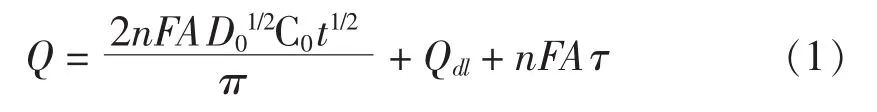

图4 SY(1)、(3)和空白溶液(2)、(4)在 GCE(A)、PLA-ERGO/GCE(B)的计时电量曲线和 Q~ t1/2关系曲线(C)、(D)Fig.4 Chronocoulometrys of SY(1)、(3)and blank soultion(2)、(4)and the plots of Q~t1/2(C)、(D)at GCE(A)and PLA-ERGO/GCE(B)
计算结果为SY在裸电极表面的吸附量为2.4×10-9mol/cm2,在修饰电极表面的吸附量为3.8×10-9mol/cm2。 说明电极修饰后,表面积增大,吸附量增加,灵敏度提高,这和实验结果一致。
2.5 SY的定量分析
用DPV法对SY进行测定,实验结果见图5。仪器最佳参数如下,电位增量:5 mV;脉冲幅度:50 mV;脉冲宽度:60 ms;脉冲间隔:200 ms;静置时间:3 min。定量分析的线性范围、回归方程、相关系数和检出限见表1。
2.6 精密度和稳定性
对1.00×10-5mol/L SY进行20次平行实验,RSD分别为3.2%,将该电极在室温下放置15 d,相同条件下再次测定时,峰电位和峰电流较为稳定,表明该修饰电极具有良好的重现性和稳定性。
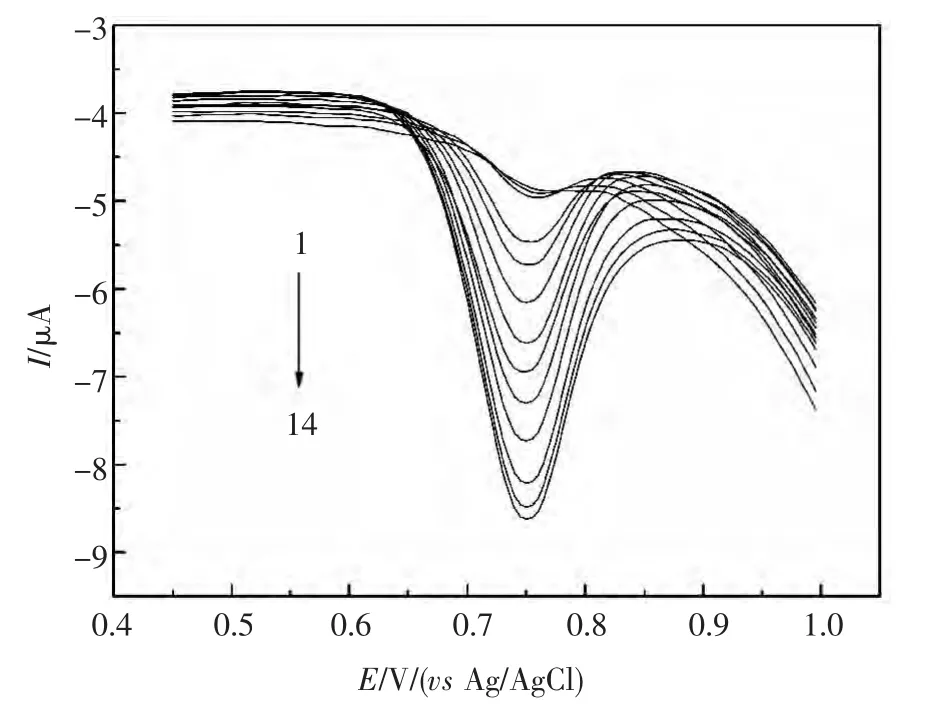
图5 测定SY的DPV曲线Fig.5 DPVs of different concentrations of SY(from 1 to 14:7.50×10-7,1.00×10-6,2.50×10-6,5.00×10-6,7.50×10-6,1.00×10-5,2.50×10-5,5.00×10-5,7.50×10-5,1.00×10-4,2.50×10-4,5.00×10-4,7.50×10-4,1.00×10-3mol/L)

表1 测定SY的线性范围、回归方程、相关系数和检出限Tab.1 Linear range,regression equation,correlation coefficient and detection limit for determination of SY on PLA-ERGO/GCE
2.7 干扰实验
对浓度为1.00×10-5mol/L SY溶液进行测定,允许误差控制在-5%~+5%之间,共存物质的允许量 (mg)为:K+、SO42-、NO3-、Cl-、Na+、Ca2+、Al3+、Mg2+、Zn2+、Fe2+、Co2+、草酸、柠檬酸、葡萄糖、淀粉、L-苏氨酸、L-酪氨酸、L-组氨酸 (≥1.0mg,未做最高限),Cu2+、抗坏血酸、Cr3+(0.2 mg),Fe3+(0.1 mg),胭脂红(0.3 mg)、Pb2+(0.5 mg)不干扰测定。
2.8 样品分析
将市场销售的碳酸饮料样品通氮气除去CO2,移取一定量的样品于10 mL容量瓶中,加入PBS=3.5的缓冲溶液,并加水定容,测定结果如表2所示。

表2 样品中日落黄的分析结果(n=5)Tab.2 Analysis results for determination of SY in sample(n=5)
3 结论
该实验通过简单的方法制备了PLA-ERGO/GCE,并用于研究SY的电化学行为。实验表明,SY在PLA-ERGO/GCE上的电化学过程为吸附控制过程,电极修饰后,吸附量明显增加,从而产生较灵敏的响应信号。检测的灵敏度和精密度提高,且电极稳定性好,便于保存。用于样品中日落黄的测定,结果令人满意。
[1]Zhang Y L,Liu Y P,He J M,et al.Electrochemical be-havior of graphene/Nafion/AzureI/Au nanoparticles composites modified glass carbon electrode and its application as nonenzymatichydrogen peroxide sensor[J].Electrochim Acta,2013,90:550-555.
[2]Rao C N R, Sood A K, Subrahmanyam K S, et al.Graphene:the new two-dimensional nanomaterial[J].Angew.Chem.Int.Ed.,2009,48(42):7752-7777.
[3]Allen M J,Tung V C,Kaner R B.Honeycomb carbon:a review of graphene[J].Chem.Rev.,2010,110(1):132-145.
[4]Wang H,Su H,Qian H,et al.Structure-dependent allopticalswitchingingraphene-nanoribbon-likemolecules:Fully conjugated tri(perylene bisimides)[J].J.Phys.Chem.A,2010,114(34):9130-9135.
[5]Zhang F Y,Wang Z H,Zhang Y Z.Simultaneous electrochemical determination of uric acid,xanthine and hypoxanthine based on poly(l-arginine)/graphene composite film modified electrode[J].Talanta,2012,93:320-325.
[6]王朝霞,陈美凤,马心英.石墨烯修饰玻碳电极用于循环伏安法测定抗坏血酸[J].理化检验-化学分册,2012,48(3):321-327.
[7]Alves S P,Brum D M,Branco de Andrade E C,et al.Determination of synthetic dyes in selected foodstuffs by high performance liquid chromatog-raphy with UV-DAD detection[J].Food Chemistry,2008,107(1):489-496.
[8]陈美凤,马心英.日落黄在聚结晶紫膜修饰电极上的电化学行为及其测定[J].食品工业科技,2014,35(3):279-283.
[9]Fuh M R,Chia K J.Determination of sulphonated azo dyes in food by ion-pair liquid chromatography with photodiode array and electrospray mass spectrometry detection[J].Talanta,2002,56(4):663-671.
[10]刘宇,谢志海,蔡清,等.荧光光谱法测定饮料中的日落黄[J].分析科学学报, 2012, 28(4):535-538.
[11]Ni Y N,Wang Y,Kokot S.Simultaneous Kinetic spectrophotometric analysis of five synthetic food colorants with the aid of chemometrics[J].Talanta,2009,78(2):432-441.
[12]Tian X Q,Cheng C M,Yuan H Y.Simultaneous determination of l-ascorbic acid,dopamine and uric acid with gold nanoparticles-β-cyclodextrin–graphene-modified electrode by square wave voltammetry[J].Talanta,2012,93:79-85.
[13]Guo H L,Wang X F,Qian Q Y.A green approach to the synthesis of graphene nanosheets[J].ACS Nano,2009,3(9):2653-2659.
[14]王毅,于浩,简选,等.直接电化学方法制备石墨烯修饰电极及对肼的检测[J].分析测试学报,2012,31(12):1581-1585.
