基于CdTe量子点荧光猝灭法测定水体中结晶紫
2015-10-18毛永强
毛永强, 李 娜, 毛 晶
(1.辽宁工程技术大学理学院,辽宁阜新 123000;2.辽宁工程技术大学安全科学与工程学院,矿山热动力灾害与防治教育部重点实验室,辽宁阜新 123000;3.天津大学材料科学与工程学院,天津市材料复合与功能化重点实验室,天津 300072)
近年来,量子点(QDs)以吸收光谱宽、发射光谱窄、光稳定性好等优势引起研究者的关注[1,2]。量子点表面轻微的变化会引起其光学性能急剧的变化,因此以量子点为荧光探针建立的荧光检测方法,已广泛应用于金属离子[3,4]、兽药[5,6]、农药[7]等领域的分析检测。
结晶紫(Crystal Violet,CV)是一种人工合成的三苯甲烷类染料,易溶于水,曾作为杀虫剂和杀菌剂在水产养殖业中广泛应用。医学研究表明结晶紫具有潜在的致畸、致癌、致突变等毒副作用[9],欧盟、美国、日本等国家已禁止其在水产品养殖过程中使用,我国也于2005年将其列为禁用药物。但由于结晶紫价格低廉且使用方便,仍存在违规使用,因此对结晶紫的常规监控格外重要。目前,结晶紫含量的检测方法主要为液相色谱法[8,9]、液相色谱-质谱联用法[10,11]等,但这些方法仪器设备昂贵、过程复杂耗时,广泛应用受到极大限制。
本文合成巯基乙酸修饰的CdTe QDs,以CdTe QDs为能量供体、结晶紫为能量受体,构建荧光共振能量转移体系,通过结晶紫对CdTe QDs的荧光猝灭作用,建立新的检测结晶紫含量的新方法。该方法操作简便、灵敏度高,已成功用于水样中结晶紫含量的测定。
1 实验部分
1.1 仪器与试剂
F-4500型荧光分光光度计,UV-3010型紫外-可见分光光度计(日本,日立公司);pHS-3C型pH计(上海雷磁仪器厂);JEM-2100型透射电子显微镜(日本,电子公司);DF-101S型集热式恒温加热磁力搅拌器(山东鄄城华鲁电热仪器有限公司);KQ-50DB型数控超声波清洗器(江苏昆山市超声仪器有限公司)。
碲粉(天津市科密欧化学试剂开发中心);NaBH4(国药集团化学试剂有限公司);巯基乙酸(TGA,天津市光复精细化工研究所);CdCl2·2.5H2O(天津市科密欧化学试剂开发中心);结晶紫(CV,阿拉丁试剂公司),其余所用试剂均为分析纯。实验用水为去离子水。
1.2 CdTe QDs的合成
采用水热法[12]合成CdTe QDs。将4 mmol NaBH4和2 mmol碲粉置于10 mL试管中,加入5 mL去离子水后,冰水浴中反应3 h得到淡紫色的NaHTe前驱体。将10 mmol TGA加入到4 mmol CdCl2溶液中,用1 mol·L-1NaOH溶液调节溶液pH值为11.0,通N2除氧10 min,迅速加入新配制的NaHTe溶液,在N2保护和磁力搅拌条件下,100 ℃加热回流反应2 h后,得到实验所需的巯基乙酸修饰CdTe QDs。向CdTe QDs溶液中加入无水乙醇,离心后收集沉淀,并用去离子水复溶,以除去未反应的离子和小分子后,置于冰箱中4 ℃保存备用。CdTe QDs浓度以溶液中Cd2+浓度计算[13]。
1.3 结晶紫的测定
于5 mL比色管中依次加入1.6 mL 4.0 μmol·L-1CdTe QDs,1.0 mL 50 mmol·L-1Tris-HCl缓冲溶液(pH=7.5)和一定量的结晶紫标准溶液,去离子水定容至刻度并混匀。室温反应5 min,以330 nm为激发波长,激发和发射狭缝宽度均为5 nm,分别测定加入结晶紫溶液前后体系在518 nm处的荧光强度F0和F,计算体系的荧光猝灭强度△F,△F=F0-F。
2 结果与讨论
2.1 CdTe QDs的表征

图1 CdTe QDs的透射电镜(TEM)图
图1为巯基乙酸修饰CdTe QDs的高分辨透射电镜(TEM)图。由图1可知,所合成的CdTe QDs近似球形,在水溶液中单分散性较好,并且粒径分布均匀,平均粒径约为4.2 nm。
2.2 CdTe QDs的光谱表征
图2为巯基乙酸修饰CdTe QDs的紫外-可见吸收光谱(曲线a)和荧光发射光谱(曲线b)。由图2可知,所合成的CdTe QDs紫外吸收峰为425 nm,且具有良好的荧光性能;以330 nm为激发波长,其荧光发射峰位于518 nm。CdTe QDs溶液中加入结晶紫后,考察不同浓度结晶紫溶液对CdTe QDs荧光光谱的影响,如图3所示。由图3可知,加入结晶紫溶液后,CdTe QDs荧光发射峰位置无明显变化,但荧光强度显著降低。实验选择518 nm作为荧光检测波长。

图2 CdTe QDs的紫外-可见吸收光谱(a)和荧光发射光谱(b)

图3 不同浓度结晶紫溶液存在时CdTe QDs的荧光发射光谱的变化
2.3 缓冲溶液pH值的影响
缓冲溶液pH值对体系荧光强度影响较大,考察不同pH值的Tris-HCl缓冲溶液对体系荧光猝灭强度的影响,如图4所示。由图4可知,在酸性或碱性的Tris-HCl缓冲溶液中,对CdTe QDs溶液的荧光强度猝灭较大,体系荧光猝灭强度△F也较小;当Tris-HCl缓冲溶液pH为7.5时,△F达到最大且稳定。因此实验选择Tris-HCl缓冲溶液最佳pH值为7.5。
2.4 量子点浓度的影响
量子点浓度太高或太低,在一定程度上会影响结晶紫测定的线性范围和灵敏度。考察量子点浓度对体系荧光猝灭强度的影响,如图5所示。由图5可知,CdTe QDs溶液中加入结晶紫后,随着量子点浓度的增大,体系△F逐渐增加,线性范围逐渐增大;但当量子点浓度大于4.0 μmol·L-1时,△F反而逐渐降低,灵敏度逐渐降低;当量子点浓度为4.0 μmol·L-1时,△F达到最大。考虑到线性范围和灵敏度,实验选择CdTe QDs的最佳浓度为4.0 μmol·L-1。

图4 pH值对体系荧光猝灭强度△F的影响
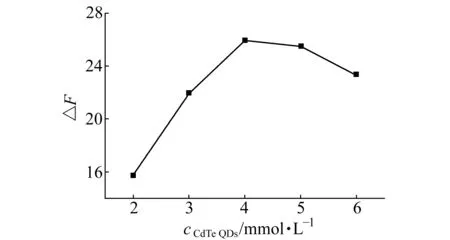
图5 CdTe QDs浓度对体系荧光猝灭强度△F的影响
2.5 反应时间与稳定性
考察了反应时间对体系荧光猝灭强度的影响。结果显示,CdTe QDs溶液中加入结晶紫后,带正电荷的结晶紫和带负电荷的CdTe QDs通过静电吸引而结合,体系荧光猝灭强度△F迅速增大,反应5 min后△F达到稳定,且在25 min内保持不变。因此实验选择反应5 min后测定体系的荧光强度。
2.6 方法的线性方程及检出限
在优化实验条件下,结晶紫浓度在1.0~10.0 μmol·L-1范围内与体系荧光猝灭强度△F呈良好的线性关系,线性方程为:△F=0.78022+5.17149c(μmol·L-1),相关系数r=0.9986,检出限(以3σ计,n=10)为0.026 μmol·L-1。按上述方法重复10次测定5.0 μmol·L-1的结晶紫溶液,相对标准偏差为2.2%,说明该方法具有良好的重现性和精密度。
2.7 干扰实验


表1 共存离子对CdTe量子点荧光强度的影响(n=6)
2.8 实际水样测定
取某养殖户水样,用0.22 μm滤膜过滤,然后加入一定量EDTA掩蔽剂。取适量处理后水样,按实验方法测定水样中结晶紫含量,同时进行加标回收试验,如表2所示。从表2可知,水样中未检出结晶紫(低于检出限),加标回收率为96.2%~103.1%,相对标准偏差(RSD)不高于2.5%,说明本方法可用于水样中结晶紫含量的测定。

表2 水样中结晶紫的测定结果及回收试验(n=6)
ND:not detected.
2.9 机理探讨
共振光散射(Resonance Light Scattering,RLS)技术是一种常用的检测手段,图6为CdTe QDs、结晶紫及CdTe QDs-结晶紫体系的共振光散射光谱。从图6可以看到,在200~700 nm范围内,CdTe QDs(曲线a)和结晶紫(曲线b)的共振光散射强度均很弱;但在CdTe QDs溶液中加入结晶紫,反应体系(曲线c)的共振光散射强度显著增强,且峰形也发生改变。这表明结晶紫和CdTe QDs之间通过静电引力而发生相互作用,形成颗粒较大的聚集体。
图7为结晶紫的紫外-可见吸收光谱(曲线a)和CdTe QDs的荧光发射光谱(曲线b)。从图7可知,结晶紫在580 nm处有最大紫外吸收峰,CdTe QDs在518 nm处有最大荧光发射峰,在475~600 nm范围内二者的光谱有较好重叠。在实验条件下,结晶紫带正电荷,而巯基乙酸修饰的CdTe QDs表面带负电荷,二者可能通过静电引力而结合,从而为二者发生荧光共振能量转移(Fluorescence Resonance Energy Transfer,FRET)提供条件[14]。

图6 CdTe QDs(a)、结晶紫(b)及CdTe QDs-结晶紫(c)体系的共振光散射光谱

图7 结晶紫的紫外-可见吸收光谱(a)和CdTe QDs的荧光发射光谱(b)
由于结晶紫是一种非荧光染料,只能通过CdTe QDs荧光强度的变化来考察体系中荧光共振能量转移的发生。从图3可以看出,随着结晶紫浓度的增大,CdTe QDs的荧光强度逐渐降低;由此推断结晶紫吸收CdTe QDs所发射的荧光能量,导致CdTe QDs的荧光强度降低,二者之间发生有效能量转移,可构建以CdTe QDs为供体,结晶紫为受体的荧光共振能量转移体系。通过测定CdTe QDs荧光强度的变化,从而实现结晶紫含量的定量测定。
3 结论
本文采用水热法,以巯基乙酸为稳定剂合成CdTe QDs。基于结晶紫对CdTe量子点的荧光猝灭效应,建立一种测定结晶紫含量的荧光分析新方法,并成功用于水样中结晶紫含量的测定。同时,采用紫外-可见吸收光谱和共振光散射光谱研究结晶紫与CdTe QDs之间的荧光猝灭反应机理,结果表明为结晶紫和CdTe QDs构建荧光共振能量转移体系所致。
