含活性炭纤维敷料类产品的体外细胞毒性研究
2015-10-18尹玉霞侯丽王鸾鸾李海心郑雯雯
尹玉霞,侯丽,王鸾鸾,李海心,郑雯雯
(山东省医疗器械产品质量检验中心;山东省医疗器械生物学评价重点实验室,济南 250101)
1 引 言
体外细胞毒性试验是评价医疗器械生物相容性的一种简便、快速、高敏感性的检测方法。因其试验周期短,结果重复性好、节省动物等优点,被列为医疗器械生物安全性评价中首选试验项目,是评价材料毒性的重要指标[1]。其中浸提液法是目前应用最广泛的一种细胞毒性筛查法[2]。活性炭纤维是由有机纤维先驱体制得的一种理想的高效吸附材料。活性炭纤维以其特殊的表面化学结构和物理吸附特性广泛应用于环境保护、电子工业、化工、医疗卫生等各个领域。目前活性炭纤维在医疗卫生领域的应用主要有制作血液过滤器、人工肝脏及辅助装置、人工肾脏、活性炭口罩、防毒面具、活性炭敷料等[3]。在日常的体外细胞毒性检测中,含活性炭类产品常常不能得到很好的检验结果。由于体外细胞毒性试验方法制订的目的不是规定一个单一的试验方法,而是规定一个试验方案,需要在一系列试验步骤中判断,以选出最合适的试验方法[4]。为准确客观的评价含活性炭产品的细胞毒性,本实验在遵循医疗器械生物学评价相关标准的基础上,以活性炭敷料类产品为检测对象,设计不同的浸提液制备方法,通过MTT比色法,寻找适合含活性炭产品的浸提方法。
2 材料与方法
2.1 细胞系
小鼠成纤维细胞L929购自上海中科院细胞库。原种细胞解冻后,在试验之前传代2~3次。细胞消化后在96孔板上接种100 μL密度为1×105个细胞/mL的细胞悬液(=1×104个细胞/孔),维持培养24 h(~1倍周期),至形成半融合单层用于试验。
2.2 试剂和器具
MTT(Sigma),溶于不含酚红的MEM中,浓度为1 mg/mL,溶液采用过滤器(孔径≤0.22 μm)经无菌过滤法除菌,过滤后当天使用;MEM培养基(Gibco);胰蛋白酶(Gibco);新生牛血清(NBCS,四季青)。
倒置显微镜(Olympus TH4-200),全自动酶标仪(Thermo Multiskan MK3)。
2.3 试验样品及处理
样品一:含活性炭的闭合用伤口敷料,来自科云生医科技股份有限公司。
样品二:含活性炭的阴道填塞敷料,来自山东朱氏堂医疗器械有限公司。
对照样品:不含活性炭的伤口敷料,来自科云生医科技股份有限公司。
阴性对照:高密度聚乙烯,购自日本Hatano Research Institute。
阳性对照:含有二乙基二硫代氨基甲酸锌的聚氨酯膜(SPU-ZDEC),购自日本Hatano Research Institute。
2.4 浸提液制备
根据GB/T16886.12-2005,医疗器械生物学评价 第12部分:样品制备与参照样品[5]制备浸提液。试验样品按照除吸收容量外,0.1 g/mL的比例,在37±1 ℃的条件下浸提24±2 h制备浸提液,浸提介质分别为含或不含10%NBCS的MEM培养基。阴性对照和阳性对照分别选取含或不含10%NBCS的MEM培养基为浸提介质,按照0.1 g/mL的比例,在37±1 ℃的条件下浸提24±2 h,制备浸提液。
2.5 试验分组
试验组分为2组: A组用含10%NBCS的MEM培养基作浸提介质;B组用不含NBCS的MEM培养基作浸提介质,浸提结束后,加入NBCS至终浓度10%。另外,分别设相应的空白对照组、阴性对照组和阳性对照组,各组设6平行孔。
2.6 试验方法及评价指标
按照GB/T14233.2 MTT法进行检测并评价。为反映浸提液对细胞毒性作用的趋势,选择浸提液与细胞接触时间分别为24、48、72 h。
3 结果
3.1 显微镜观察法:
加样后24、48、72 h镜下观察孔内细胞,可见空白对照组和阴性对照组细胞贴壁良好,无空泡,无细胞溶解,细胞形态呈长条梭形或不规则多边形,胞浆内有离散颗粒,无细胞增殖下降。阳性对照组细胞多数固缩呈圆形,无折光性,数量基本没有增加。显微镜观察法显示阴性对照组细胞毒性反应不大于1级,阳性对照组细胞毒性反应为4级,达到了有效测试的标准。各试验组细胞状态有不同程度的损伤及生长抑制现象。
3.2 MTT比色法
由表1可以看出,细胞毒性反应阴道填塞(2级)>含炭伤口敷料(2级)>对照样品(1级),随着接触时间的延长,含活性炭的两种样品的毒性反应随之增大,而对照样品的毒性反应未发现明显变化。用含10%NBCS的MEM培养基作浸提介质(A组)的含活性炭样品,在各时间段均出现最严重的毒性反应。用不含NBCS的MEM培养基作浸提介质,浸提结束后,加入NBCS至终浓度10%(B组)后,细胞毒性有所减弱。
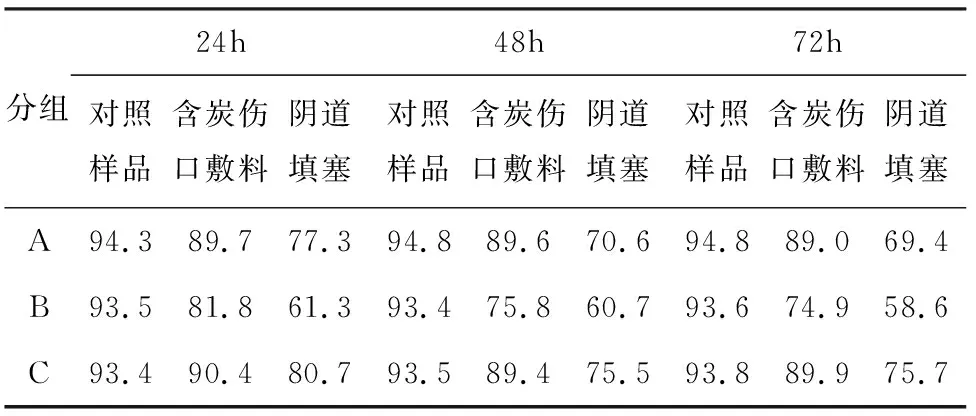
表1 加样后不同周期各组相对存活率(RGR)
4 讨论
目前,活性炭类产品广泛应用于医疗卫生领域,根据其与人体的接触类型和时间,涵盖了一类、二类、三类医疗器械产品。按照生物学评价标准的要求,这些医疗器械产品无一例外都需要做细胞毒性试验。针对细胞毒性浸提介质的选择,国内外相关标准[4,6]推荐的有含血清的培养基、无血清培养基和生理盐水等。出于对活性炭高吸附性的考虑,本实验设计不同的浸提液制备方法,通过显微镜观察法和MTT比色法,寻找适合含活性炭产品的浸提方法。
血清中含有多种细胞生长必需的营养因子,能够有效促进细胞的正常生长繁殖[7]。此外,含血清培养基具有浸提极性和非极性两种物质的能力并近似的模拟体内环境,能够更好地反映医疗器械的生物安全风险[8]。因此,对大部分医疗器械产品,我们均采用含血清培养基做浸提介质以保证细胞稳步生长。但是,在用含血清培养基对活性炭类产品进行浸提时,我们发现,活性炭类产品能够吸附血清蛋白等其他未知营养成分,吸附能力随炭膜的厚度增加而增大。用含血清培养基做浸提介质的浸提液培养细胞,降低了细胞生长的营养物质,造成毒性增加,易出现假阳性结果,我们的结果验证了这一点。与不含活性炭的对照样品比,同一公司产的含活性炭伤口敷料细胞毒性相对较大,而炭膜更厚的阴道填塞毒性更大;在存活率上,含血清培养基做浸提介质组甚至和无血清培养基浸提组接近。因此,我们设计了在无血清培养基浸提的基础上后加入10%血清,在很大程度上缓解了毒性。虽然细胞毒性结果仍为2级,但是达到了对医疗器械细胞毒性评价的标准。
本研究对比分析了浸提介质的选择对含活性炭敷料类产品的体外细胞毒性的影响,并初步分析了原因,认为在实际检验过程中,不能千篇一律套用标准的方法,所用浸提介质和浸提条件应与最终产品的属性和试验目的相适应。因此,在无血清培养基浸提的基础上,后加入10%血清更为合理的评价含活性炭类产品的细胞毒性。
