葡萄糖氧化酶在纳米金/壳聚糖/离子液体BMIMPF6修饰电极上的直接电化学及其应用
2015-10-16蔡志芳刘计敏郑崇涛高永平郭满栋
蔡志芳, 刘计敏, 郑崇涛, 高永平, 郭满栋
(山西师范大学化学与材料科学学院,山西临汾 041004)
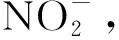
本文采用简便、快捷的滴涂方法,将葡萄糖氧化酶(GOD)滴涂在钠米金(Nano -Au)、壳聚糖(CS)、离子液体1-丁基-3-甲基咪唑六氟磷酸盐(BMIMPF6)复合膜修饰的金电极表面,制备了一种新型葡萄糖生物传感器。研究了该传感器的制作方法、最佳实验条件及电极表面的电子转移机理。该传感器具有制作简单,灵敏度高,稳定性好的特点。
1 实验部分
1.1 主要仪器与试剂
LK2005A型电化学工作站(天津兰力科电子高科技有限公司),三电极体系:裸金电极及修饰电极为工作电极,Ag/AgCl(饱和KCl)电极为参比电极,铂丝电极为辅助电极。JB-2定时双向磁力加热搅拌器(江苏金坛市金城国胜实验仪器厂);雷磁PXSJ-216型离子计(上海精科);KQ-250B型超声波清洗器(昆仑市超声波仪器制造厂)。
1%柠檬酸钠储备溶液:称取1.0101 g柠檬酸钠,溶解并定容至100 mL棕色容量瓶中,4 ℃下避光保存。K3[Fe(CN)6]、K4[Fe(CN)6]、KNO3(0.4 mol·L-1)储备溶液:分别称取0.0827 g K3[Fe(CN)6]、0.1061 g K4[Fe(CN)6]、10.21 g KNO3,溶解并定容至250 mL容量瓶中,4 ℃下避光保存。壳聚糖(CS)储备溶液:将0.004 g CS溶于0.2 mL冰乙酸,稀释至1 mL,在超声波清洗器中超声至完全溶解。葡萄糖氧化酶(GOD)储备溶液:称取0.05 mg GOD(美国Sigma),用二次蒸馏水稀释,并定容至10 mL容量瓶中,4 ℃下避光保存。H2SO4:0.5 mol·L-1。离子液体1-丁基-3甲基咪唑六氟磷酸盐(BMIMPF6),D -葡萄糖,Na2HPO4,NaH2PO4。所用试剂均为分析纯,实验用水为二次蒸馏水。
1.2 实验过程
1.2.1纳米金溶胶的制备按照文献报道方法[13],称取0.01607 g HAuCl4溶于50 mL水中,并在磁力搅拌器上搅拌加热至沸腾后,加入1.5 mL 1%的柠檬酸钠溶液,继续在沸腾情况下搅拌15~30 min,待溶液由蓝色变为酒红色时即形成纳米金溶胶。移去热源后继续搅拌10 min,在室温下冷却后,将制备好的纳米金溶胶置于棕色试剂瓶中,于冰箱中4 ℃保存待用。
1.2.2金电极的预处理将金电极用Al2O3粉抛光,分别在二次水、无水乙醇、丙酮、硝酸(1+1)、二次水中各超声5 min,并重复3次,然后将电极置于0.5 mol·L-1的H2SO4中用循环伏安法(电位区间:-0.4~1.5 V,扫速:0.1 V·s-1)活化处理,除去清洗过程中电极表面残留的微量杂质,最后将其用氮气吹干,待用。
1.2.3化学修饰电极的制备Nano -Au/CS/BMIMPF6/Au电极的制备:用微型进样器移取10 μL BMIMPF6于上述CS储备液中,在超声波清洗器中超声至完全溶解,然后用移液枪移取一定量(200 μL)新配制的Nano -Au溶胶于CS与离子液体BMIMPF6的混合溶液中,再次超声混匀,最后用微型进样器取5 μL该混合溶液滴涂在预处理好的金电极表面,于室温下晾干。
GOD/Nano -Au/CS/BMIMPF6/Au电极的制备:在温度4 ℃下,将制备好的Nano -Au/CS/BMIMPF6/Au电极浸泡在5.0 mg·mL-1GOD中,浸泡4 h,或者将GOD氧化酶滴涂到Nano -Au/CS/BMIMPF6/Au电极表面,即制得GOD/Nano -Au/CS/BMIMPF6/Au电极(12 h后使用)。
1.2.4实验方法采用三电极体系,在磷酸盐缓冲溶液(PBS)中进行了电化学测定。
2 结果与讨论
2.1 修饰电极的表征
2.1.1扫描电镜表征图1是用滴涂法修饰的各种修饰电极表面的扫描电镜(SEM)图。从图1(A)中可以看出, CS呈网状结构。从图1(B)中可以看出,Nano -Au、BMIMPF6在CS上分散均匀、质地紧密。从图1(C)中可以看出,GOD与Nano -Au、BMIMPF6、CS牢固的结合,说明GOD能够很好地固载在修饰电极表面。

图1 CS(A),Nano -Au/CS/BMIMPF6(B),GOD -Nano -Au/CS/BMIMPF6(C)的扫描电镜(SEM)图Fig.1 SEM images of CS(A),Nano -Au/CS/BMIMPF6(B) and GOD -Nano -Au/CS/BMIMPF6(C)
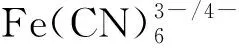
2.2 GOD -Nano -Au/CS/BMIMPF6/Au电极的电化学行为
图3是GOD -Nano -Au/BMIMPF6/CS/Au修饰电极分别在浓度为1.0×10-4mol·L-1葡萄糖溶液(曲线a)和空白溶液(曲线b)中的循环伏安图。从图中可以看出在加入葡萄糖溶液后出现了一对较灵敏的氧化还原峰,说明建立了保持生物活性的微环境,使制备的生物传感器有较高的灵敏度。在曲线b中还原峰Ⅰ和氧化峰Ⅱ的峰电位和峰电流分别为:EpⅠ=-0.0087 V(ipⅠ=47.6215 μA),EpⅡ=0.4789 V(ipⅡ=11.2051 μA),其△E=EpⅡ-EpⅠ=0.4702 V,ipⅠ/ipⅡ=4.25≠1,由此可知,葡萄糖在GOD -Nano -Au/BMIMPF6/CS/Au电极上的电极反应过程是不可逆过程。
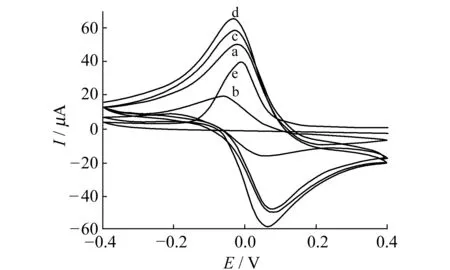
图2 不同电极在溶液中的循环伏安图Fig.2 Cyclic voltammograms of different electrodes in solution(a)Bare gold electrode;(b)CS/Au;(c) BMIMPF6/CS/Au;(d)Nano -Au/BMIMPF6/CS/Au;(e)GOD/Nano Au/CS/BMIMPF6/Au.scan rate:0.1 V·s-1.
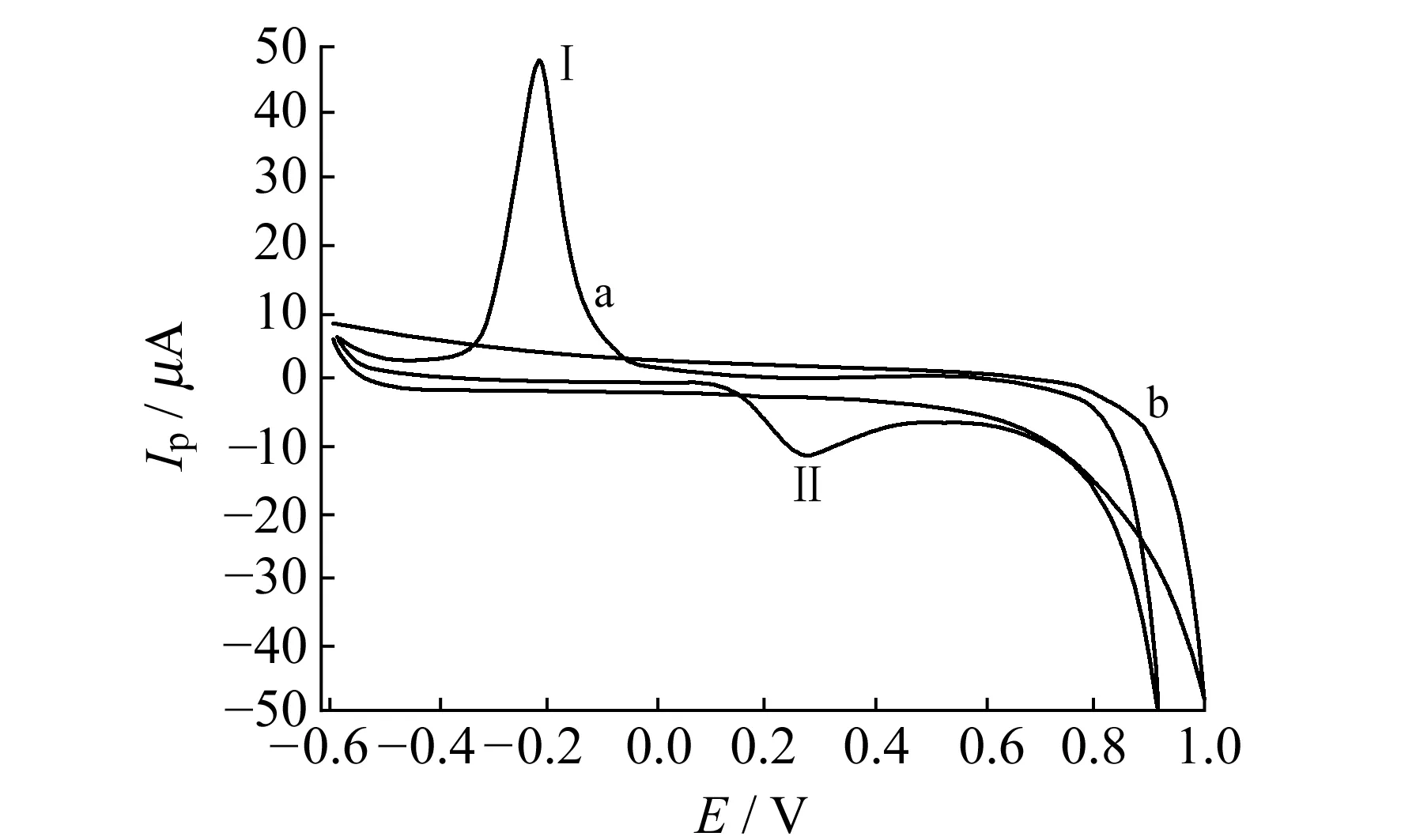
图3 GOD -Nano -Au/CS/BMIMPF6/Au在葡萄糖(a)与空白溶液(b)中的循环伏安图Fig.3 Cyclic voltammograms of GOD -Nano -Au/CS/BMIMPF6/Au in glucose(a)and blank solution(b)scan rate:0.1 V·s-1.
2.3 实验条件的优化
2.3.1底液及其pH值的选择用循环伏安法分别考察了GOD -Nano -Au/BMIMPF6/CS/Au电极在PBS(pH=7.1)、KH2PO4-Na2B4O7(pH=7.4)、Na2B4O7-HCl(pH=8.8)、Na2B4O7-NaOH(pH=10.2)等支持电解质中的电化学行为。采用三电极体系,在-0.4~1.5 V的电位范围内,以0.1 V·s-1的扫描速率进行循环伏安扫描。研究表明,在PBS中的循环伏安图峰形良好,峰电流高、背景电流低,所以最终选择PBS为底液。
用循环伏安法测定修饰电极置于不同pH值的PBS底液中峰电流的变化情况。结果表明,pH值不同时对应的峰电流的大小明显不同。当pH≤7.1时,峰电流随着pH值的增加而增加;当pH>7.1随着pH值的增加,峰电流反而减小。在pH值为7.1的PBS中,GOD -Nano -Au/BMIMPF6/CS/Au修饰电极对葡萄糖的响应最好,其氧化还原峰的峰形最好,且相应的峰电流也是最高的。所以本实验选用pH值为7.1的PBS为底液。
2.3.2离子液体浓度及富集时间的选择在Nano -Au和CS的混合液中,分别加入不同量的BMIMPF6(1、2、3、4、5、6、7、8、9、10 μL),结果表明加入10 μL时,Nano -Au、CS和BMIMPF6三者能够互溶,且峰电流最高。在选定的实验条件下,改变富集时间(0~350 s),结果表明随着富集时间的增加,峰电流几乎呈直线增加。当富集时间达到180 s时,峰电流增加缓慢,说明电极表面的吸附趋于饱和,故选择富集时间为180 s。

图4 GOD -Nano -Au/BMIMPF6/CS/Au电极在不同扫速下的循环伏安图Fig.4 Cyclic voltammograms of GOD -Nano -Au/CS/BMIMPF6/Au at different scan ratescan rate(a→k):0.05,0.07,0.09,0.11,0.13,0.15,0.17,0.19,0.21,0.23,0.25 V·s-1.
2.3.3扫描速率的影响图4是GOD/Nano-Au/CS/BMIMPF6/Au修饰电极在不同扫速下的循环伏安图,随着扫速的增加,阳极峰电位正移,阴极峰电位负移,氧化还原峰电位差△Ep也逐渐增大。在0.05~0.25 V·s-1扫速范围内,扫速平方根(v1/2)与峰电流呈线性关系,说明葡萄糖在GOD -Nano -Au/BMIMPF6/CS/Au电极上是受扩散控制的反应过程,从而可得出此反应是一个不可逆反应,其回归方程为:ipc=198.55v1/2-19.764(ipc:μA;v:V·s-1),r=0.9976。扫速在0.05~0.25 V·s-1范围,还原峰电流与扫速的对数呈良好线性。Epc-lgv的线性方程为:Epc=-0.0602lgv+0.0381,r=0.9687。通过做塔菲尔曲线可知:峰电位与还原峰电流的对数值的线性方程为:E(V)=-0.1817lgIp(A)-0.0878,r=0.9990。
由上可得α=0.1817,代入Epc-lgv方程的斜率(0.5×2.303RT×(anF)-1)可得n≈2。由此可知,葡萄糖在GOD -Nano -Au/BMIMPF6/CS/Au修饰电极上发生了两个电子交换的氧化还原反应。
2.4 线性范围和检出限
用线性溶出伏安扫描法研究了GOD -Nano -Au/CS/BMIMPF6/Au电极在不同浓度葡萄糖溶液中的线性关系。结果表明,该传感器对葡萄糖浓度在1.0×10-4~1.0×10-6mol·L-1范围内有良好的线性关系,其线性方程为:y=0.0871x+37.889(r=0.9995)。在选定实验条件下,检出限为3.85×10-8mol·L-1,说明该方法灵敏度较高。
2.5 稳定性和重现性
同时制备5支GOD -Nano -Au/BMIMPF6/CS/Au电极,分别对1.0×10-5mol·L-1葡萄糖溶液进行测定,测定3次,相对标准偏差(RSD)为4.51%。用同一电极对1.0×10-5mol·L-1葡萄糖溶液进行平行测定10次,RSD为3.26%,说明GOD -Nano -Au/BMIMPF6/CS/Au电极的重现性较好。
将制备好的GOD -Nano -Au/BMIMPF6/CS/Au电极储存在4 ℃下,放置两周后进行测定,其响应性能基本保持不变,一个月后,电极响应性能是原始的88.3%,说明GOD -Nano -Au/BMIMPF6/CS/Au电极的稳定性较好。
2.6 干扰试验及回收率
最佳实验条件下,在浓度为1.0×10-5mol·L-1的葡萄糖溶液中,分别加入10倍的尿酸(UA)、抗坏血酸(AA),200倍的Ca2+、Mg2+、K+、Zn2+时,测定其对葡萄糖生物传感器响应信号的干扰。结果表明,这些物质均无明显干扰。说明GOD -Nano -Au/BMIMPF6/CS/Au电极对葡萄糖有很好的选择性。
选取pH=7.1的PBS为测试底液,分别向底液中加入3个浓度的葡萄糖溶液,用制备好的葡萄糖传感器测定其响应电流变化值。结果表明,葡萄糖传感器有较好回收率,见表1。

表1 测试结果及方法的回收率
3 结论
本实验采用金电极为基体电极,在金电极表面滴涂由Nano -Au、CS和 BMIMPF6制备的复合材料,然后再将GOD修饰到Nano -Au/BMIMPF6/CS/Au电极表面,制得了一种新的葡萄糖生物传感器。由于几种修饰物的共同作用,使得制得的传感器具有响应速度快、灵敏度高、稳定性好的优点。
