电镀光亮镍-钛合金工艺的研究
2015-09-26左正忠李玉梁宋文超
胡 哲,左正忠,杨 娟,李玉梁,宋文超
(1.武汉吉和昌化工科技有限公司,湖北武汉 430023;2.武汉大学化学与分子科学学院,湖北武汉 430072)
引 言
在通常的装饰性电镀生产中,多用镀铬层作为表面镀层,这是因为铬镀层具有光亮、洁白的外观,硬度高、耐磨性强、耐腐蚀和耐高温的特点。但是,由于镀铬工艺采用毒性较大的六价铬盐,对环境、水源、大气及人体带来很大的危害,故研究开发新的、与环境友好的代铬镀层,具有很大的应用前景和经济效益。镍-钛合金电镀工艺即为代铬电镀的技术之一。迄今为止,仅有张允诚等[1]极其简略地提及有电镀Cd-Ti合金(在氰化物溶液中)外,尚未见有关在水溶液中电镀钛及钛合金的工艺技术的专利及文献报道。
钛是一种耐热性很好的银白色金属,密度为4.54g/cm3,熔点高达1668℃。在常温下对强酸强碱有优异的耐蚀性,甚至王水都不能腐蚀它。它具有质量轻、强度高、抗氧化性强及耐低温的特点,被誉为“太空金属”。
镍也是一种银白色金属,密度为8.9g/cm3,熔点1455℃,是一种较贵重的金属,具有较好的抗氧化能力。目前是较紧俏的战略物质之一。
本文介绍的电镀光亮镍-钛合金工艺,可节约用镍、替代有毒性有污染的六价铬电镀。研究表明,10% ~30%钛的镍-钛合金镀层,比相同厚度的镍镀层和“镍+铬”层耐磨性能相当、抗蚀性提高40% ~60%,其韧性增长一倍以上。因此,电镀10% ~30%钛的镍-钛合金层在工业、军事、国防、航空航天及潜艇船舶领域有极重要的作用。
1 实验
实验Ni-Ti合金镀液中包括镍盐、钛盐、硼酸、配位剂、辅助配位剂、光亮剂及辅助剂。
1.1 实验药品
硼酸、柠檬酸三钠、胺辅助配位剂(JC-An)、硫酸镍和氯化镍(均为CP级试剂),钛盐溶液(自制),光亮剂及辅助剂(武汉吉和昌化工科技有限公司)。
1.2 实验仪器
267mL Hull Cell槽(台湾骏光公司),HH-W型恒温水槽,DS-1型数显温度计,AR2140型电子天平,1.0~5.0L塑料小型镀槽。8511B型恒电位仪(吉林延边永恒电化学仪器厂),XY-3086型X-Y函数记录仪(重庆仪表四厂)。JSM6510LV型扫描电子显微镜(SEM)(日本),D8A25型X-射线衍射仪(XRD)(德国)。
1.3 Ni-Ti合金溶液组成及操作条件
Ni-Ti合金镀液组成为:50g/L NiSO4·6H2O,10g/L NiCl2·6H2O,50 ~125mL/L Ti盐液,40g/L H3BO3,50g/L Na3C6H5O7·2H2O,10g/L JC-An,4mL/L光亮剂,10mL/L辅助剂。pH 为3.5~5.0,θ 为40 ~60℃,Jκ为1.0 ~5.0A/dm2,阳极为镍板、不锈钢板或钌-钛合金板。
1.4 实验方法
1.4.1 赫尔槽试验
实验是在267mL的赫尔槽中进行,赫尔槽置于恒温水槽中。I=1A,t=10min。
1.4.2 电化学性能测试
采用三电极体系,在50mL容积的H型电解池中进行,分别测试阴极极化和循环伏安曲线。工作电极均为 d1.0mm×5mm的 Pt丝,辅助电极为5.0mm×10.0mm的Pt片,参比电极为饱和甘汞电极。测试液均为去离子水配制。扫描速度为100mV/s,扫描范围为 +0.4 ~ -1.0V(vs SCE)。
1.4.3 Ni-Ti合金镀层测试
采用JSM6510LV型扫描电子显微镜和D8A25型X-射线衍射仪,对Ni-Ti合金镀层进行了形貌和衍射测试。
1.4.4 镀液性能的测试
1)阴极电流效率的测试
采用称量法。在2.0L工艺槽中电镀Ni-Ti合金,不锈钢为阳极,称出电镀Ni-Ti合金层的质量,记录总电流I和时间t;再分别分析出合金中Ni、Ti的质量分数,根据合金沉积时阴极电流效率的公式[2-3]计算阴极电流效率:
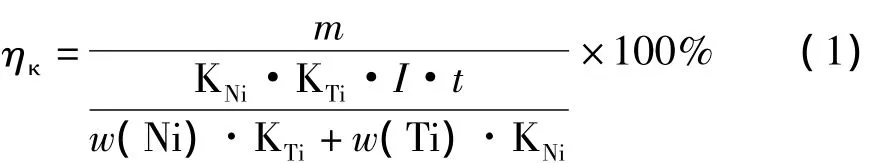
式中:m为实际得到的合金质量,g;KNi为Ni的电化当量,g/Ah;KTi为Ti的电化当量,g/Ah;w(Ni)为合金层中Ni的质量分数,%;w(Ti)为合金层中Ti的质量分数,%;I为通过的总电流,A;t为电镀总时间,h。
2)Ni-Ti合金镀液深镀能力的测定
深度能力测定在 1.0L烧杯中进行。将10mm×100mm的铜片,插入 d10mm×100mm的塑料管内,与双不锈钢阳极平行悬挂,电镀 t=10min,Jκ=5A/dm2,θ=48.8℃。测量 Ni-Ti合金镀层的总长度(mm)除以试片的长度(100mm),乘以百分数,即为镀液的深镀能力。
3)合金镀层的腐蚀质量损失测定
腐蚀质量损失测定在3000mL的容器中悬挂试片进行,5%的NaCl溶液,pH=6,液温与2013年4月中旬~5月中旬武汉的环境气温一致。试片分别为3个镀Ni片和3个镀Ni-Ti合金片,用以对比。基体均为 3.2cm ×5.0cm ×0.1cm 的铁板,Ni、Ni-Ti合金镀层的δ均为0.03mm.试片进出溶液前、后,须经擦拭、水洗、乙醇脱水、吹干,然后称量。
进行对比的镀 Ni溶液的组成是:300g/L NiSO4·6H2O,50g/L NiCl2·6H2O,45g/L H3BO3,8mL/L光亮剂。
1.4.5 Ni-Ti合金镀层中 Ti的分析
将在不锈钢上沉积的Ni-Ti合金镀层用小刀剥下→称量→用王水溶解→加水稀释→加入络合剂(配位剂)→补水定容→吸取一定量待分析液至锥型瓶内→加入指示剂→用标准液滴定→记下耗用滴定液→计算出Ni-Ti合金中钛的含量(具体的分析方法、计算公式将有专文发表)。
2 结果与讨论
2.1 Ni-Ti合金镀液中各成分的作用
由于Ti/Ti2+电化学氧化/还原电极电势太负的缘故,为 -1.63V[4-5],水溶液中不可能在电极上电沉积出来。然而,借助一些配位剂及某些金属物,就有可能以合金的形式沉积出来。本文介绍的镀液能够电镀出Ni-Ti合金镀层。
首先,溶液中的 NiSO4·6H2O、NiCl2·6H2O、Ti盐液是主盐,为电沉积Ni-Ti合金提供Ni、Ti离子,而Na3C6H5O7为主配位剂,Jc-An为辅助配位剂含有结构式为:
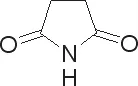
H3BO3、光亮剂和辅助剂,分别在电镀过程中起缓冲溶液的pH和使合金镀层均匀、柔和和光亮的作用。
赫尔槽试验以及1.0~5.0L小槽电镀表明,在pH 为 3.0 ~5.5、θ为 40 ~60℃、Jκ为 1.0 ~5.0A/dm2的范围内,均可得到光亮、均匀、韧性好的Ni-Ti合金镀层。Jκ为 1.0 ~3.0A/dm2内,镀层中Ti的质量分数为10% ~40%。
溶液的pH、温度和阴极电流密度对合金镀层的外观影响不明显;均可获得似镀Cr层色泽外观。对沉积速度即阴极电流效率有影响,pH、温度和阴极电流密度升高,阴极电流效率上升;反之,则相反。
阴极电流密度对Ni-Ti合金层中Ti的质量分数影响很大,如表1。
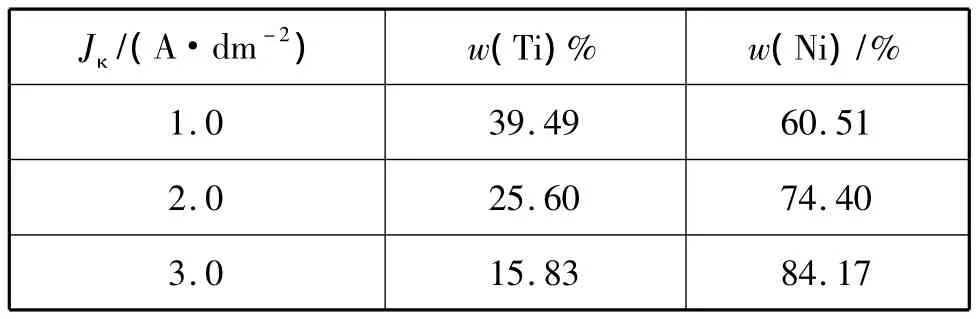
表1 电流密度对Ni-Ti合金镀层中Ti的影响
溶液中配位剂的质量浓度影响着溶液的性能,含量太高,阴极极化亦大,电流效率降低。这是因为伴随着极化的增大,析氢亦增大的缘故。此外,质量浓度过高,也会使Ni-Ti合金层中Ti太低,因配位剂仅对Ti离子进行配位,配位剂太多,Ti配位体在阴极上放电困难。即镀层中的Ti质量分数与溶液中的钛盐质量浓度成正比关系。
研究的Ni-Ti合金溶液中,还含有乙氧基醇醚和羟甲基磺酸钠的光亮剂,以及羟丙基硫代硫酸钠的辅助剂。光亮剂的作用是使镍-钛合金镀层结晶细致光亮、无针孔、无麻点;辅助剂是改善镀液分散性和均镀能力,并使镀层无脆性、光亮度柔和及结合力好。
2.2 Ni-Ti合金镀液的电化学行为
为测试Ni-Ti合金镀液的阴极极化曲线和循环伏安曲线(CV),配制了下列测试液:
1﹟液:30g/L H3BO3,50g/L Na3C6H5O7·2H2O,8g/L JC-An;2﹟液:1﹟液+100mL/L Ti盐液(2g/L Ti2+);3﹟液:1﹟液 +50g/L NiSO4·6H2O,15g/L NiCl2·6H2O;4﹟液:3﹟液+100mL/L Ti盐液(2g/L Ti2+)。图1为阴极极化曲线。从图1看到,曲线①是1﹟镀液;曲线②为2#镀液,是在1#镀液中加入100mL/L(Ti2+2g/L Ti盐液,其极化曲线降低了很多,电位正移了约800mV,在2﹟液中无Ti电沉积出来,由此说明在1﹟液中,Ti盐液的加入起了导电盐的作用、增大了溶液的导电能力,降低了阴极极化。曲线③是在1﹟液中加入了Ni盐的镀液,用来与加入Ti盐后的行为进行比较,表明加入Ni盐后比1﹟基本液有更大的极化程度。曲线④是Ti盐、Ni盐共存于1﹟液中镀液。曲线④比曲线①、③电位正而比曲线②负。这正是Ni-Ti合金电沉积析出的行为,这种现象属于合金电镀的“诱导共沉积”[6]。
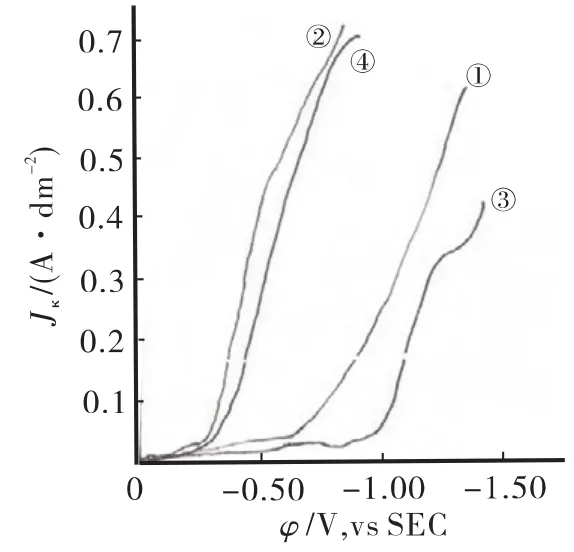
图1 Ni-Ti合金镀液的阴极极化曲线
图2 为比较Ni、Ni-Ti合金的循环伏安曲线图。图2中Ni曲线是1﹟液中的循环伏安曲线图,与Ni-Ti合金的C-V曲线有很大的不同。Ni-Ti合金的C-V 曲线上,正向扫描时,在 -0.35 ~ -0.40V,有一“滞后环”,表明合金刚生成的晶核粒子在-0.35V开始加快长大。这种情况说明,在电镀过程中,虽然需要阴极极化,但极化程度不要太大;否则,当晶粒长大的速度大于晶粒形成的速度时,将会使合金镀层的表面粗糙。反向扫描时,在+0.05~ +0.15V又有一“滞后环”,代表着刚经过氧化的合金表面又开始了新的“结晶极化”,新的晶核又开始生成。这一对共轭的“滞后环”,揭示了Ni-Ti合金电镀过程中,可使阴极持续地保持着清洁的表面,以利晶核的生成、长大。即使说,有利于长时间的电镀而加厚镀层,如同修复工件时的电镀硬铬。在 1000mL的小槽中,1dm2试片上,以2.0A/dm2连续镀 120min,镀层表面光亮,均匀,无起皮、鼓泡及脱皮现象。
从图2看出,反向扫描时,Ni约在-0.90V时开始溶解,-0.15V时,有一最大阳极溶解电流峰;而Ni-Ti合金的起始溶解电势比Ni的“滞后”,约在-0.40V才开始溶解,推迟了500mV;Ni-Ti合金的最大溶解峰电流比Ni的低,展示了其有很好的耐蚀性能。在5%NaCl溶液中腐蚀质量损失的数据中得到了支持。
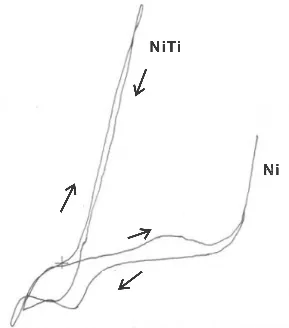
图2 Ni、Ni-Ti合金的循环伏安曲线
2.3 Ni-Ti合金镀层的测试
图3 是镀液中Ti质量浓度不同时沉积的Ni-Ti合金层的X-射线衍射(XRD)谱图。在2θ=43°处,呈现了Ni-Ti峰,证实了在该溶液中镀出的是Ni-Ti合金层;峰形很尖锐,说明其结构属于晶体结构。其次,随着溶液中Ti2+质量浓度的增加,镀层中合金峰的强度亦增强,表明合金层中Ti质量分数增大,与对镀层的分析结果一致。
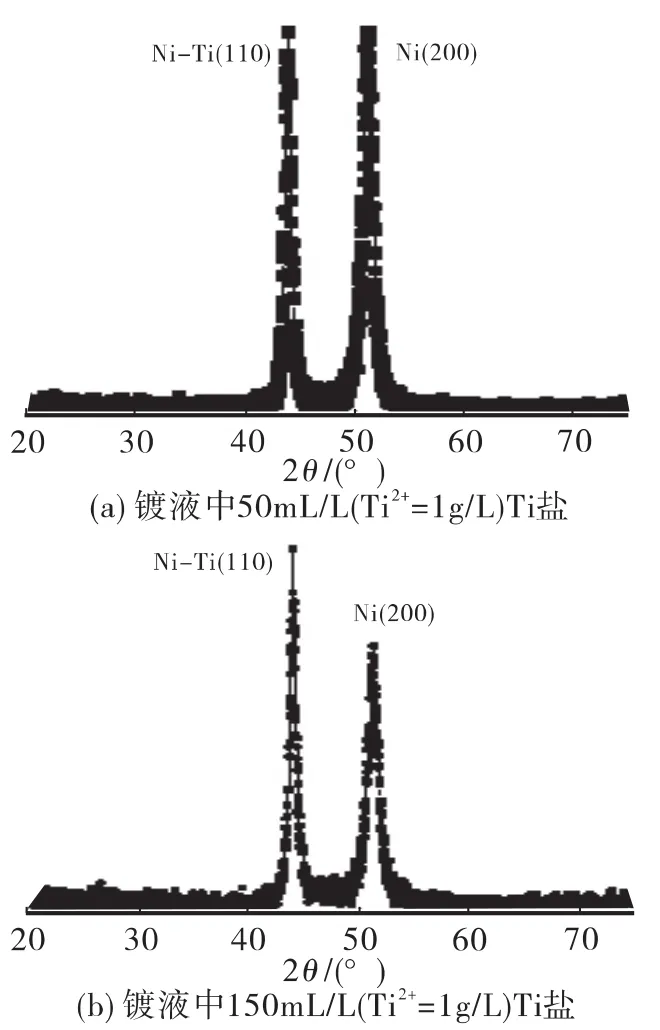
图3 Ni-Ti合金层的XRD谱图
图4 为在本溶液中得到的Ni-Ti合金镀层横断面的扫描电子显微镜(SEM)照片;图4(a)、图4(b)为含24.6%Ti的Ni-Ti合金镀层分别放大2000倍和5000倍SEM照片,显示出合金晶粒呈有序地、层状地排列,且比较均匀。这也提供了Ni-Ti合金镀层比单一的Ni层或Ni+Cr层的耐蚀性能好、可作为代Cr层的缘由。
图4 (a)、图4(b)为镀液中Ti2+质量浓度为1.0 g/L时的Ni-Ti合金镀层的SEM照片,图4(c)是Ti2+质量浓度为3.0g/L时Ni-Ti合金镀层放大200倍的SEM照片。由图4看到,镀液中Ti2+质量浓度加大,镀层的晶粒尺寸增大;这是因为金属离子浓度的提高相当于增加了溶液的导电盐、提高了溶液的导电能力、降低了阴极极化作用的结果。如果电沉积过程在很低的极化(很“正”的阴极电势)下进行,则镀层往往由粗大的晶粒所组成[7]。因此,在电镀光亮Ni-Ti合金溶液中,Ti盐的质量浓度不宜过大,在50~100mL/L即可,工作中宜采用少加勤加的原则。

图4 Ni-Ti合金镀层的SEM照片
2.4 Ni-Ti合金镀液及镀层的性能
表2 是Ti质量分数为22%的Ni-Ti合金镀层在5%NaCl溶液中21d的腐蚀质量损失试验与亮Ni镀层的对比。比较可知,Ni-Ti合金镀层的耐蚀性能比Ni镀层约提高了40%,具有良好的抗蚀性,可作为代Cr镀层。
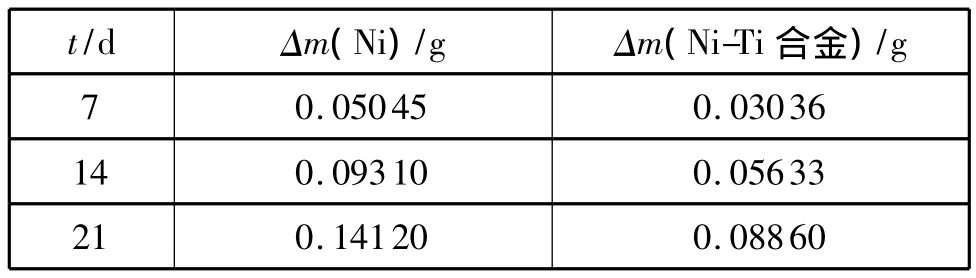
表2 Ni-Ti合金与Ni镀层的腐蚀质量损失对比
对Ni-Ti合金镀液的阴极电流效率进行测定。在 θ=55℃、pH=5.5、Jκ=2A/dm2条件下,电流效率为70.56%。阴极电流效率与θ、pH成正比,与Jκ成反比关系。有利于镀层的整平能力和厚度分布的均匀性。本研究还测定了Ni-Ti合金镀液的深镀能力为40%~45%。
3 结论
提出了可代替镀Ni或镀Ni+Cr的电镀光亮Ni-Ti合金工艺。运用赫尔槽和小槽实验,通过阴极极化曲线、循环伏安曲线测定以及SEM、XRD等方法,研究了Ni-Ti合金镀液及合金镀层的性能。结果显示,研究的镀液,电流效率较高,所得的Ni-Ti合金层Ti的质量分数在10% ~30%,其亮度好、均匀及平整。在5%NaCl溶液中的腐蚀质量损失比Ni镀层降低40%,表明Ni-Ti合金镀层有良好的耐蚀性能。
推荐的电镀光亮Ni-Ti合金溶液组成及操作条件是:50~60g/L NiSO4·6H2O,0~15g/L NiCl2·6H2O,50~125mL/L Ti盐液,35~40g/L H3BO3,50 ~60g/L Na3C6H5O7·2H2O,10 ~15g/L JC-An,2~4mL/L光亮剂,8~10mL/L辅助剂,pH为 3.5 ~5.0,θ为 40 ~60℃,Jκ为1.0 ~5.0A/dm2,阳极为镍板、不锈钢板或钌-钛合金板。
[1]张允诚,胡如南,向荣.电镀手册,[M].第2版.北京:国防工业出版社,1997:540-541.
[2]宋文超,左正忠,胡哲,等.碱性镀液中电镀光亮Zn-Ni合金[J].材料保护,2011,44(10):1-4.
[3]曹浪,左正忠,田志斌,等.焦磷酸盐-柠檬酸盐体系电镀光亮Zn-Ni合金的研究[J].电镀与精饰,2011,33(1):30-33.
[4](苏)B A拉宾诺维奇.尹承烈译.简明化学手册[M].北京:化学工业出版社 ,1983:635.
[5][日]藤嶋昭,相澤益男,井上徹.蔡生民译.电化学测定方法[M].北京:北京大学出版社,1994:442.
[6]屠振密.电镀合金原理与工艺[M].北京:国防工业出版社,1993:56-59。
[7]查全性.电极过程动力学导论[M].第3版.北京:科学出版社,2002:310-311.
