ABS塑料表面镀铜工艺的研究
2015-09-26陈尔跃杨晓超郭祥峰
陈尔跃,杨晓超,徐 娟,郭祥峰
(齐齐哈尔大学化学与化学工程学院,黑龙江齐齐哈尔 161006)
引 言
ABS塑料具有质量轻、绝缘好及化学稳定性高等特点[1],是现代工业不可或缺的材料。通过在ABS塑料表面沉积金属以使ABS塑料同时具备塑料和金属的优良特性,而随着特种镀层开发更使其如虎添翼[2-4]。目前表面金属化的ABS塑料被广泛应用在电子工程、石油化工以及国防工程等领域[5-7]。塑料表面上沉积金属方法主要有化学镀法、真空镀膜法[8]及直接电镀法。近几年来一些研究者尝试使用硅烷偶联剂接枝纳米金属粒子等[9],虽然新的方法不断被发掘,从性能到工艺条件远不如化学镀法成熟。因此本文选择了化学镀法作为ABS塑料表面金属化方法。
本文研究了ABS塑料金属化前处理、化学镀铜及电镀铜的最佳条件,讨论了不同条件对化学镀铜镀速的影响,并优化了化学镀铜镀液的配方。通过扫描电子显微镜、X-射线衍射仪和光电子能谱仪对ABS塑料、化学镀铜和电镀铜层的形貌、晶型、元素组成及价态进行分析。
1 实验方法
1.1 ABS塑料前处理
ABS塑料前处理基本流程为[10]:
去应力→应力检查→除油→化学粗化→敏化→活化→还原→备用。
1)去应力。将ABS塑料置入80℃的水浴中8h左右。
2)应力检查。将处理后的ABS塑料放入冰醋酸中浸泡3min,清洗、晾干,用40倍放大镜观察表面有无明显的裂纹。
3)除油。5g/L NaOH,20g/L无水 Na2CO3,20g/L Na3PO4·12H2O,1g/L OP-10,θ为 60 ~65℃,t为30min,用1%硫酸溶液冲洗。
4)化学粗化。400g/L CrO3,400g/L H2SO4,θ为60~75℃,t为20~30min,稀盐酸溶液浸泡10~20min。
5)敏化。10g/L SnCl2,70mL/L 浓 HCl,室温,t为3~10min。
6)活化。2g/L AgNO3,150mL/L NH3·H2O,室温,t为3~5min。
7)还原。1g/L NaOH,1g/L NaBH4,室温,t为1~2min。
1.2 ABS塑料化学镀铜溶液组成及操作条件
1)A 溶 液。7g/L CuSO4·5H2O,20g/L C4O6H4KNa,5g/L NaOH,0~20g/L无水碳酸钠,1g/L氯化镍;2)B溶液。35%的HCHO溶液。化学镀铜液的配制为V(A液)∶V(B液)=4∶1混合。pH 为11.0 ~12.5、θ为25 ~40℃、反应 t为30min。
1.3 ABS塑料电镀铜溶液组成及操作条件
150g/L CuSO4·5H2O,47g/L H2SO4,0.03g/L NaCl,0.5g/L 2-巯基苯并咪唑,阳极为磷铜电极,室温,Jκ为 0.5 ~1.5A/dm2,磁力搅拌。
1.4 沉积速率
将处理后的ABS塑料基板进行称量,化学镀铜30min后,水洗,干燥,称量。根据下面公式计算出沉积速率。
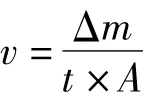
式中:Δm为反应前后镀件质量差,mg;t为反应时间,min;A为镀件面积,m2;v为化学镀铜沉积速率,mg/(min·m2)。
1.5 镀层的形貌、晶型、元素价态检测
为了进一步观察镀层表面的形貌、晶型、元素价态及沉积效果。分别选取最优粗化、化学镀铜和电镀铜条件下的镀件,截取5mm×5mm的小片,用无水乙醇擦拭表面后,通过S-4300扫描电子显微镜(SEM)、D8-FOCUSX-射线衍射仪(XRD)和 ESCALAB 250Xi光电子能谱仪(XPS)分别对表面进行表征。
2 结果讨论
2.1 最佳ABS前处理条件
ABS塑料在生产过程中其表面难免沾有油污,会对粗化的效果和镀层的结合力有很大的影响,因此需要除油。除油是利用碱性物质与油污发生皂化反应以达到除去油污目的,加入表面活性剂可以除去皂化反应无法除去的油污。除油操作时温度不宜过高,θ在60℃,t在30min左右即可,搅拌有利于皂化反应的进行,并对ABS塑料表面有冲刷作用,提高除油效率。
粗化是利用粗化剂强氧化性在ABS塑料表面腐蚀出细小微孔,以达到粘附敏化液和提高镀层与基体表面结合力作用。粗化操作时间不宜过长,时间过长会使ABS塑料表面残留大量铬酸,影响后续操作。通过实验得出,如果粗化θ在70℃时,粗化t不宜超过20min;如果粗化θ在60℃时,粗化t不宜超过30min。粗化后的ABS塑料表面具有磨砂质感,通过肉眼观察光泽度不如未经粗化的 ABS塑料。
2.2 化学镀铜条件选择
2.2.1 pH、温度对沉积速率的影响
化学镀铜是以甲醛为还原剂,由于镀液呈碱性,Cu2+与OH-结合生成沉淀,因此需要加入络合剂与Cu2+形成络合离子,增加铜离子在碱性镀液的稳定性。其反应为[11-12]:
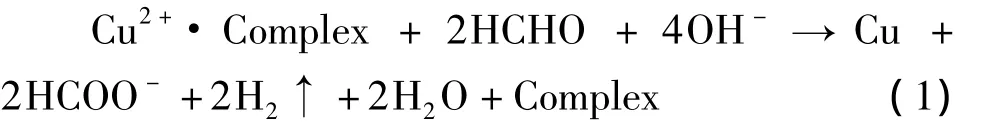
上述反应式中 Cu2+·Complex表示的是络合Cu2+,此反应需要在经过粗化、敏化及活化后的塑料表面才能进行。这是因为ABS塑料经过敏化、活化后表面上有Ag存在,对于上述反应中Ag是一种催化剂,使Cu以其为中心沉积,沉积后的Cu作为催化剂让反应继续进行。根据反应原理,在其他条件稳定的情况下镀液的pH、温度是影响反应速率的关键,因此根据不同pH和温度对化学镀铜沉积速率影响绘制成三维曲面如图1。如图1所示,反应θ在26~36℃时沉积速率随着pH增大而增大;反应θ在36~40℃时沉积速率随着pH增大是先增大后减小。这是因为随着温度、pH的增大反应速率会不断增大,Cu在ABS塑料表面沉积量也会增大,但是当温度和pH达到一定的条件后,镀液会自分解,即直接在镀液内析出Cu颗粒,而不在ABS塑料表面沉积。
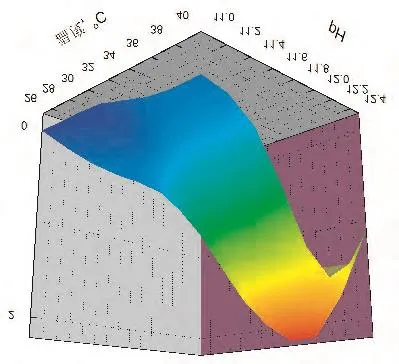
图1 pH、温度对沉积速率的影响
根据实验现象,镀液 pH 在12.0~12.4时,反应θ在30~40℃区域内镀层变焦、发黑;镀液的pH在11.0~11.5,反应θ在20~30℃区域内的镀层上出现漏镀或者不上镀的现象;镀液的pH在11.0~11.5,反应θ在30~35℃,所得镀层光亮、平整,没有出现镀焦或者漏镀现象。因此反应条件的控制pH 为11.0 ~11.5、θ为30~35℃。
2.2.2 无水碳酸钠加入量对沉积速率的影响
当反应温度恒定、镀液中各个组分含量稳定的情况下,pH是影响沉积速率唯一的因素。随着反应的进行HCHO被氧化成HCOOH消耗溶液中OH-,反应液的pH会逐渐降低,反应速率也会随之降低,与此同时沉积速率也随之降低,因此保证反应时反应液pH的稳定是关键。无水Na2CO3是一种很好的pH调节剂,它通过吸收反应过程中甲酸放出的H+形成HCO3-起到调节镀液pH作用,而且不影响镀液稳定性。Na2CO3对沉积速度和pH的影响如图2所示。
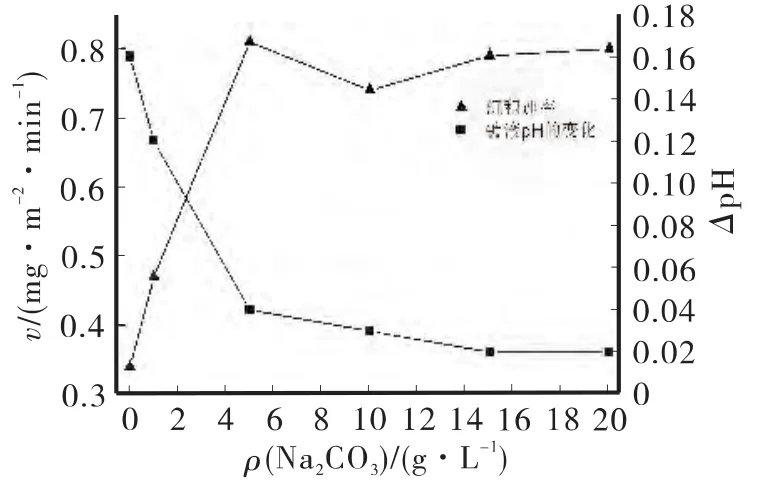
图2 无水Na2CO3对镀速及镀液pH的影响
图2 中左侧纵坐标为沉积速率,右侧纵坐标为反应前镀液pH与反应后镀液pH之差,既反应前后镀液的pH变化量。如图2所示,无水Na2CO3质量浓度在0~6g/L时,镀速随无水Na2CO3的增大而增大。无水 Na2CO3在 6~20g/L,镀速随无水Na2CO3的增大基本保持不变,反应前后镀液pH变化量随无水Na2CO3的增大而减小。因此反应过程中反应液pH的变化对化学镀铜沉积速率影响极大。无水Na2CO3的质量浓度在4~5g/L为最益。
2.2.3 搅拌方式对沉积速率的影响
常见的搅拌方式有多种,本文选择了机械搅拌、以空气和氮气为气源的气动搅拌,以无搅拌为对照组,如图3所示。机械搅拌下的镀件沉积速率明显高于空气搅拌,以及对照组;空气搅拌下镀件的沉积速率远低于参照组;空气搅拌和对照组镀件表面均有漏镀现象,空气搅拌更为严重,氮气搅拌的沉积速率略高于机械搅拌,镀层表面光亮度与机械搅拌基本一致。对于这种现象可能是因为,在反应过程中甲醛放出氢气,在表面张力作用下会附着在镀件表面,继而影响表面与反应液的接触,因此对照组会有漏镀现象;而空气搅拌,则是因为空气中二氧化碳在空气动力作用下增大在反应液中溶解度,使碱性镀液的pH变小降低了反应速率,由于镀液的pH降低铜在表面沉积速率也会相应降低;氮气搅拌首先其对镀层组成和pH没有影响,氮气通入镀液后有助于镀件表面生成气体排除,继而增大反应面积,所以氮气搅拌比机械搅拌的沉积速率略高。在实际操作中利用机械搅拌或氮气搅拌均可。
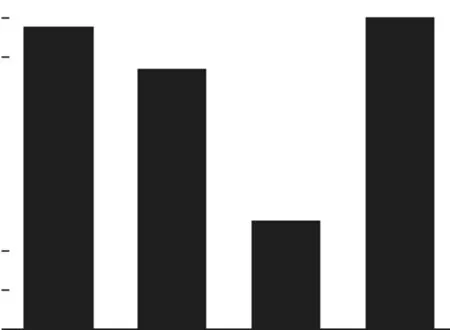
图3 不同搅拌方式对镀速的影响
2.3 电镀铜最佳条件选择
化学镀铜沉积的铜层在耐蚀、硬度等性能上很差,因此需要电镀铜加厚后,再进行后续处理,如装饰镀、特种镀等。加厚镀液采用的是酸性镀铜液,酸性镀铜液的优点在于镀液的组成成分简单,沉积速度快,电流效率高;缺点是电镀时镀件表面的化学镀层容易分解,所以在电镀前首先在阴极通电后放入镀液内。为了防止双极现象采用小电流密度电镀1min即可,需要注意的是小电流密度电镀时间不可太长否则镀层易发生脱落。整个电镀时间不要过长,会对表面的平整度有一定影响,在20~25min为宜。
2.4 表面检测
2.4.1 表面元素分析
采用光电子能谱仪(XPS)对ABS塑料、化学镀铜和电镀铜进行全谱扫描,如图4所示。
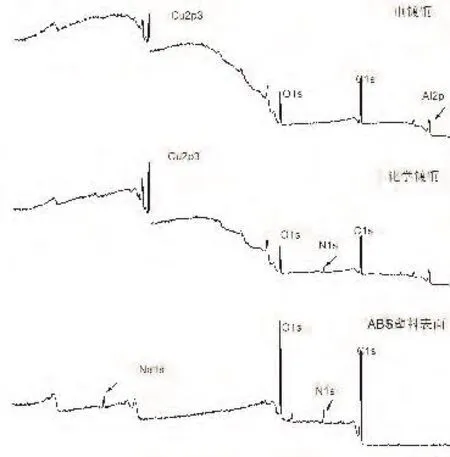
图4 ABS塑料、化学镀铜及电镀铜层XPS分析
由图4可以看出,粗化后的ABS表面主要以C、O、N元素为主,化学镀铜、电镀铜后ABS塑料表面主要以Cu、O元素为主,还需要利用Cu元素高分辨XPS谱图,具体分析Cu元素在表面价态与构成,如图5所示。
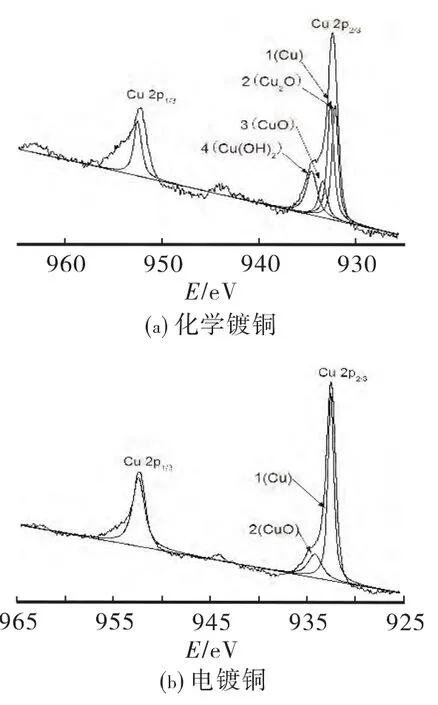
图5 化学镀铜、电镀铜后中Cu2p峰的分解XPS谱图
图5 (a)是化学镀铜表面Cu2p结合能在925~965eV之间的高分辨XPS谱图,从图谱能够确定4个峰,峰1的结合能为932.23eV,对应的是单质铜;峰2 的结合能为 932.698eV,对应的是 Cu2O[13],这是因为在沉积过程中除了主反应发生外还会有如下副反应[14]:
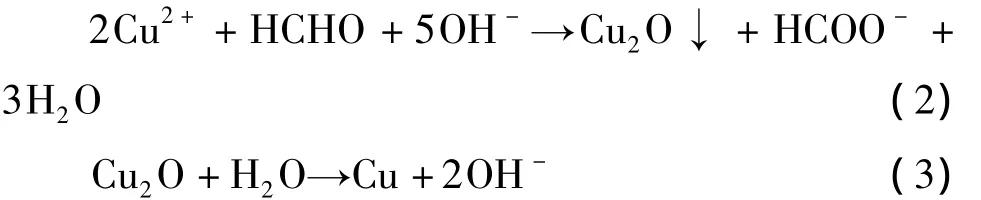
该反应产生的部分Cu2O和Cu在表面共同沉积,因此表面有Cu2O;峰3的结合能为933.492eV,对应的是CuO,由于Cu在空气中被氧化造成的;峰4的结合能为 934.640eV,对应的是Cu(OH)2。Cu(OH)2在表面的出现可能是由于碱性镀液,少量Cu2+与OH-结合沉积在镀层表面缘故;图5(b)是电镀铜表面的Cu2p结合能在925~965eV之间的高分辨XPS谱图,峰1的结合能为932.6eV,对应的是单质铜;峰2的结合能为934.25eV,对应的是CuO,是Cu在空气中被氧化造成的[15]。
2.4.2 X-射线衍射检测
分别对经过粗化、化学镀铜和电镀铜后的ABS塑料表面进行X-射线衍射(XRD)分析,如图6所示。由图 6可以看出,化学镀铜层表面 2θ为43.795°、51.008°和 74.675°系单质铜的特征衍射峰;电镀铜层表面 2θ为 43.427°、50.561°和74.215°系单质铜的特征衍射峰,化学镀层和电镀层均具备单质铜晶体特征,但是电镀铜与化学镀铜峰型相比较,电镀铜层峰型较窄,而化学镀铜则较宽,证明电镀铜形成晶粒比化学镀铜要小。2θ为29.884°、47.940°系 ABS 塑料粗化后表面特征峰,化学镀铜层表面依旧有2θ为29.884°峰的存在,证明化学镀铜并未将ABS塑料表面完全覆盖,而电镀铜没有ABS塑料粗化后表面特征峰出现只有单质铜特征峰,证明通过电镀已经将表面完全包裹上单质铜。
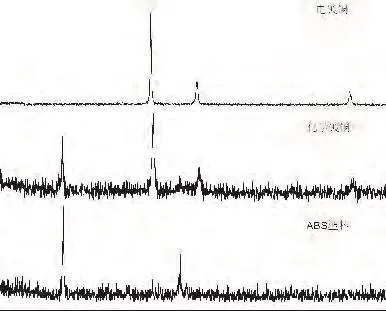
图6 ABS塑料、化学镀铜和电镀铜层XRD谱图
2.4.3 表面形貌分析
图7 为放大1000倍的ABS塑料及粗化后的化学镀铜和电镀铜层扫描电子显微镜(SEM)照片。

图7 ABS塑料、ABS塑料粗化后、化学镀铜和电镀铜层SEM照片
由图7可以看出,粗化后的ABS塑料表面有孔径不均的孔道,这是因为ABS塑料是由苯乙烯(A成分)和丙烯腈(S成分)构成骨架,而丁二烯(B成分)以细微球状分布在骨架上,由于粗化液具有强氧化性将表面的丁二烯腐蚀掉,所以ABS塑料表面布满孔道[16-17]。经过化学镀铜ABS塑料表面大部分孔道被覆盖、填满,仍有较大孔道未被填满或覆盖;电镀铜后表面较为平整、光滑,所有孔道均已填满,且结晶表面更致密,这与XRD的检测结果相对应。
3 结论
1)ABS塑料前处理。最佳除油θ在60℃,t为30min;最佳粗化液 θ为70℃时粗化 t不宜超过20min;粗化θ为60℃时粗化t不宜超过30min。化学镀铜在机械搅拌或氮气搅拌下,θ为30~35℃,pH 11.0 ~11.5,4 ~5g/L 碳酸钠。
2)ABS塑料经过粗化、化学镀铜和电镀铜后的XRD分析,化学镀铜、电镀铜表面均具有单质铜晶体特征衍射峰;利用XPS对化学镀铜和电镀铜的价态分析,Cu在镀层表面的价态构成为 Cu、CuO、Cu2O、Cu(OH)2和 Cu、CuO。SEM 检测表明,化学镀铜可以将ABS塑料表面上大面积覆盖上铜,沉积表面存在少量孔道,电镀铜后ABS塑料表面完全被覆盖且结晶表面更致密。
[1]Xu S L,Zhang L X,Lin Y J.Layered double hydroxides used as flame retardant for engineering plastic acrylonitrile-butadiene-styrene(ABS)[J].Journal of Physics and Chemistry of Solids,2012,73:1514-1514.
[2]张静玉,刘庆峰,刘茜.Ti对Zn-Al合金薄膜耐腐蚀性能的影响[J].金属学报,2009,45(10):1167-1167.
[3]Liu F C,Liao J,Nakata K.Joining of metal to plastic using friction lap welding[J].Materials and Design,2014,54:236-236.
[4]Bazzaoui M,Martins J I,Bazzaoui E A,et al.Environmentally friendly process for nickel electroplating of ABS[J].Applied Surface Science,2012,258:7968-7968.
[5]杨锋,周少雄,孙永红.化学镀在电磁屏蔽中的应用[J].表面技术,2009,38(4):70-71.
[6]刘仁志.电子电镀技术[M].北京:化学工业出版社,2008:226-226.
[7]Tang X J,Cao M,BI C L,et al.Research on a new surface activation process for electroless plating on ABS plastic[J].Materials Letters,2008,62:1089-1089.
[8]陈亮,仵亚婷,甘雪萍,等.塑料表面化学镀金属化的进展[J].电镀与涂饰,2007,26(12):10-11.
[9]张勇,闫军,崔海萍,等.偶联剂在PVC塑料化学镀Ni-Cu-P前处理中的应用[J].材料保护,2008,41(1):65-65.
[10]Gan X P,Zhou K C,HU W B,et al.Role of additives in electroless copper plating using hypophosphite as reducing agent[J].Surface & Coatings Technology,2012,206:3406-3406.
[11]Chen W S,Luo G Q,Li M J,et al.Effect of 2,2`-dipyridyl on the plating rate,microstructureand performance of copper-coated tungsten composite powders prepared using electroless plating[J].Applied Surface Science,2014,301:87-87.
[12]Lin Y M,Yen S C.Effect of additives and chelating agent on electroless copper plating[J].Applied Surface Science,2001,178:117-117.
[13]张允诚,胡如南,向荣.电镀手册[M].北京:国防工业出版社,2011:552-552.
[14]郑雅杰,邹伟红,易丹青,等.酒石酸钾钠和EDTA2Na盐化学镀铜体系[J].中南大学学报(自然科学版),2005,36(6):974-974.
[15]王光君,王德志,周杰,等.Mo粉表面化学镀Cu及其反应机理[J].金属学报,2009,45(4):409-409.
[16]Magallón-Cacho L,Pérez-Bueno J J,Meas-Vong Y,et al.Surface modification of acrylonitrile-butadiene-styrene(ABS)with heterogeneous photocatalysis(TiO2)for the substitution of the etching stage in the electoless process[J].Surface & CoatingsTechnology,2011,206:1411-1411.
[17]叶龙.镀覆前表面处理[M].北京:化学工业出版社,2006:201-202.
