亚临界水中化学反应的研究进展
2015-09-02戚聿妍王荣春
戚聿妍,王荣春
(哈尔滨工业大学化工学院,黑龙江 哈尔滨 150090)
亚临界水中化学反应的研究进展
戚聿妍,王荣春
(哈尔滨工业大学化工学院,黑龙江 哈尔滨 150090)
近年来,亚临界水以其绿色、无毒、方便、高效等特点受到了学者们的广泛关注。在外加压力的作用下,水在100~374℃之间仍然可以保持液体状态,这种水即为亚临界水。本文对亚临界水的特性及优势进行了阐述,介绍了亚临界水中发生的反应类型,主要包括合成反应与降解反应,以及亚临界水对发生于其中的反应起到的作用主要有作为反应媒介、充当反应物或酸碱催化剂等;并简要介绍了两种亚临界水反应的装置。同时对于亚临界水反应的研究进展进行了概述,指出了在工业生产中可以利用亚临界水进行降解自然界中的大分子物质和进行合成反应,并对其今后的广阔前景进行了展望,提出亚临界水现阶段应用中所存在的问题,这些问题值得继续进行探索以期将亚临界水的应用推向更广泛的领域。
亚临界水;特性;化学反应;降解;合成
目前有机溶剂的使用涉及到生产时产生相关污染物、使用后则需进行废液处理等问题。而随着人们对于环保概念的日益加深,对于有机溶剂的使用越来越谨慎,亚临界水以它的无毒、方便、高效等特点逐渐走入人们的视野。越来越多的学者使用亚临界水对天然基质中的营养物质进行提取。例如:Plaza等[1]已经研究从迷迭香、百里香和马鞭草等天然样品中提取抗氧化物质;Wang等[2]对从苹果渣和柑橘皮中提取果胶进行了研究;Reddy等[3]研究从湿海藻中提取生物柴油;He等[4]从石榴籽中提取酚类化合物并对其抗氧化性进行了研究;Matilde等[5]对使用亚临界水从酿酒葡萄残渣中提取儿茶酚和原花青素进行了研究等。然而亚临界水的应用不仅可以应用于天然产物的提取,近年来,人们研究的目光逐渐转移到在亚临界水条件下可能发生的化学反应以及产物的功能性研究,并期望利用亚临界水产生有用物质或改变物质的某些功能性质(如溶解性、乳化性等),应用于工业化生产、垃圾处理及食品行业中。
1 亚临界水特性
亚临界水(subcritical water)是指水在一定压力下(≤22.05MPa),从常压沸点温度(100℃)加热到它的超临界点(374℃)时仍然保持液体状态的水,也称为过热水、高温水、高压热水或热液态水[6]。在实际应用中,亚临界水的温度一般在200℃以上[7]。在亚临界状态下,水分子热运动增加,因此许多特性会显著改变(见表1)[8],主要有以下3点:①随着温度的升高,水的自电离也升高,水在临界点附近时的离子积比室温状态下增加了超过103倍,H+和OH-浓度较常温水高,这使得亚临界水具有酸、碱催化剂的催化功能[9];②水的介电常数会降低,表现出类似于有机溶剂的特性[10]。水在室温条件下介电常数值为78F/m,但是当温度升高到250℃时,介电常数值减少到30F/m,这与甲醇或丙酮的介电常数相似,因此许多弱极性物质都能溶解到亚临界水中[1]。产生这种特性的主要原因是由于在亚临界条件下,大量的氢键结构开始断裂,使得亚临界水的极性降低;③此外,还有许多参数也发生了变化,例如水的黏性、表面张力和溶解度参数(solubility parameter)。水的黏性和表面张力随温度的升高而降低,这使得水在反应基质中有更好的渗透性,质量传递增加,可以提高提取速率,提取产量更高并且溶剂可以大量回收;同时溶解度参数也降低了,接近从较小极性化合物中得到的值[11],两种溶解度参数接近的物质,互溶性将得以提高。因此,亚临界水已经被提出可以作为弱极性有机溶剂的替代品。
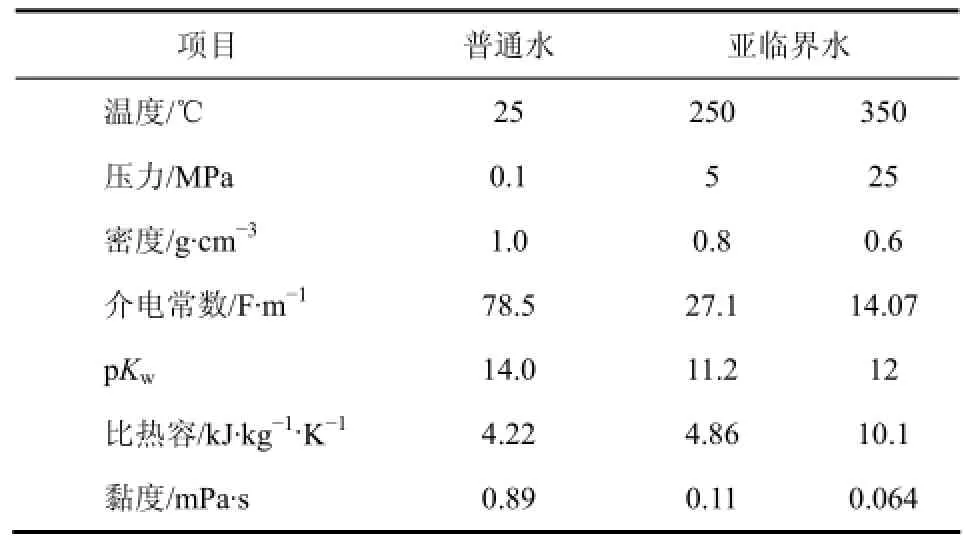
表1 不同条件下水的特征
2 亚临界水在反应中的作用
亚临界水中的化学反应相对复杂,可能有几个反应同时进行,水在不同的反应中也起着不同的作用。其作用主要是可以分为3类:作为反应媒介、充当反应物和酸碱催化剂。
2.1作为反应媒介可部分代替传统的有机溶剂
亚临界水的特殊性质会影响其作为反应媒介在化学反应中起作用。水在分子间能量传递过程中作为碰撞体,在许多基元反应中碰撞体会产生或者消耗掉关键活性中间体(例如OH、HO2、H2O2),在类似气体密度时,水密度的增大就会促进反应的进行[12]。在化学反应进程中,一个好的分离方法是至关重要的,由于水是一种便宜、无毒的溶剂,并且易于分离,某些情况还不必从产物中除去;且由于介电常数的降低,亚临界水中弱极性物质的溶解度得以提高,因此亚临界水作为反应溶剂受到了广泛关注。徐永威等[13]研究了硝基苯在亚(超)临界水中的氧化反应,在温度460℃、压力28MPa、氧气用量15倍计量倍数,停留时间不小于7s时,废水经处理后硝基苯含量低于3mg/L,总有机碳含量低于6mg/L。
2.2水可以作为反应物参与到反应之中
亚临界水除了作为反应媒介之外,其本身也可以作为反应物参与到反应中,主要的反应是水解反应。水解是指通过水的作用或水与盐反应生成的酸或碱的作用,使得化学键断裂的一种化学反应。在亚临界水状态下,水的电离常数(Kw)增加,这使得水更容易电离成H+和OH-,这就增加了水解反应的程度。Watchararuji等[14]的研究显示,米糠和大豆粉经过亚临界水处理后产生的水解产物——蛋白质和氨基酸的产量要比传统方法高许多;Cheng等[15]研究了生物废弃物在亚临界水条件下可以水解产生氨基酸、不饱和脂肪酸、油脂、多聚糖和甲烷。
有机化合物在亚临界水条件下的水解目前研究广泛,对复杂的聚合材料进行水解提出了一种回收有价值化学资源的潜在的方法。目前研究的主要有机物有醚、酯、酰胺、腈、硝基烷、环氧树脂、酚醛树脂等。表2列举了其中一些有机化合物在亚临界水条件下的水解反应进程[16]。
生物废弃物和有机化合物在亚临界水条件下的水解及其水解产物提供了一种“废物利用”的新方法,使得有价值的物质可以最大限度地发挥出其功效。

表2 在亚临界水条件下一些有机物的水解反应
2.3作为酸碱催化剂催化反应的进程
在亚临界水状态下,酸/碱能够催化反应较快进行,并且与常温状态相比,仅仅需要很少的酸/碱催化剂即可,一方面因为反应中较高的热能有利于反应的进行;另一方面在亚临界水状态下,水的电离增加,H+和OH-浓度也增加,因此亚临界水可以作为酸、碱催化剂前体在反应中起作用,在需要很强的无机酸或碱作为催化剂的反应中,即便缺少了催化剂在亚临界水状态下也可快速地进行反应。Bicker等[17]研究了在亚临界水条件下,水可以催化糖类产生乳酸,为乳酸的产生发现了新的化学方法,在300℃、25MPa的条件下,添加Co2+、Ni2+、Zn2+等金属离子可以使得蔗糖产生42%的乳酸,二羟基丙酮产生86%的乳酸。Asghari等[18]研究果糖在亚临界水条件下,可被催化分解生成5-羟甲基糠醛(HMF),在温度为240℃、反应时间120s的条件下,HMF获得了最大的产量(65%),同时对其他单糖和多糖进行研究,发现己酮糖分解产生HMF的量大于己醛糖分解产生的。Ilker等[19]发现洋麻杆在亚临界水条件下能够被催化进行水解反应,超声波处理洋麻杆-水混合物、改变水解温度和压力、使用CO2和N2作为增压气体对水解效率都有影响,在更高的温度和使用CO2作为增压气体会获得更有效水解。研究发现,亚临界水作为酸/碱催化剂也是反应速度加快和产物产量增高的主要原因之一。
3 亚临界水反应类型
亚临界水中的化学反应通常是许多反应同时进行,反应体系较为复杂,反应类型主要可以分为两类:降解反应与合成反应。
3.1降解反应
在降解反应中,主要包括水解反应(hydrolysis reaction)、热裂反应(pyrolysis)和热氧化反应(thermal oxidation reaction)等[20]。在水解反应中,水同时起着溶剂、反应物和催化剂前体的作用。在室温条件下,某些化合物要想发生反应需要添加无机酸(HCl等)作为催化剂,但是在亚临界水状态下,由于水的自电离程度加大,产生的高浓度的H+和OH-使得无需额外添加催化剂就能发生水解反应。Fujii等[21]研究了脂肪酸酯在亚临界水状态下的水解反应:对酰基链长度为8~16的甲基脂肪酸酯进行水解反应,研究发现水解反应遵循一级动力学,由于水的电离有利于形成质子化的酯,并且质子化的酯的亲核攻击作为限速步骤,最终形成酸和醇。Sasaki等[22]研究了纤维二糖在亚临界水中的水解反应,并且发现增加溶质局部水密度促进了水解的速率,亚临界水中游离出来的质子攻击纤维二糖分子中的糖苷碳原子或者从亚临界水中游离出来的氧原子对纤维二糖分子中的糖苷碳原子的亲核攻击,从而发生水解。
在亚临界水中通常是几个反应同时进行,在较高温度条件下同时会发生热裂解反应与热氧化反应。热会使得化合物发生均裂而产生自由基,即为热裂解反应,Buhler等[23]对甘油在亚临界水条件下的分解途径进行了研究,研究发现分解途径中存在着两种竞争反应途径:离子反应与热裂解反应,离子反应更易在高压/低温条件下进行,而热裂解更易在低压/高温条件下进行。甘油降解的主要产物有:甲醇、乙醛、丙醛、丙烯醛、烯丙醇等。Akiya等[16]认为自由基在氧化过程中的所生成的过氧化物通常分解生成分子较小的化合物,这种断裂迅速进行直至生成甲酸或乙酸为止,甲酸和乙酸继续被氧化,最终转化为CO2和水。酚类物质经氧化反应会生成二聚体(羟基二苯醚、双苯酚、二苯呋喃等)、单环化合物(对苯二酚)、开环产物(马来酸、水合乙醛酸和其他有机酸)、气体(CO、CO2)等[24-26]。
3.2合成反应
美拉德反应可在亚临界水中发生,为合成反应,在食品加工和储藏中是最常见的食物反应,是由还原糖的羰基,即醛或酮,与氨基酸、肽、蛋白质或任何含氮物质的游离伯胺进行的缩合反应。Plaza等[27]研究了在亚临界水条件下,3种不同氨基酸、精氨酸、赖氨酸和丙氨酸组成的混合物与葡萄糖以摩尔比为1∶4进行的美拉德反应,由葡萄糖和单独的氨基酸组成的样品作为对照,通过分析游离氨基的减少或美拉德反应产物的形成来确定糖基化的程度;同时通过ABTS和ORACFL自由基清除试验,证明其最终产物有抗氧化功效。Li等[28]研究了在亚临界水条件下ε-聚赖氨酸和葡聚多糖发生的美拉德反应,并且对最终结合物的功能特性进行了测定,发现最终产物具有良好的乳化特性,这主要是由于亚临界水的极性降低,弥补了ε-聚赖氨酸由于缺少疏水基团而造成的乳化能力不强的特点。研究者们还对亚临界水温度、压力、时间、pH值、反应物质量比对ε-聚赖氨酸与葡萄糖之间的美拉德反应速率的影响进行研究,通过测定接枝度和褐变指数评价各种因素对美拉德反应的影响[29]。结果表明,褐变指数与温度、时间、pH值呈正相关,与压力呈负相关;时间、pH值、反应物质量比对接枝度的影响均是先增大后减小。同时,美拉德反应也是在亚临界水提取、合成反应过程中产生褐变的原因之一。
当反应底物为碳水化合物时,在经过亚临界水处理后,还会发生焦糖化反应。焦糖化反应是指糖类尤其是单糖在没有氨基化合物存在的情况下,加热到熔点以上的高温时,单糖发生脱水与降解,会发生褐变反应。经焦糖化反应裂解产生的挥发性的醛、酮类物质进一步缩合、聚合最终形成深色物质。通常经过亚临界水处理后的溶液都会发生褐变,焦糖化反应就是另一原因。
4 亚临界水的反应器
亚临界水的反应器根据反应需求不同也是多种多样的。如图1为管式流通反应器(continuous tubular reactor),它可以准确控制反应时间,但是只能进行小批量试验来确定优化条件,大容量反应时由于产物的溶解性问题会造成管路堵塞。研究时一般为了防止氧气带来的影响,会对基质溶液(1)进行脱气处理,并连接惰性气体(2)以防止空气中氧气的溶解,通过可精确控制流速的高效液相色谱泵(3)将基质溶液运送到反应器中。反应器为一段定长的不锈钢管(4),浸没于可控高温的油浴(5)中,(6)为搅拌器,为了能快速地终止反应,反应液在反应后被运输至冷却管(7),冷却管浸没于冰浴中(8),在不锈钢管的尾部连以背压阀(9)用来控制整个反应体系的压力,经背压阀后计入样品瓶(10)。如果需要进行大批量的试验,可以在确定优化条件后换成批量式反应器(batch reactor)进行大容量的反应。
如图2所示的仪器原理图为Sushkova等[30]从植物基质中提取苯并芘进行分析所用仪器。该提取装置由两端带螺丝帽的不锈钢材料制成,包括压力传感器(2)、再热蒸汽保温器(3)、恒温调节器(4)等,压力计包括一个压力释放阀,使得内部压力可以维持在10.1×106Pa,样品与水放置于一个连有温度调节器的提取装置盒里。

图1 管式流通反应器
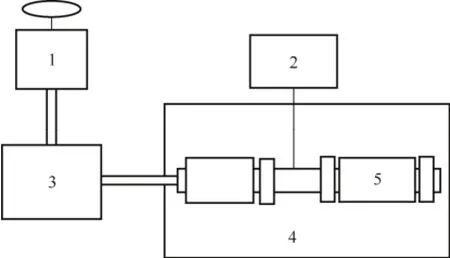
图2 从固体基质样品中提取苯并芘的反应装置[30]
5 亚临界水反应的研究进展
由于亚临界水的无毒、可回收等特点,作为一种对环境无污染的反应物,近年来有越来越多的学者对亚临界水进行研究,对在亚临界水中发生的反应的研究也逐渐受到了重视,目前,国内外的研究主要集中在以下两个方面:降解自然界中的大分子物质与合成新物质。
5.1降解自然界中的大分子
将自然界中的生物大分子利用亚临界水降解成小分子加以利用是目前研究的热点,例如Meillisa等[31]对利用亚临界水将褐藻中存在的海洋多糖降解为单糖和一些生物活性物质进行了研究,研究人员对比例为1∶25(g/mL)多糖和水进行加热加压,使其达到亚临界水状态,温度控制在180~260℃,并且使用蚁酸作为催化剂,通过实验发现产物的抗氧化活性在180℃的时候达到最高。Rogalinski等[32]研究了在亚临界水状态下,一些生物聚合物(淀粉、纤维素、蛋白质)能降解成单体(葡萄糖和氨基酸),并对其分解动力学进行了研究,高分子聚合物在亚临界水状态下仅需很短的时间即可反应完全并且具有很高的转化率。Prado等[33]利用亚临界水从椰子壳、脱脂葡萄籽和压制棕纤维中分解出可发酵的糖,反应分别在208℃和257℃反应30min,水的流速设定为33mL/min,椰子壳、脱脂葡萄籽和压制棕纤维的总还原糖的产量分别为11.7%、6.4%和11.9%。Abdelmoez等[34]应用亚临界水技术水解麦秸来产生还原糖。研究人员在不同条件下进行麦秸水解实验,并且研究出最佳水解参数:温度为190℃,水解时间为30min,水与麦秸的比例为6∶1,原料颗粒尺寸为180~355μm。在最佳条件下获得的还原糖产量为原料麦秸质量的51.5%,对于产生的还原糖进行HPLC分析,发现葡萄糖占总还原糖的3.2%,木糖为7.6%,其他还原糖包括果胶糖和半乳糖等。赵蒙蒙[35]研究了木质素在亚临界水中的降解条件与机理,通过实验发现,温度从240℃升高到280℃时明显促进了木质素的降解,并且根据对降解产物进行分析,探讨出木质素的降解机理:亚临界水体系中的水合离子通过对木质素的亲电作用而引发其发生降解反应,首先是C—O键合部分C—C键发生裂解,其降解后的液态产物主要为苯酚等小分子芳香族化合物。
亚临界水在降解生物大分子方面应用广泛,相比较传统方法,除了具有环保、无毒、无污染,废液易处理等优势,由于亚临界水的独特性质,还可以使得自然界中很难降解的生物大分子通过氧化反应、热裂反应等得到彻底降解。同时,许多有毒废弃物通过亚临界水也可以得到降解,从而实现了环境的治理。
5.2合成反应
除了降解大分子物质之外,亚临界水的另外一个研究热点就是合成新物质。涂宗财等[36]对亚临界水条件下葡萄糖-天冬酰胺的美拉德反应物进行了分析,在亚临界水不同处理时间、温度条件下发生反应,研究产物中类黑精、丙烯酰胺的生成量和产物抗氧化活性及其相关性,结果表明,在120℃、140℃处理时,类黑精生成量及产物抗氧化活性均随处理时间的延长而增加,180℃长时间热处理类黑精生成量及抗氧化活性均有略微降低的趋势。Lee等[37]对LiFePO4在亚临界水中能合成微米级微粒进行了研究,并且发现其只能在中性或碱性环境中进行合成,反应温度、pH值、时间和反应物的浓度对于生成物的尺寸和形态均有影响。葛辉[38]研究了在亚临界水条件下的酪蛋白-乳糖体系的美拉德反应进程,发现亚临界水能促进美拉德反应的进程,使酪蛋白与乳糖发生共价交联,产生高分子聚合物,并且发现亚临界水处理可以有效提高美拉德产物的抗氧化能力。Ding等[39]发现由于亚临界水具有能够溶解芳香化合物及分子氧的能力,因此亚临界水可以被用来对一些化合物进行氧化修饰,在特定的过渡金属元素作为催化剂的条件下,烷基芳香化合物可以被分子氧氧化成醛、酮和酸,二甲苯、乙苯和甲苯等可以直接被氧化成对应的酸,一些芳香亚甲基可以被氧化成酮。在同样条件下,蒽可以被氧化成蒽醌,研究发现,使用MnBr2和CoBr2作为催化剂反应过程最为洁净,同时产物的产量也最高[40]。
6 亚临界水中反应前景
水作为自然界中最常见的绿色介质,已经在化学反应中得到了广泛的应用。而亚临界水由于其独特的性质,可以作为天然无毒的提取溶剂、作为酸/碱催化剂,对于化学反应来说还可以作为反应物参与到反应中,因此在亚临界水中反应的应用前景非常广阔。目前主要集中在从废弃生物基质中提取活性物质、降解或合成新物质等,例如从迷迭香中制取疏水性芳香烃物质,产量要比使用蒸汽蒸馏要高很多[41];从红球藻中提取抗氧化成分和抑菌性成分,并且通过实验表明温度越高产物的产量越多,抗氧化性越强,但是温度对于抑菌性没有很明显的影响[42];从沙棘叶中提取抗氧化物质,通过化学成分分析,发现总酚的含量为76.07~93.72mg/g,类黄酮的含量为47.06~66.03mg/g[43];从亚麻稿杆中催化分解出糠醛,在250℃、6.0MPa条件下获得最大的产量[44];从葡萄皮、黑秘米糠中提取抗氧化成分等,并且发现这些物质同样有抑菌性、抗病毒性和抗真菌活力[45-46];处理垃圾渗滤液,利用亚(超)临界水的特殊性质,使有机物和氧气在其中迅速发生氧化反应来彻底分解有机物[47];对于污水和污染的土壤,利用亚临界水可以降解农药、炸药等高分子化合物。但是以上仍存在着某些待研究的部分,例如对于天然基质经过亚临界水反应后所获得的新生的活性物质的反应机理还知之甚少,由于亚临界水反应的产物多为混合物,如何通过控制反应条件达到产生某种人们所需要的物质,这些问题仍然需要继续研究,并且对于将亚临界水推广到更广泛的领域有着重要的意义。
[1] Plaza M,Benavent M A,Castillo M D,et al. Facts about the formation of new antioxidants in natural samples after subcritical water extraction[J]. Food Research International,2010,43(10):2341-2348.
[2] Wang X,Chen Q R,Lu X. Pectin extracted from apple pomace and citrus peel by subcritical water[J]. Food Hydrocolloids,2014,38:129-137.
[3] Reddy H K,Muppaneni T,Sun Y Q. Subcritical water extraction of lipids from wet algae for biodiesel production[J]. Fuel,2014,133:73-81.
[4] He L,Zhang X F,Xu H G,et al. Subcritical water extraction of phenolic compounds from pomegranate(Punica granatum L.) seed residues and investigation into their antioxidant activities with HPLC-ABTS+assay[J]. Food and Bioproducts Processing,2012,90(2):215-223.
[5] Garcia-Marino M,Rivas-Gonzala J C,Ibanez E,et al. Recovery of catechins and proanthocyanidins from winery by-products using subcritical water extraction[J]. Analytica Chimica Acta,2006,563(1-2):44-50.
[6] 赵健,赵国华. 亚临界水萃取技术及其在食品方面的应用[J]. 食品工业科技,2009,30(4):364-367.
[7] Mazaheri H,Lee K T,Bhatia S,et al. Subcritical water liquefaction of oil palm fruit press fiber for the production of bio-oil:Effect of catalysts[J]. Bioresource Technology,2010,101(2):745-51.
[8] Kruse A,Dinjus E. Hot compressed water as reaction medium and reactant properties and synthesis reactions[J]. The Journal of Supercritical Fluids,2007,39(3):362-380.
[9] Wang R C,Neoh T L,Kobayashi T,et al. Antioxidative capacity of the degradation products of glucuronic and galacturonic acid from subcritical water treatment[J]. Chemical Engineering Technology,2011,34(9):1514-1520.
[10] 徐万邦,蒋忠军. 亚临界水萃取在食品药品分析中的应用[J]. 中国民族民间医药,2014(19):14-15.
[11] Ravber M,Knez Z,Skerget M. Simultaneous extraction of oil-and water-soluble phase from sunflower seeds with subcritical water[J]. Food Chemistry,2015,166:316-323.
[12] Eckert C A,Chandler K. Tuning fluid solvents for chemical reactions[J]. Journal of Supercritical Fluids,1998,13(1-3):187-195.
[13] 徐永威,董秀芹,张敏华. 硝基苯在超临界水中的催化氧化工艺研究[J]. 化学反应工程与工艺,2006,22(5):434-438.
[14] Watchararuji K,Goto M,Sasaki M,et al. Value-added subcritical water hydrolysate from rice bran and soybean meal[J]. Bioresource Technology,2008,99(14):6207-6213.
[15] Cheng H B,Zhu X,Zhu C,et al. Hydrolysis technology of biomass waste to produce amino acids in subcritical water[J]. Bioresource Technology,2008,99(9):3337-3341.
[16] Akiya N,Savage P E. Roles of water for chemical reactions in high-temperature water[J]. Chemical Reviews,2002,102(8):2725-2750.
[17] Bicker M,Endres S,Ott L,et al. Catalytical conversion of carbohydrates in subcritical water:A new chemical proceess for lactic acid production[J]. Journal of Molecular Catalysis A:Chemical,2005,239(1-2):151-157.
[18] Asghari F S,Yoshida H. Acid-caralyzed production of 5-hydroxymethyl furfural from D-fructose in subcritical water[J]. Industrial & Engineering Chemistry Research,2006,45(7):2163-2173.
[19] Ozturk I,Irmak S,Hesenov A,et al. Hydrolysis of kenaf (Hibiscus cannabinus L.) stems by catalytical thermal treatment in subcritical water[J]. Biomass and Bioenergy,2010,34(11):1578-1585.
[20] 王荣春,卢卫红,马莺. 亚临界水的特性及其技术应用[J]. 食品工业科技,2013,34(8):373-377.
[21] Khuwijitjaru P,Fujii T,Adachi S,et al. Kinetics on the hydrolysis of fatty acid esters in subcritical water[J]. Chemical Engineering Journal,2004,99(1):1-4.
[22] Sasaki M,Furukawa M. Kinetics and mechanism of cellobiose hydrolysis and retro-aldol condensation in subcritical and supercritical water[J]. Industrial & Engineering Chemistry Research,2002,41(26):6642-6649.
[23] Buhler W,Dinjus E,Ederer H J,et al. Ionic reactions and pyrolysis of glycerol as competing reaction pathways in near- and supercritical water[J]. Journal of Supercritical Fluids,2002,22(1):37-35.
[24] Rice S F,Steeper R R. Oxidation rates of common organic compounds in supercritical water[J]. Journal of Hazardous Materials,1998,59(2-3):261-278.
[25] Krajnc M,Levec J. On the kinetics of phenol oxidation in supercritical water[J]. AlChE Journal,1996,42(7):1977-1984.[26] Martino C J,Savage P E. Supercritical water oxidation kinetics,products,and pathways for CH3— and CHO— substituted phenols[J]. Ind. Eng. Chem. Res.,1997,36(5):1391-1400.
[27] Plaza M,Benavent M A,Castillo M D,et al. Neoformation of antioxidants in glycation model systems treated under subcritical water extraction conditions[J]. Food Research International,2010,43(4):1123-1129.
[28] Li C L,Liu F G,Gong Y,et al. Investigation into the Maillard reaction between ε-polylysine and dextran in subcritical water and evaluation of the functional properties of the conjugates[J]. LWT-Food Science and Technology,2014,57(2):612-617.
[29] 李春林,高彦祥,袁芳,等. 亚临界水中反应参数对ε-聚赖氨酸与葡聚糖美拉德反应的影响[J]. 食品工业科技,2012,33(2):261-264.
[30] Sushkova S N,Vasilyeva G K,et al. New method for benzo[α]pyrene analysis in plant material using subcritical water extraction[J]. Journal of Geochemical Exploration,2014,144:267-272.
[31] Meillisa A,Woo H C,Chun B S. Production of monosaccharides and bio-active compounds derived from marine polysaccharides using subcritical water hydrolysis[J]. Food Chemistry,2015,171:70-77.
[32] Rogalinski T,Liu K,Albrecht T,et al. Hydrolysis kinetics of biopolymers in subcritical water[J]. The Journal of Supercritical Fluids,2008,46(3):335-341.
[33] Prado J M,Carneiro T F,Rostagno M A,et al. Obtaining sugars fromcoconut Husk,defatted grape seed,and pressed palm fiber by hydrolysis with subcritical water[J]. The Journal of Supercritical Fluids,2014,89:89-98.
[34] Abdelmoez W,Nage S M,Bastawess A,et al. Subcritical water technology for wheat straw hydrolysis to produce value added products[J]. Journal of Cleaner Production,2014,70:68-77.
[35] 赵蒙蒙. 亚临界水中木质素的降解条件与机理探索[D]. 成都:西南交通大学,2013.
[36] 涂宗财,张璆,王辉,等. 亚临界水条件下葡萄糖-天冬酰胺反应产物的分析及其抗氧化活性[J]. 食品与发酵工业,2014,40(09):29-33.
[37] Lee J W,Teja A S. Characteristics of Lithium Iron phosphate(LiFePO4) particles synthesized in subcritical and supercritical water[J]. The Journal of Supercritical Fluids,2005,35(1):83-90.
[38] 葛辉. 亚临界水对酪蛋白及其与乳糖体系结构和性质的影响[D].南昌:南昌大学,2014.
[39] Ding Z Y,Frisch M A,Li L X,et al. Catalytic oxidation in supercritical water[J]. Ind. Eng. Chem. Res.,1996,35(10):3257-3279.
[40] Holliday R L,Jong B Y M,Kolis J W. Organic synthesis in subcritical water oxidation of alkyl aromatics[J]. Journal of Supercritical Fluids,1998,12(3):255-260.
[41] Basile A,Jim Nez-Carmona M M,Clifford A A. Extraction of rosemary by superheated water[J]. Journal of Agricultural and Food Chemistry,1998,46(12):5205-5209.
[42] Rodr Guez-Meizoso I,Jaime L,Santoyo S,et al. Subcritical water extraction and characterization of bioactive compounds from haematococcus pluvialis microalgae[J]. Journal of Pharmaceutical and Biomedical Analysis,2010,51(2):456-463.
[43] Kumar M S Y,Dutta R,Prasad D,et al. Subcritical water extraction of antioxidant compounds from Seabuckthorn (Hippophae rhamnoides ) leaves for the comparative evaluation of antioxidant activity[J]. Food Chemistry,2011,127(3):1309-1316.
[44] Harry I,Ibrahim H,Thring R,et al. Catalytic subcritical water liquefaction of flax straw for high yield of furfural[J]. Biomass and Bioenergy,2014,71:381-393.
[45] Herrero M,Cifuentes A,Ibanez E. Sub- and supercritical fluid extraction of functional ingredients from different natural sources:Plant,food-by-products,algae and microalgae——A review[J]. Food Chemistry,2006,98(1):136-148.
[46] Ju Z,Howard L R. Subcritical water and sulfured water extraction of anthocyanins and other phenolics from dried red grape skin[J]. Journal of Food Science,2005,70(4):270-276.
[47] 公彦猛,王树众,肖旻砚,等. 垃圾渗滤液超临界水氧化处理的研究现状[J]. 工业水处理,2014,34(1):5-9.
Chemical reaction in subcritical water
QI Yuyan,WANG Rongchun
(School of Chemical Engineering and Technology,Harbin Institute of Technology,Harbin 150090,Heilongjiang,China)
In recent years,subcritical water has attracted wide attentions with its characteristics,such as environmental-friendly、non-toxic、convenient and efficient. Subcritical water maintains liquid state from 100℃ to 374℃ under external pressure. This research elaborated the properties and advantages of subcritical water, introduced the reaction types in subcritical water including synthesis and degradation,and discussed the roles of water in reactions. Subcritical water could be regarded as the reaction medium,the reactant and the acid/base catalysts. This paper also briefly introduced two kinds of reaction devices. Research progress in the research of subcritical water reaction was summarized,and the potential application of subcritical water in the degradation of macromolecules in nature and synthetize materials were pointed out. The possible solutions to the problems in subcritical water applications were also discussed.
subcritical water;characteristics;chemical reactions;degradation;synthesis
TS 201.2
A
1000-6613(2015)10-3557-07
10.16085/j.issn.1000-6613.2015.10.006
2015-04-02;修改稿日期:2015-05-20。
中国自然科学基金(31201403)及中国博士后基金面上项目(2012M510977)。
戚聿妍(1990—),女,硕士研究生,研究方向为食品科学。联系人:王荣春,副教授,硕士生导师,研究方向为食品科学。E-mail wangrongchun@hit.edu.cn。
