硒化低聚氨基多糖制备工艺优化及其抗氧化活性研究
2015-08-30郭向阳王友明闻正顺关丽萍曲有乐
郭向阳,王友明,高 阳,闻正顺,关丽萍,曲有乐
(1.浙江海洋学院食品与医药学院,浙江舟山 316022;2.浙江大学动物科学学院,浙江杭州 310058;3.浙江海洋学院水产学院,浙江舟山 316022)
硒化低聚氨基多糖制备工艺优化及其抗氧化活性研究
郭向阳1,王友明2,高阳3,闻正顺1,关丽萍1,曲有乐1
(1.浙江海洋学院食品与医药学院,浙江舟山316022;2.浙江大学动物科学学院,浙江杭州310058;3.浙江海洋学院水产学院,浙江舟山316022)
硒化低聚氨基多糖(LSA)是由免疫活性的硒和低聚氨基多糖(LA)化合而成的硒多糖。通过正交试验,探讨了氨基多糖硒化修饰的最佳工艺条件,当硒化剂添加量为1.2 g,反应温度70℃,pH=3,反应时间8 h;硒化低聚氨基多糖中硒含量为27.3 mg/g。当硒化低聚氨基多糖浓度为4 mg/mL时,对DPPH、羟基自由基、超氧阴离子清除率分别为84.8%、71.6%、51.8%,还原力为0.33,硒化低聚氨基多糖的抗氧化能力要强于低聚氨基多糖。
低聚氨基多糖;硒化;抗氧化
低聚氨基多糖是将虾、蟹壳中的甲壳素通过脱乙酰基获得的一种动物多糖,具有良好的生物活性和医学性能。甲壳素是天然有机化合物中数量仅次于纤维素的一大类含氮有机化合物[1],因此低聚氨基多糖具有很好的开发前景。硒是人体必需的微量元素,有预防心血管疾病、克山病、抑制癌症、抗衰老、抑炎等作用[2],补硒有助于提高机体免疫力,增强体质的功效。硒的存在形式分为无机硒和有机硒两种,无机补硒剂像亚硒酸钠其活性和毒性范围窄,且不易被人体吸收,其应用受到限制,相对而言有机硒毒性低、副作用小,更易被人体吸收,能够更好地发挥硒的生理活性[3]。
因此该研究将硒与低聚氨基多糖有机结合使之转化为有机硒化合物硒化低聚氨基多糖,既保持了多糖的基本构型和生理功能,且硒的毒性和副作用大大降低,更易被人体吸收。本文对硒化低聚氨基多糖制备工艺进行优化并研究其抗氧化活性。
1 材料与方法
1.1材料与试剂
低聚氨基多糖,购于浙江金壳生物化学有限公司。冰醋酸、亚硒酸钠硝酸、高氯酸、盐酸、EDTA-2Na、盐酸羟胺、邻苯二胺、甲苯;抗坏血酸、无水乙醇、DPPH(阿拉丁)、FeSO4·7H2O、H2O2、水杨酸、Tris-HCl、邻苯三酚、PBS、铁氰化钾、三氯乙酸、FeCl3以上均为国药试剂分析纯。
1.2仪器与设备
紫外分光光度计,UV-1100,上海美谱达仪器有限公司;旋转蒸发仪,N-1100,EYELA;精密pH计,PHS-3C,上海虹益仪器仪表有限公司;冷冻干燥机,FD-1000,北京德天佑科技发展有限公司;恒温磁力搅拌器,常州国华电器有限公司;分析天平,赛多利斯科学仪器(北京)有限公司。
1.3试验方法
1.3.1硒化低聚氨基多糖的制备
称取1.0 g低聚氨基多糖溶于50 mL 2%醋酸水溶液中,搅拌溶解,至溶液澄清,取适量亚硒酸钠溶于少量水中缓慢加入到低聚氨基多糖溶液中,一定温度条件下磁力搅拌一定时间后,反应液透析2 d,以抗坏血酸检测透析液,不显红色即可,减压浓缩至适当体积,冷冻干燥,即得硒化低聚氨基多糖[4-5]。
1.3.2单因素试验
测定不同反应液pH,反应温度、反应时间、硒化剂添加量对硒化低聚氨基多糖中硒含量的影响[6]。
1.3.2.1反应溶液pH对硒含量的影响
以硒化剂添加量0.8 g,反应时间8 h,温度60℃,反应体系pH依次设为3、3.5、4、4.5、5,按本文1.3.1试验方法操作以硒化低聚氨基多糖中硒含量为指标,研究反应溶液pH对硒化低聚氨基多糖中硒含量的影响。
1.3.2.2反应时间对硒含量的影响
以硒化剂添加量0.8 g,pH调为3.5,温度60℃,反应时间依次设为2、4、6、8、10、12 h,按本文1.3.1试验方法操作以硒化低聚氨基多糖中硒含量为指标,研究反应时间对硒含量的影响。
1.3.2.3反应温度对硒含量的影响
以硒化剂添加量0.8 g,反应时间8 h,pH调为3.5,反应温度分别为20、30、40、50、60、70、80℃,按
1.3.1试验方法操作,以硒化低聚氨基多糖中硒含量为指标,研究反应温度对硒含量的影响。
1.3.2.4硒化剂添加量对硒含量的影响
将反应液pH调为3.5,温度60℃,反应时间8 h,硒化剂添加量依次为0.4、0.8、1.2、1.6、2.0 g,按本文
1.3.1试验方法操作以硒化低聚氨基多糖中硒含量为指标,研究加硒量对硒含量的影响。
1.3.3正交试验
根据单因素实验结果设立四因素三水平正交试验[7],加硒量选取0.4 g、0.8 g、1.2 g,反应温度选取50℃、60℃、70℃,反应时间选取6 h、8 h、10 h,pH依次设为3、3.5、4,试验因素和水平设计见表1。

表1 正交实验因素水平表Tab.1 The levels and factors of the orthogonal test
1.3.4硒化低聚氨基多糖中硒含量的测定
1.3.4.1标准曲线的测定
准确称取硒粉0.1 g,置于小烧杯中,加硝酸10 mL。在水浴中溶解,放冷,定量转移到100 mL容量瓶中,加纯水稀释至刻度,摇匀,备用。取备用液1 mL,置250 mL量瓶中,加纯水定容,摇匀,即得硒标准品溶液,置棕色瓶中,放冰箱保存备用(浓度:4 μg/mL)。准确吸取硒标准溶液0、2、4、6、8、10、12 mL,分别置于100 mL三角烧瓶中,加水至25 mL,用1 mol/L盐酸溶液调pH=2,加1%邻苯二胺溶液2 mL,摇匀,避光放置2 h,加甲苯10 mL,用力振摇2 min,萃取,静置10 min,用移液器吸取甲苯层,以不含样品的甲苯液为空白对照,以335 nm为检测波长,测定吸光度值。以浓度对吸收度进行回归。
1.3.4.2样品中硒含量的测定
准确称取0.05 g样品置于50 mL锥形瓶,加入混酸HClO4+HNO3(1:4)10 mL,加盖隔夜消化,次日电热板加热消化,保持低温微沸状态至溶液清澈透明(加热至瓶内产生浓白烟),稍冷后加10 mL 6 mol/L HCl,继续加热至瓶内产生浓白烟,取下放冷、转移至50 mL容量瓶中,定容备用。吸取消解液5 mL,放于100 mL三角烧瓶中,加水补至25 mL,以下操作同标准曲线操作,根据样品吸光度,代入标准曲线中计算Se含量。
1.3.5硒化低聚氨基多糖体外抗氧化试验
1.3.5.1硒化低聚氨基多糖,低聚氨基多糖对DPPH自由基的清除
用0.1 mol/L稀醋酸配制硒化低聚氨基多糖,低聚氨基多糖,浓度依次为(0.5、1、2、3、4 mg/mL),取4 mg DPPH用无水乙醇定容100 mL,分别吸取2 mL样品溶液置于试管内,然后加入2 mL DPPH,摇匀,黑暗中静置30 min,517 nm测定吸光度,并以下式计算其清除率:
清除率(%)=[A0-(Ai-Aj)]/A0×100%,A0是对照组,Ai是样品组,Aj是空白组。
1.3.5.2硒化低聚氨基多糖,低聚氨基多糖对羟基自由基的清除
分别取1 mL不同浓度的硒化低聚氨基多糖,低聚氨基多糖溶液,分别加入6 mmol/L FeSO4溶液1 mL,再加入6 mmol/L水杨酸溶液1 mL,混匀,然后加入6 mmol/L H2O21 mL启动反应,避光静置30 min后于510 nm处测定吸光度Ai,以不加水杨酸的为Aj,样品溶液以蒸馏水代替测定A0,羟基自由基清除率计算公式同1.3.5.1[11]。
1.3.5.3硒化低聚氨基多糖,低聚氨基多糖对超氧阴离子自由基的清除
取0.05 mol/L的Tris-HCl缓冲溶液(pH=8.2)4.5 mL,置于25℃水浴锅中预热25 min,分别加入1 mL样品溶液和0.12 mL 10 mmol/L的邻苯三酚溶液,混匀,在25℃水浴中反应5 min,加入1 ml 8 mol/L盐酸终止反应,于299 nm处测吸光度。空白组以0.1 mol/L HAc代替多糖溶液。
1.3.5.4硒化低聚氨基多糖,低聚氨基多糖还原能力的测定
取1 mL样品溶液,加入pH=6.6的磷酸缓冲溶液2.5 mL、1%铁氰化钾2.5 mL,混匀,于50℃水浴中保温20 min,再加入10%的三氯乙酸2.5 mL,混匀以3 000 r/min离心10 min,移取上清液2.5 mL于试管中,加蒸馏水2.5 mL和0.1%FeCl3 0.5mL,常温反应5 min后于700 nm处测定吸光度Ai,对照组溶液A0,空白组Aj[12-13]。
2 结果与讨论
2.1硒含量标准曲线
以硒含量对吸光度做标准曲线,得回归方程为y=0.212 x+0.006,R2=0.9995。
2.2单因素试验分析
2.2.1反应液pH对硒含量的影响
随着醋酸添加量的增加,反应液pH降低,硒化反应更易进行,硒含量不断增加,当pH达到3时,硒含量达到15.1 mg/g,由于考虑到实际应用中醋酸的消耗,设定最小pH为3。
2.2.2反应时间对硒含量的影响
从0~8 h,随着反应时间的延长,硒化反应进行的更充分,但在8 h之后,硒含量逐步降低,可能由于反应液在较高温度,较酸环境下,低聚氨基多糖不断降解,低分子量的硒化低聚氨基多糖在透析时流失,导致最终硒含量逐渐降低。
2.2.3反应温度对硒含量的影响
从图3可以得出随着反应温度的上升,硒化低聚氨基多糖中的硒含量不断上升,在50~70℃上升比较明显,超过70℃硒含量则上升的比较缓慢,考虑到实际功耗,选择50、60、70℃作为优化反应的三个温度。
2.2.4硒化剂添加量对硒含量的影响
从图4中可以得出,随着硒化剂添加量的增加,最终硒化低聚氨基多糖中的硒含量不断上升,但在加硒量超过1.2 g时,增加比缓慢,硒利用率逐步降低。
2.3正交试验结果分析
根据极差R分析,硒含量影响因素主次顺序为温度>pH>加硒量>反应时间,最优组合A3B3C1D2,即当反应条件为1.2 g,70℃,pH=3,8 h,硒含量27.3 mg/g,硒化率0.05(表2)。
硒化率影响因素主次顺序,温度>加硒量>pH>反应时间,最优组合A1B3C1D2即0.4 g,70℃,pH=3,8 h,硒含量18.19 mg/g,硒化率达到0.099。

图1 pH对硒含量的影响Fig.1 Effect of pH on selenium content
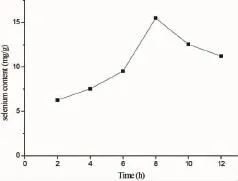
图2 反应时间对硒含量的影响Fig.2 Effect of time on selenium content
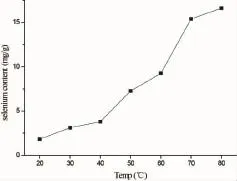
图3 反应温度对硒含量的影响Fig.3 Effect of temperature on selenium content

图4 硒化剂添加量对硒含量的影响Fig.4 Effect of selenium addition on selenium content

表2 正交试验设计及结果Tab.2 The design and result of the orthogonal test
2.4体外抗氧化试验
2.4.1清除DPPH自由基能力测定
从图5可以看出,硒化低聚氨基多糖和低聚氨基多糖和对DPPH自由基均有不同程度的抑制作用,且均随着多糖浓度(0.5~4 mg/mL)增加而增强,在4 mg/ mL时硒化低聚氨基多糖和低聚氨基多糖对DPPH自由基清除率分别达到84.8%和75.2%。

图5 LSA、LA对DPPH自由基的清除作用Fig.5 Scavenging effects of LSA and LA on DPPH free radical
2.4.2清除羟基自由基能力测定
从图6可以看出,硒化低聚氨基多糖和低聚氨基多糖对羟基自由基均有不同程度的清除作用,且均随着多糖浓度(0.5~4 mg/mL)内增加而增强,硒化低聚氨基多糖和低聚氨基多糖在4 mg/mL对羟基自由基的清除率达到71.6%和63.3%。
2.4.3清除超氧阴离子自由基能力测定
从图7可以看出,硒化低聚氨基多糖和低聚氨基多糖对超氧阴离子自由基均有不同程度的清除作用,且均随着多糖浓度(0.5~4 mg/mL)内增加而增强,硒化低聚氨基多糖和低聚氨基多糖在4 mg/mL对超氧阴离子自由基的清除率达到51.8%和44.8%。

图6 LSA、LA对羟基自由基的清除作用Fig.6 Scavenging effects of LSA and LA on hydroxyl radicals
2.4.4还原力能力的测定
从图8可以看出,硒化低聚氨基多糖和低聚氨基多糖都有一定的还原能力,且均随着多糖浓度(0.5~4 mg/mL)内增加而增强,硒化低聚氨基多糖和低聚氨基多糖在4 mg/ml时还原力达到0.33和0.26。

图7 LSA、LA对超氧阴离子自由基的清除作用Fig.7 Scavenging effects of LSA and LA on superoxide anion free radical

图8 LSA、LA还原力能力的测定Fig.8 Reducing power of LSA and LA
3 结论
在试验剂量范围内,影响硒含量的因素顺序为温度>pH>加硒量>反应时间,影响硒转化率的顺序为温度>加硒量>pH>反应时间,最高硒含量27.3 mg/g,另外对硒化低聚氨基多糖的进行抗氧化活性的研究表明,硒化低聚氨基多糖对DPPH,羟基自由基具有良好的清除作用,硒化低聚氨基多糖的抗氧化能力要强于低聚氨基多糖,且具有一定的还原力。
[1]蒋挺大.壳聚糖[M].北京:化学工业出版社,2007:1-14.
[2]MONICA P,LUIGI F,PATRIZIA M.Determination of selenium in Italian rice by differential pulse cathodic stripping voltammetry[J].Food Chemistry,2007,2:1-8.
[3]王艳预,吴海歌,高大彬,等.硒多糖的研究进展[J].化学与生物工程,2008,25(2):7-9;18.
[4]李柱来,林媚,王津,等.硒化壳聚糖的制备及其表征[J].海峡药学,2005,17(3):10-13.
[5]孙兰萍,张胜义,许晖.硒化壳聚糖的制备及理化性质的研究[J].食品工业科技,2006,27(2):145-146;151.
[6]颜炳祥,潘道东,曾小群.乳酸菌胞外多糖硒化修饰及其抗氧化活性研究[J].中国食品学报,2012,12(2):15-23.
[7]JI Y-B,DONG F,LANG L,et al.Optimization of Synthesis,Characterization and Cytotoxic Activity of Seleno-Capparis spionosa L.Polysaccharide[J].International Journal of Molecular Sciences,2012;13(12):17 275-17 289.
[8]史丽英.微量元素硒的测定方法综述[J].微量元素与健康研究,2007,7(4):10-11.
[9]刘有芹,杨庆辉,黄函,等.紫外分光光度法测定枸杞子、陈皮、生姜中硒含量[J].理化检验(化学分册),2010(3):329-330.
[10]邓斌,蒋刚彪,陈六平.紫外分光光度法测定石榴皮中微量元素硒[J].微量元素与健康研究,2008,25(1):40-4l.
[11]杨方美,王林,胡秋辉.鼠尾藻多糖的制备及其抗氧化活性[J].食品科学,2005,26(2):224-227.
[12]徐春兰,钦传光,牛卫宁,等.硒化壳聚糖的制备及其体外抗氧化活性研究[J].化学与生物工程,2009,26(9):45-48.
[13]WANG J,ZHAO B,WANG X,et al.Synthesis of selenium-containing polysaccharides and evaluation of antioxidant activity in vitro[J].International journal of biological macromolecules,2012,51(5):987-991.
Preparation of Seleno-aminopolysaccharide and Study on its Antioxidant Activity
GUO Xiang-yang1,WANG You-ming2,GAO Yang3,et al
(1.Food and Pharmacy School of Zhejiang Ocean University,Zhoushan316022;2.College of Animal Science,Zhejiang University,Hangzhou310058;3.Fishery School of Zhejiang Ocean University,Zhoushan316022,China)
Low molecular seleno-aminopolysaccharide(LSA)is organic selenium compounds consisted of inorganic selenium and low molecular aminopolysaccharide(LA).The optimal selenium modification conditions of low molecular aminopolysaccharide was studied by orthogonal experiment.When the dosage of selenium agent was 1.2 g,the temperature was 70℃,pH=3,and reaction time was 8 h,the selenium content was 27.3 mg/g.The scavenging rate ofDPPH free radical,hydroxyl radicals and superoxide anion free radical was 84.8%,71.6%and 51.8%and the reduction ability was 0.33 when the LSA concentration was 4 mg/mL.The antioxidant capability of LSA was stronger than that of LA.
aminopolysaccharide;selenium modification;antioxidant activity
Q539
A
1008-830X(2015)03-0216-06
2014-09-10
国家自然科学基金项目(31301982);浙江海洋学院2012年科研计划项目(面上项目)(X12M05);浙江海洋学院科研启动经费资助项目;浙江海洋学院校级重大项目(X12ZD08);浙江省教育厅2013年度科研计划项目(Y201328199)
郭向阳(1987-),男,河南洛阳人,硕士研究生,研究方向:海洋天然产物与健康.
闻正顺,男,副教授,博士,研究方向:海洋天然产物与健康.E-mail:ashun789@163.com.
