液质联用分析金钱草醇提物中的化学成分
2015-08-01吴志军谢万霓
汪 丹,蔡 甜,吴志军,谢万霓,邹 亮
(1.成都大学 基础医学与护理学院,四川 成都 610106;2.四川大学 华西药学院,四川 成都 610041;3.中国科学院 成都有机化学所,四川 成都 610041;4.中国科学院 成都生物研究所,四川 成都 610041;5.四川省医学科学院·四川省人民医院,四川 成都 610072)
0 引 言
金钱草是一种常见中药材,它为报春花科植物过路黄的干燥全草.中医认为,金钱草主治湿热黄疸、痈肿疔疮等症[1].研究表明,金钱草含有多种化学成分,如黄酮、酚酸、萜类等[2-4].中药材的成分组成和含量与药材产地及生长周期密切相关,传统的分离纯化鉴定方法费时费力,且存在大量已知的化学成分被多次重复分离的问题,而分离所消耗的原药材和试剂的用量大,不便于快速筛选不同产地之间金钱草的化学成分的差异及寻找未报到的新化合物[5-6].此外,传统的高效液相色谱法在缺乏对照品时,难以对所检测到的色谱峰提供有效的检测信息,故需要用一种灵敏度高、专属性好的分析方法对天然产物的成分来进行快速准确检测[7-8].目前,已有文献记录采用液质联用的方式分析天然产物的化学成分,依靠质谱检测到准分子离子峰或碎片离子峰并进行分析,能快速获取分子式及结构信息,并经过鉴定得到其化学成分[9].在此基础上,本研究建立了一种LC-ESI-MS(Q-TOF)方法,来对野生采集的金钱草进行定性检测分析.
1 材料与方法
1.1 材料、试剂与仪器
1.1.1 材 料.
金钱草采集于四川省资阳市雁江区,经中国科学院成都生物研究所顾建教授鉴定为报春花科植物过路黄的全草.
1.1.2 试 剂.
实验所用试剂包括:甲醇(Fisher Scientic Pittsburgh,PA,USA),无水乙醇(成都市科龙化工试剂厂),蒸馏水.
1.1.3 仪 器.
实验所用仪器包括:Agilent 1100 系列高效液相色谱仪(四元泵、二极管阵列检测器、自动进样器和柱温箱使用)(美国安捷伦仪器公司),Bruker micrOTOF-Q 质谱仪(德国布鲁克道尔顿仪器公司),FW-100型高速万能粉碎机(北京中兴伟业仪器有限公司),SHIMADZU AUX120 万分之一电子天平(日本岛津仪器公司)RE2000 型旋蒸挥发仪(上海雅荣仪器公司).
1.2 方 法
1.2.1 金钱草粗提物的制备.
称取金钱草粉末(1.000 g),精密称定,置于50 mL 圆底烧瓶中,加入25 mL 80%乙醇溶液,浸渍24 h 后,于50 ℃超声提取30 min,过滤;药渣再加25 mL 80%乙醇,超声提取1 次,过滤;合并两次提取的滤液,于40 ℃下减压回收制备金钱草粗提物.
1.2.2 空白样品制备.
同“1.2.1”项下制备方法,不加药材,制备得空白样品.
1.2.3 样品及空白样品溶液的制备.
将“1.2.1”项和“1.2.2”项制备的金钱草粗提取物和空白样品,用2 mL 80%乙醇溶液超声15 min溶解,离心(12 000 r/min),取上清液,制得样品和空白样品溶液,待LC-MS 测定分析.
1.2.4 色谱条件.
色谱柱为,Inertsil ODS-4(C18 柱,5μm 4.6 mm×250 mm,Inertsil ODS-4 GL Sciences Inc),柱温30℃.二元线性梯度洗脱,流动相为,A 相[水(1‰甲酸)]、B 相(甲醇).梯度为:0 ~2 min 100%A;6 min 92%A 8%B;8 min 65%A 35%B;10 min 50%A 50%B;14 min 40% A 60%B;20 min 30%A 70%B;26 min 20%A 80%B;32 min 10%A 90%B;52 min 6%A 94%B;62~80 min 100%B.流速为0.8 mL/min,进样量为20 μL.
1.2.5 质谱条件.
质量分辨率为,10 ×103FWHM(半峰全宽)、922 u.氦气用作碰撞气体,高纯度氮气作为雾化器和干燥气体的流速为0.5 L/min 和4.0 L/min.ESI源条件为:毛细管电压为-4 500 V,端板电压-4 000 V;毛细管出口电压120 V,干燥气体的温度180 ℃.将0.8 mL/min 的液相流出液,利用三通管分流去掉约93%后,再连接进入质谱进样,采集二级质谱时,分别用15 eV、35 eV 的碰撞能量对样品进行轰击,以获得碎片离子峰.同时,用布鲁克指南针软件(Data Analysis 处理4.0 软件)对数据进行分析处理.
在实验中,共检测到295 个准分子离子峰,其中筛除掉空白样品的离子峰、在一级质谱中出现的二级质谱碎片离子峰、糖类物质离子峰后,获得能确定分子式的物质峰共计43 个.在检测到的这43 种物质中,已有文献报道的物质有12 个[2-8],剩余的31个物质,在金钱草化学成分中未被报道过.本研究依据检测到的这31 种化合物的分子量,首次报道确立了其分子式、结构特征,并依据结构特征峰,推论新发现黄酮类化合物2 个.所测到的43 种物质峰详情见表1.
2 结果与讨论
本研究利用LC-ESI-MS 方法检测到的新化合物集中在图1 中的14 min 到39 min 之间出现,其各峰的保留时间、测得的精确分子量、误差、检测到的准分子式、化合物分子式、结构推理等信息见表1.
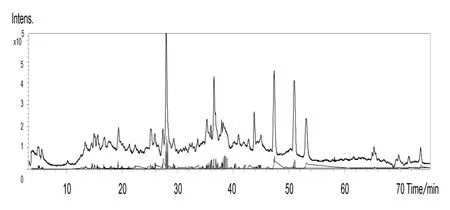
图1 一级质谱及二级质谱总离子流图
表1 中,化合物4、6、8、10、11、14、15、16、17、18、19、25、27、31 的质谱二级碎片显示其结构为黄酮类化合物,其中,化合物4 和化合物10 在已有的文献中未被报道过,属于第一次发现的新化合物,化合物25、27 用标准品对比确认为槲皮素和山奈酚,其余的化合物与化合物25 或化合物27 有相同的黄酮母核,故确定上述检测化合物均为黄酮类化合物.因在负离子模式下能够检测到物质峰的化合物必须含有羧酸根或多羟基的结构,故化合物1、2、3、5、7、9、12、13、16、20、21、22、23、24、26、29、30、32、33、34、35、36、37、38、39、40、41、42、43 均为酚类或酸类化合物,其中,化合物37、38、42 为不易打碎的链状结构,故推论为脂肪酸.
3 结 语
利用LC-ESI-MS 分析方法可以快速而准确地对金钱草乙醇提取物进行分析.本研究通过对资阳产金钱草的相关分析,共检测到化学成分43 种,其中除已有文献报到的黄酮类组分12 种,还检测到31 种未知化学组分,尤其是发现了该产地的金钱草中含有2 种未被报道过的黄酮类活性成分(化合物4 和化合物10).本研究表明,LC-ESI-MS 方法可为不同产地金钱草药材化学成分的鉴定、有效成分的快速筛选与发现新的活性成分,提供一种有效的解决方案.
[1]国家药典委员会.中华人民共和国药典(一部)[S].北京:化学工业出版社,2010.
[2]沈联德,姚福润.金钱草化学成分的研究[J].华西药学杂志,1988,3(2):71-75.
[3]侯冬岩,回瑞华,李铁纯,等.金钱草化学成分的分析[J].鞍山师范学院学报,2004,6(2):36-38.
[4]Sun D X,Dong L H,Guo P P,et al.Simultaneous detection of flavonoids and phenolic acids in Herba Lysimachiae and Herba Desmodii Styracifolii using liquid chromatography tandem mass spectrometry[J].Food Chem,2013,138(1):139-147.
[5]杨念云,段佥廒,李萍,等.金钱草中黄酮类化合物的分离与结构鉴定[J].中国药学杂志,2006,54(21):1621-1624.
[6]王宇杰,孙启时.金钱草的化学成分研究[J].中国药物化学杂志,2005,16(6):357-359.
[7]闫婷.金钱草化学成分及质量标准研究[D].沈阳:辽宁中医药大学,2007.
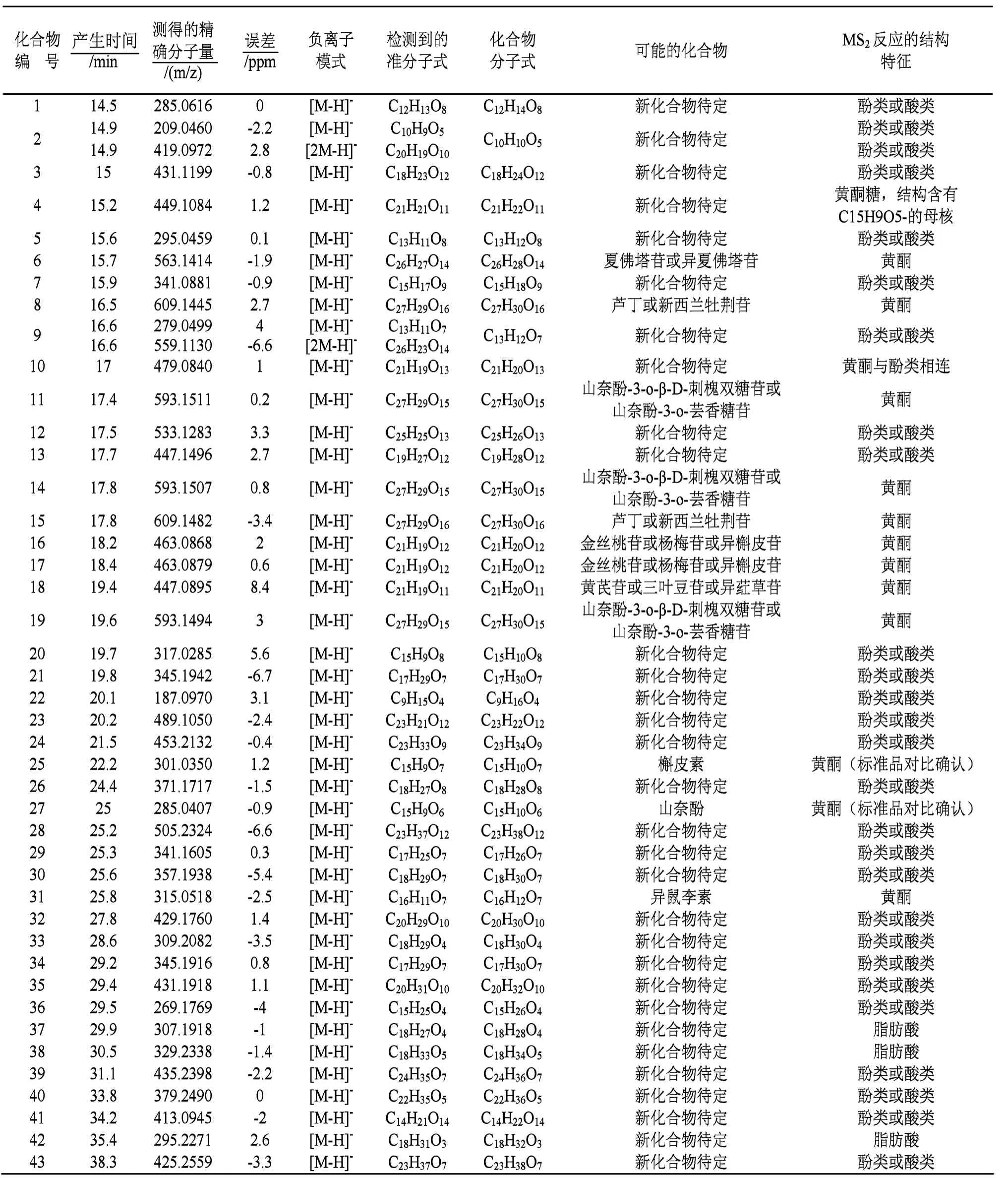
表1 新化合物的质谱数据信息及分子式
[8]高飞飞.金钱草的化学成分研究[D].重庆:西南大学,2013.
[9]戴雨霖,于珊珊,张颖,等.葛花中异黄酮类化学成分的RRLC-Q-TOF MS/MS 研究[J].高等学校化学研究,2014,35(7):1396-1402.
