阿米卡星印迹微球的制备及其性能
2015-07-24田一方郭利辉梅晓芸张新爱陈冠华
田一方,郭利辉,梅晓芸,张新爱,陈冠华
(江苏大学 食品与生物工程学院,江苏 镇江 212013)
氨基糖苷类抗生素是一类高效广谱抗菌药物,在畜牧和水产业中主要运用于治疗由革兰氏阴性杆菌如大肠杆菌、产气杆菌、痢疾杆菌、鼠疫杆菌、布鲁氏菌等引起的病症,且常被添加到饲料中,用于促进动物生长发育[1-2].然而往往由于其不合理使用,导致在动物源性食品中过量残留,长期食用会危害人体健康,引起各种不良反应[3-5].因此,对食品中该类抗生素残留的检测势在必行,很多国家和组织都规定了其最大残留限量(MRL)[6-7].针对动物性食品中氨基糖苷类抗生素的多残留检测,其方法可能受样品基质的复杂性和检测设备的影响,建立一种可快速、准确将其从样品中分离净化出来甚至达到富集效果的方法成为重中之重.固相萃取法是一种集提取净化和富集作用于一体的前处理方法,已被运用于氨基糖苷类残留检测中[8].然而目前市场上使用的大多数固相萃取柱都是非特异选择性的萃取柱,其并不能对某类特定的目标分子进行高选择性的净化与富集.因此,寻找一种能简便有效净化和富集样品中氨基糖苷类的方法是极需解决的问题.
分子印迹技术是一种分子识别技术,利用该技术合成的聚合物中具有与模板分子空间结构相匹配的空穴,并且空穴内还具有与其功能基团正好互补的作用位点,对特定类别的目标分子具有很高的选择性吸附能力,可应用于结构类似化合物的分离、仿生传感、催化等[9].利用这种技术所制的聚合物被称为分子印迹聚合物(MIP).由于其高效的识别性能和独特的理化特点,分子印迹技术依然成为一个受人关注的研究方向,在食品安全检测中展现了十分广泛的应用前景[10-12].沉淀聚合是MIP制备方法中的一种,可制备出能直接用作固相萃取柱填料的微球形聚合物,避免了后期研磨粉碎对聚合物中某些结合位点的破坏.阿米卡星是氨基糖苷类抗生素中的一种,以该抗生素作为模板,可制备对氨基糖苷类抗生素具有特异选择性的固相萃取填料,为高效净化和富集氨基糖苷类残留奠定物质基础.
1 实验部分
1.1 仪器与试剂
B5500S-MT 超声清洗机(上海必能信超声有限公司);BS 124S 电子分析天平(赛多利斯公司);WW-1601 紫外可见分光光度计(北京瑞利分析仪器公司);索式抽提器(镇江华东器化玻有限公司);HH-S8 数显恒温水浴锅(金坛市医疗仪器厂);SHA-B 水浴恒温振荡器(江苏金坛市中大仪器厂);H-180 超高速冷冻离心机(湖南湘仪实验室仪器开发有限公司);真空干燥器(河南郑州中天实验仪器有限公司);MultiMode8 原子力显微镜(美国布鲁克公司).
阿米卡星原药(AMK,质量分数98%,西安博昌科技有限公司);甲基丙烯酸(MAA)、乙二醇二甲基丙烯酸酯(EGDMA)、偶氮二异丁腈(AIBN)、四氢呋喃(THF)、甲醇和冰乙酸均为分析纯试剂.MAA 和EGDMA 使用前需经减压蒸馏提纯,MAA 的馏分温度为60~63 ℃,EGDMA 馏分温度为98~100 ℃,AIBN 用甲醇重结晶后使用.实验用水为超纯水.
1.2 AMK MIP微球的制备方法
分别称取模板分子AMK 和功能单体MAA 0.05mmol和0.2mmol,溶于一定量的THF-水(体积比为7:1),置于室温下过夜,使得模板分子和功能单体能够充分结合.然后,依次加入交联剂EDGMA 1mmol、引发剂AIBN 10mg.混合液超声5min后,通氮气5min,密封置于60 ℃的水浴恒温振荡器中持续反应24h.反应结束后,过滤聚合物,并依次用水、甲醇对其进行冲洗.用索氏提取器配以甲醇与乙酸体积比为9:1的溶液对处理过的聚合物进行洗脱,去除模板分子.通过调节水浴锅的温度,使洗脱溶剂45min循环1次,直到洗脱液无模板分子(紫外分光光度计测定洗脱液,未见紫外吸收).用甲醇去除残留的乙酸,洗至中性.最后,取出真空干燥并备用.非印迹聚合物(NIP)的制备过程,除不加模板分子外,其余步骤同MIP的制备.
1.3 标准曲线
配制浓度为0.3,0.5,1,2,3,4,5 mmol/L 的AMK THF-水(体积比7:1)溶液,在波长196nm 下,以溶剂为空白,用紫外分光光度计进行检测,得到线性回归方程.图1为AMK 标准曲线,其方程为A=0.427c-0.093,其中c为AMK 浓度.该标准曲线用于条件优化以及MIP性能研究.
1.4 MIP吸附性能测定方法
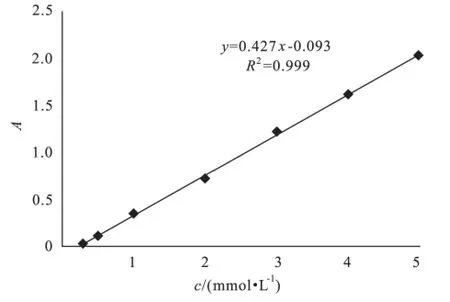
图1 AMK 标准曲线Fig.1 Calibration curve of AMK
精确称取MIP及NIP微球各50mg,置于10mL 比色管中,分别加入5mL AMK 的THF水溶液,在室温下振荡一定时间后以10 000r/min离心10min,取上层清液过0.45μm 滤膜,检测吸附后AMK 的浓度.根据吸附前后溶液中AMK 浓度的变化,计算MIP 和NIP的吸附量Q(μmol/g).

式中c0为AMK 的初始浓度(mmol/L);cx为AMK 的平衡浓度(mmol/L),V 为溶液的体积(mL),m 为所用聚合物的质量(g).
2 结果与讨论
2.1 功能单体与模板分子比例的优化
在分子印迹过程中,功能单体的一端以氢键形式与模板分子结合,另一端则与交联剂形成聚合物网络,其间形成诸多空穴,并与模板分子相匹配.聚合物中形成的空穴数量对该聚合物的识别能力有着很大的影响,而这取决于功能单体和模板分子的比例.因此,首先要优化其比例.固定AMK 浓度为0.5mmol/L,逐渐增加MAA 的浓度.超声10min后静置过夜,以相对应浓度的MAA 作为参比溶液,分别测定其紫外吸收光谱,结果见表1.由于MAA 和AMK 形成了复合物致使其最大吸收波长由AMK 的196nm 发生显著的红移.随着MAA的增加,形成的复合物的量逐渐变化,并且其吸光度在1:4时出现峰值.因此,可以初步确定AMK 和MAA 的最佳比例为1:4.
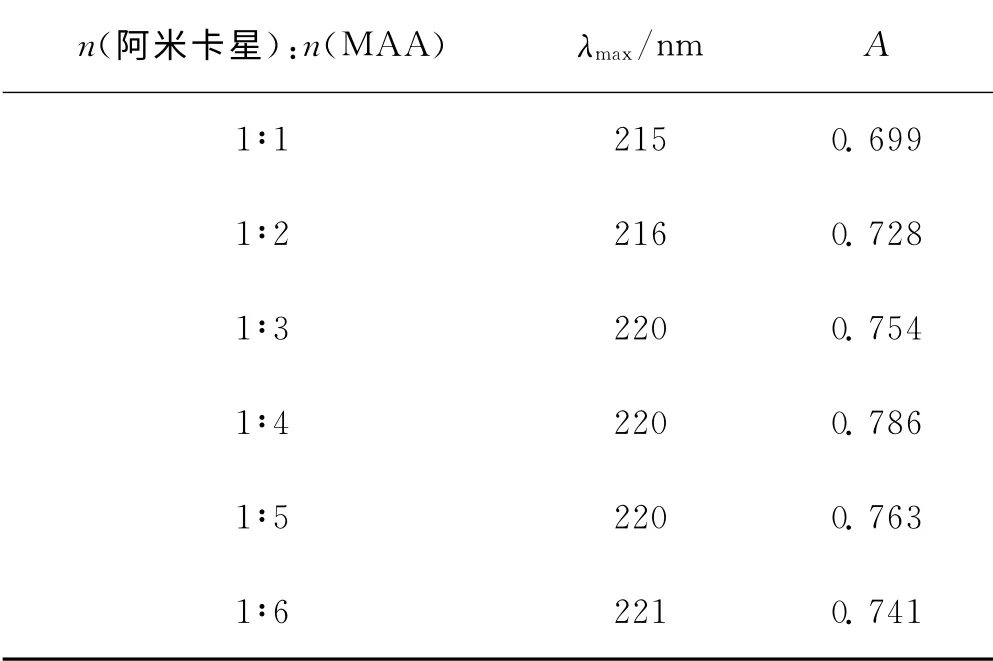
表1 AMK 和MAA比例对吸光度的影响Tab.1 Effect of ratios of amikacin and MAA on absorbance
在实际合成中分别使AMK 和MAA 物质的量以1:1,1:2,1:3,1:4,1:5,1:6的比例进行聚合,用合成的MIP分别对5mmol/L的AMK 吸附24h后进行吸附量(Q)测定,结果如图2所示.最终,确定模板分子与功能单体的最优物质的量比为1:4.
2.2 溶剂的用量
在制备MIP过程中,溶剂的作用是使反应物能够溶解于其中,便于其发生聚合反应,同时使形成的聚合物中产生多孔结构,有助于选择性空穴的构成.因此,溶剂应能对功能单体和模板都具有较好的溶解性,同时还不会对两者间的氢键相互作用产生显著影响.包括AMK 在内的氨基糖苷类物质在分子印迹中常用的溶剂如乙腈、二氯甲烷、氯仿等中的溶解度很小,而在THF 中有较好的溶解度,同时THF 对MAA 也有较好的溶解度,故THF 被用作溶剂之一.由于氨基糖苷类在水中有极好的溶解度,为充分发挥溶剂在反应中的作用,水也被用作溶剂.但是,水可对功能单体和模板间的氢键相互作用产生破坏,影响选择性空穴的形成,故其用量应进行优化.此外,溶剂功能单体或模板分子的配比决定了它们在溶剂中的浓度,当溶剂用量太小时,反应会趋向于本体聚合,反应物黏度增大,使得溶剂无法充分进入聚合网络中从而形成块状物;而当溶剂用量太大时,会使MIP强度降低,其孔状空穴结构不稳定,无法形成微球沉淀.因此,溶剂的配比和用量也至关重要,需对其进行优化.固定水的体积为1mL,使得水与THF 的体积比分别为1:4,1:5,1:6,1:7,1:8,1:9,向上述溶液中分别加入等量的阿米卡星0.05mmol和MAA 0.2mmol静置过夜,然后依次加入EGDMA 1mmol和AIBN 10 mg.按1.2 和1.4 的方法制备和测定,其中吸附实验所用AMK 溶液浓度为5 mmol/L,结果如图3所示.当溶剂用量为8mL(即水与THF的体积比1:7)时,聚合物微球吸附能力最好.

图2 功能单体用量对MIP吸附性能的影响(n=3)Fig.2 Effect of amount of the functional monomer on adsorption capacity of MIP(n=3)
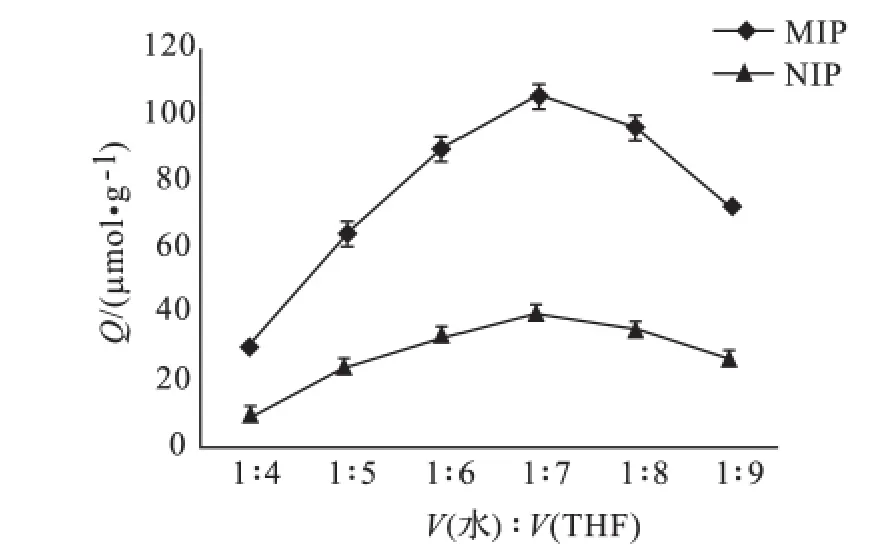
图3 溶剂的用量对MIP吸附性能的影响(n=3)Fig.3 Effect of solvent volume on adsorption capacity of MIP(n=3)
2.3 交联剂的用量
在制备MIP时,为了获得较高的专一性,需要使功能单体彼此聚合后的聚合物链之间具有一定的交联度,以形成聚合物网络.当交联剂用量太少时,形成的印迹空穴易变形,不能确保互补官能团的定位,使得其识别能力降低.而当交联剂用量太大时,所形成的聚合物刚性变强,不易溶胀,使识别位点减少,并且高度交联会阻碍分子传递,导致吸附量Q 降低.因此,需要对交联剂的用量进行优化.EGDMA 在MIP的合成中经常被用作交联剂,在AMK 用量为0.05mmol时,使其与EGDMA 物质的量比为1:10,1:15,1:20,1:25,1:30,在60℃下聚合24h,测定各聚合物的吸附性能,其结果如图4.当物质的量比为1:10时制得的MIP量较少,且吸附能力较弱,识别能力不强.随着交联剂用量增大,其MIP吸附量不断变化,并在物质的量比为1:20时出现最高峰.因此,选取模板分子与交联剂EGDMA的最佳物质的量比为1:20.
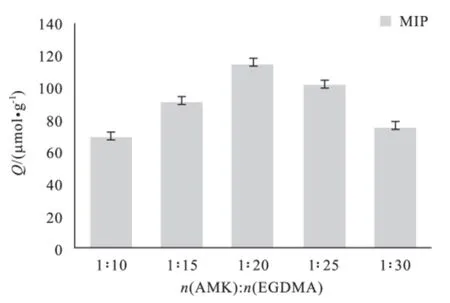
图4 交联剂用量对MIP吸附性能的影响(n=3)Fig.4 Effect of amount of EGDMA on adsorption capacity of MIP(n=3)
2.4 AMK 印迹微球的吸附等温线
MIP的吸附等温线可以反映模板分子平衡吸附量与溶液浓度变化的关系,为获得MIP中结合位点的类型和数量等重要信息提供基础数据.按照1.4所述方法测定常温下MIP对不同浓度AMK 的吸附情况,吸附时间20h,得到吸附等温线如图5 所示.结果表明,随着AMK 浓度的增大,MIP的吸附量逐渐增大.当AMK 浓度大于4.0mmol/L时,MIP曲线呈趋于平缓的状态.而在同浓度范围内,NIP 的吸附量随着AMK 浓度的增加而呈非饱和趋势增加.这表明MIP中确实形成了对AMK 具有特异选择性的吸附作用位点,NIP中则无此类位点.
2.5 AMK 印迹微球的Scatchard分析
分子印迹中常用Scatchard[13]方程来评价MIP的结合特性,其方程式如下:

其中,Q(μmol/g)为吸附量,Qmax是最大表观吸附量,c(mmol/L)为模板分子平衡浓度,Kd(mmol/L)为结合位点的平衡常数.在AMK 浓度范围内,以Q/c对Q 作图得图6,其呈现分段线性关系.

图5 MIP和NIP的吸附等温线(n=3)Fig.5 Adsorption isotherm of MIP and NIP(n=3)

图6 MIP吸附性能的Scatchard分析Fig.6 Scatchard anaiysis on adsorption capacity of MIP
分别对两段线性部分进行线性回归,可得方程

对照方程(2)可知,方程(3)和(4)的截距和斜率分别对应Qmax/Kd和-1/Kd,根据方程(3)可求得MIP对AMK 的高亲和力结合位点的Kd为1.244mmol/L,Qmax为85.99μmol/g;根据方程(4)可求得MIP低亲和力结合位点的Kd为15.385mmol/L,Qmax为596.48μmol/g.
2.6 AMK 印迹微球的吸附动力学曲线
吸附动力学曲线可以反映一定质量的MIP对固定浓度溶液中模板的吸附量随时间变化的情况以及不同时刻对模板吸附速率的情况,可为实际样品固相萃取方案的制定提供依据.参照1.4方法测定在不同时间后MIP对5mmol/L AMK 溶液的吸附量,结果如图7所示.MIP的吸附量随着时间的增加而逐渐增大,最终趋于平缓.随着时间的推移,空穴逐渐被AMK 分子所占据,并且在360min后达到饱和吸附,而NIP达到平衡所需的时间更短,这是因为其无特异性结合位点.因此,MIP的饱和吸附量要远远大于NIP的饱和吸附量.
2.7 AMK 印迹微球的IPB值
在分子印迹中,印迹效果也可以用IPB(imprinting-induced promotion of binding)值[14]进行评价,其表达式为

其中,QMIP(μmol/g)为MIP对于模板分子的吸附量,QNIP(μmol/g)为NIP 对于模板分子的吸附量.QMIP和QNIP相差越大,即IPB值越大,表明相比于NIP,MIP的效果越好.AMK 溶液浓度为5mmol/L 时分别测定MIP和NIP的吸附量,得IPB值为122.18%,说明特异性选择位点所产生的吸附量超过非选择性位点的吸附量,表明印迹效果良好.
2.8 AMK 印迹微球对氨基糖苷类抗生素的吸附选择性
MIP能否对同类抗生素产生选择性将决定其能否在该类抗生素多残留检测中用于样品的净化与富集.按1.4方法分别测定了MIP和NIP对5mmol/L链霉素、庆大霉素、卡那霉素、奈替米星以及妥布霉素溶液的吸附量,吸附20h,结果表明,MIP 和NIP吸附量(μmol/g)分别为61.5和28.3,55.6和26.9,89,2和33.8,82.0和31.3,72.1 和29.8.其中,MIP 对其吸附量分别为模板吸附量的53.9%,48.8%,78.2%,71.9%,63.2%,而NIP对测试的各氨基糖苷类的吸附量差别很小.说明NIP产生的吸附是非选择性的,而MIP对测试的各氨基糖苷类的吸附量主要来源于其中选择性吸附位点的作用,进而说明该MIP具有用于部分氨基糖苷类抗生素多残留固相萃取净化和富集的潜力.
2.9 AMK 印迹微球的重复使用性能
MIP的可重复使用性将决定其用于实际样品测定中的成本.MIP按1.4方法反复操作,再生次数为横坐标,吸附容量为纵坐标作图,得图8.图中显示,AMK 印迹微球经10次重复使用后,其吸附性能基本无下降,说明该MIP具备重复使用性能,可用作固相萃取柱填料.

图7 MIP和NIP的动态吸附曲线(n=3)Fig.7 Dynamic adsorption curve of NIP and MIP(n=3)

图8 使用次数对MIP吸附性能的影响(n=3)Fig.8 Effect of reuse times on adsorption of MIP(n=3)
2.10 AMK 印迹微球的形态
用原子力显微镜对AMK 印迹微球的形态进行观察,见图9.该图的宽度等效于显微镜视野中5μm 长度,由此可见,合成的印迹微球基本呈球形,粒径为0.3~0.5μm.

图9 MIP微球的原子力显微镜图像Fig.9 Image of MIP by atomic force microscope
3 结论
在优化条件下合成的微球形AMK MIP对模板分子展现了良好的特异吸附性能,对与AMK 结构类似的氨基糖苷类也表现出不同程度的特异吸附性能,具有用于氨基糖苷类抗生素多残留检测中样品净化和预富集前处理的潜力.
[1] 龙朝阳,许秀敏.动物源性食品中氨基糖苷类抗生素兽药残留分析[J].中国食品卫生杂志,2006,18(2):148-151.LONG Chaoyang,XU Xiumin.Delerminotion of aminoglycosides veterinary residues in animal foods[J].Chinese Joumal of Food Hygiene,2006,18(2):148-151.
[2] WOODWARD K N,SHEARER G.Chemical analysis for antibiotic used in agriculture[J].AOAC International,1995,3(5):426-432.
[3] GAUDIN V,CADIEU N,SANDERS P.Results of a European proficiency test for the detection of streptomycin/dihydrostreptomycin,gentamicin and neomycin in milk by ELISA and biosensor methods[J].Analytica Chimica Acta,2005,529(1):273-283.
[4] BAXTER G A,FERGUSON J P,O'CONNO M C,et al.Detection of streptomycin residues in whole milk using an optical immunobiosensor[J].Journal of Agricultural and Food Chemistry,2001,49(7):3204-3207.
[5] WALSH F,INGENFELD A,ZAMPICOLLI M,et al.Real-time PCR methods for quantitative monitoring of streptomycin and tetracycline resistance genes in agricultural ecosystems[J].Journal of Microbiological Methods,2011,86(2):150-155.
[6] 葛志容.食品中农业化学品残留限量[M].中国标准出版社,2006.
[7] 林维宣.各国食品中农药兽药残留限量规定[M].大连海事大学出版社,2002.
[8] 孙雷,张骊,黄耀凌,等.超高效液相色谱-串联质谱法检测动物源食品中8种氨基糖苷类药物残留[J].质谱学报,2009,30(1):60-64.SUN Lei,ZHANG Li,HUANG Yaoling,et al.Determination of aminoglycosides in foodstutts of animal origin by UBLCMC/MS[J].Fournal of Chinese Mass Spectrometry Society,2009,30(1):60-64.
[9] GONZáLEZ G P,HERNANDO P F,DURAND ALEGRíA J S.A morphological study of molecularly imprinted polymers using the scanning electron microscope[J].Analytica Chim Acta,2006,557(1-2):179-183.
[10] LOK C M,SON R.Application of molecularly imprinted polymers in food sample analysis-aperspective[J].International Food Research Journal,2009,16(2):127-140.
[11] LIU Yongliang,HE Yonghuan,Jin Yulong,et al.Preparation of monodispersed macroporous core-shell molecularly imprinted particles and their application in the determination of 2,4-dichlorophenoxyacetic acid[J].Journal of Chromatography A,2014,1323(1):11-17.
[12] FU Xuwei,WU Yanjiao,QU Jinrong.et al.Preparation and utilization of molecularly imprinted polymer for chlorsulfuron extraction from water,soil,and wheat plant[J].Environmental Monitoring and Assessment,2012,184(7):4161-4170.
[13] ZHOU Jie,HE Xiwen.Study of the nature of recognition in molecularly imprinted polymer selective for 2-aminopyridine[J].Analytica Chimica Acta,1999,381(1):85-91.
[14] HISHIYA T,SHIBATA M ,KAZU M,et al.Molecularly imprinted cyclodextrins as selective receptors for steroids[J].Macromolecules,1999,32(17):2265-2269.
