复方甘草酸苷联合丹参酮治疗中度痤疮的疗效观察
2015-07-12郑庆虎史玉玲
龚 瑜, 徐 徉, 郑庆虎, 史玉玲
(1. 同济大学附属第十人民医院皮肤科,上海 200072; 2. 第二军医大学附属长海医院皮肤科,上海 200433; 3. 解放军153中心医院皮肤科,河南 郑州 450042)
·临床研究·
复方甘草酸苷联合丹参酮治疗中度痤疮的疗效观察
龚 瑜1, 徐 徉2, 郑庆虎3, 史玉玲1
(1. 同济大学附属第十人民医院皮肤科,上海 200072; 2. 第二军医大学附属长海医院皮肤科,上海 200433; 3. 解放军153中心医院皮肤科,河南 郑州 450042)
目的 观察复方甘草酸苷联合丹参酮胶囊治疗中度寻常型痤疮的疗效与安全性。方法 79例中度寻常型痤疮患者随机分为两组。治疗组40例,口服复方甘草酸苷片和丹参酮胶囊;对照组39例,口服丹参酮胶囊。两组患者在口服药物同时均外用护肤粉刺霜。疗程均为8周。于用药前、用药后2、4、8周末分别记录面部各种皮损的实际数目、全身以及局部不良反应。并分别在用药前、用药后8周检测血清肿瘤坏死因子α(TNF-α)、白介素8(IL-8)、白介素10(IL-10)水平。结果 治疗8周后治疗组与对照组有效率分别为82.5%、60.52%(P=0.028),表明治疗组有效率明显高于对照组;复方甘草酸苷联合丹参酮治疗后痤疮复发率低、无明显不良反应。此外,治疗组患者血清IL-8水平由153.9±17.74pg/ml降为80.5±23.91pg/ml(P<0.01);TNF-α水平由45.3±6.49pg/ml下降到19.5±4.87pg/ml(P<0.01);IL-10水平由153.0±38.89pg/ml上升至261.3±15.60pg/ml(P<0.01)。对照组患者血清IL-8水平由156.2±18.40pg/ml下降为129.7±6.24pg/ml(P<0.01);TNF-α水平由46.5±7.46pg/ml下降为30.9±2.63pg/ml(P<0.01)。对照组血清IL-10水平在治疗前后无明显改变(P>0.05)。治疗后,治疗组血清IL-8、TNF-α的水平均较对照组显著降低(P<0.01)而治疗组IL-10的水平较对照组显著升高(P<0.01)。结论 复方甘草酸苷联合丹参酮是治疗中度寻常型痤疮安全、有效的方法,且具有调节患者血清TNF-α、IL-8、IL-10水平的作用。
痤疮; 复方甘草酸苷; 丹参酮; 炎症因子
寻常痤疮是一种皮肤科常见的累及毛囊皮脂腺的慢性炎症性皮肤病[1]。大约累及85%左右的青少年及40%以上的成年人。严重者产生囊肿和脓疮,治疗不当往往引起感染、色素沉着,影响患者生活质量。目前临床上治疗痤疮的方法很多,抗生素、维甲酸类药物、抗雄激素制剂等,这些药物对于大部分患者均能较好地控制病情,但对一些患者,尤其是育龄期患者,由于某些副作用导致临床应用受到不同程度的限制。我科于2012年6月至2013年12月对40例中度寻常型痤疮患者采用复方甘草酸苷联合丹参酮治疗,同时采用酶联免疫吸附法检测患者治疗前后血清中肿瘤坏死因子α(TNF-α)、白介素8(IL-8)、白介素10(IL-10)的水平,观察分析复方甘草酸苷联合丹参酮胶囊治疗中度寻常型痤疮患者的疗效以及对患者血清炎症因子水平的调节作用,报告如下。
1 资料与方法
1.1 一般资料
入选标准: 年龄18岁以上;临床表现符合中度寻常型痤疮Ⅱ~Ⅲ级(按照国际改良分级法)诊断标准;近1个月未系统使用抗生素及糖皮质激素,近8周内未系统使用维A酸类药物。排除标准: 妊娠及哺乳期妇女;有其它任何皮肤疾患或严重系统疾患;职业性或药物继发性痤疮。剔除标准: 在观察期间合并使用其他治疗痤疮药物者;资料不全者;无故失访者;由于药物不良反应终止治疗者,计入不良反应,但不计入总疗效统计。治疗组40例患者,男26例,女14例;年龄18~32岁,病程6个月~6年,治疗前患者皮损严重程度Ⅱ级23例,Ⅲ级17例。对照组39例患者,男20例,女19例;年龄18~34岁,病程5个月至7年;治疗前患者皮损严重程度Ⅱ级21例,Ⅲ级18例。两组患者年龄、病程以及疾病严重程度分级无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
治疗组口服复方甘草酸苷片(商品名: 美能,日本米诺发源制药株式会社生产)50mg,tid,口服丹参酮胶囊(河北兴隆希力药业有限公司)1g,tid,外用护肤粉刺霜(医院自制药物,主要成份为: 地塞米松、甲硝唑、氯霉素等),bid;对照组口服丹参酮胶囊(河北兴隆希力药业有限公司)1g,tid,外用护肤粉刺霜,bid。疗程均为8周,第2周末进行第一次复诊,第4周末进行第2次复诊,第8周末进行第3次复诊,分别记录患者面部炎症性皮损(丘疹、脓疱、结节)以及非炎症性皮损(白头、黑头粉刺)的数量,第8周疗程结束时观察其疗效。疗程结束后4周随访了解复发情况;对疗效以及不良反应进行评估登记。
1.3 疗效判定
基本痊愈: 皮损数量减少≥90%;显效: 60%≤皮损数量减少<90%;改善: 20%≤皮损数量减少<60%;无效: 皮损数量减少<20%。有效率=(基本痊愈例数+显效例数)/本组患者例数。
1.4 血清学检测
在治疗前及治疗第8周分别抽取治疗组和对照组患者清晨空腹静脉血,用酶联免疫吸附法(ELISA)测定血清白细胞介素-8(IL-8)、白细胞介素-10(IL-10)以及肿瘤坏死因子α(TNF-α)(上海文乐生物科技有限公司)的浓度。测定方法: 采用双抗体夹心ELISA法,严格按照试剂盒说明书步骤进行操作。
1.5 统计学方法
应用统计软件SPSS 13.0进行等级资料秩和检验、卡方检验和相关分析,计量资料以均数±标本差表示,两组间比较采用t检验。P<0.05为有统计学意义。
2 结 果
2.1 疗效
两组疗效比较见表1。治疗组有效率显著高于对照组(χ2=1.91,P<0.05)。
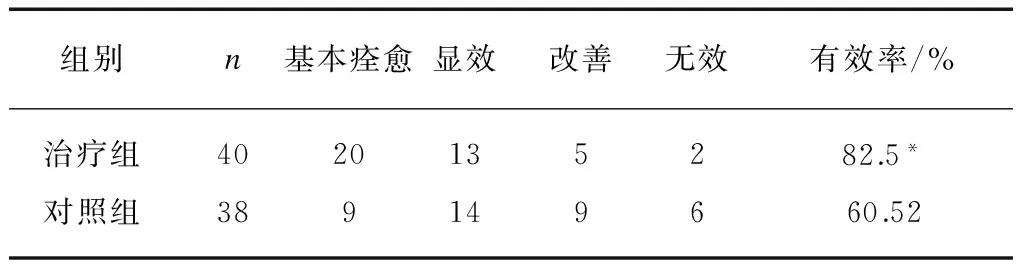
表1 两组治疗效果比较
注: 治疗组和对照组间有效率存在显著差异(χ2=1.91,*P<0.05)
2.2 不良反应
治疗组与对照组均未见明显不良反应,对照组有1例患者外用护肤粉刺霜后出现面部瘙痒,未予处理,停药后恢复正常。
2.3 血清学检测
治疗前治疗组与对照组血清IL-8、IL-10及TNF-α水平差异无统计学意义,治疗组与对照组治疗后血清IL-8、TNF-α水平较治疗前均明显降低,差异有统计学意义(P<0.01),见图1、2。同时治疗组在治疗后血清IL-8和TNF-α水平显著低于对照组治疗后的水平(P<0.01),见图1、2。治疗后治疗组血清IL-10水平显著高于对照组(P<0.01)且高于该组治疗前水平(P<0.01),见图3。

图1 治疗组与对照组治疗前后血清IL-8水平变化(*P<0.01)Fig.1 Changes of serum IL-8 levels after treatment in trial and control groups (*P< 0.01)

图2 治疗组与对照组治疗前后血清TNF-α水平变化(*P<0.01)Fig.2 Changes of serum TNF-α levels after treatment in trial and control groups (*P< 0.01)
对照组和治疗组在治疗后血清IL-8的水平均较治疗前显著降低(*P<0.01);两组在治疗后,血清IL-8的水平在治疗组较对照组降低更为显著(*P<0.01)。
治疗组和对照组在治疗后血清TNF-α的水平均较治疗前显著降低(*P<0.01);治疗后,治疗组血清TNF-α的水平较对照组降低更为显著(*P<0.01)。

图3 治疗组与对照组治疗前后血清IL-10水平变化(*P<0.01)Fig.3 Changes of serum IL-10 levels after treatment in trial and control groups (*P< 0.01)
治疗组血清IL-10的水平在治疗后较治疗前显著升高(*P<0.01);对照组血清IL-10的水平在治疗前后未见显著差异(P>0.05);治疗组治疗后血清IL-10的水平较对照组治疗后的水平显著升高 (*P<0.01)。
2.4 随访
治疗组中基本痊愈20例,显效13例,随访4月内29例未见复发,4例分别在停止治疗后2~4个月复发,复发率为12.1%。复发皮疹均较治疗前减轻,患者继续口服复方甘草酸苷联合丹参酮治疗仍有良好效果;对照组中基本痊愈9例、显效14例,停止治疗后1~3个月复发7例。复发率30.4%。
3 讨 论
痤疮是一种毛囊、皮脂腺结构的慢性、炎症性皮肤病。它是一种多因素疾病,其发病主要与皮脂腺大量分泌、痤疮丙酸杆菌的增殖、毛囊皮脂腺导管的角化异常和炎症等因素有关。据统计,全世界约有80%~90%的人口在某个时期患有不同程度的痤疮。主要表现为黑、白头粉刺、炎性丘疹、脓疱、结节、囊肿。易形成色素沉着、毛孔粗大,甚至瘢痕损害,影响美容甚至导致毁容,给患者造成极大的心理压力和精神痛苦。痤疮的病程从3个月到5~40年不等,并且有80%的患者30岁前均不能自愈[2]。本病的治疗方法较多。常用治疗方法包括维甲酸类、过氧化苯甲酰、抗生素、激素类药物治疗等,但均有一定的局限性,药效因人而易,易致耐药且有潜在的毒副作用,尤其对育龄期男女生育有所影响。
复方甘草酸苷片(美能)是日本从甘草中提取的一种含甘草酸苷、甘氨酸、盐酸半胱胺酸的复合物,其主要成分甘草酸苷具有抗雄激素活性、抗炎活性及免疫调节等作用。中药丹参性微寒、味苦、无毒,有活血、通络、凉血、消肿等功效。丹参酮胶囊内的隐丹参酮为其主要成分,具有广谱抗菌作用,能够杀灭痤疮棒状杆菌、白色葡萄球菌等痤疮致炎性微生物,抑制皮脂过多分泌,且是一种温和的雌性激素样物质,并有抗雄性激素样作用本研究发现固酮的灭活,从而发挥类固醇样作用。本研究应用复方甘草酸苷联合丹参酮胶囊治疗中度寻常型痤疮,标本兼治,有效率为82.5%,明显高于对照组(60.5%),两组比较差异有统计学意义(P=0.028)[3]。
如上所述,痤疮是一种多因素疾病,其发生与雄激素代谢、毛囊口异常角化及痤疮丙酸杆菌大量繁殖等多种因素有关。临床治疗上,多采用消炎杀菌、调节激素水平、改善毛囊口异常角化等措施,控制炎症是治疗痤疮的关键环节。痤疮丙酸杆菌、促炎因子、脂质、白三烯B4过氧化物酶激活受体-α及神经因素等均可能与痤疮炎症有关。在寻常痤疮的组织病理中发现真皮有大量的淋巴细胞、单核细胞等炎细胞的浸润,当皮脂腺导管破裂后大量的中性粒细胞聚集形成了微脓肿,而随后的肉芽肿形成和纤维化增殖导致了痤疮结节的形成。研究还表明即使在痤疮发生的早期已有大量的多核巨细胞在皮脂腺单元周围聚集,在皮脂腺单元被破坏前已存在大量的中性粒细胞的聚集,表明炎症以及一些炎细胞的趋化因子等参与了痤疮的发生发展过程另外,痤疮丙酸杆菌能刺激单核细胞产生大量的前炎症因子,IL-8以及TNF-α[4]。课题研究中发现治疗组和对照组在治疗后IL-8、TNF-α的水平均较治疗前有所下降,这表明丹参酮和复方甘草酸苷均能通过抑制炎症因子的产生而达到抗炎的治疗效果。另外,研究发现治疗组患者血清中的IL-10水平在治疗后较治疗前明显增高,而对照组治疗前后IL-10的水平没有显著改变。IL-10主要是由Th2细胞、B淋巴细胞、单核巨噬细胞分泌,是一种细胞因子合成抑制因子,与Th2免疫应答有密切关系,可抑制Th1细胞增殖及Th1细胞介导的细胞免疫应答。IL-10抑制促炎性细胞因子的合成与释放,具有重要的抗炎作用;抑制巨噬细胞的活化[4]。因此,本课题研究表明复方甘草酸苷联合丹参酮的治疗不仅能降低患者血清中促炎因子(IL-8、TNF-α)的水平,还能增加抑炎因子IL-10的水平,更大承担的发挥抗炎作用而治疗痤疮。
综上所述,复方甘草酸苷联合丹参酮治疗中度寻常型痤疮安全有效,推测其可能通过抑制促炎因子的产生,促进抗炎因子的产生从而达到治疗痤疮的目的。
[1] 赵辨.临床皮肤病学[M].4版.南京: 江苏科学技术出版社,2010.
[2] Gollnick H, Cunliffe W, Berson D, et al. Management of acne: a report from a Global Alliance to improve outcomes in acne[J]. J Am Acad Dermatol, 2003,49(1 Suppl): S1-S37.
[3] Sugisaki H, Yamanaka K, Kakeda M, et al. Increased interferon-gamma, interleukin-12p40 and IL-8 production in Propionibacterium acnes-treated peripheral blood mononuclear cells from patient with acne vulgaris: host response but not bacterial species is the determinant factor of the disease[J]. J Dermatol Sci, 2009,55(1): 47-52.
[4] 唐艳琼,瞿焱.异维A酸对重度痤疮患者可溶性IL-2R和IL-10的影响[J].中国麻风皮肤病杂志,2012,28(1): 23-25.
Efficacy of tanshinone capsule combined with compound glycyrrhizin in treatment of moderate vulgaris acne
GONGYu1,XUYang2,ZHENGQing-hu3,SHIYu-ling1
(1. Dept. of Dermatology, Tenth People’s Hospital, Tongji University, Shanghai 200072, China; 2. Dept. of Dermatology, Changhai Hospital, Second Military Medical University of PLA, Shanghai 200433, China; 3. Dept. of Dermatology, No.153 Hospital of PLA, Zhengzhou 450042, China)
Objective To assess the therapeutic efficacy and safety of tanshinone capsule combined with compound glycyrrhizin in treatment of moderate vulgaris acne. Methods Seventy nine patients with moderate vulgaris acne were randomly assigned to trial group (n=40) or control group (n=39). Patients in trial group were treated with tanshinone capsule combined with tablet compound glycyrrhizin, and those in control group received tanshinone capsule alone. The hospital-prepared skin acne cream was locally applied onto the eruptions for patients in both groups. The course of treatment in both groups lasted for 8 weeks. The number of lesions and adverse reactions were recorded before and after 2,4,8 week of treatment. The serum levels of tumor necrosis factor α (TNF-α), interleukin-8 (IL-8) and interleukin-10 (IL-10) were detected before and after treatment. Results The overall effective rate was 82.5% in trial group and 60.52% in control group (P=0.028) after the therapy,respectively. In trial group, recurrence rate was lower and no major adverse reactions were encountered. In trial group the serum IL-8 levels were decreased from 153.9±17.74 pg/ml to 80.5±23.91 pg/ml (P<0.01), TNF-α levels decreased from 45.3±6.49 pg/ml to 19.5±4.87 pg/ml (P<0.01); IL-10 levels increased from 153.0±38.89 pg/ml to 261.3±15.60 pg/ml (P<0.01). In control group, the serum IL-8 levels were decreased from 156.2±18.40 pg/ml to 129.7±6.24pg/ml (P<0.01); TNF-α levels decreased from 46.5±7.46 pg/ml to 30.9±2.63 pg/ml (P<0.01); however, there was no change in IL-10 levels after treatment (P>0.05). After treatment, the IL-8 and TNF-α levels in trial group was lower than control group (P<0.01), and IL-10 levels was higher than control group (P<0.01). Conclusion Tanshinone capsule combined with compound glycyrrhizin is safe and effective in treatment of moderate vulgaris acne, which may be associated with its regulative effects on serum IL-8, IL-10 and TNF-α in the patients.
acne; compound glycyrrhizin; tanshinone; inflammatory factor
10.16118/j.1008-0392.2015.03.024
2014-07-4
龚 瑜(1985—),女,住院导师,硕士研究生.E-mail: 76464241@qq.com
史玉玲.E-mail: shiyuling1973@126.com
R 246.7
A
1008-0392(2015)03-0109-04
