溶胶凝胶辅助水热可控合成ZnO不同形貌分级结构光催化剂
2015-06-01武广利赵晓华李珍珍李彩珠娄向东
武广利 赵晓华 李 萌 李珍珍 李彩珠 娄向东
(河南师范大学化学与化工学院,新乡453007)
溶胶凝胶辅助水热可控合成ZnO不同形貌分级结构光催化剂
武广利 赵晓华 李 萌 李珍珍 李彩珠 娄向东*
(河南师范大学化学与化工学院,新乡453007)
以Zn(NO3)2·6H2O、柠檬酸和NaOH为原料,采用溶胶凝胶(sol-gel)辅助水热法,仅通过改变水热时间,就可得到片花、棒花及梭状3种不同形貌ZnO分级结构。利用XRD、SEM、UV-Vis DRS、光致发光光谱(PL)和氮低温吸附-脱附等手段对合成的ZnO样品进行了表征。推测了合成条件下不同形貌ZnO分级结构形成的机理。以活性翠兰(KGL)为模拟印染废水,考察了其光催化活性。结果表明,虽然所合成的不同形貌的ZnO样品在光照120 min后均能使KGL降解78%以上,但其中水热4 h得到的片花状ZnO光催化性能最好,可降解99%的KGL,这与其片花状的形貌、较大的比表面积、较多的表面氧缺陷和极性面有关。
sol-gel辅助水热法;ZnO;形貌;分级结构;光催化
光催化降解染料废水因具有催化活性高、降解彻底、不产生二次污染等优点而备受重视,已成为水处理领域的研究热点[1]。当光催化剂被能量等于或大于其带隙能的光照射时,受激发电子从价带跃迁至导带,同时在价带处留下光生空穴,水体中的有机污染物就会在光催化剂的表面与光生电子或空穴发生一系列的氧化还原反应而被降解[2]。因此,在光催化过程中,选择高性能的光催化剂非常重要。
ZnO作为一种宽禁带(3.37 eV),高激子能(60 meV)的半导体氧化物因具有无毒、制备工艺简单、形貌易控、价格低廉、可塑性强等优点,而备受人们关注[3]。为了提高ZnO的光催化性能,人们采取各种措施,如改变形貌[4-5]、对其掺杂[2,6]、复合[7]等,其中改变形貌是一种简单易行却很重要的手段。迄今,人们已经利用各种方法合成了不同形貌的ZnO光催化材料,如棒状[5]、线状[5]、球状[8]、管状[9]、哑铃状[10]及花状[6]等。相对于低维结构,3D分级结构的ZnO在光催化过程中可以提供相对较大的比表面积,能更有效的防止颗粒聚集,因而可以加强光催化活性[6]。在合成ZnO 3D分级结构的众多方法中,水热法是应用较多的一种方法,在水热过程中,人们常通过改变原料来源[4,11]、原料配比[11-12]、水热温度[11-12]等手段获得不同的分级结构,而对于水热时间的研究主要是为了了解某种特定形貌的生长机理。如本课题组曾采用sol-gel辅助水热法制备ZnO光催化剂,研究了pH值、水热时间、水热温度等因素对ZnO形貌及光催化性能的影响[13-14],发现在反应物配比不变的情况下,改变溶液的pH值,ZnO光催化剂形貌会发生变化,光催化性能随之改变;当固定pH=14时,无论改变水热温度,还是水热时间,ZnO光催化剂均为3D片花状形貌,该形貌具有良好的光催化性能。为了进一步研究该方法中原料配比及pH值对产物形貌及性能的影响,课题组改变原料配比,发现在新的配比条件下当pH=13时,仅改变水热时间就能得到片花状、棒花状和梭状3种不同分级结构的ZnO,这与之前的研究结果即随着水热时间变化ZnO形貌逐渐完善但基本不变是不同的。目前文献中关于随着水热时间变化,晶体从一种形貌发生显著改变形成另一种形貌,主要生长晶面随之发生变化的研究鲜有报道。
因此,本工作研究了不同水热时间下得到的片花状、棒花状和梭状不同分级结构的ZnO的光催化性能,并对其生长机理进行了推测。结果表明,所获得的不同形貌的ZnO均能较好的降解活性翠蓝KGL,但水热4 h得到的片花状ZnO光催化性能最好,这与其形貌、比表面积、表面氧缺陷浓度及极性面等有密切关系。
1 实验部分
1.1 ZnO不同分级结构的制备
将硝酸锌(Zn(NO3)2·6H2O,国药集团化学试剂有限公司,分析纯)与柠檬酸(C6H8O7·H2O,国药集团化学试剂有限公司,分析纯)按物质的量之比为nZn(NO3)2·6H2O∶n柠檬酸=1∶4混合溶解在100 mL去离子水中,70℃加热搅拌形成溶胶后,在干燥箱中对其进行干燥,100℃形成凝胶。将NaOH(天津市德恩化学试剂有限公司,分析纯)溶液逐滴加入凝胶中搅拌,至pH=13停止,形成悬浊液。将悬浊液转移入带有聚四氟乙烯内衬的水热釜中,保持120℃恒温不变,水热时间分别设定为0、4、8、12及17 h,反应停止后自然冷却至室温。产物经离心、洗涤、干燥后即可得到具有不同分级结构的氧化锌产品。对应于不同水热时间制备的样品分别标记为Z-0、Z-4、Z-8、Z-12及Z-17。
1.2 样品表征
采用X射线衍射仪(XRD,德国D8 Advance Bruker公司)测定样品的晶体结构(Cu Kα1辐射,λ= 0.154 06 nm,电压40 kV,电流100 mA);采用扫描电镜(SEM,日本JEOL JSM-6390LV)观察样品的形貌;采用UV-1700 PharmaSpec紫外-可见分光光度计表征样品的光吸收特性;采用Lambda 950型UV-Vis分光光度计检测样品的UV-Vis漫反射波谱(DRS);采用SHIMADZU RF-5301PC型荧光光谱仪检测样品的荧光光谱(PL),激发波长λ=350 nm;采用Quantachrome NovaWin2型比表面分析仪(BET)对样品进行低温氮吸附/脱附,测定样品的比表面积。
1.3 光催化性能测试
将一定浓度的活性翠兰KGL溶液250 mL放入光催化反应器,加入100 mg催化剂样品。在磁力搅拌作用下,暗反应20 min,使光催化剂分散均匀并达到吸附-脱附平衡。以300 W高压汞灯作为光源(λmax=365 nm)。光照开始后,每隔20 min取样一次,取样后立即进行离心分离。用UV-5100紫外可见分光光度计在其最大波长处测定上清液的吸光度值。以染料溶液的脱色率D表示该样品的催化活性:
1.4 COD的测定
光催化降解反应前后染料液的COD测定采用国标(GB 11914-1989)重铬酸钾法,COD去除率(%)=其中,COD0和CODt分别是初始染料液和反应t时刻染料液的化学需氧量,mg·L-1。
2 结果与讨论
2.1 样品结构与形貌的表征
图1a是不同水热时间制备样品的XRD图。通过与标准图对照,各样品的衍射峰与标准图中六方纤锌矿ZnO(PDF No.36-1451)衍射峰的位置完全吻合,无其他杂质峰存在,表明制备的样品均为ZnO,包括不经过水热反应(水热时间为0 h)制备的样品。随着水热时间的延长,样品衍射峰的强度在逐渐增强,半峰宽逐渐变窄,这说明随着水热时间的延长,ZnO样品的结晶度逐步提高。从图中还可以看出不同水热时间得到的样品中(100)、(002)、(101)晶面相对强度也不一样,这是由于所得样品形貌不同引起的[15],样品Z-0、Z-4、Z-8、Z-12及Z-17中(002)极性面与(100)非极性面强度之比I(002)/I(100)分别约为0.8、1.0、0.7、0.4、0.4,高的I(002)/I(100)比值在一定程度上反映出晶体中存在相对大的极性面[3]。

图1不同水热时间制备ZnO样品的XRD图(a)及SEM图:Z-0(b);Z-4(c);Z-8(d,e,f);Z-12(g);Z-17(h)Fig.1 XRD patterns(a)and SEM images of Z-0(b);Z-4(c);Z-8(d,e,f);Z-12(g);Z-17(h)
图1 b-h分别是不同水热时间制备的ZnO样品的SEM图。根据XRD结果可知,虽然0 h得到的也是ZnO,但此时的样品无特定形貌,仅由一些纳米片无序组成(图1b)。当水热时间延长至4 h(图1c)时,这些纳米片相互交叉,形成直径约为4 μm的片花状ZnO。随着水热时间延长至8 h(图1d),片花状形貌已经消失,取而代之的是棒花状形貌及一些散落的棒,这些棒呈顶部较尖的六棱柱状。在水热时间为8 h的样品中时常还可以看到图1e和图1f所示的形貌,总体呈花状,但“花瓣”由底部粘连,前端已经出现分叉的厚片,或底部粘连,前端呈六棱柱状的棒组成,这应该是样品从片花状形貌向棒花状形貌转变时的一种过渡形貌。继续延长水热时间至12 h(图1g),过渡形貌已经完全消失,留下的是棒花状的形貌,以及从棒花上散落的组合棒,这些棒的顶端较尖。当水热时间进一步延长至17 h(图1h)时,棒花状的形貌基本消失,棒完全从棒花结构中脱落,呈两端均尖的六棱柱结构即梭状结构,这些梭棒长度为3~4 μm,直径约为1 μm。由此可见,在本实验条件下,随着水热时间的变化,ZnO的形貌发生显著变化,对应的晶面生长也相应发生变化,这与XRD表征结果中不同晶面的比值发生变化相一致,也将对ZnO的光催化性能产生影响。
2.2 不同形貌ZnO分级结构形成机理
根据以上表征结果,结合有关文献,分析不同形貌ZnO分级结构随着水热时间变化的形成机理如下(图2):首先,在溶胶过程中,锌离子和柠檬酸发生配位作用生成锌离子-柠檬酸的配合物(Zncitric acid chelate complexes)[12]。之后,当NaOH溶液逐滴加入到凝胶后,凝胶会发生部分水解。在此过程中,一部分OH-离子与柠檬酸提供的H+离子发生中和反应,另一部分OH-离子则可能与锌离子-柠檬酸配合物反应生成[Zn(OH)4]2-生长基元,而[Zn(OH)4]2-生长基元在溶液中易分解形成ZnO晶核[16],方程式如下:
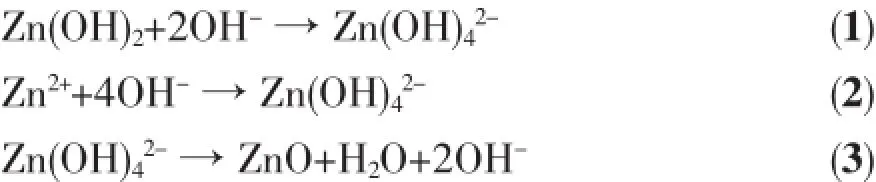
由于ZnO的各向异性,其各个晶面的生长速率依次为:v[001]>>v[010]>>v[001][4,16]。因此,通常情况下制备出的ZnO易沿c轴生长形成六棱棒状。但在本实验的初始阶段,由于加入大量NaOH(pH=13),溶液中会存在大量的OH-以及柠檬酸根离子,这些带负电荷的OH-和柠檬酸根离子会吸附在带正电荷的Zn (001)面,使得ZnO在c轴方向的生长受到抑制,从而沿着[001]和[010]方向在(210)面内生长,形成片状结构的ZnO[11]。因此不经过水热反应也可得到图1b所示的片状ZnO晶体。而经过水热过程,在表面能和静电力的驱使下,这些片状的ZnO晶体相互交错形成片花状结构[17](图1c)。结合XRD结果,Z-4样品中(002)极性面与(100)非极性面之比I(002)/I(100)约为1.0,说明此时片花状的ZnO样品中存在较多的极性面,而这些极性面是高活性的,在水热环境下不稳定,这与之前采用该方法(nZn(NO3)2·6H2O∶n柠檬酸=1∶2,pH= 14)[14]获得片花状ZnO的生长过程很相似。但是在本工作的水热过程中ZnO形貌发生了显著变化,这可能是柠檬酸用量增加(nZn(NO3)2·6H2O∶n柠檬酸=1∶4)及溶液pH值(pH=13)降低引起的。其原因是随着水热时间的延长,锌离子-柠檬酸配合物不断释放锌离子,这些锌离子与溶液中的OH-不断形成新的[Zn(OH)4]2-生长基元,同时由于OH-的逐渐消耗,c轴方向的抑制逐渐消除,导致极性面将会逐渐减少,对应的形貌也就会发生变化,所以,水热反应8 h时,可以看到一些过渡形貌出现(图1e,f),片状结构逐渐消失,择优取向生长方向表现出来,棒状结构逐渐出现,是晶体溶解后再结晶的结果。由于棒花状结构的顶端ZnO与溶液中OH-离子的接触较多,易导致分解,从而产生棒顶部的尖端结构[18](图1d)。因此,水热8 h后,ZnO的极性面与非极性面的比值I(002)/I(100)降为0.7。当水热时间延长至12 h,片花结构已经完全转变为棒花结构,且在水热环境下,为了保持表面能最小,一部分棒从棒花结构的连接处脱落(图1g)。当水热时间进一步延长至17 h时,棒基本完全从棒花上脱落,同时在溶液中,棒脱落处的那一端(未形成尖端的)与过量的OH-离子的接触、腐蚀,最终导致两端较尖的梭状ZnO的形成(图1h)。

图2 不同形貌ZnO的形成机理示意图Fig.2 Schematic illustration for the formation mechanism of the ZnO with different morphologies
2.3 样品的光学特性
由于0 h制备的样品无特定形貌且结晶度稍差,故以下不对其进行进一步的表征和测试。图3a是不同水热时间得到的不同形貌ZnO样品的UVVis漫反射光谱图,从图中可以看出,所有样品均在375 nm附近有明显的吸收峰,该峰对应于ZnO的本征吸收,进一步说明所合成的样品为ZnO[19],与XRD结果相一致。图3b是不同水热时间ZnO样品的室温光致发光(PL)光谱,从图中可以看出,4种样品均在紫外光和可见光区出现2种发射峰,一种在紫外区380 nm附近,主要对应于ZnO的带边发射,另一种在400~650 nm蓝绿黄可见光区,主要对应于ZnO的表面氧缺陷[20],PL峰强度越强,代表氧缺陷浓度越高[3],光生电子-空穴对的寿命越长,越有利于光催化性质的提高,从图中可以看出,Z-4样品的PL强度最强,因此,在所测试的4种样品中有可能其光催化性能将最好。
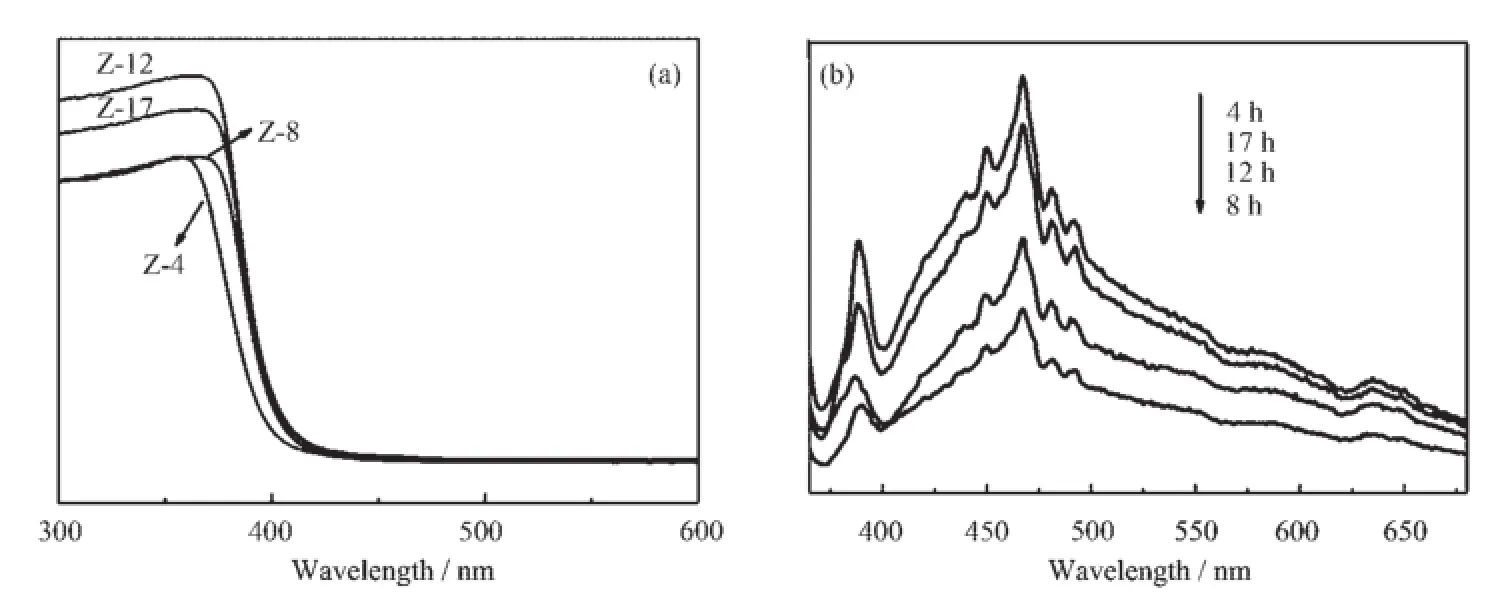
图3 不同形貌ZnO样品的(a)UV-Vis漫反射光谱图(b)荧光光谱图Fig.3 UV-Vis diffuse reflectance spectra(a)and PL patterns(b)of ZnO samples with different morphologies
2.4 光催化性能
为了研究所合成的ZnO样品在染料废水处理方面的潜在应用,以新乡市印染厂的活性翠兰KGL染料为模拟降解对象,对Z-4、Z-8、Z-12及Z-17样品进行光催化性能测试。图4a为不同样品在120 min内对20 mg·L-1活性翠兰KGL的光催化降解效率图。从图中可以看出,仅有光照或催化剂,活性翠兰KGL脱色率变化很少,可以忽略。但在既有光照又有催化剂的前提下,随着光催化时间的延长,染料脱色率逐渐增大。在120 min时,Z-4、Z-8、Z-12及Z-17对染料的光催化降解脱色率分别为99%,78%,83%和95%。可见,所合成的ZnO样品均对KGL有较好的光催化降解效果,其中,Z-4即片花状的ZnO具有最好的光催化效果,梭状的Z-17和棒花状的Z-12光催化效果次之,具有过渡形貌的Z-8样品效果相对较差。与之前本课题组所合成的片花状ZnO相比[14],在同样水热4 h的合成条件下,Z-4具有更高的光催化性能,这可能与其具有较高的比表面积有关(本实验条件下各样品的BET比表面积测试结果见表1)。图4b为120 min光照后各样品对不同浓度活性翠兰KGL的光催化降解效率图。可以看出,120 min光照后各样品均能很好的降解10 mg·L-1活性翠兰KGL。实验过程中发现Z-4、Z-12、Z-17样品则分别在光照80、120、100 min后就能使活性翠兰100%脱色。当染料液浓度增加到30 mg·L-1时,各样品对染料的脱色率均有所下降。这可能是由于染料浓度增大,一方面导致过多的染料分子吸附在ZnO表面有效活性位点上,阻抑了光催化反应过程;另一方面导致溶液的透光率减小,从而使ZnO对紫外光的利用率降低[21]。虽然随着染料液浓度的增加,各样品对染料的脱色率有所下降,但是这几种样品对染料的降解能力顺序不变,即Z-4>Z-17>Z-12>Z-8。图4c是以Z-4为光催化剂,光催化降解20 mg· L-1活性翠兰KGL的紫外-可见吸收光谱随时间的变化图。由图可知,随着反应时间的延长,活性翠兰KGL在最强吸收608 nm处的峰强度逐渐减弱,说明活性翠兰KGL分子结构被逐渐破坏,光照120 min后,溶液的吸收峰基本消失,活性翠兰KGL溶液基本脱色,说明活性翠兰KGL的发色基团被完全破坏。图4d为120 min光照后20 mg·L-1活性翠兰KGL的COD去除率。由图可知,光照120 min后各样品对KGL的COD去除率也不相同,其中Z-4样品对染料的COD去除率最高,结合脱色率结果,可以看出样品对染料的脱色降解率越高,COD去除率也就越大。但样品对染料COD的去除率皆低于其脱色率,表明经过光催化反应,KGL的发光基团被破坏,但是这些破坏的基团并没有完全矿化,只有一部分染料分子被分解为无机小分子。
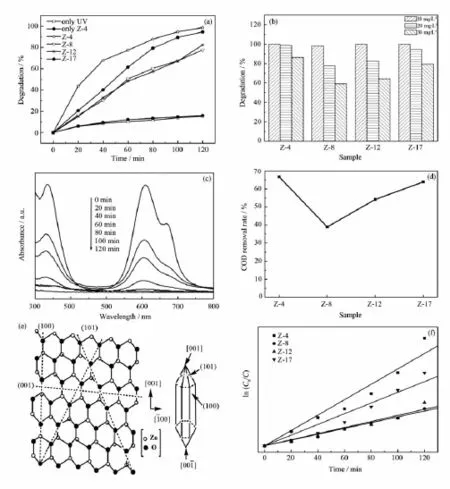
图4 (a)不同条件下光催化降解20 mg·L-1活性翠兰KGL溶液效果图,(b)光催化120 min后不同浓度活性翠兰KGL的降解效果比较,(c)不同时间Z-4样品光催化降解20 mg·L-1活性翠兰KGL的紫外-可见吸收谱,(d)光催化120 min后20 mg·L-1活性翠兰溶液COD的去除率,(e)六方纤锌矿ZnO晶体沿[120]晶面原子堆积模型和梭状ZnO晶面,(f)一阶线性动力学曲线Fig.4 (a)Photocatalytic degradation of 20 mg·L-1KGL at different conditions,(b)Comparison of degradation rate with different initial concentrations of KGL,(c)Time-dependent absorption spectra of 20 mg·L-1KGL solution in the presence of Z-4 sample after UV irradiation,(d)The COD removal rate of 20 mg·L-1KGL after 120 min photocatalytic degradation, (e)Atomic stacking model of wurtzite ZnO project along[120]and schematic illustration of the morphology models for spindle-like ZnO,(f)Pseudo-first order kinetics of the as-prepared ZnO samples
影响ZnO样品光催化性能的因素很多,如形貌、比表面积、表面氧缺陷、极性面等[16]。在本工作中,水热时间4 h合成的ZnO(Z-4)光催化效率之所以优于其它水热时间下的ZnO样品,可能是由以下几方面原因综合作用的结果。
(1)形貌与比表面积。由前面的SEM结果可知,水热4 h后得到的ZnO(Z-4)为片花结构,该结构是由诸多纳米片相互交叉形成,与其它水热时间得到的Z-8、Z-12、Z-17样品相比较而言,这些纳米片之间有较大的空隙,这样的结构一方面可以有效的防止颗粒之间的团聚以及纳米片之间的重叠,另一方面又能提供较大比表面积,以增大光催化剂与染料溶液的接触面积,提供更多的活性位点,从而提高其光催化活性[16]。BET比表面积测试结果(表1)也证明了这4种样品中Z-4具有最大的比表面积(14 m2· g-1),Z-17次之,而Z-8最小(<1 m2·g-1)。
(2)表面氧缺陷。表面氧缺陷被认为是ZnO的有效活性位点[5]。原因是适当数量的氧缺陷可以捕获ZnO中的光生电子,降低其与光生空穴的复合几率,使光生空穴能够扩散至ZnO表面,从而氧化降解有机染料。在2.3部分已提及室温光致发光(PL)光谱来可以表征ZnO表面氧缺陷的浓度。ZnO样品的PL峰强度越强,代表氧缺陷浓度越高[3],越有利于光催化性质的提高,在图3b中,4种样品的PL强度依次为Z-4>Z-17>Z-12>Z-8,与光催化测试结果吻合,说明表面氧缺陷浓度在该光催化反应中起主要作用。
(3)极性面。近年来不断有文献报道,具有高表面能极性面的光催化剂相应的具有较高的光催化活性。在ZnO的不同晶面中,(001)面具有最高的表面能[4],因此,在4个样品中具有较多(001)极性面的ZnO样品应具有较高的光催化活性。在前面2.2部分ZnO不同形貌形成机理中,已分析过片花状的Z-4样品具有较多的(001)面,而梭状的Z-17样品主要由(100)和(101)面组成(图4e)。其中,(100)晶面是由等量的Zn2+和O2-离子组成的,为非极性面,具有较低的表面能和化学活性。(101)晶面是由O2-离子组成,为带负电的极性面,在光催化反应过程中(101)晶面吸附O2的能力相对较弱[22],相应的光催化性能也会相对稍差一些。这一点可以从前面2.1部分XRD分析结果得到证明,Z-4、Z-8、Z-12及Z-17中(002)极性面与(100)非极性面强度之比I(002)/I(100)分别约为1.0、0.7、0.4和0.4,因此,Z-4在4个样品中具有相对多的(001)极性面,光催化性质也就最好。
(4)从动力学角度分析。由于光催化降解时,活性染料的浓度较低,因此可采用一阶动力学方程来描述该光催化反应动力学过程:

上式中,k表示一阶反应速率常数[4]。图4f为四种样品光催化降解20 mg·L-1活性翠兰KGL动力学曲线图,对应的k值列于表1,从表1中可以看出,采用不同样品做光催化剂降解活性翠兰KGL时,k值也明显不同,Z-4样品对应的k值最大,Z-8最小,其中,Z-4的k值约为Z-8的3倍,因此其光催化效率明显高于Z-8。
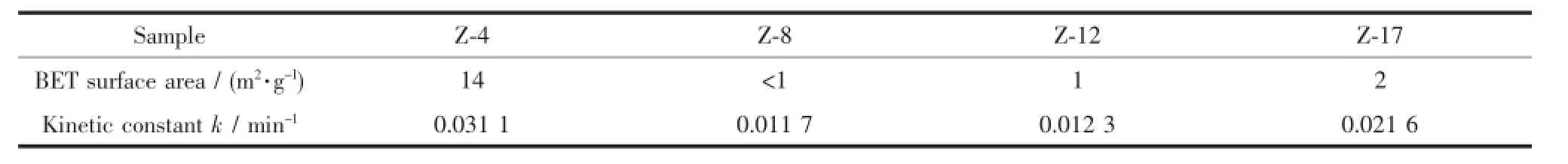
表1 不同形貌ZnO光催化剂比表面积及降解速率常数的比较Table1 Specific surface area and photodegradation rate constant of ZnO photocatalysts with different morphologies
3 结论
采用sol-gel辅助水热法,在120℃水热温度下,利用不同水热时间制备了片花、棒花以及梭状不同形貌的ZnO分级结构。通过对其光催化性能测试发现,所合成的不同形貌ZnO在光照120 min后均能使活性翠兰KGL降解78%以上,但水热反应4 h后制备的片花状ZnO光催化效率最好。所合成样品的光催化性能与其形貌、比表面积、表面氧缺陷及极性面有显著关系。
[1]Gupta V K,Ali I,Saleh T A,et al.RSC Adv.,2012,2(16): 6380-6388
[2]Lang X J,Chen X D,Zhao J C.Chem.Soc.Rev.,2014,43 (1):473-486
[3]Lu Y C,Wang L L,Wang D J,et al.Mater.Chem.Phys., 2011,129(1):281-287
[4]Xu L P,Hu Y L,Pelligra C,et al.Chem.Mater.,2009,21 (13):2875-2885
[5]Liu Y,Kang Z H,Chen Z H,et al.Cryst.Growth Des.,2009, 9(7):3222-3227
[6]Lai Y L,Meng M,Yu Y F.Appl.Catal.B:Environ., 2010,100(3):491-501
[7]WU Zhen-Yu(吴振玉),LI Feng-Jie(李奉杰),LI Cun(李村), et al.Chinese J.Inorg.Chem.(无机化学学报),2013,29(10): 2091-2098
[8]CAI Feng-Shi(蔡锋石),WANG Jing(王菁),SUN Yue(孙悦), et al.Chinese J.Inorg.Chem.(无机化学学报),2011,27(6): 1116-1120
[9]Sun Y,Fuge G M,Fox N A,et al.Adv.Mater.,2005,17(20): 2477-2481
[10]Sun J H,Dong S Y,Wang Y K,et al.J.Hazard.Mater., 2009,172(2/3):1520-1526
[11]Sun Y G,Hu J Q,Wang N,et al.New J.Chem.,2010,34 (4):732-737
[12]Zhang H,Yang D R,Li S Z,et al.Mater.Lett.,2005,59 (13):1696-1700
[13]Zhao X H,Li M,Lou X D.Adv.Powder Technol.,2014,25 (1):372-378
[14]Zhao X H,Lou F J,Li M,et al.Ceram.Int.,2014,40(4): 5507-5514
[15]Chen M,Wang Z H,Han D M,et al.Sens.Actuators B: Chem.,2011,157(2):565-574
[16]Umar A,Chauhan M S,Chauhan S,et al.J.Colloid Interface Sci.,2011,363(2):521-528
[17]Wahab R,Mishra A,Yun S I,et al.Biomass Bioenerg, 2012,39:227-236
[18]KAN Bao-Tao(阚保涛),WANG Xin(汪鑫),YE Chun-Li (叶春丽),et al.Chinese J.Lumin.(发光学报),2012,32(12): 1205-1209
[19]Stankovi A,Stojanovi Z,Veselinovi L,et al.Mater.Sci. Eng.B,2012,177(13):1038-1045
[20]Yousefi R,Kamaluddin B.Appl.Surf.Sci.,2009,255(23): 9376-9380
[21]Muthirulan P,Devi C N,Sundaram M M.Ceram.Int.,2014, 40(4):5945-5957
[22]Wang H H,Xie C S,Zhang W,et al.J.Hazard.Mater., 2007,141(3):645-652
Controllable Synthesis of Hierarchical Structure ZnO Photocatalysts with Different Morphologies via Sol-Gel Assisted Hydrothermal Method
WU Guang-LiZHAO Xiao-HuaLI MengLI Zhen-ZhenLI Cai-ZhuLOU Xiang-Dong*
(School of Chemistry and Chemical Engineering,Henan Normal University,Xinxiang,Henan 453007,China)
Hierarchical structure ZnO samples with different morphologies were synthesized by sol-gel assisted hydrothermal method,using Zn(NO3)2·6H2O,citric acid and NaOH as raw materials.Nanosheets flower-like ZnO, nanorods flower-like ZnO and spind-like ZnO microstructures could be synthesized only by controlling the time of hydrothermalreaction.Theas-preparedsampleswerecharacterizedbyXRD,SEM,UV-Vis,DRS, photoluminescence(PL)and low temperature nitrogen adsorption-desorption.The formation mechanism of different morphologies of ZnO hierarchical structures was proposed.The photocatalytic activities of the samples were evaluated by the degradation of Reactive Blue 14(KGL)under UV irradiation.The results demonstrated that different morphologies of ZnO samples all showed good photocatalytic performance,with the degradation degree of KGL exceeding 78%after 120 min.But the sample prepared at 120℃for 4 h exhibited superior photocatalytic activity to other ZnO samples,and the degradation rate of KGL can reach 99%.It might be attributed to the morphology,larger specific surface area,more oxygen surface defect and surface polarity.
sol-gel assisted hydrothermal;ZnO;morphology;hierarchical structure;photocatalytic
O643.36
A
1001-4861(2015)01-0061-08
10.11862/CJIC.2015.004
2014-06-17。收修改稿日期:2014-09-26。
国家自然科学基金(No.21073055)资助项目。
*通讯联系人。E-mail:chemenglxd@126.com,Tel:13623731736。
