玉溪市322例肺结核患者抗结核治疗不良反应分析
2015-05-18王智璇
唐 南,许 琳,王智璇
(云南省疾病预防控制中心,云南 昆明 650022)
玉溪市322例肺结核患者抗结核治疗不良反应分析
唐 南,许 琳,王智璇
(云南省疾病预防控制中心,云南 昆明 650022)
[目的]了解云南省玉溪市8个县322例结核病人不良反应发生情况,以此为基础评价不良反应发生对云南省结核病控制产生的影响,为预防和降低不良反应发生提供依据。[方法]由经过培训的结防科门诊医生通过调查问卷形式收集相关数据,并用统计软件对数据进行分析。[结果]共出现药物不良反应153例(47.5%),ADRs主要集中于前8周(52.7%),报告最多的是胃肠反应(25.5%),强化期内肝功能异常患者比例逐渐增多,随着疗程周期的进行,ADRs的发生率以及发生人数均呈现下降的趋势。[结论]目前DOTs策略下的标准化疗抗结核药物不良反应的发生率较高,强化期比起其他治疗阶段更容易出现药物不良反应,医务人员在强化期内应密切注意患者肝功能。同时对轻度反应的患者给予安慰、安抚,鼓励坚持疗程,提高患者依从性,降低初次治疗患者转变为复治患者的可能,避免结核耐药菌株的产生。
肺结核;抗结核治疗;药物不良反应
结核病是一种广泛传播的慢性传染病,化学疗法是目前控制结核病最有效的措施,但是因其治疗疗程长,剂量大,需要多种药物联合应用,因此治疗中容易出现不良反应(ADRs)[1]。药物不良反应(ADRs),指的是药物在正常人服用剂量下,发生的对于人体有害的与用药目的无关的反应[2]。由于抗结核药品不良反应发生率高,类型多样,轻则给患者带来痛苦,重则可能危及生命[3],且抗结核药物不良反应的有效处理直接影响着患者治疗的依从性,是影响抗结核治疗成败的关键因素,因此正确认识和处理抗结核药物不良反应,是提高患者对治疗的依从性、保证化疗持续进行并取得成效的关键。由于多种抗结核药的联合使用,在治疗过程中难免会发生药物不良反应,本研究对抗结核药物不良反应的发生率、转归以及相关因素等资料进行收集分析,以此为基础评估发生不良反应的可能的危险因素,旨在提高后续结核病患者服药依从性。
1 资料与方法
1.1 研究对象
2011年1月至2012年12月,玉溪市8个县疾控中心结核门诊登记并接受抗结核治疗的涂阳肺结核患者,经患者知情同意后,连续纳入。所有病例均按照国家DOTS策略规范治疗和管理[4],即初治涂阳病人接受6个月标准短程化疗方案(2H3R3Z3E3/4H3R3或2HRZE/4HR);复治病人接受8个月的化疗方案(2H3R3Z3E3/6H3R3E3)。
1.2 资料收集
玉溪市8个县疾控中心门诊的各1名医生经过培训后,通过问卷调查收集纳入对象的基本信息、病程记录、随访记录,ADR报告资料。
1.3 资料分析
采用Epidata 3.0软件对数据进行双录入;计量资料的描述采用均数、标准差等指标;计数资料描述采用率、构成比等指标;分析采用SPSS 17.0软件包,单因素分析采用卡方检验;显著性水平α值取0.05。
2 结果
2.1 纳入患者情况
本研究共纳入322例涂片阳性患者,男性202例,女性120例,男女比例约2:1, 平均年龄(42.1±18.19)岁,最大的82岁,最小的13岁。农民占大多数(66.15%),汉族居多(61.8%),总体文化程度相对较低,文盲以及小学占到48.4%;初治患者319例(99%),复治患者3例;采用隔日疗法的涂阳患者290例(90.1%),采用每日疗法的涂阳患者32例。
2.2 不良反应发生情况
2.2.1 ADRs报告率、类型以及肝功检测结果
322例患者中药物不良反应者153例(47.5%),未出现因不良反应停药或者死亡的病例;153例患者累计报告不良反应734次,人均报告次数4.79次,报告次数的中位数为2.0次;采用隔日疗法的患者有138人发生不良反应,有152人没有发生不良反应,采用每日疗法的患者有15人发生不良反应,有17人没有不良反应发生。在报告的153例发生不良反应患者中,有73人只发生一种不良反应(47.7%),43人联合发生2种不良反应(28.1%),26人联合发生3种不良反应(16.9%),仅有11人联合发生3种以上不良反应,有3人联合发生6种不良反应。经卡方检验不同性别、年龄、治疗方案以及结核治疗史的患者ADRs发生率卡方检验P值均大于0.05,差异无统计学意义。
153例不良反应患者中,报告最多的症状是消化系统症状,共报告82人(25.5%)。其中报告消化系统最多的症状是恶心(84.1%);其次为神经系统症状,共报告79人(24.5%),报告最多的是头痛症状(81.0%);再次为过敏反应,共报告有31人(9.6%),过敏症状中报告最多的是皮疹(100%);另外报告14人(4.3%)发生关节疼痛;其他症状27人(8.4%),包括视听异常、胸闷腰痛等。
肝功能检测结果显示,从治疗开始前直至第五个月末,各个治疗周期内均检测到有患者的ALT异常值(AL>40U/L)。强化期内随着疗程周期的进行,肝功能异常患者比例呈逐渐增多的趋势,强化期结束后又有所减少治疗最后一个月末与强化期相比肝功异常患者比例明显减少,经卡方检验分析,χ2=9.528,P=0.002,差异有统计学意义,见表1。
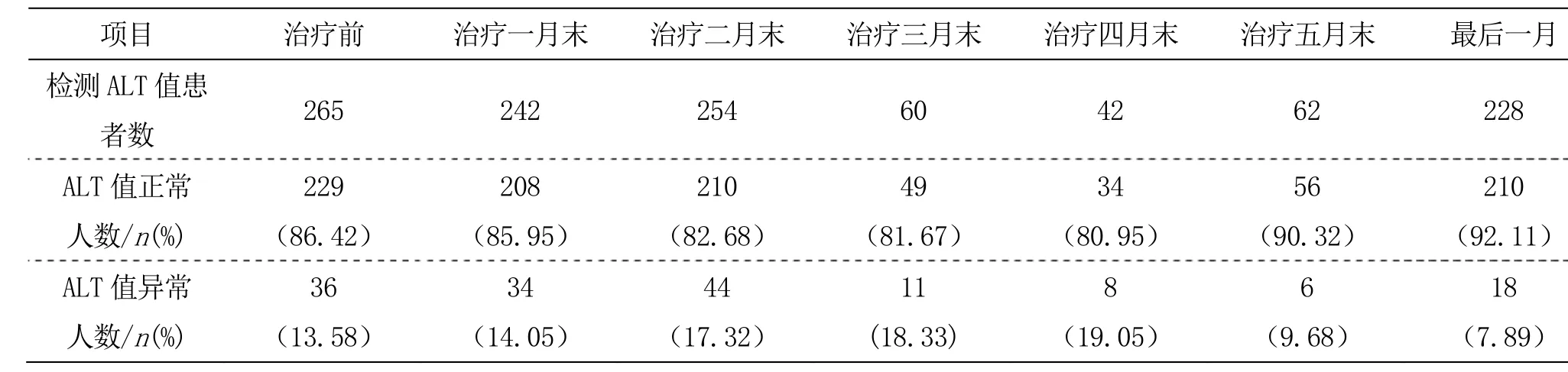
表1 不同治疗周期肝功能异常患者数
2.2.2 ADRs报告时间分布
以4个周为一个记录周期记录ADRs报告的时间,第1至第4周内有110人报告抗结核不良反应,报告ADRs次数为223次;第5至第8周有94人发生不良反应,报告ADRs次数为174次;第9至第12周有41人发生不良反应, 报告ADRs次数为111次;第13至16周报告不良反应人数为35人,报告ADRs79次;第17至20周报告37人,78次;第21至24周报告23人,69次。将不同疗程周期的不良反应次数做卡方检验,χ2=138.632,P<0.001,差异有统计学意义,说明随着治疗的进行,ADRs的发生率以及发生人数均呈现下降的趋势,见图1。
有50人(32.3%)的首次不良反应症状出现在第一周内,有27人(17.4%)在第二周出现,有17人(11.0%在第三周出现,有13人(8.4%)第四周出现,首次发生不良反应症状的出现随着治疗的进行也呈逐渐减少趋势。
3 讨论
目前直接面视下督导化疗是我国治疗结核病的主要方式,结核病人的依从性常被认为是结核病治疗的最大障碍[5],而现阶段的抗结核药物治疗特点是疗程长、剂量大、药物不良反应(ADRs)较常见,直接影响患者对治疗的依从性。本次研究的322例患者中,共153例患者发生药物不良反应,ADRs发生率47.5%,高于文献[1,6-8]报道的9.38%~43.6%,主要ADRs为胃肠道反应和神经损害,有别于金卫东报道的以肝功能损害、位听神经损害为主(86.0%)[7]。另外,25.5%的患者在治疗过程中出现胃肠反应,低于Shin等[9]胃肠道反应的发生率75.4%的报道,52.3%的患者发生至少1种不良反应,低于文献报道的69.0%~73.3%[9,10]。这可能与国内外用药剂量的不同以及个体差异有关。此外,胃肠道反应发生率偏高也提示在抗结核治疗的同时应该密切注意患者胃肠道反应。
强化期内随着疗程周期的进行,肝功能异常患者比例呈逐渐增多的趋势,直至强化期结束后比例减少,这也提示有很大可能是强化期内药物造成的肝损伤,特别在强化期多种药物联合服用的情况下,应该密切注意患者肝功情况。首次出现不良反应的时间以及不良反应发生较为频繁的时间段均集中于前八个周,可能是因为开始治疗的前两个月内是强化期联合用药,服药方式为清晨空腹顿服,药物浓度较大、半衰期长,导致患者对药物的不耐受而易产生ADRs。但是本次调查不良反应持续时间均不长,多数在一周内出现后消失,并无因ADRs而退组或放弃治疗的情况发生,最长的不良反应时间仅维持在2~3周,之后给予相应处理即消退。
结果表明,目前DOTs策略下的标准化疗抗结核药物不良反应的发生率较高,而且前八个周的强化期是ADRs最容易出现的时期,也是ADRs发生率较高的时期,提示医务人员在此期间应密切注意抗结核药物不良反应发生,在此同时,对轻度反应的患者给予安慰、安抚,提高患者依从性,从而减少因不良反应而自行停药的情况,降低初次治疗患者转变为复治患者的可能,也避免产生结核耐药菌株的出现。
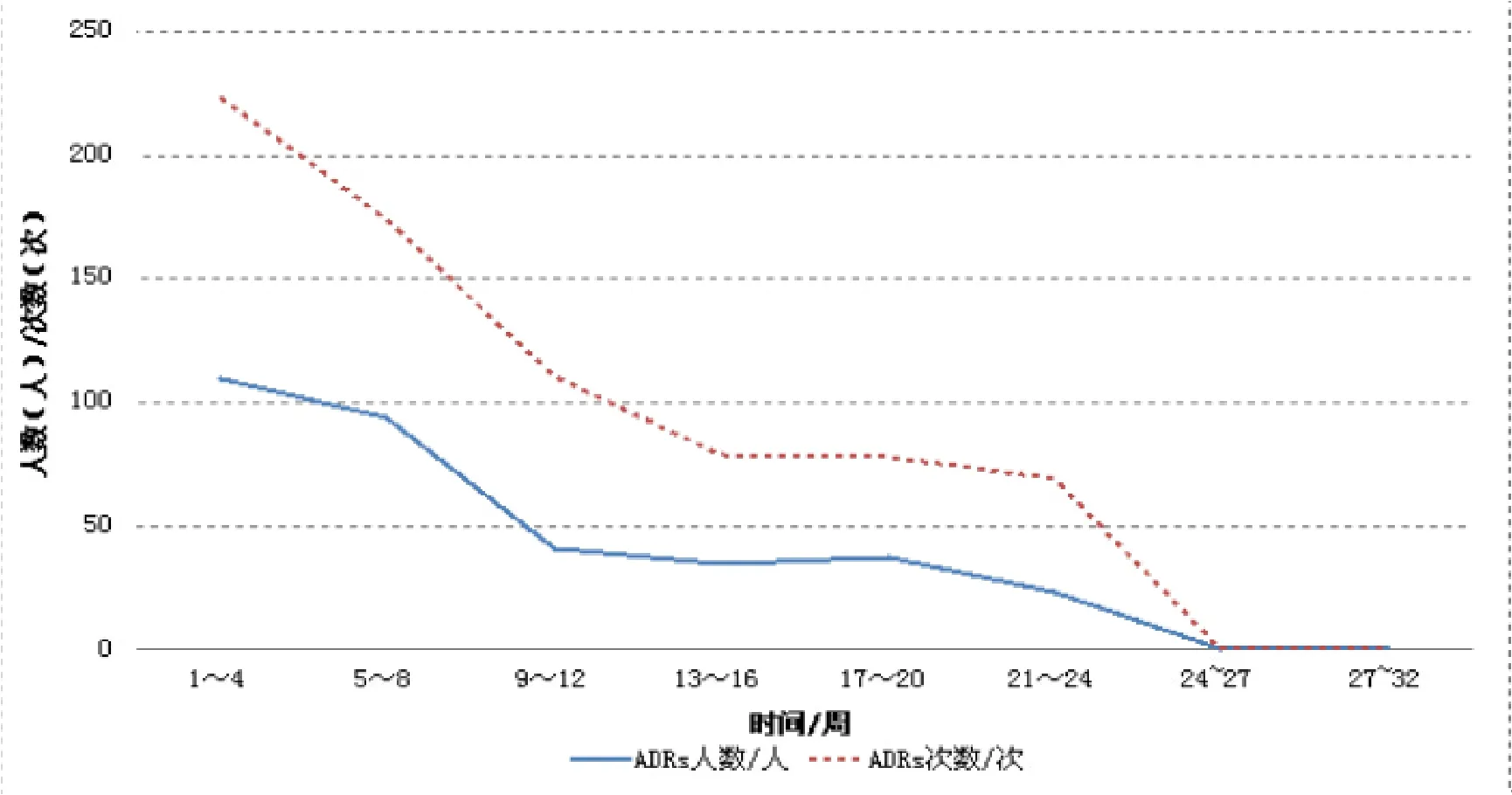
图1 各疗程周期ADRs报告情况
[1] 夏惜倍,詹思延.国内抗结核药品不良反应发生率的综合分析[J].中华结核和呼吸杂志,2007,30(6):419-423.
[2] 崔国强.一线抗结核药不良反应发生情况及对继续治疗的影响[J].职业与健康,2012,28(19):1-2.
[3] 冼翠平.药物不良反应对肺结核患者全程规律治疗的影响[J].广东药学,2003,13(3):55-57.
[4] 卫生部疾病预防控制局,卫生部医政司,中国疾病预防控制中心.中国结核病防治规划实施工作指南(2008版)[M].北京:中国协和医科大学出版社,2008.
[5] ARIEL PABLOS.Non-adherence in Tuberculosis Treatment: Predictors and Consequences in New York City[J].The American Journal of Medicine, 1997,102(2):164-170.
[6] 高 星,欧阳松,林 鸳,等.453例抗结核药物引起副作用的临床分析[J].江西医药,2010,45(4):334-335.
[7] 金卫东,王自立,马小民,等.156例脊柱结核患者抗结核药物副作用临床分析[J].第三军医大学学报,2009,31(20):1932-1935.
[8] 孙碧慧,赵安贵.常用抗结核药物不良反应监测前瞻性研究[J].中国医药导报,2012,9(19):155-156.
[9] SHIN SS,PASECHNIKOV AD,GELMANOVA IY,et al.Adverse reactions among patients being treated for MDR-TB in Tomsk,Russia[J].Int J Tuberc Lung Dis,2007,11(12):1314 -1320.
[10] FURIN JJ,MITNICK CD,SHIN SS,et al. Occurrence of serious adverse effects in patients receiving community-based therapy for multidrug-resistant tuberculosis[J].Int J Tuberc Lung Dis,2001,5(7):648-655.
(本文编辑:谢碧钰)
Analysis on adverse drug reactions of 322 cases anti-tuberculosis therapy in Yuxi
TANG Nan,XU Lin,WANG Zhi-xuan
(Yunnan CDC., Kunming Yunnan 650022, China)
ObjectiveTo know adverse drug reactions (ADRs) occurrence of 322 cases anti-tuberculosis therapy in 8 counties. Evaluated the impact of the occurrence of adverse drug reactions to TB control in Yunnan province, so as to provide the basis for preventing and reducing adverse reactions occurrence.MethodsTrained outpatient doctors collected data through questionnaire, and analyzed the data by statistical software.Results153 patients (47.5%) appeared adverse drug reactions, ADRs symptoms mainly occurred in front 8 weeks(52.7%), the most frequently symptoms was gastrointestinal reaction(25.5%). The proportion of patients with liver dysfunction gradually increased in intensive period. With the course of treatment continued, both of the number of ADRs and the frequency were showed down trend(x2=138.632,P<0.001).ConclusionsThe occurrence rate of standard chemotherapy anti-tuberculosis adverse drug reactions was high under present DOTs strategy. Medical staffs should pay close attention to the patients’liver function. Encouraged slight reaction patients to insist treatment, so as to increase patients compliance. Reduce the possibility of initial naprapath to retreatment, avoid the producing of tuberculosis drug resistant strain.
tuberculosis, anti-tuberculosis treatment, adverse drug reactions (ADRs)
R181.8
:B
:1003-2800(2015)04-0236-03
2014-12-10
唐 南(1988-),男,云南昆明人,硕士在读研究生,主要从事结核病预防与控制方面的工作。
许 琳(1973-),女,云南人,副主任医师,主要从事结核病预防和控制方面的研究。
