铀在木纤维上的吸附行为及机理分析
2015-05-15易发成
王 哲,易发成,冯 媛
(1.西南科技大学核废物与环境安全国防重点学科实验室,四川绵阳 621010;2.中国科学技术大学地球与空间科学学院,安徽合肥 230026)
铀在木纤维上的吸附行为及机理分析
王 哲1,2,易发成1,冯 媛1
(1.西南科技大学核废物与环境安全国防重点学科实验室,四川绵阳 621010;2.中国科学技术大学地球与空间科学学院,安徽合肥 230026)
为了解木纤维对铀的吸附特性,通过静态吸附实验,研究了木纤维的粒度、吸附时间、用量、温度及溶液的pH值和初始浓度等因素对模拟含铀废水中U(Ⅵ)去除率的影响,并从热力学和动力学方面对吸附过程进行了分析。结果表明:溶液初始pH≈3时,木纤维对铀的吸附平衡时间为4h,且吸附剂粒径越小、温度越高、用量越大,越有利于铀的去除;铀在木纤维上的吸附过程符合Langmuir等温吸附方程,吸附动力学过程可用准二级吸附动力学模型描述,表明化学吸附主要受动力学控制;木纤维吸附铀是自发的吸热反应。SEM、FT-IR和EDS分析结果表明,木纤维吸附铀后表面形态发生了改变,且在吸附过程中铀主要与木纤维表面活性基团螯合并形成配合物,存在表面络合吸附行为;吸附铀前后的能谱对比分析表明,吸附过程中存在离子交换行为。因此,木纤维对铀的吸附机理是以离子交换和表面络合吸附为主、物理吸附为辅的混合吸附过程。
木纤维;铀;吸附性能;吸附行为;吸附机理
在核燃料循环过程中铀矿开采、水冶、后处理及应用过程中会产生大量含铀废水,这些废水若不妥善处理将对生态环境构成严重威胁,因此,对含铀废水处理日益受到重视。传统的处理方法效率低,生物吸附是一种很有潜力的方法,能克服传统方法的诸多不足[1]。已有研究[2-13]表明,细菌、真菌、藻类和黏土矿物等对铀具有一定的富集作用,但固液分离及吸附处理效果均不太理想;也有少数研究者将农林废弃物用于铀的吸附,该方法处理成本低、二次污染少、易再生利用、回收铀的可能性大。本文以木纤维作为吸附剂来处理模拟含铀废水,通过研究影响吸附性能的因素,以及吸附过程中的吸附热力学和动力学,分析木纤维吸附铀的机理,为利用农林废弃物处理含铀废水提供新的思路。
1 实验
1.1 主要仪器设备
WGJ-Ⅲ型微量铀分析仪:杭州大吉光电仪器有限公司;Spectrum One型傅里叶变换红外光谱仪(FT-IR):美国PE公司;TM-1000型扫描电子显微镜(SEM):日立公司;FA1104电子天平(精度为0.000 1g):上海良平仪器仪表有限公司;PHS-25A型酸度计:上海大中分析仪器厂;KS康氏振荡器:金坛市富华仪器有限公司;80-2型离心沉淀机(转速0~4 000r/min):深圳市沙头角国华仪器厂;SHA-C型往返水浴恒温振荡器:江苏大地自动化仪器厂。
1.2 吸附剂及模拟含铀废水
1)吸附剂
本文所用吸附剂为木纤维,由四川省生物质改性材料工程技术研究中心提供。首先将木纤维自然风干后磨成粉末状,然后在50℃下烘干至恒重,过120目筛再烘干至恒重,放入干燥箱内冷却至室温,最后装袋密封、置于干燥器内备用。
2)模拟含铀废水的配置
采用电子天平称取0.019 8g硝酸铀酰(UO2(NO3)2·6H2O)(精确到0.000 1g),放入烧杯中溶解,然后倒入1 000mL容量瓶中,烧杯和玻璃棒用去离子水反复冲洗3~5次,洗液也置入容量瓶中,最后用去离子水定容,塞紧,反复倒置容量瓶摇晃3~5次,即制得浓度为50μmol/L模拟含铀废水溶液,避光储存备用。在实验过程中,根据实验方案,采用分析纯NaOH和HCl试剂调节模拟含铀废水溶液的初始pH值。
1.3 实验方法与计算公式
1)根据实验方案,取100mL锥形瓶(用蒸馏水洗净、烘干)数个,用电子天平称量0.1g(精确到0.000 1g)吸附剂数份,分别置于各锥形瓶内,再用50mL量筒量取50mL模拟含铀废水溶液倒入锥形瓶内,塞紧。
2)在预定实验条件下,将锥形瓶置于KS康氏振荡器上在75r/min下振荡吸附。
3)振荡结束后,将锥形瓶从振荡器上取下静置几min,再用移液管取一定量上层清液于离心机内,以3 500r/min离心分离20min。
4)离心结束后,用移液管取一定量上层清液,采用WGJ-Ⅲ型微量铀分析仪测量上清液中铀的浓度,根据式(1)计算木纤维对铀的吸附容量:


式中:Q为吸附容量,mg/g;V为溶液体积,mL;c0为溶液的初始浓度,mg/L;ct为t时刻溶液的浓度,mg/L;W为吸附剂用量,g;η为吸附率,%。
5)通过研究木纤维对模拟放射性废水中铀的吸附等温线和吸附动力学,并对吸附前后木纤维进行SEM、FT-IR和能谱(EDS)分析来综合探讨其对铀的吸附机理。
2 结果及讨论
2.1 木纤维粒度对吸附率的影响
室温下,分别将质量为0.1g,粒度为20、40、60、80、100、120目的木纤维加入体积为50mL模拟含铀废水中,恒温振荡吸附4h,研究吸附剂粒度对铀吸附率的影响,结果示于图1。由图1可见:当木纤维粒度为20~100目时,对铀酰离子的吸附率随粒径的减小而增大;当木纤维粒度为100~120目时,吸附率的增大趋势随吸附剂粒径的减小而变缓,说明该粒度范围内木纤维对铀酰离子的吸附率受粒度影响较小。这是由于木纤维粒径越小,比表面积越大,暴露出的有效吸附位点越多,铀酰离子与其接触的机会就越多,从而导致吸附率增大;当木纤维粒度大于100目时,暴露出的有效吸附位点趋于稳定,从而出现吸附率与吸附剂粒度关系曲线末段趋于平缓的现象。因此,本实验吸附剂粒度选择控制在120目,并在此基础上开展其他相关实验研究。
2.2 吸附时间对吸附率的影响
2.1节中其他条件不变,木纤维粒度为120目,预定振荡时间为0.5、1、1.5、2、3、4、6h,研究吸附时间对铀吸附率的影响,结果示于图2。由图2可见:在开始的1h内,随着吸附时间的延长,木纤维对铀酰离子的吸附率快速增大,1h时其吸附率已达49.7%,这是因为在吸附初期,木纤维对铀酰离子吸附主要是在其外表面和部分微孔内进行,在短时间内即可完成;之后,随着吸附接近饱和,加上浓度不断减小,吸附推动力减弱,导致吸附速率变慢,并在4h时吸附率达53.5%,之后趋于平缓。说明木纤维对铀酰离子的吸附已达到平衡。因此,确定木纤维对铀的吸附时间为4h。

图1 吸附剂粒度对铀吸附率的影响Fig.1 Effect of adsorbent particle size on removal rate of uranium

图2 吸附时间对铀吸附率的影响Fig.2 Effect of adsorption time on removal rate of uranium
2.3 木纤维用量对吸附率的影响
2.1节中其他条件不变,改变120目木纤维的用量(0.1、0.2、0.4、0.6、0.8、1.0g),研究其对铀吸附率的影响,结果示于图3。由图3可见,铀的吸附率随木纤维用量的增大而增大。这是因为木纤维用量的增加使得总比表面积增大,导致其与铀酰离子的接触面积也增大;同时,吸附位点和参与吸附的官能团的数量增多,从而增大了铀酰离子的吸附率。因此在处理含铀废水时,加大木纤维的加入量能更好地去除废水中的铀酰离子。
2.4 温度对吸附率的影响
2.1节中其他条件不变,改变反应温度为15、30、45、60℃,研究温度对铀吸附率的影响,结果示于图4。图4表明,木纤维对铀酰离子的吸附率随温度的升高逐渐增加,说明温度对铀酰离子的吸附影响较大。这是由于温度升高时,铀酰离子的运动加快,提高了外扩散和内扩散速率,有利于克服化学吸附活化能的障碍,且吸附主要发生在木纤维的表面,因而提高了木纤维对铀酰离子的吸附率。因此,升高温度有利于吸附废水中的铀酰离子。

图3 木纤维用量对铀吸附率的影响Fig.3 Effect of wood fiber dosage on removal rate of uranium

图4 温度对铀吸附率的影响Fig.4 Effect of temperature on removal rate of uranium
2.5 pH值对吸附率的影响

浓度,H+与UO2+2发生竞争吸附,H+与木纤维官能团结合,占据了活性位点,所以木纤维在低pH值时,对铀的吸附率较低,随着pH值的增大,溶液中UO2+2浓度高于H+浓度,UO2+2与木纤维官能团结合,占据了活性位点,导致其吸附率增大,表现为曲线上升;当pH>3时,UO2+2开始水解,并形成UO2(OH)2,沉积在木纤维表面,覆盖了部分活性位点而导致吸附率降低;当pH值接近中性时,溶液中的铀主要以UO2OH+、(UO2)2(OH)2+2、(UO2)3(OH)+5等络合离子的形式存在[15],这些带正电荷的阳离子与带负电荷的木纤维官能团产生强烈的络合吸附,同时,还会形成微量的铀沉淀,表现为曲线缓慢下降;当pH>7时,溶液中的UO2+2等离子与OH-生成UO2(OH)2沉淀,并富集在木纤维表面,最终导致其吸附率趋于稳定。
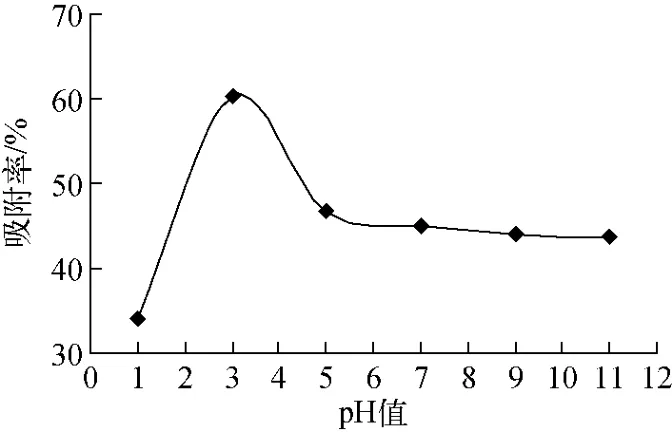
图5 初始pH值对铀吸附率的影响Fig.5 Effect of pH on removal rate of uranium
2.6 初始浓度对吸附率的影响
2.1节中其他条件不变,改变模拟含铀废水的初始浓度为0.01、0.02、0.05、0.1、0.2、0.5mmol/L,研究溶液初始浓度对吸附率的影响,结果示于图6。图6显示,木纤维对铀的吸附率随铀初始浓度的增大而减小。这一方面是由于溶液中添加的木纤维数量一定,其提供的可吸附位点有限,而与有限的吸附位点相比,较高的初始浓度使得铀酰离子较多,吸附达到过饱和而制约了吸附过程的顺利进行,从而造成吸附率降低;另一方面由于溶液初始pH值控制在6.5~7.0之间,铀酰离子的初始浓度越高,其生成的UO2(OH)2沉淀越多,富集在木纤维表面的也越多,抑制了木纤维表面吸附铀酰离子的活性位点,从而导致溶液浓度越大,吸附率越小。此外,由于高浓度的模拟含铀废水可能导致木纤维细胞壁结构的破坏,导致有效吸附位点减少。

图6 含铀废水初始浓度对铀吸附率的影响Fig.6 Effect of initial concentration on removal rate of uranium
3 吸附行为及机理分析
3.1 吸附等温线分析
常用Langmuir、Freundlieh和D-R(Dubinin-Radushkevich)等吸附等温式模型来描述吸附达到平衡后,吸附质在固/液两相间的分配。其中,Langmuir吸附等温式模型为:


Freundlich吸附等温式模型为:

D-R吸附等温式模型为:1



式中:ce为平衡浓度,mg/L;Qe为平衡吸附量,mg/g;Qm为最大吸附量,mg/g;KL、KF为吸附平衡系数;n为Freundlich吸附指数;ε为Polanyi电位,kJ/mol;β为平均吸附自由能活度系数,mol2/kJ2;R为气体常数,8.314J/(mol·K);T为热力学温度,K;E为平均吸附自由能(由溶液相转入吸附剂表而所引起的自由能变化),kJ/mol。
参照2.6节中静态吸附实验,将含U(Ⅵ)模拟废液的初始浓度c0分别调至91.25、57.02、28.39、14.25、5.74、2.85mg/L,在达到吸附平衡时,木纤维对U(Ⅵ)的平衡吸附量Qe分别为9.26、8.84、6.36、3.69、1.64、0.90mg/g,溶液相中U(Ⅵ)的浓度ce分别为72.74、39.35、15.67、6.87、2.46、1.05mg/L。分别以ce/Qe对ce、lg Qe对lg ce及ln Qe对ε2作图,结果示于图7。根据图7各直线的斜率和截距得到Langmuir模型参数Qm=11.04mg/g,KL=0.80L/mg,RL=0.12、0.18、0.31、0.47、0.69、0.81;Freundlich模型参数KF=1.023L/mg、1/n=0.575;D-R模型参数Qm=75.90mg/g、β=0.004 9mol2/kJ2、E=10.102kJ/mol。

图7 等温吸附式模型拟合曲线Fig.7 Fitting line of isothermal adsorption model
由图7可知,Langmuir、Freundlich和D-R吸附等温式模型均能较好地描述木纤维对U(Ⅵ)的吸附过程,但Langmuir吸附等温式模型的相关系数R2>0.99,相对于Freundlich和D-R吸附等温式模型,Langmuir吸附等温式模型更适合描述木纤维对U(Ⅵ)的吸附过程,这说明木纤维对U(Ⅵ)的吸附介于单分子层和多分子层之间,且化学吸附在U(Ⅵ)与木纤维的表面的相互作用过程中占主导地位,即木纤维分子中每个吸附点位均只能吸附一个铀酰离子,当所有的吸附点位均被占据后,吸附达到动态平衡。同时,由图4还可知,随着温度的升高,木纤维对铀的吸附率增大,说明温度升高有利于木纤维对U(Ⅵ)的吸附,其吸附过程是吸热反应,也侧面验证了该吸附过程符合单分子层吸附理论。
此外,可通过RL、1/n和E等参数来评价木纤维对U(Ⅵ)的吸附性能[16]。
1)根据分离因子RL来判断木纤维是否适用于对U(Ⅵ)的吸附。RL>1时,不利于吸附,不适合吸附该核素离子;0<RL<1时,有利于吸附,适合用作处理该核素的吸附剂;RL=0时,为不可逆吸附;RL=1时,为线性吸附。根据不同初始浓度下计算得到的RL均小于1,表明木纤维吸附U(Ⅵ)是个有利的吸附过程。
2)n为Freundlich吸附指数,表征吸附强度的量度,当0.1<1/n<0.5时,吸附易于进行,当1/n>2时,吸附难以进行。根据计算得到的1/n=0.575,说明吸附较易进行。
3)通过E值可判断木纤维对核素的吸附机理。当8kJ/mol≤E≤16kJ/mol时,吸附主要通过离子交换过程来完成;当E≤8kJ/mol时,物理吸附的作用可能是吸附的主要机理;当E≥16kJ/mol时,扩散很可能是吸附的主要方式。根据计算得到的平均吸附能E=10.102kJ/mol,可判断吸附反应属于化学吸附,且以离子交换反应为主。
3.2 吸附热力学分析
吸附自由能是吸附推动力和吸附优惠性的体现,而温度是影响放射性核素在固-液界面吸附的一个很重要的参数。根据不同温度下的吸咐等温线可得到吸附质在吸附剂上吸附的相关热力学参数:吉布斯自由能变(ΔG0)、焓变(ΔH0)和熵变(ΔS0),相关计算公式如下:

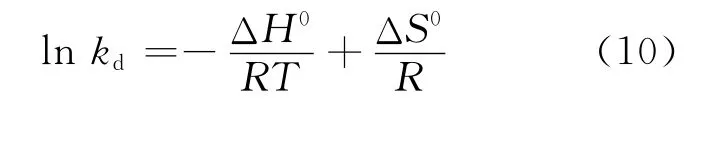

式中:cad为平衡时吸附质在吸附剂上的浓度,mg/L;kd表观吸附平衡常数。
按照式(10),对ln kd-1/T作图,如图8所示。由于是实际溶液,根据不同温度下所得直线的斜率和截距,可求得不同温度下的表观ΔG0、ΔH0和ΔS0,其热力学参数的计算结果列于表1。由表1可见,ΔH0=10.172kJ/mol>0,说明U(Ⅵ)在木纤维表面上的吸附是一个吸热过程;ΔG0为负值,说明U(Ⅵ)在木纤维上的吸附是一个自发进行的过程,并随着温度的升高,ΔG0减小,说明高温有利于反应的进行;ΔS0=35.32J/(mol·K)>0,一方面说明在吸附过程中吸附质并不以简单的离子形式存在,它们经常会与水结合(水化作用或水解作用)生成水合离子或分子,当吸附质的水合离子或分子被吸收时,其结合水可能会离解出来,重新回到溶液中,这个过程会增加系统的熵,2.5节中pH值对吸附率影响特征也说明了这点;另一方面,在吸附过程中木纤维的微观结构发生了改变,这也是导致熵增加的主要原因,因此,两种因素的共同作用导致了系统的熵增大。

图8 温度对U(Ⅵ)在木纤维上的表观吸附常数的影响Fig.8 Effect of temperature on apparent equilibrium adsorption constant of U(Ⅵ)adsorption on wood fiber
3.3 吸附动力学分析
吸附动力学用于预测不同吸附时间下可达到的吸附效率。在固-液静态吸附的研究领域中,常用准一级动力学模型和准二级动力学模型描述吸附动力学行为,其中准二级动力学模型的速率控制步骤是化学吸附过程。两种模型的动力学方程如下:

表1 U(Ⅵ)在木纤维上的吸附过程热力学参数Table 1 Thermodynamic parameters for adsorption of U(Ⅵ)on wood fiber


当t→0时,可得到准二级吸附动力学模型的初始吸附速率h:

式中:Qt为t时刻的吸附量,mg/g;k1、k2分别为准一级和准二级吸附速率常数;t为时间,min。
当初始浓度c0=14.57mg/L,木纤维用量为0.1g,模拟含铀废水体积为50mL,T=30℃,t=30、60、90、120、180、240、360min时,用以上方程对所得实验数据进行拟合得到吸附动力学参数。结果显示,达到吸附平衡时Qe=3.93mg/g,不同时间对应的吸附量分别为Qt=3.36、3.62、3.71、3.79、3.86、3.90、3.93mg/g。对lg(Qe-Qt)-t作图,拟合出的准一级动力学模型线性图如图9a所示,通过计算图9a的直线斜率和截距可分别得到Qe=0.758mg/g和k1=0.013g/(mg·min);对t/Qt-t作图,拟合出的准二级动力学模型线性图如图9b所示,通过计算图9b中直线的斜率可得到Qe=3.995mg/g、k2=0.039 9g/(mg· min)、h=0.638mg/(g·min)。因此,由准一级动力学模型计算得到的Qe(0.758mg/g)与实测值(3.93mg/g)不吻合,且R2相对较低;而准二级动力学模型计算得到的Qe(3.995 mg/g)与实测值(3.93mg/g)较接近,且R2=1.000。说明采用准二级动力学模型能很好地描述木纤维对U(Ⅵ)的吸附过程,表明化学吸附过程是吸附动力学的主要控制步骤。
3.4 吸附机理探讨
1)木纤维吸附铀前后的SEM分析
图10为木纤维吸附U(Ⅵ)前后的SEM图像。由图10a可见,木纤维纹路较清晰,表面较粗糙,分布有较多的空隙和空洞,呈现不规则的多孔结构,空洞和孔隙张开度较大,且孔结构粗糙、呈毛刺状。孔隙和空洞的存在一方面增大材料的表面积,使更多的吸附位点暴露出来,另一方面为吸附水中的金属离子提供了必要的通道及足够的吸附空间,便于核素离子向内部扩散,这种表面粗糙和多孔的结构有利于对U(Ⅵ)的吸附。对比吸附前后的SEM图像可知,吸附U(Ⅵ)后,木纤维表面上分布的空隙和空洞被U(Ⅵ)填充,细小裂隙减少或基本不见,毛刺消失,空洞变小且相对光滑圆润。表明木纤维对U(Ⅵ)存在内部孔道吸附,木纤维主要由木质素和纤维素等构成,这些物质可提供大量的有机基团,与作为配体和有空轨道的铀酰离子相互键合,从而改变了其表面形态。正是由于木纤维的这种表面形态的改变,增加了吸附系统的熵值,使系统的无序度增强,这与3.2节中实验分析结果相吻合。

图9 吸附动力学方程拟合曲线Fig.9 Fitting curve of adsorption kinetics equation

图10 木纤维吸附U(Ⅵ)前(a)、后(b)的SEM图像Fig.10 SEM images of wood fiber before(a)and after(b)adsorption of U(Ⅵ)
2)木纤维吸附铀前后的FT-IR分析
木纤维成分复杂,内含纤维素、木质素等。样品在整个波数范围内均有明显的吸收,使得某些峰未能表现出来,一些不太灵敏的吸收峰被掩盖。

图11 木纤维吸附U(Ⅵ)前、后的FT-IR谱Fig.11 FT-IR analyses of wood fiber before and after adsorption of U(Ⅵ)
图11中曲线a为木纤维吸附U(Ⅵ)前的FT-IR谱,按文献[17]对吸收谱带进行归属:3 411.5cm-1处的强且宽的吸收峰为缔合的O—H伸缩振动峰,说明木纤维表面存在羟基,该伸缩振动可能是由于木纤维表面的硅醇基(Si—OH)、其他羟基和吸收的水分中游离和缔合的羟基振动引起的;2 923.6cm-1处的吸收峰为甲基(—CH3)、亚甲基(—CH2)和次甲基(—CH)的不对称伸缩振动峰;1 635.8cm-1处的吸收峰为羧基和羰基中的C—O伸缩振动峰;1 606.3cm-1和1 511cm-1处的吸收峰是由于木质素中芳香环骨架的伸缩振动而引起的,而1 463.2cm-1的吸收峰为甲基(—CH3)和亚甲基(—CH2)中C—H键的不对称弯曲振动峰;1 423.6cm-1和1 227.7cm-1处的吸收峰可能是由木质素中酚羟基的O—H伸缩振动引起的。这些特征谱带证明木纤维中含有木质素成分;1 375.1cm-1处的吸收峰为纤维素和半纤维素中甲基(—CH3)的C—H键对称弯曲振动峰,1 335.9cm-1和1 319cm-1处的弱吸收峰是纤维素的醇羟基的面内振动峰,1 267.8cm-1是纤维素的羟基平面振动吸收峰,而1 058.9cm-1及1 033~1 162cm-1处的一系列纤维素特征振动峰,主要产生于O—H的弯曲振动和C—O—C非对称伸缩振动,可能含有P—O—C的伸缩振动及Si—O—Si振动作用;896.5cm-1处的吸收峰由环状C—O—C不对称面外伸缩振动引起的;876.9、838.8和812.2cm-1处的吸收峰为芳香环中C—H弯曲振动引起的;617.8cm-1附近的吸收峰是醇羟基中O—H的面外变形振动引起的。由此可推断,木纤维中大量存在的主要官能团是处于缔合状态的羟基、羧基、羰基、P—O和Si—O等,它们处于木纤维表面,对于吸附U(Ⅵ)起到关键作用。
木纤维吸附U(Ⅵ)后的红外光谱如图11中曲线b所示。总地来说,吸附U(Ⅵ)后的光谱与吸附前相比变化不大,红外光谱谱峰并无明显改变,仅出现了漂移,并无新的谱带出现,这表明木纤维吸附U(Ⅵ)后,自身结构并未发生改变。其中,3 411.5cm-1处—OH峰向低波数移动了11.5cm-1(3 400cm-1),峰强减弱;1 635.8cm-1处羧基和羰基峰则向低波数移动不明显,但峰强减弱;1 423.6cm-1和1 227.7cm-1处的酚羟基峰向低波数移动了约1cm-1,峰强减弱;1 335.9、1 319和617.8cm-1处的醇羟基峰向低波数移动了1~2cm-1,峰强减弱;1 058.9cm-1和1 033~1162cm-1处的O—H、C—O、P—O和Si—O的振动峰移动不明显,但峰强增强;896.5cm-1处的C—O的振动峰移动不明显,但峰强减弱。以上结果表明,木纤维吸附U(Ⅵ)后,其结构仍保持相对完整,缔合羟基、羧基、羰基、P—O和Si—O等活性基团在U(Ⅵ)吸附过程中起着重要作用,而铀主要与这些活性基团螯合并形成配合物,其木纤维对U(Ⅵ)的吸附主要由以下步骤完成:U(Ⅵ)→木纤维固液界面→木纤维表面→木纤维微孔→与活性位置结合。因此,木纤维对铀吸附的机理存在表面络合吸附。
3)木纤维吸附铀前后的EDS分析
木纤维吸附铀前后的EDS谱示于图12,元素分析结果列于表2。由图12可见,木纤维中主要含有C、O、Na、K、Si、P、Cl等元素。对比图12a、b和表2可见,木纤维吸附U(Ⅵ)后Na和K的峰值和含量均降低,而木纤维样品中出现U(Ⅵ)的特征峰,同时U(Ⅵ)含量从0%增加到2.61%,这是由于吸附过程中存在离子交换而使Na+和K+溶解到了液相中,而液相中的U(Ⅵ)被吸附进入木纤维孔道内。同时,对吸附后的溶液进行X射线荧光光谱分析(X-RF),结果显示,溶液中确实存在Na+和K+。由此说明,木纤维吸附U(Ⅵ)的过程中存在离子交换,与3.1节中实验分析结果相吻合。

图12 木纤维吸附U(Ⅵ)前(a)、后(b)的EDS谱Fig.12 EDS spectra of wood fiber before(a)and after(b)adsorption of U(Ⅵ)

表2 木纤维吸附U(Ⅵ)前、后元素含量变化Table 2 Element content change in wood filber before and after adsorption of U(Ⅵ)
4 结论
1)溶液初始pH≈3时,木纤维对铀的吸附平衡时间为4h,且吸附剂粒径越小、温度越高、用量越大,越有利于铀的去除。
2)木纤维对铀的吸附符合Langmuir吸附等温式模型,表明木纤维对铀的吸附介于单分子层和多分子层之间,在铀与木纤维的表面相互作用过程存在化学吸附,而这种化学吸附又以离子交换反应为主。EDS谱、X-RF谱分析进一步证明了木纤维吸附铀过程中存在离子交换反应。
3)木纤维吸附铀是自发的、吸热的吸附反应,且高温有利于反应的进行。
4)木纤维对铀的吸附动力学行为符合准二级动力学模型,相关系数R2=1.000,表明其吸附过程中存在化学吸附。
5)木纤维吸附U(Ⅵ)前后的SEM图像对比表明,木纤维对铀存在内部孔道吸附,而铀主要与木纤维表面的羟基、羧基、羰基、P—O和Si—O等活性基团螯合并形成配合物,表明木纤维对铀吸附的机理也存在表面络合吸附。
6)木纤维吸附铀前后的FT-IR谱表明,木纤维的基本结构仍保持完整。
[1] 徐伟昌.生物技术在核工业中的应用[M].长沙:国防科技大学出版社,2002.
[2] TSEZOS M,VOLESKY B.Biosorption of uranium and thorium[J].Biotechnology and Bioengineering,1981,23(3):583-604.
[3] TSEZOS M.Biosorption of uranium and thorium[R].Montreal,Canada:Mc Gill University,1980.
[4] FREER J,BAEZA J,MATURANA H,et al.Removal and recovery of uranium by modified Pinus radiata D.Don bark[J].Journal of Chemical Technology and Biotechnology,1989,46(1):41-48.
[5] AKHTAR K,WAHEED A M,KHALID A M.Removal and recovery of uranium from aqueous solutions by Trichoderma harzianum[J].Water Research,2007,41(6):1 366-1 378.
[6] BAYRAMOGˇLU G,ÇELIK G,ARICA M Y.Studies on accumulation of uranium by fungus Lentinus sajor-caju[J].Journal of Hazardous Materials,2006,136(2):345-353.
[7] TSURUTA T.Removal and recovery of uranium using microorganisms isolated from Japanese uranium deposits[J].Journal of Nuclear Science and Technology,2006,43(8):896-902.
[8] TSURUTA T.Removal and recovery of uranyl ion using various microorganisms[J].Journal of Bioscience and Bioengineering,2002,94(1):23-28.
[9] 宋金如,龚治湘,罗明标,等.凹凸棒石粘土吸附铀的性能研究及应用[J].华东地质学院学报,1998,21(3):265-272.
SONG Jinru,GONG Zhixiang,LUO Mingbiao,et al.Study on the performance of adsorbing uranium by attapulgite clay and its application[J].Jourmal of East China Geological Institute,1998,21(3):265-272(in Chinese).
[10]刘艳,易发成,王哲.膨润土对铀的吸附研究[J].非金属矿,2010,33(1):52-53,57.
LIU Yan,YI Facheng,WANG Zhe.Study on sorption of bentonite to uranium[J].Non-Metal-lic Mines,2010,33(1):52-53,57(in Chinese).
[11]夏良树,谭凯旋,王晓,等.铀在榕树叶上的吸附行为及其机理分析[J].原子能科学技术,2010,44(3):278-284.
XIA Liangshu,TAN Kaixuan,WANG Xiao,et al.Adsorption behavior of uranium and mechanism analysis on banyan leaves[J].Atomic Energy Science and Technology,2010,44(3):278-284(in Chinese).
[12]王翠苹,徐伟昌,庞红顺.榕树叶对铀吸附的研究[J].环境科学与技术,2004,27(2):19-20.
WANG Cuiping,XU Weichang,PANG Hongshun.Study on uranium biosorption by banyan leave[J].Environmental Science and Technology,2004,27(2):19-20(in Chinese).
[13]冯媛,易发成.稻壳对铀吸附性能的研究[J].原子能科学技术,2011,45(2):161-167.
FENG Yuan,YI Facheng.Adsorptive property of rice husk for uranium[J].Atomic Energy Science and Technology,2011,45(2):161-167(in Chinese).
[14]ESPOSITO A,PAGNANELLI F,VEGLIO F.pH-related equilibria models for biosorption in single metal systems[J].Chemical Engineering Science,2002,57(3):307-313.
[15]PSAREVA T S,ZAKUTEVSKYY O I,CHUBAR N I,et al.Uranium sorption on cork biomass[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2005,252(2):231-236.
[16]BAYRAMOGLU G,DENIZLI A,BEKTAS S,et al.Entrapment of Lentinus sajor-caju into Caalginategel beads for removal of Cd(Ⅱ)ions from aqueous solution:Preparation and biosorption kinetics analysis[J].Microchemical Journal,2002,72(1):63-76.
[17]卢涌泉,邓振华.实用红外光谱解析[M].北京:电子工业出版社,1989:21.
Adsorption Behavior and Mechanism of Uranium on Wood Fiber
WANG Zhe1,2,YI Fa-cheng1,FENG Yuan1
(1.Fundamental Science on Nuclear Wastes and Environmental Safety Laboratory,
Southwest University of Science and Technology,Mianyang621010,China;2.School of Earth and Space Sciences,University of Science and Technology of China,Hefei 230026,China)
The adsorption performance of uranium on wood fiber was studied with static experiment.The influence factors on the U(Ⅵ)removal rate such as wood fiber particle size,adsorption time,dosage,temperature,pH and initial concentration were researched,and the adsorption process was analyzed in terms of thermodynamics and kinetics.The results show that the adsorption equilibrium time is 4hours.When the pH reaches 3for uranium-containing wastewater,uranium can be removed with the decrease of the size of adsorbent and with the increase of adsorbent dosage and temperature.The equilibrium adsorption data fit to Langmuir isotherms.The kinetic analysis shows that the adsorption rate is mainly controlled by chemical adsorption.The adsorption process can be described by an equation of pseudo 2nd-order model.The thermodynamic data indicate that the synergistic uranium bio-sorption by wood fiber is a spontaneous and endothermal adsorption process.The adsorption mechanism was analyzed with SEM,FT-IR and EDS.The results show that the surface form of wood fiber is changed and uranium mainly chelates with active groups on the fiber’s surface and forms the complexes.These indicate that the adsorption of uranium should be of surface coordination.The analyses of EDS before and after adsorption of uranium prove that the behavior of adsorption is ion exchange.The above results indicate that the adsorption mechanism is mainly surface coordination and ion exchange adsorption,followed by physical absorption.
wood fiber;uranium;adsorption performance;adsorption behavior;adsorption mechanism
O647.3
A
1000-6931(2015)02-0263-10
10.7538/yzk.2015.49.02.0263
2013-10-21;
2014-07-22
国家自然科学基金资助项目(41402248);四川省教育厅科技创新团队资助项目(12zd1106);固体废物处理与资源化教育部重点实验室基金资助项目(12zxgk11);非金属复合与功能材料重点实验室基金资助项目(11zxfk06);核废物与环境安全国防重点学科实验室团队基金资助项目(13zxnk08)
王 哲(1979—),男,吉林乾安人,讲师,博士研究生,环境科学专业
